胆囊切除术后Hem-o-lok夹胆管移位3例报告
2022-02-10中国人民解放军联勤保障部队第九四医院付振东范瑞芳李月胜许树林蔺志鹏缪佰纹庞耀平秦建伟
中国人民解放军联勤保障部队第九四〇医院 付振东,范瑞芳,党 政,李月胜,许树林,蔺志鹏,缪佰纹,庞耀平,秦建伟
近年,随着饮食结构的改变,成年人中10%~15%患有胆道系统结石性疾病,其中1%~3%每年发生急性胆囊炎或急性胆管炎[1-2]。随着腹腔镜技术的发展,腹腔镜胆囊切除术(laparoscopic cholecystectomy,LC)及腹腔镜胆总管探查术(laparoscopic common bile duct exploration,LCBDE)越来越多地用于治疗胆囊结石及胆总管结石。LC术中结扎夹的使用可使胆囊管与血管有效闭合,节省手术时间。Hem-o-lok结扎夹是由不可吸收的多聚合物材料制成,具有组织反应性小、结扎范围广、闭合力度均匀、无组织切割等优点,是目前夹闭胆囊管及胆囊血管的常用方法之一[3]。近年,有关LC术后Hem-o-lok结扎夹移位的报道逐渐增多,回顾文献报道,Hem-o-lok夹向胆道迁移或诱发结石形成的病例有33例,其中多数为LC+LCBDE术后出现,少数为LC术后出现[2-15]。本文回顾性分析我院3例Hem-o-lok夹迁移入胆总管患者的临床资料,结合既往病例报道,探讨其发生机制、治疗及预防策略。病例1,男,43岁,既往因“胆囊结石伴慢性胆囊炎”于外院行LC,手术顺利,术后恢复良好。术后4个月患者出现皮肤巩膜黄染并进行性加重,无腹痛、发热等,外院CT及我院腹部B超提示:胆管腔内数枚结石并胆管扩张;胆囊切除术后。遂行LCBDE+胆道镜取石术,胆总管切开探查见2枚Hem-o-lok夹完全迁移至胆道内,周围散在碎屑样结石,未见胆管明显狭窄(图1)。胆管外未见其他Hem-o-lok夹,取出Hem-o-lok夹并一期缝合胆总管,随访6个月,患者恢复良好。病例2,女,61岁,因胆囊结石伴急性胆囊炎在当地医院行LC,术中分别使用2枚Hem-o-lok夹闭胆囊管、胆囊动脉。术后5个月出现皮肤巩膜黄染。MRCP提示:胆总管局部截断,致肝内外胆管扩张,肝内胆管炎(图2)。术前考虑胆囊切除术中医源性胆道损伤及瘢痕愈合致胆道狭窄,拟行剖腹探查术+胆总管探查+胆肠吻合术。术中探查见胆囊管残端与肝总管汇合处可见一约2 cm大的不规则纤维包块,压迫胆总管,遂切开病变胆管段,见胆管腔内4枚Hem-o-lok夹及胆总管内黑色胆色素性结石(图3)。清理Hem-o-lok夹及结石后行胆肠吻合术并修整胆管,随访6个月患者恢复良好。病例3,女,51岁,因先天性胆总管囊肿(Ⅰ型)于我院行LC+胆总管囊肿切除术+胆管空肠吻合术,术中用两枚Hem-o-lok夹闭胆囊管与胆囊动脉。术后3个月患者出现间歇性高热、全身黄染症状;上腹部CT提示:胆肠吻合口高密度异物影,胆管-空肠吻合肠壁略厚并肝内胆管轻度扩张(图4)。术前考虑吻合口缝线致结石形成,阻塞吻合口引起胆管炎症状,遂再次行腹腔镜手术探查,沿原胆肠吻合口肠袢侧向上切开吻合口,见两枚Hem-o-lok夹移行于胆总管内,其中1枚部分嵌顿于胆管壁(图5、图6),周围泥沙样结石,吻合口局部瘢痕形成致吻合口狭窄,取出Hem-o-lok夹,修整并再次吻合胆管空肠,随访3个月患者恢复良好。
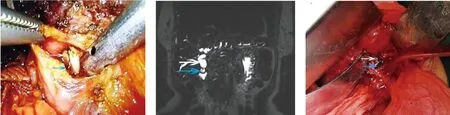
图1 胆总管管壁结构清晰,周围未见明显炎症及粘连,腔内见2枚Hem-o-lok夹(白色箭头)及泥沙样结石(蓝色箭头)

图4 CT水平面胆肠吻合口见两枚Hem-o-lok夹(蓝色箭头)
讨 论 Hem-o-lok夹由不可吸收的聚合材料构成,于1999年引入临床,其所具有的卡扣结构极大降低了脱落风险,缩短了手术时间,提高了管道闭合的安全性,并且不干扰影像学检查,传统观念认为是安全的手术材料[6]。近年,随着Hem-o-lok在临床的广泛使用及其相关并发症的报道,临床工作者对其临床使用的安全性有了新的认识。研究显示,非金属夹用于夹闭胆囊管及胆囊动脉,术后夹子移位至胆总管的发生率为1.8%[6],而针对1 600例使用Hem-o-lok夹的LC患者进行调查,发现术后8例发生Hem-o-lok移位,发生率为0.5%,且术后数天内Hem-o-lok发生移位可能导致LC术后出血与胆漏[7]。虽然Hem-o-lok移位率并不高,但其导致的并发症严重影响预后且增加患者的经济负担,因此,了解Hem-o-lok术后移位的发生机制及预防策略利于降低Hem-o-lok移位的发生率,进而提高临床工作质量,改善预后。
目前,有关Hem-o-lok术后移位的发生机制尚不明确,针对其移位原因的分析各报道也存在差异。炎症是影响其移位的一个重要因素,有关研究发现,急性化脓性胆囊炎患者术后Hem-o-lok更容易发生移位[8],可能因炎症的发生会引起局部组织发生粘连,并使周围组织的脆性增加,导致Hem-o-lok移位。LC+LCBDE胆道一期缝合术后存在较高的胆漏风险[16],胆漏的发生会导致局部炎症的发生,从而导致Hem-o-lok从胆囊管/动脉残端脱落并通过胆总管切口迁移至胆道[9],这可能是LC+LCBDE较LC术后更容易出现Hem-o-lok移位的原因。除炎症介导外,Hem-o-lok的移位还与术者的操作技术、胆囊炎症程度、组织缺血坏死、机体排异反应、胆道探查、机械切割、胆管或胃肠壁损伤伴充血及水肿、Hem-o-lok夹闭胆囊管/动脉位置不正确、使用Hem-o-lok的数量等因素有关[5,10]。有关报道显示,LC术中金属夹的使用可导致胆漏,或周围结构压迫金属夹致其移位[17-18],上述因素也可能导致Hem-o-lok移位至胆总管。Hem-o-lok移位以胆总管常见,也有迁移至十二指肠球部并导致溃疡的报道[19-22],发生机制可能与Hem-o-lok夹闭不全、放置位置不当或炎症反应等有关,炎症反应可引起十二指肠粘连、质地变脆,Hem-o-lok缓慢切开质脆的十二指肠进入肠壁[23]。Hem-o-lok属于不可吸收的多聚合物夹,近年,可吸收的组织夹逐渐被推广,虽然价格昂贵,但有望成为降低游走风险的首选[24]。关于Hem-o-lok夹与可吸收夹临床应用的选择性,有研究者从手术时间、术后住院时间、术后并发症、耗材费用方面进行对比分析,表明Hem-o-lok性价比更高[25]。对于两者临床应用的选择尚存在争议,且缺乏全面系统的对比研究为临床选择提供理论支持。值得注意的是,此类报道中,术前对于Hem-o-lok移位至胆总管的诊断并不明确,患者多因胆总管再发结石导致胆管炎及胰腺炎而就诊,临床表现与原发或继发性胆管结石引起的症状相似[26],这提示临床工作者对于LC或LC+ LCBDE术后患者出现上述症状时,应考虑是否由Hem-o-lok移位引起。
为降低Hem-o-lok移位的发生率,炎症控制是重要手段。对于急性胆囊炎的处理,主刀尽量具备丰富的临床经验,且应准确辨识及分离胆囊周围结构,尽量减少周围组织的创伤,避免误伤胆总管,准确夹闭胆囊管及胆囊动脉,以减少术后组织炎症及纤维化,减少Hem-o-lok夹移位。此外,应注意Hem-o-lok所夹位置及使用方法,术中Hem-o-lok的夹闭位置应距胆囊管与肝总管汇合处约0.5 cm,以减少术后瘢痕挛缩所致的结扎夹移位[5,11]。患者若为排异体质,临床医生则需要考虑使用可吸收夹或其他方式替代Hem-o-lok,从而避免Hem-o-lok的移位。对于是否用可吸收夹取代Hem-o-lok,以减少术后移位,笔者不予赞同,虽然Hem-o-lok及可吸收夹用于夹闭胆囊管及胆囊动脉均是安全、可靠的,但相比而言,Hem-o-lok性价比更高,值得在LC中推广应用[25]。
病例2中,患者既往因胆囊结石伴急性胆囊炎行LC,术后胆囊管残端局部炎症并纤维化包裹胆囊管及胆囊动脉处的Hem-o-lok,导致Hem-o-lok移位至胆总管。胆囊急性炎症更容易诱发局部炎症及排异反应发生,导致局部纤维化及Hem-o-lok移位,因此急性胆囊炎术后应积极予以抗感染、营养支持等治疗,避免术后术区炎症反复发作及纤维化形成,进而降低Hem-o-lok移位的风险。
近年,谐波超声刀等逐渐应用于胆囊切除术,Kandil等进行的一项前瞻性随机研究中指出,与传统LC相比,利用谐波刀行LC手术时间短,止血效果更好,是安全的替代方案[27],可有效避免Hem-o-lok移位的发生。但由于谐波刀装置昂贵,用于LC需考虑成本问题。
总之,LC或LC+LCBDE术后诸多因素促使Hem-o-lok移位,并促使胆总管结石形成,诱发胆管炎、胰腺炎等,但具体发生机制尚未明确,进一步病理学研究明确其发生机制是必要的。术者在熟练掌握LC手术要点、提升LC学习曲线的基础上,Hem-o-lok仍然可作为夹闭胆囊管、胆囊动脉安全有效的方法。当然,为减少术后Hem-o-lok的移位,可选择排斥反应小的可吸收生物夹及可吸收缝线替代,或选择谐波刀等,进而提升手术安全性、缩短手术时间、减轻术后疼痛。
