沉积温度和氢气浓度对CVD法合成Ti3SiC2 涂层的影响
2022-02-06茅思佳刘瑶瑶王梦千李爱军彭雨晴
朱 界,茅思佳,刘瑶瑶,王梦千,李爱军,彭雨晴
(上海大学 材料科学与工程学院 材料所,上海 200444)
1 前 言
Ti3SiC2被认为是一种新型可加工的功能陶瓷材料受到了广泛关注。将其作为涂层可有效提高复合材料的导电性能、电磁屏蔽性能及耐腐蚀性能等,在能源、航空航天和军事领域有较好的应用前景[1-2]。例如在燃料电池领域,涂层会提高金属双极板的耐蚀性,但同时会降低金属双极板的导电效率,因此需要电涂层具有高电导率,Ti3SiC2涂层的研发可以同时提高双极板耐蚀性和电导率。目前Ti3SiC2涂层的制备方法主要有化学气相沉积法(CVD)[3]、物理气相沉积法(PVD)[4]和热喷涂法[5]等。
CVD由于其独特的绕镀性以及工艺环节的可控性,是制备涂层最常用的技术。通过对CVD 工艺参数如沉积温度、前驱体浓度的精准调控等,可以直接改变涂层的质量[6-7]。前驱体的裂解激活能受到沉积温度的影响,从而影响涂层的结构及组成。Nickel等[8]以SiCl4-TiCl4-CCl4-H2为反应体系利用CVD 法合成了Ti3SiC2单晶。研究表明当反应温度低于1 473 K时,沉积产物为多晶层,当温度高于1 573 K 时,产物为板状单晶。杨钢宜等[9]研究发现在1 273~1 523 K温度下,以TiCl4-CH3SiCl3-H2-Ar作为前驱体采用CVD法制备的Ti3SiC2涂层,物相组成和微观结构均会随温度发生改变。H2浓度的变化对化学气相沉积的速率、涂层的元素比例、形貌结构也有重要影响[10]。Racault等[11]提出了H2对促进TiCl4裂解的重要性,H2浓度越大,Ti3SiC2的晶粒尺寸和晶粒数量都会增加。此外,沉积温度和H2浓度对涂层的沉积动力学也会产生影响,决定了涂层的沉积是由表面化学反应控制还是由质量传输过程控制。因此,沉积温度和H2浓度是化学气相沉积制备高纯度Ti3SiC2涂层及其均匀性的关键参数,然而,在CVD法制备Ti3SiC2涂层中,对于不同的前驱体体系,沉积温度和H2浓度的影响至今没有一个确定的机理。
本研究采用CVD法,在采用CH3SiCl3-H2-Ar体系制备SiC涂层的基础上[12],引入TiCl4前驱体,将TiCl4-CH3SiCl3-H2-Ar作为新颖的前驱体系统,在石墨片上合成Ti3SiC2涂层,研究了不同沉积温度和H2浓度对Ti3SiC2涂层的沉积速率、表面形貌和组成的影响。对TiCl4-CH3SiCl3-H2-Ar体系合成Ti3SiC2涂层的前驱体裂解过程和表面反应过程进行了分析,提出了在该前驱体体系中,Ti3SiC2涂层合成的主要反应路径。
2 实 验
2.1 实验原料
反应器采用立式垂直热壁化学气相沉积炉,如图1 所示。四氯化钛(TiCl4)和三氯甲基硅烷(CH3Cl3Si)纯度分别为99.9%和99%,H2和Ar纯度为99.99%。
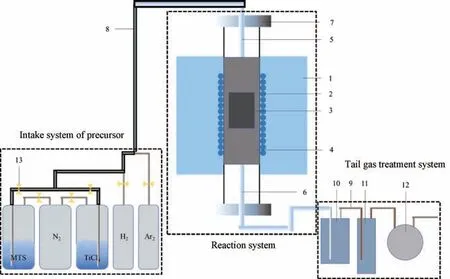
图1 立式垂直热壁化学气相沉积炉Fig.1 Vertical hot-wall chemical vapor deposition furnace(1 furnace body,2 heating wires,3 reaction molds,4 thermal insulation bricks,5 inlet pipe,6 outlet pipe,7 sealing cover,8 constant temperature belt,9 gas pipe,10 cold trap,11 tail gas filter tank,12 vacuum pressure pump,13 valve)
2.2 试样制备

2.3 测试方法
通过测定距离气体入口处1~8 cm 的多孔陶瓷片的质量变化,计算Ti3SiC2涂层的沉积速率。每次沉积完成后,采用METTLER TOLEDO MT104型电子天平对多孔陶瓷片进行称重,沉积速率的计算方式如下:

式中:v为Ti3SiC2涂层在单位时间单位面积的沉积速率(g·m-2·h);m0和m1分别表示沉积前后的质量(g);A 为多孔陶瓷片的总表面积(m2);t为沉积时间(h)。采用扫描电子显微镜(SEM,JSM-7500F,5 k V)对Ti3SiC2涂层进行形貌表征,结合X 射线能谱仪(EDS)分析涂层中的元素含量,采用X 射线衍射仪(XRD,PANayltical Empyrean powder X-ray diffractometer,Cu)对涂层的物相进行分析,利用X射线光电子能谱分析仪(XPS,ESCALAB 250Xi,Al K Alpha)分析涂层表面元素信息。
3 结果与讨论
3.1 Ti3 SiC2 涂层的沉积速率
根据不同的沉积温度、H2浓度,多孔陶瓷片的重量变化,研究其沉积速率随工艺的变化,由此可以分析不同参数对涂层沉积动力学的影响。
3.1.1 不同温度下Ti3SiC2涂层的沉积速率 图2a显示了沉积速率随着与进气口距离增大的变化。在1 273~1 373 K的范围内,涂层的沉积速率沿着气体流动方向逐渐减小,这是因为前驱体TiCl4和MTS在高温下发生快速裂解,产生大量的活性气相组分,沿气体流动方向吸附在基底上发生表面化学反应,在沿程方向上活性气相组分逐渐被消耗,从而沉积速率快速降低。同时,由于表面反应会产生大量的气相副产物HCl,与基体发生脱附,向气相主体扩散,阻碍了部分活性组分向基底吸附的路径,也会抑制表面反应的进行。根据流体力学理论,随着进入管道的距离增加,流体与管壁间的边界层厚度会不断增加,边界层内的气体流动性差,表面反应速率降低,因此远离进气口的沉积位置,沉积速率最小。在1 423 K 时,沿程沉积速率波动性较大,这是由于温度升高,前驱体TiCl4和MTS裂解更为迅速,在1~3 cm 处活性气相组分快速累积,沉积速率呈上升趋势,随着表面反应的剧烈程度增加,气相副产物HCl的浓度随之增加,导致3~7 cm 处沉积速率不断下降。在接近出气口位置的沉积速率有所增加,这是由于气体在出气口处流速会有所增加,气相副产物HCl的浓度相对减少,对表面反应的抑制作用降低。
图2b显示在1 273~1 373 K 内,温度升高,涂层的沉积速率呈指数形式增加,说明沉积过程主要受表面化学反应控制;当温度高于1 373 K 时,随着温度的升高,涂层的沉积速率降低,因为在高温下TiCl4和MTS快速充分裂解,气相反应和表面反应剧烈程度增加,产生大量气相副产物从表面脱附,根据Langmuir理论,这会降低气相活性组分向表面吸附的趋势,从而抑制涂层沉积,所以在高温下涂层的沉积速率主要受传质过程控制。

图2 不同温度下的Ti3 SiC2 涂层沉积速率(P=5 kPa,α=50%) (a)沿程沉积速率; (b)平均沉积速率Fig.2 Deposition rate of Ti3 SiC2 coatings at different temperatures(P=5 kPa,α=50%)(a)deposition rate along the mold; (b)average deposition rate
根据Arrhenius公式可以得到沉积温度的倒数与沉积速率对数的关系图(图3),Arrhenius曲线的斜率随温度升高由负变为正,斜率体现的是不同温度范围内各种活性气相组分的综合反应活化能,是不同气相组分促进和抑制沉积过程共同作用的表现,可以有效反映出温度对反应速率的影响。在低温区Ⅰ(1 273~1 373 K),Arrhenius曲线的斜率为负,Ti3SiC2涂层的沉积反应活化能Ea在107.6 kJ/mol左右,是典型的表面反应控制过程。在高温区Ⅱ(1 373~1 423 K),由于气相裂解和表面反应剧烈,活性物质扩散较慢,沉积速率主要受传质控制。
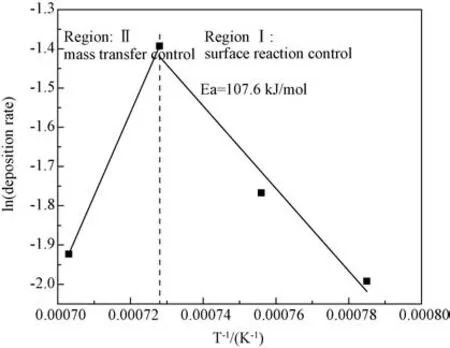
图3 不同温度下的Arrhenius曲线Fig.3 Arrhenius curve of different temperatures
3.1.2 不同H2浓度下Ti3SiC2涂层的沉积速率
在以TiCl4-CH3SiCl3-H2-Ar作为前驱体的化学气相沉积过程中,H2一方面作为载气,负责将TiCl4和CH3SiCl3输送到沉积室内,另一方面作为反应气体促进TiCl4和MTS在气相中的裂解。因此改变H2浓度α,对Ti3SiC2涂层的沉积速率有着重要影响。

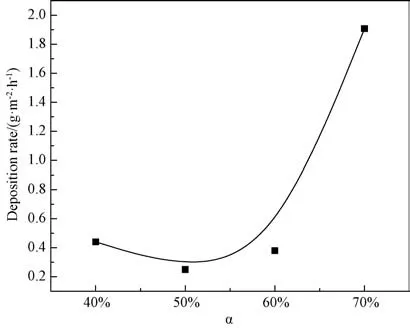
图4 不同位置处Ti3 SiC2 涂层的平均沉积速率随氢气浓度α的变化(T=1 373 K,P=5 kPa)Fig.4 Average deposition rate of Ti3 SiC2 coating varies with hydrogen concentration at different locations(T=1 373 K,P=5 kPa)
图5为不同α下沉积速率的变化趋势。从图可见距离进气口1~4 cm 处,随着与进气口距离的增加沉积速率快速降低,说明α对靠近进气口的位置的Ti3SiC2涂层沉积有一定的促进作用,在距离进气口4~8 cm 处,α的变化对涂层沉积速率的影响很小。从图中还可以发现,当α=50%时,沿程沉积速率的变化趋势最小,在这个参数下有利于薄膜的均匀沉积。
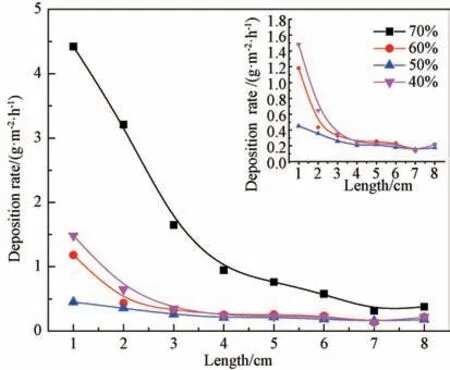
图5 不同氢气浓度α下沿程沉积速率的变化趋势(T=1 373 K,P=5 kPa)Fig.5 Deposition rate at different hydrogen concentrations(T=1 373 K,P=5 k Pa)
3.2 Ti3 SiC2 涂层的微观结构
3.2.1 温度对Ti3SiC2涂层表面形貌和组成的影响
如图6所示,在1 273和1 323 K 的较低温度下,涂层由200~400 nm 的小颗粒构成,结构疏松,这些颗粒通过聚集团簇形成了1μm 左右的球状,或沿平行于基底的某一方向择优生长为蠕虫状,在1 273 K时(图6a),球状和蠕虫状沉积物表面还有很多大小在50 nm 左右的小颗粒,这是由于在1 273 K 的低温下晶粒长大速率很小,小晶核无法及时生长并与大晶核融合,当温度达到1 323 K 时,50 nm 左右的小颗粒发生了融合长大,形成表面光滑的蠕虫状沉积物,涂层变得更加致密,如图6b中可以看到背底形成了较为完整的涂层。当沉积温度为1 373 K 时(图6c),涂层较1 273和1 323 K 更为致密,蠕虫状的沉积物消失,涂层由200~400 nm 的多边形颗粒融合成的层状结构组成,层状结构平行于基底表面,沿水平方向扩展生长,沿垂直于基底的方向层叠堆积,这些多边形小颗粒与Racault等[11]在透射电镜下观察到的Ti3SiC2单晶形貌一样。当沉积温度达到1 423 K 时(图6d),涂层致密度进一步提高,涂层由大量不规则的多边形板状结构组成。表1为采用EDS对不同沉积温度下的涂层表面进行点扫,从表可见,随着温度的增加,涂层表面C含量呈先减后增,在1 373 K 达到最小值,而Ti和Si的含量变化与之相反,分别在1 373和1 323 K达到最多,其中当沉积温度为1 373 K 时,Ti、Si、C 的比例最接近Ti3SiC2的化学计量比。
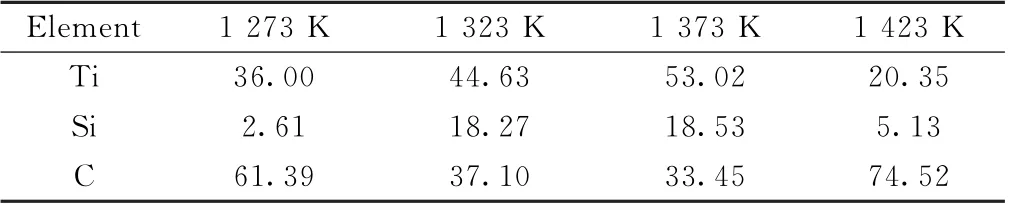
表1 不同沉积温度下涂层的EDS点扫结果Table 1 EDS point sweep results of coating at different deposition temperatures

图6 不同温度下Ti3 SiC2 涂层的表面形貌图(P=5 kPa,α=50%) (a)1 273 K; (b)1 323 K; (c)1 373 K; (d)1 423 K Fig.6 SEM images of Ti3 SiC2 coatings at different temperatures(P=5 k Pa,α=50%)(a)1 273 K; (b)1 323 K; (c)1 373 K; (d)1 423 K
3.2.2 H2浓度对Ti3SiC2涂层表面形貌和组成的影响
H2对Ti3SiC2涂层表面形貌有着重要的影响,如图7 所示,当α=40%时,涂层是由长度为300~500 nm,直径100 nm 左右的棒状颗粒堆积构成的。图7b是在P=5 k Pa,T=1 373 K,α=50%的参数下生长的涂层,结构与图6c相同。当α=60%时,涂层由直径为500 nm 左右的小颗粒紧密堆积构成,致密度增加,具有平行于基底表面的择优取向。α=70%时涂层表面相对致密,涂层由1μm 左右的颗粒融合堆积构成,这些1μm 左右的颗粒表面还能看到100 nm左右的小颗粒,说明1μm 左右的颗粒是由100 nm 左右的小颗粒长大并互相吞并融合形成的,与Pickering等[14]所描述的表面形貌类似。根据表2所示的不同H2浓度下涂层的EDS点扫结果,发现H2浓度对Ti、Si、C三种元素比例的影响很大,随着H2浓度的增加,Ti的含量呈先增后减的趋势,而Si和C 的变化趋势于Ti相反。

图7 不同氢气浓度下Ti3 SiC2 涂层的表面形貌图片(P=5 kPa,T=1 373 K) (a)α=40%;(b)α=50%;(c)α=60%;(d)α=70%Fig.7 SEM images of Ti3 SiC2 coating at different hydrogen concentrations(P=5 k Pa,T=1 373 K)(a)α=40%; (b)α=50%; (c)α=60%; (d)α=70%

表2 不同氢气浓度下涂层的EDS点扫结果Table 2 EDS point scanning results of the coating under different hydrogen concentration
3.3 Ti3 SiC2 涂层的成分分析
图8 显示涂层中物相主要包括Ti3SiC2、TiC、SiC、TiSi2、Ti5Si3和Ti5Si4。随 沉 积 温 度 的 升 高,Ti3SiC2的各个峰开始出现,在1 373 K 时涂层中Ti3SiC2的峰明显最多,当温度达到1423 K 时,Ti3SiC2相基本消失。当α=50%时,可以看到明显的Ti3SiC2峰,当α 进一步增大,涂层中的物相主要为TiC 和SiC。结合标准PDF 卡片(74-0310),发现CVD-Ti3SiC2在(105)、(107)、(108)、(110)具有一定的择优取向,而(008)由于与(110)面是垂直关系[14],因此非常弱。

图8 Ti3 SiC2 涂层的XRD图谱 (a) 不同沉积温度; (b) 不同H 2 浓度Fig.8 XRD patterns of Ti3 SiC2 coatings (a)different deposition temperatures; (b)different hydrogen concentrations
根据XRD 的分析结果,可以发现以TiCl4-CH3SiCl3-H2-Ar作为前驱体通过CVD 合成Ti3SiC2涂层的实验中,当T=1 373 K,P=5 k Pa,α=50%时,涂层中Ti3SiC2相作为主相。为了进一步探究涂层表面成分信息,进行XPS分析,图9为此参数下涂层的XPS图谱,均以C 的标准峰位284.6 e V 进行电荷校正。图9(a)是全谱图,图中主要是Ti、Si、C 的峰以及由于样品与空气接触而产生的O 的峰。对C 1s高分辨率图谱进行了拟合分析,如图9(b)所示,284.6 和281.8 e V 处的峰位分别对应了C—C 和Ti—C 键的结合能[15],而在较高的能量处出现的两个峰分别属于Ti3SiC2和TiC 混 合 物 中 的C—O—R 和CO2—R键[16-17]。图9(c)是对Ti 2p高分辨率图谱进行分峰拟合分析的结果,可以看到TiO2的Ti 2p1/2和Ti 2p3/2之间的能量分离为6 e V,此数值与Riley 等[16,18]对Ti3SiC2研究的结果相符合。在Ti3SiC2的晶体结构中,Ti、Si、C三种原子是以Ti2—C—Ti1—C—Ti2—Si链的方式按Z字形式连接的[19],因此Ti在其中有两种不同的化学环境,分别是代表Ti—C键的C—Ti1—C(454.8 e V)和 表 示 碳 硅 化 学 的 C—Ti2—Si(453.7 e V),由此推测图9(b)中Ti3SiC2的Ti 2p3/2结合能包含了C—Ti1—C和C—Ti2—Si键的结合能,而TiC的Ti 2p3/2结合能与TiC中Ti—C键的结合能(255.9 e V)[20]相匹配。
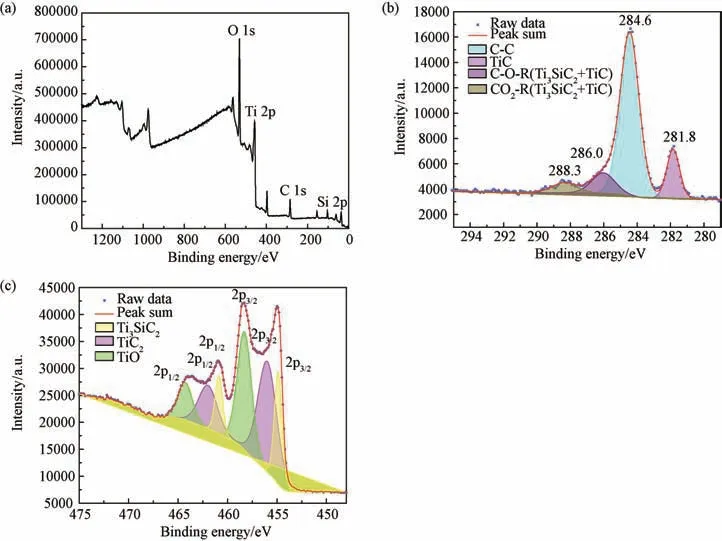
图9 Ti3 SiC2 涂层的XPS谱图(T=1 373 K,α=50%,P=5 kPa) (a) 全谱图;(b)C 1s谱图; (c)Ti 2p谱图Fig.9 XPS spectra of Ti3 SiC2 coating(T=1 373 K,=50%,P=5 kPa)(a)Full; (b)C 1s; (c)Ti 2p
3.4 TiCl4-CH3 SiCl3-H2-Ar体系合成Ti3 SiC2 涂层的沉积过程
以TiCl4-CH3SiCl3-H2-Ar作为前驱体系统,采用CVD 法制备Ti3SiC2主要经历以下几个过程:前驱体裂解、气体组分向基底表面扩散、气体分子在基底表面吸附、表面非均相反应、气相副产物脱附和扩散。在一定温度下,TiCl4在H2的作用下会发生裂解反应,主要是式(1)和式(2):

根据Francis Teyssandier[21]对Ti-Cl-H 体系气相反应的热力学和动力学研究分析可知,TiCl4和H2在高温下首先会发生TiCl4的单分子键裂解,一旦TiCl4裂解产生Cl-就会立刻与H2反应生成HCl,使Cl-和H+达到相对平衡,同时还会发生双分子反应,产生TiCl3和TiCl2,所以TiCl4在高温下由于H2的作用,其裂解机理可以总结如下:

根据卢翠英等[13]的研究,三氯甲基硅烷MTS分子的裂解主要是其化学键发生断裂,最初始裂解如式(7)所示得到自由基SiCl3·和CH3·。
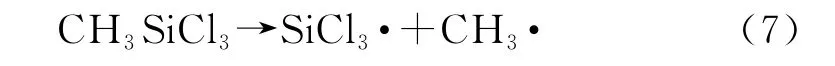
之后前驱体中以SiCl3·和CH3·为主进行二级裂解,主要是自由基SiCl3·的脱Cl和CH3·的脱H 反应,产生SiCl2··和CH2··,由于SiCl3·的Cl断键摩尔反应热约为CH3·的H 断键摩尔反应热的一半,因此CH3·的脱H 反应相对于SiCl3·的脱Cl反应更加困难。同时SiCl3·和CH3·还会与MTS发生反应,促使MTS发生进一步的裂解,提高前驱体组分中烃类气体的浓度。在TiCl4-H2-MTS-Ar体系中H2作为反应过程中的还原剂,不仅促进了前驱体的裂解,还在一定程度上增加了前驱体的碰撞机率,从而降低了前驱体裂解所需的活化能。在高温下,活性最高的H2会分解成H·自由基,参与到前驱体气相反应中。式(8)~(18)为相关的主要反应:
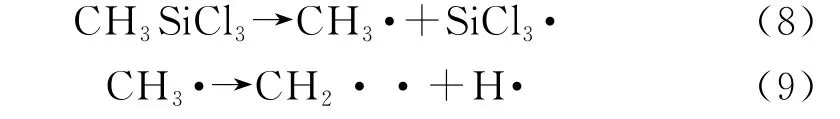

根据上述分析,以TiCl4-CH3SiCl3-H2-Ar体系作为前驱体系统,Ti3SiC2沉积过程的主要反应路径为:可能需要经历下列主要反应:
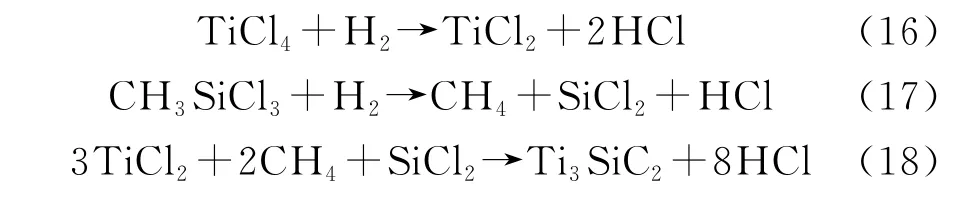
4 结 论
1.CVD-Ti3SiC2涂层沉积在1 273~1 423 K 的沉积温度范围包含了两种沉积机理。温度以1 373 K为转折点,随着温度的升高,沉积机理由表面化学反应控制为主转为传质控制为主。当沉积温度分别为1 273 K 和1 323 K 时,涂层形貌主要呈球状和蠕虫状;当沉积温度升高至1 373 K 和1 423 K 时,涂层形貌转变为层状结构。
2.沉积温度为1 373 K 时,氢气浓度对沉积速率的影响先减小后增加,以H2浓度α=50%为拐点。涂层形貌在不同的 H2浓度α 下分别为:棒状(α=40%),板 状(α=50%,α=60%)及 球 状(α=70%)。
3.CVD 法制备Ti3SiC2涂层的最优参数为:T=1 373 K,α=50%,P=5 kPa,此涂层中主相为Ti3SiC2,杂质相为TiC 和SiC,Ti3SiC2呈现择优取向。
