一种测量锂电池三元正极材料中添加剂的方法
2022-01-28刘向悦吴景林
刘向悦,吴景林,孙 超
(天津巴莫科技有限责任公司,天津 300380)
随着能源危机和环境污染问题的日益突出,开发可持续发展的新能源材料成为当今社会发展的当务之急。锂离子电池具有高电压、高容量和循环性能好的优点,迅速成为了近年来广为关注的研究热点。已经实用化的锂离子电池主要概况为以下三类:第一是具有层状结构的锂离子金属氧化物,主要包括钴酸锂、三元镍钴锰及镍钴铝酸锂;第二类是尖晶石结构的材料,LiMn2O4;第三类是聚阴离子结构的化合物,LiFePO4。其中三元正极材料因具有成本低、放电容量大、循环性能好、热稳定性高等优点,成为了最具发展前景的锂离子电池正极材料之一。由于三元材料具有的一些本征特点,例如高电压下稳定性差,容易与空气中的O2和H2O 反应进而引起气胀和循环性能差,以及高脱锂状态下Ni4+的强氧化性趋于还原生成Ni3+而释放氧气造成热稳定性不好,常常需要通过离子掺杂、表面包覆等方法来改善材料的电化学性能。随着材料的不断改进,单包覆或者单掺杂已经无法达到较好的效果,目前都是采用多种元素共包覆、掺杂来提高材料性能。锆、锶、钇、钛、镁(Zr、Sr、Y、Ti、Mg)为目前正极材料中最常用的包覆掺杂元素[1-3]。但这些元素掺杂或包覆量过高,会导致材料产生较高的过电位或降低材料容量,而较低的添加剂含量则不能对活性材料产生很好的保护作用或提高材料的电导率。因此在实际生产中,包覆掺杂的元素量的精准测量是制备优良材料的先决条件。
目前,对三元材料中主含量以及Li 元素的测量主要采用滴定法或重量法[4-7],而对于Zr 及含Zr 体系下Sr 和Y 含量的测量分析技术研究较少。Zr 在电池材料中部分会以二氧化锆的形式存在,难以溶于常规的酸溶液,在进行表征时通常收率较低。且根据相关资料显示,通常二氧化锆难溶于水、盐酸和稀硫酸,只能溶于热浓氢氟酸和浓硫酸[8]。浓硫酸溶解的样品粘度较大,不利于ICP 进样,氢氟酸会增加实验过程中的风险。此外,当样品中同时存在Y 和Sr 时,测试将更为复杂。在材料制备过程中,Y 和Sr 可以与Zr 形成ZrSrOx或者ZrYOx化合物,给分析造成进一步的困难。且包覆或掺杂的元素都是微量元素,化合物状态基本都为无定形态,很难使用X 射线衍射(XRD)、能量散射光谱(EDS)等对其进行定量分析。因此,如何能同时对含Zr 三元正极材料中的Zr、Sr、Y、Ti、Mg 等元素进行简单准确的定量分析,成了本领域中的技术难题。
本文采用电感耦合等离子体发射光谱法(ICP-OES),采用盐酸-硫酸-硫酸铵体系溶解样品,对三元正极材料中Zr、Y、Sr、Ti、Mg 元素实现同时测定,通过优化仪器工作条件,可以快速准确地检测出材料的添加剂含量。
1 实验
1.1 仪器及工作条件
Thermo ICP 7400 series 全谱直读电感耦合等离子体发射光谱仪(美国Thermo 公司),固态RF 发生器,带有Qtegra 操作软件。可调温电阻丝加热炉、容量瓶、三角瓶等。
发生器的功率RF 功率为1 150 W;雾化压力为1.8~2.2 MPa,雾化器流量为0.5 L/min;样品冲洗时间为30 s,曝光重复3 次;辅助气流量0.5 L/min;积分时间长波5 s,短波15 s,冲洗泵速75 r/min,分析泵速50 r/min,泵稳定时间为5 s。保证精密度满足分析测试要求。
1.2 主要试剂及标准溶液
盐酸、硫酸、硫酸铵均为优纯级,实验用水为超纯水,国家标准溶液,钛GSB G 62014-90(2201),镁GSB G 6005-90(1201),锆GSB G 62033-90(4001),锶GSB G 62031-90(3801),钇GSB G 62032-90(3901)。
1.3 实验方法
1.3.1 工作曲线标准溶液的制备
在配置标准工作溶液前,分别移取10 mL 的1 000 μg/mL的Zr、Y、Sr、Ti、Mg 的单标国标溶液于容量瓶中,配置含有Zr、Y、Sr、Ti、Mg 五种元素、浓度为100 mg/L 的混标作为标准储备溶液。分别准确称取5 份(0.1±0.000 1) g 的不含Zr、Y、Sr、Ti、Mg 元素添加的三元正极材料做为测试基体置于三角瓶中,依次向三角瓶中加入5 mL 盐酸并置于电阻丝加热炉上加热,温度设定为300~500 ℃。待样品溶解后,将样品取下并依次加入1 mL 浓硫酸、1 g 硫酸铵,然后继续置于电阻丝加热炉上加热,待白烟冒进,冷却至室温,转移至100 mL 容量瓶中。用移液管移取一定量的标准溶液贮备液至容量瓶中,根据移取液体积的不同,分别将其记为KB、No.1、No.2、No.3、No.4。然后将溶液瓶定容至刻度线,摇匀,将其作为标准溶液。其标准溶液的不同浓度,如表1 所示。
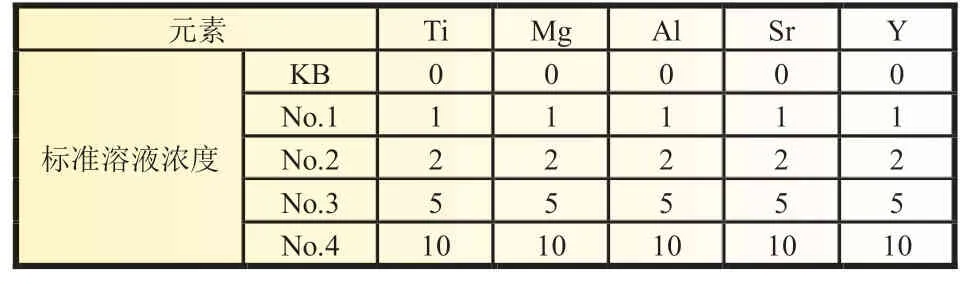
表1 掺杂元素的标准溶液 mg/L
1.3.2 样品待测液的制备
用天平准确称取(0.1±0.000 1) g 三元材料样品,置于100 mL 小三角瓶中,加入5 mL 盐酸并置于电阻丝加热炉上加热,温度设定为300~500 ℃。待样品溶解后,将样品取下并依次加入1 mL 浓硫酸、1 g 硫酸铵,然后继续置于电阻丝加热炉上加热,待白烟冒进,冷却至室温,转移至100 mL 容量瓶中,定容,摇匀。
1.3.3 加标回收率待测液的配制
用天平准确称取(0.1±0.000 1) g 三元材料样品,置于100 mL 小三角瓶中,加入5 mL 盐酸并置于电阻丝加热炉上加热,温度设定为300~500 ℃。待样品溶解后,将样品取下并依次加入1 mL 浓硫酸、1 g 硫酸铵,然后继续置于电阻丝加热炉上加热,待白烟冒进,冷却至室温,转移至100 mL 容量瓶中,记为溶液B、C。准确移取1 mL 的标准溶液No.3 于溶液B 中定容,摇匀,移取1 mL 的标准溶液No.4 于溶液C 中定容,摇匀。
2 结果与讨论
2.1 消解样品时硫酸和硫酸铵比例选择
利用硫酸和硫酸铵溶样,最重要的是要保证在溶解样品的过程中,防止浓硫酸在高温状态不稳定而发生喷溅。称量(0.1±0.000 1)g 样品加入5 mL 盐酸,待样品完全溶解后,分别向溶液中加入不同比例的浓硫酸和硫酸铵,寻找最佳的溶解比例,结果如表2 所示。
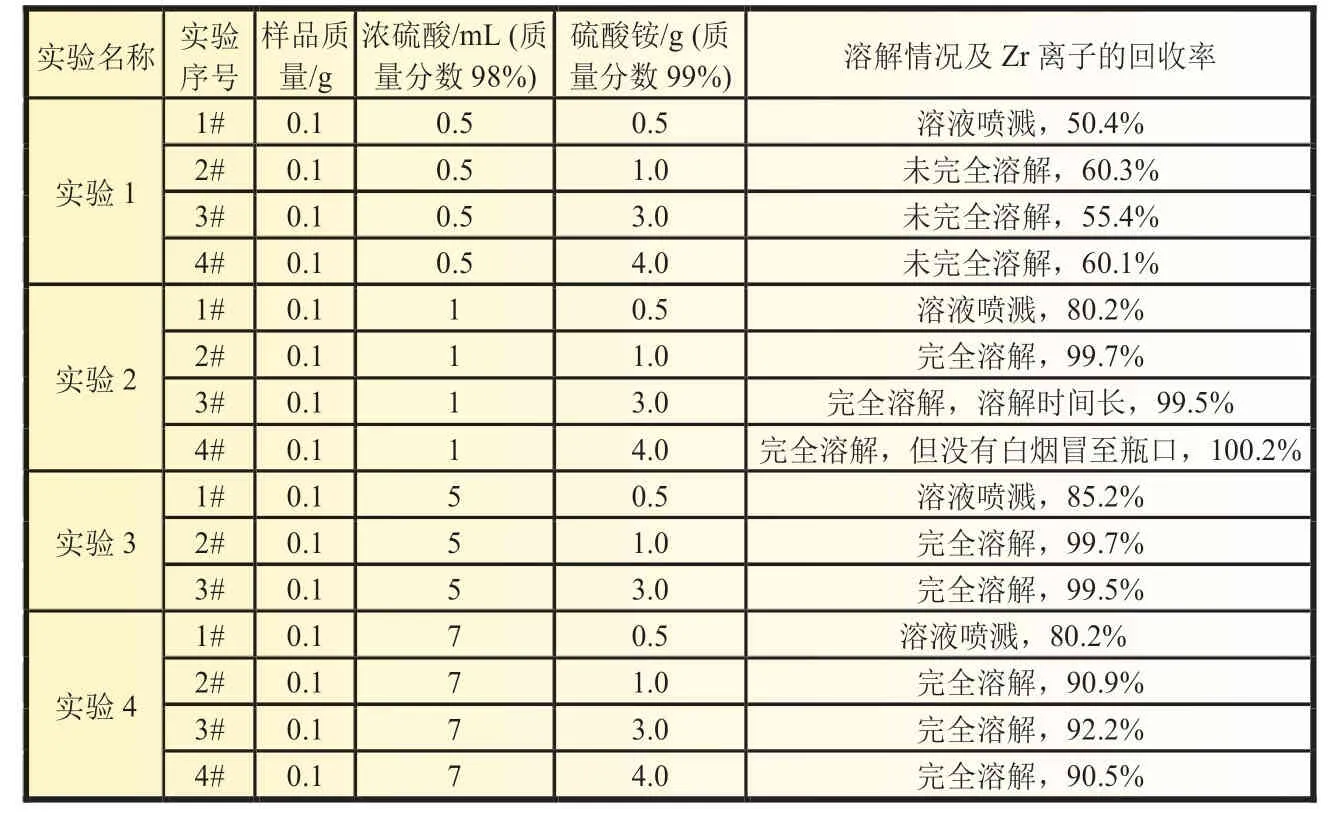
表2 硫酸和硫酸铵比例对溶解情况的影响
通过实验结果可以看出,在消解过程中加入硫酸铵,可以减少消解Zr 过程中产生的爆沸现象,提高Zr 消解效率,排除其他元素对测试结果的影响,并且可以减少浓硫酸的用量,降低溶液黏度,其原理是含有Zr 元素的待测样品在消解过程中,会发生如下反应:
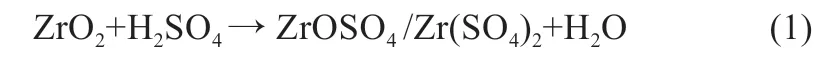
但该反应的反应速率较慢,因此常常反应不完全,ZrO2中的Zr 无法完全消解,测试结果往往不准确。且该反应温度过高,高温下浓硫酸并不稳定,易发生喷溅,因此要在反应的过程中加入少量的硫酸铵,增加硫酸根离子浓度,增加反应活度,提高反应速度。此外,浓硫酸、硫酸铵以及样品的比例对于实验结果也有显著影响:硫酸铵加入过少,会导致溶液喷溅,而硫酸铵加入过多,不仅不能加快氧化锆被完全溶解的速度,反而会因硫酸铵用量的增加,造成溶解过程中反应时间过长。测试过程中,抑制其他元素的分析信号,达不到准确分析测定的目的。通过实验研究,发现称取待测样品的质量、加入盐酸的体积、加入浓硫酸的体积、加入硫酸铵的质量依据0.1 g∶5 mL∶1 mL∶1.0 g 的比例,可以产生合适的酸度,使得离子能最大限度地溶解,且引入较少的杂质及干扰元素。
2.2 精密度实验
平行称取三元材料样品10 份,按照1.3.2 中的实验方法进行样品制备,测试结果如表3 所示,考察方法的精密度情况。其中5 种添加剂的精密度在1.0%~2.0%,精密度能够满足添加剂分析的要求。
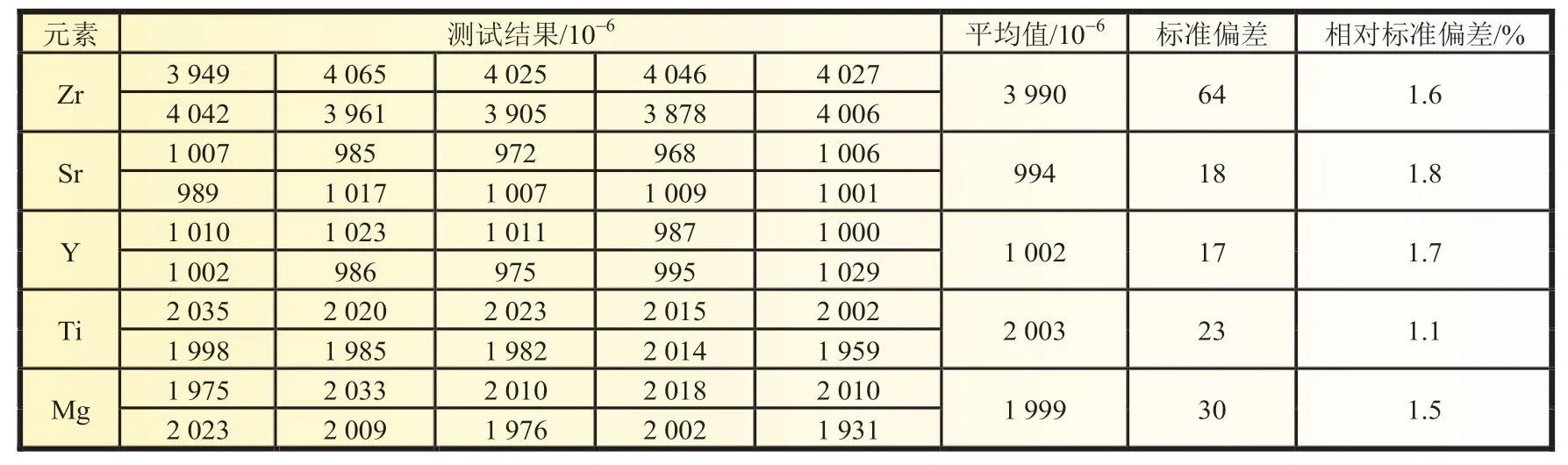
表3 精密度实验
2.3 加标回收率
选择两种加标浓度对三元材料样品进行加标回收实验,从回收率的结果来看,5 种元素的回收率都在95%~105%。根据回收率结果,一方面说明前处理的步骤对检测元素具有较好的收率;另一方面,在重复性实验和加标回收实验中采用的不含添加剂的材料进行基体匹配符合测试要求。表4 为加标回收实验结果。
3 结论
利用HCl-H2SO4-(NH4)2SO4体系溶解样品,可以实现ICPOES 同时测量锂离子电池中锆、锶、钇、钛、镁等添加剂元素的含量。本文通过实验,找到了盐酸、硫酸、硫酸铵的最优选比例,并通过精密度实验和加标回收实验证明该方法符合测试要求。实验结果表明,该方法简便、快速、准确,可以满足锂电池正极材料产业化发展中添加剂元素测量的需要。
