氯虫苯甲酰胺衍生物的合成及杀虫活性
2022-01-25杜晓华方佳琪楼佳明
杜晓华,方佳琪,楼佳明
(1.浙江工业大学 催化加氢中心,浙江 杭州 310014;2.浙江省绿色农药清洁生产技术研究重点实验室,浙江 杭州 310014;3.浙江省绿色农药协同创新中心,浙江 杭州 310014)
农药是水体污染的主要来源,过量使用农药对人的健康有害,对环境的污染也很大[1-6]。因此,减少化学农药施用量、限制有毒农药的施用以及研制开发安全高效的新型农药[7-11]是目前亟需解决的问题。氯虫苯甲酰胺是一种邻甲酰氨基苯甲酰胺类杀虫剂,具有高效、低毒等特点,应用广泛[12-15]。氯虫苯甲酰胺的大量使用会使机体产生严重的抗性,对其进行结构改造是延缓抗性发展的有效途径之一。天然氨基酸是高效、安全的生物活性分子,笔者将12 种天然氨基酸引入氯虫苯甲酰胺的分子结构中,设计并合成了一系列具有氨基酸片段的双酰胺类化合物[16-20]。
1 实验部分
1.1 试 剂
取代吡啶购自上海韶远科技有限公司;乙腈、甲醇、石油醚、二氯甲烷和乙酸乙酯购自上海凌峰化学试剂有限公司;N,N-二甲基甲酰胺购自西陇科学股份有限公司。以上试剂均为分析纯。
1.2 仪 器
玻璃仪器(普通),北京欣维尔玻璃仪器有限公司;磁力搅拌器(SM-3),上海志威电器有限公司;集热式恒温加热磁力搅拌器(DF-101S),杭州惠创仪器设备有限公司;旋转蒸发器(RE-52AA),上海亚荣生化仪器厂;循环水式多用真空泵(SHB-III),杭州惠创仪器设备有限公司;电子分析天平(AG135),Mettler Toledo;高效液相色谱仪(1260 Infinity)、气质联用仪(6890/5973 HP-5MS)和高分辨液质联用仪(6545 Q-TOF),Agilent;气相色谱仪(Trace GC Ultra)和液质联用仪(LCQ Fleet),Thermo Fisher;熔点仪(B-545),Buchi;核磁共振波谱仪(AVANCE III),Bruker。
1.3 合成路线
目标化合物设计为
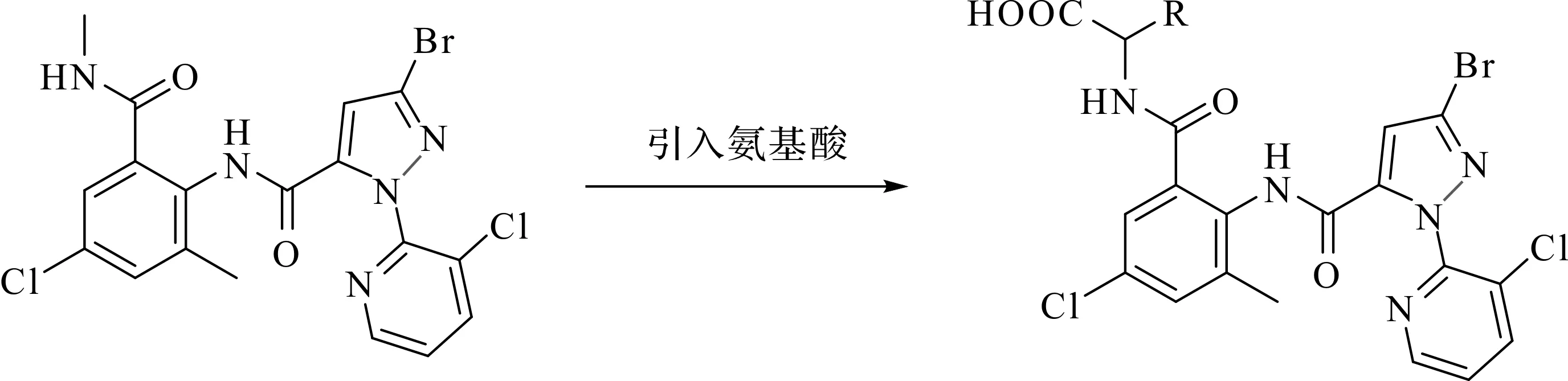
目标化合物的合成路线为
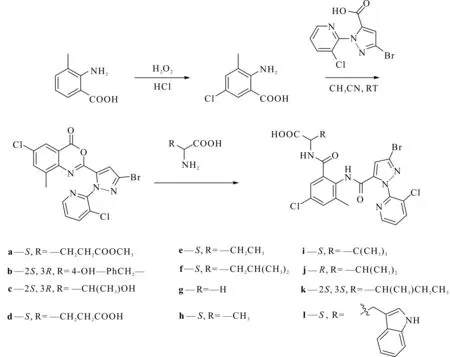
1.4 5-氯-3-甲基-2-氨基苯甲酸的合成
向反应瓶中加入3-甲基-2-氨基苯甲酸25 g(0.165 mol)和冰醋酸250 mL,在搅拌下滴加浓盐酸61.5 mL,5 min后再滴加30%的双氧水22.5 g。室温反应40 min后反应液变为棕褐色澄清溶液,加入500 mL水,有固体析出,抽滤,干燥得固体23.75 g,液相纯度96%,收率77.37%[21-27]。
1.5 6-氯-2-(3-溴-1-(3-氯吡啶-2-吡啶基)-1H-吡唑-5-基)-8-甲基-4H-3,1-苯并噁嗪-4-酮的合成
向500 mL反应瓶中加入3-溴-1-(3-氯吡啶-2-吡啶基)-1H-吡唑-5-甲酸10 g(0.033 mol),5-氯-3-甲基-2-氨基苯甲酸6.3 g (0.033 9 mol),乙腈200 mL,待降温至10 ℃后滴加3-甲基吡啶16 g(0.17 mol),30 min后加入9 g甲基磺酰氯溶于33 mL 乙腈溶液,反应液由褐色浑浊变为黄色浑浊,保温反应30 min,再升至室温反应30 min 后将反应停止,加入8.2 g HCl,加水,抽滤,干燥得到淡黄色固体12.6 g,液相纯度98%,收率82%。
1.6 目标化合物的合成
向100 mL三口瓶中加入6-氯-2-(3-溴-1-(3-氯吡啶-2-吡啶基)-1H-吡唑-5-基)-8-甲基-4H-3,1-苯并噁嗪-4-酮(0.001 mol),分别加入不同取代基的氨基酸(0.001 3 mol),10 mL DMSO,升温至60 ℃反应6 h。加入30 mL水,搅拌均匀后调酸至pH≈1,析出固体,抽滤得目标化合物a~l,液相纯度≥95%。
1.7 生物活性测试
药剂配制:将供试物用含0.1%吐温-80乳化剂的DMF溶解配制成质量分数为1.0%的母液,然后用蒸馏水稀释至实验所需的剂量备用。
生物活性测试:浸叶法,供试靶标为黏虫,将适量玉米叶在配好的药液中充分浸润后自然阴干,放入垫有滤纸的培养皿中,接黏虫3龄中期幼虫10 头/皿,置于24~27 ℃观察室内培养,2 d后调查结果,以毛笔触动虫体,无反应则视为死虫;喷雾法,供试靶标为朱砂叶螨、苜蓿蚜,分别将接有朱砂叶螨和苜蓿蚜的蚕豆叶片置于Potter喷雾塔下喷雾处理,处理后朱砂叶螨置于24~27 ℃观察室内培养,苜蓿蚜置于20~22 ℃观察室内培养,48 h后调查结果,以毛笔触动虫体,无反应则视为死虫。
2 结果与讨论
2.1 目标化合物的合成
先以2-甲基-3-氨基苯甲酸为起始原料,经过卤化生成5-氯-3-甲基-2-氨基苯甲酸;再与3-溴-1-(3-氯吡啶-2-吡啶基)-1H-吡唑-5-甲酸进行缩合反应生成6-氯-2-(3-溴-1-(3-氯吡啶-2-吡啶基)-1H-吡唑-5-基)-8-甲基-4H-3,1-苯并噁嗪-4-酮;最后引入氨基酸片段合成目标化合物。在合成目标化合物时,对反应条件进行了优化。结果表明:在进行缩合反应时,使用二甲亚砜DMSO作为溶剂反应效果最好,且温度越高反应速度越快,当温度为60 ℃时产率最高,其中f产率最高(95%)。
2.2 化合物的波谱分析
以目标化合物i为例进行谱学分析:1H NMR谱图中δ=10.56处的单峰为苯环与吡唑之间相连酰胺上氢的吸收峰;δ=8.48,8.14,7.60处的dd峰为吡啶环上氢的吸收峰;δ=8.20处的双重峰为苯环与脂肪烃间酰胺氢上的吸收峰;δ=7.51处的单峰为吡唑环上氢的吸收峰;δ=7.49,7.32处的双重峰为苯环上氢的吸收峰;δ=4.19处的双重峰为酰胺基与羧酸之间氢的吸收峰;δ=2.17处的单峰为与苯环相连的甲基;δ=0.94处的单峰为叔丁基上3 个甲基氢的吸收峰。目标化合物i的分子式为
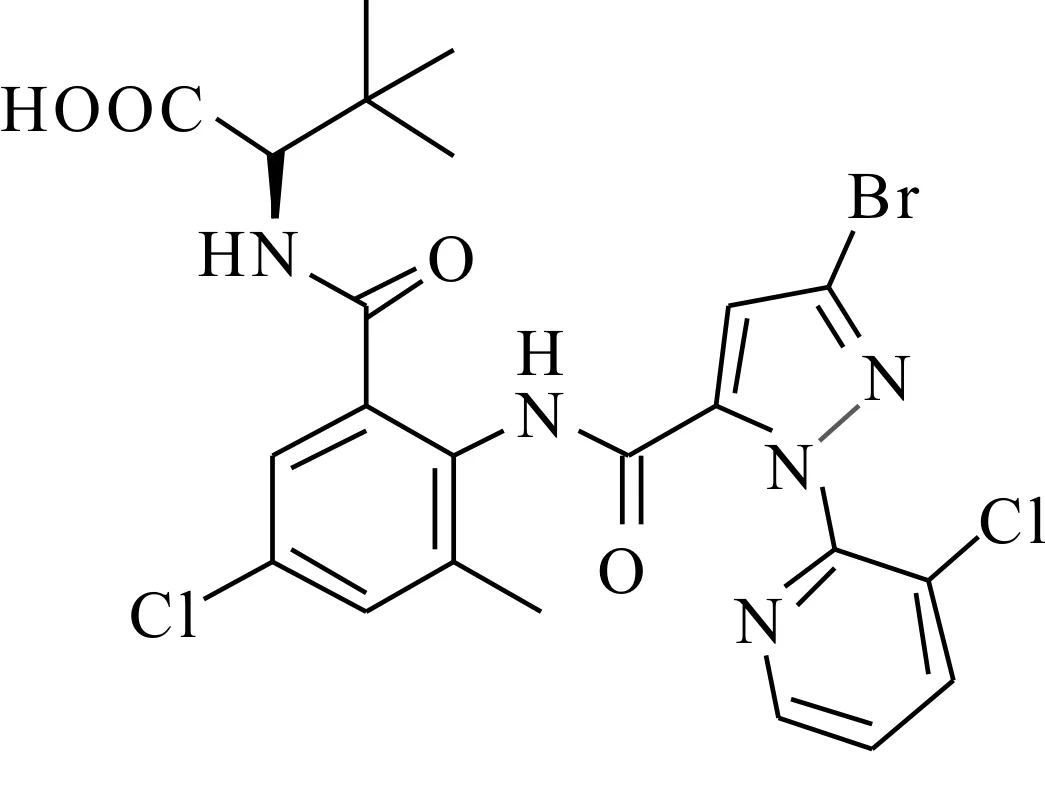
2.3 目标化合物的理化、1H NMR、13C NMR 和HRMS数据
3-溴-N-(4-氯-2-甲基-6-(5-甲氧基-5-氧戊酸-2-基氨基甲酰基)苯基)-1-(3-氯吡啶-2-基)-1H-吡唑-5-羧酰胺(a):卡其色固体,产率60%,熔点 108~111 ℃;1H NMR (500 MHz, DMSO)δ12.5(s,1H),10.25 (s,1H),8.57 (d,J=7.4 Hz,1H),8.48 (m,1H),8.14 (dd,J=8.0,1.2 Hz,1H),7.59 (dd,J=8.1,4.5 Hz,1H),7.50 (d,J=2.2 Hz,1H),7.40 (d,J=2.3 Hz,1H),7.37(d,J=3.7 Hz,1H),4.28 (m,1H),3.58(s,3H),2.34 (t,J=8.0 Hz,1H),2.28 (dd,J=11.2,3.8 Hz,1H),2.16 (s,1H),2.01 (m,1H),1.86 (m,1H);13C NMR (126 MHz, DMSO)δ174.01,173.11,172.92,166.03,155.73,148.53,147.19,139.40,139.34,139.12,135.37,131.68,131.10,128.01,127.00,126.70,125.91,52.07,51.88,51.50,30.37,30.17,30.05;HRMS calcd for C23H20BrCl2N5O6[M-H]-609.990 1, found 609.990 2。
3-溴-N-(4-氯-2-甲基-6-(酪氨酸-2-基氨基甲酰基)苯基)-1-(3-氯吡啶-2-基)-1H-吡唑-5-羧酰胺(b):棕色固体,产率50%,熔点130~133 ℃;1H NMR (500 MHz, DMSO)δ10.61 (s,1H),9.26 (s,1H),8.46 (dd,J=4.7,1.4 Hz,1H),8.10 (m,2H),7.60 (m,1H),7.50 (s,1H),7.44 (d,J=2.0 Hz,1H),7.21 (d,J=1.6 Hz,1H),6.95 (d,J=8.2 Hz,2H),6.59 (d,J=8.4 Hz,2H),4.03 (m,1H),3.02 (dd,J=13.7,4.8 Hz,1H),2.84 (dd,J=13.5,7.4 Hz,1H),2.12 (s,3H);13C NMR (126 MHz, DMSO)δ174.24,165.49,156.12,155.91,148.70,147.44,139.69,139.41,135.74,131.86,131.40,130.51,128.91,128.21,127.35,127.00,125.84,115.20,111.21,55.86,49.02,36.60;HRMS calcd for C26H20BrCl2N5O5[M-H]-629.995 2, found 629.995 0。
3-溴-N-(4-氯-2-甲基-6-(3-羟基丁酸-2-基氨基甲酰基)苯基)-1-(3-氯吡啶-2-基)-1H-吡唑-5-羧酰胺(c):黄色固体,产率80%,熔点75~77 ℃;1H NMR (500 MHz, CDCl3)δ12.65(s,1H),10.25 (s,1H),8.48 (dd,J=4.7,1.5 Hz,1H),8.14 (dd,J=8.1,1.5 Hz,1H),8.03 (d,J=8.5 Hz,1H),7.60 (dd,J=8.1,4.7 Hz,1H),7.52 (m,1H),7.45 (d,J=2.3 Hz,1H),7.38 (d,J=5.4 Hz,1H),4.32 (m,1H),4.14 (m,1H),2.17 (s,3H),1.99 (s,1H),1.03 (d,J=6.4 Hz,3H);13C NMR (126 MHz, DMSO)δ171.88,166.05,155.80,148.50,147.17,139.35,139.25,135.76,131.73,131.47,131.29,127.99,126.92,126.70,125.96,110.89,66.62,58.43,40.43,20.47,17.80;HRMS calcd for C21H18BrCl2N5O5[M-H]-567.979 6, found 567.979 6。
3-溴-N-(4-氯-2-甲基-6-(谷氨酸-2-基氨基甲酰基)苯基)-1-(3-氯吡啶-2-基)-1H-吡唑-5-羧酰胺(d):黄色固体,产率85%,熔点125~128 ℃;1H NMR (500 MHz, CDCl3)δ12.37 (s,2H),10.29 (s,1H),8.58 (d,J=7.5 Hz,1H),8.48 (dd,J=4.7,1.5 Hz 1H),8.14 (dd,J=8.1,1.5 Hz,1H),7.59 (dd,J=8.1,4.7 Hz 1H),7.50 (m,1H),7.39 (d,J=2.6 Hz,2H),4.28 (m,1H),2.28 (m,2H),2.16 (s,3H),2.01 (m,1H),1.86 (m,1H);13C NMR (126 MHz, DMSO)δ173.98,173.08,172.22,165.99,155.71,150.09,148.53,147.16,139.38,139.32,139.11,135.39,131.65,131.08,128.00,126.97,126.68,125.91,110.82,51.99,30.36,26.10;HRMS calcd for C22H18BrCl2N5O6[M-H]-595.974 5, found 595.974 1。
3-溴-N-(4-氯-2-甲基-6-(丁酸-2-基氨基甲酰基)苯基)-1-(3-氯吡啶-2-基)-1H-吡唑-5-羧酰胺(e):白色固体,产率92%,熔点139~141 ℃;1H NMR (500 MHz, CDCl3)δ12.62 (s,1H),10.60 (s,1H),8.57 (d,J=7.5 Hz,1H),8.47 (dd,J=4.6,1.2 Hz,1H),8.14 (dd,J=8.0,1.2 Hz,1H),7.59 (m,2H),7.49 (d,J=2.1 Hz,1H),7.35 (d,J=2.3 Hz,1H),4.17 (m,1H),2.16 (s,3H),1.71 (m,2H), 0.83 (t,J=7.4 Hz,3H);13C NMR (126 MHz, DMSO)δ173.32,165.93,155.72,148.60,147.19,139.32,139.18,135.96,131.54,131.43,131.20,128.04,126.91,126.74,126.05,110.95,54.10,40.02,24.11,17.83,10.67;HRMS calcd for C21H18BrCl2N5O4[M-H]-595.974 5,found 595.974 1。
3-溴-N-(4-氯-2-甲基-6-(4-甲基戊酸-2-基氨基甲酰基)苯基)-1-(3-氯吡啶-2-基)-1H-吡唑-5-羧酰胺(f):白色固体,产率95%,熔点118~121 ℃;1H NMR (500 MHz, DMSO)δ12.63 (s,1H),10.23 (s,1H),8.49 (m,2H),8.15 (dd,J=8.1,1.5 Hz,1H),7.61 (dd,J=8.1,4.7 Hz,1H),7.51 (d,J=2.0 Hz,1H),7.35 (m,2H),4.32 (m,1H),2.17 (s,3H),1.58 (m,2H),1.48 (m,1H), 0.82 (d,J=6.2 Hz,3H), 0.77 (d,J=6.2 Hz,3H);13C NMR (126 MHz, CDCl3)δ175.76,168.36,158.19,149.26,146.58,139.43,138.95,138.43,135.04,133.16,132.47,130.22,129.36,128.25,125.74,124.90,111.46,51.53,40.01,39.89,24.97,22.98,21.41;HRMS calcd for C23H22BrCl2N5O4[M-H]-580.015 9,found 580.015 3。
3-溴-N-(4-氯-2-甲基-6-(甘氨酸-2-基氨基甲酰基)苯基)-1-(3-氯吡啶-2-基)-1H-吡唑-5-羧酰胺(g):白色固体,产率82%,熔点234~236 ℃;1H NMR (500 MHz, CDCl3)δ12.67 (s,1H),10.40 (s,1H),8.74 (t,J=5.8 Hz,1H),8.49 (dd,J=4.7,1.5 Hz,1H),8.16 (dd,J=8.1,1.5 Hz,1H),7.60 (dd,J=8.1,4.7 Hz,1H),7.50 (d,J=2.1 Hz,1H),7.45 (s,1H),7.39 (d,J=2.3 Hz,1H),3.83 (d,J=5.8 Hz,2H),2.16 (s,3H);13C NMR (126 MHz, DMSO)δ171.05,166.16,155.83,148.50,147.21,139.49,139.40,139.27,135.45,131.72,131.68,131.19,127.97,126.97,126.75,125.76,110.93,41.18,17.83;HRMS calcd for C19H14BrCl2N5O4[M-H]-523.953 3,found 523.953 3。
3-溴-N-(4-氯-2-甲基-6-(丙氨酸-2-基氨基甲酰基)苯基)-1-(3-氯吡啶-2-基)-1H-吡唑-5-羧酰胺(h):白色固体,产率93%,熔点126~128 ℃;1H NMR (500 MHz, DMSO)δ12.62(s,1H),10.46 (s,1H),8.64 (d,J=7.2 Hz,1H),8.49 (dd,J=4.7,1.5 Hz,1H),8.16 (dd,J=8.1,1.5 Hz,1H),7.61 (dd,J=8.1,4.7 Hz,1H),7.50 (m,2H),7.37 (d,J=2.4 Hz,1H),4.29 (m,1H),2.17 (s,3H),1.28 (d,J=7.3 Hz,3H);13C NMR (126 MHz, DMSO)δ174.00,165.62,155.78,148.60,147.23,139.39,139.38,139.11,135.72,131.61,131.52,131.20,128.09,126.99,126.79,125.95,110.92,48.16,17.84,16.96;HRMS calcd for C20H16BrCl2N5O4[M-H]-537.969 0,found 537.969 0。
3-溴-N-(4-氯-2-甲基-6-(3,3-二甲基丁酸-2-基氨基甲酰基)苯基)-1-(3-氯吡啶-2-基)-1H-吡唑-5-羧酰胺(i):白色固体,产率84%,熔点161~164 ℃;1H NMR (500 MHz, DMSO)δ10.56 (s,1H),8.48 (dd,J=4.7,1.5 Hz,1H),8.20 (d,J=8.5 Hz,1H),8.14 (dd,J=8.1,1.5 Hz,1H),7.60 (dd,J=8.1,4.7 Hz,1H),7.5 (m,2H),7.32 (d,J=2.3 Hz,1H),4.19 (d,J=8.3 Hz,1H),2.17 (s,3H), 0.94 (s,9H);13C NMR (126 MHz, DMSO)δ172.27,166.05,156.01,148.62,147.24,142.76,139.37,139.29,139.23,136.35,131.53,131.32,128.09,126.96,126.79,126.33,110.99,62.93,61.27,33.66,26.96,17.85;HRMS calcd for C23H22BrCl2N5O4[M-H]-580.015 9, found 580.015 7。
3-溴-N-(4-氯-2-甲基-6-(3-甲基丁酸-2-基氨基甲酰基)苯基)-1-(3-氯吡啶-2-基)-1H-吡唑-5-羧酰胺(j):红棕色固体,产率81%,熔点49~51 ℃;1H NMR (500 MHz, DMSO)δ10.57 (s,1H),8.48 (dd,J=4.7,1.4 Hz,1H),8.39 (d,J=8.1 Hz,1H),8.15 (dd,J=8.1,1.4 Hz,1H),7.60 (dd,J=8.1,4.7 Hz,1H),7.53 (s,1H),7.49 (d,J=2.2 Hz,1H),7.34 (d,J=2.3 Hz,1H),4.20 (m,1H),2.17 (s,3H),2.09 (m,1H), 0.87 (d,J=6.8 Hz,6H);13C NMR (126 MHz, DMSO)δ172.72,166.00,155.77,148.57,147.15,139.27,139.26,139.17,136.13,131.46,131.34,131.18,128.01,126.85,126.69,126.17,110.94,58.15,29.66,19.18,18.51,17.80;HRMS calcd for C22H20BrCl2N5O4[M-H]-566.000 3, found 566.000 3。
3-溴-N-(4-氯-2-甲基-6-(3-甲基戊酸-2-基氨基甲酰基)苯基)-1-(3-氯吡啶-2-基)-1H-吡唑-5-羧酰胺(k):棕褐色固体,产率90%,熔点68~72 ℃;1H NMR (500 MHz, DMSO)δ10.63 (s,1H),8.48 (dd,J=4.7,1.5 Hz,1H),8.39 (d,J=7.9 Hz,1H),8.15 (dd,J=8.1,1.5 Hz,1H),7.60 (dd,J=8.1,4.7 Hz,1H),7.56 (m,1H),7.49 (d,J=2.2 Hz,1H),7.33 (d,J=2.3 Hz,1H),4.21 (m,1H),2.16 (s,3H),1.83 (m,1H),1.40 (m,1H),1.14 (m,1H), 0.84 (d,J=6.8 Hz,3H), 0.79 (t,J=7.4 Hz,3H);13C NMR (126 MHz, DMSO)δ172.68,165.77,155.74,148.57,147.11,139.22,139.20,139.16,136.28,131.39,131.22,131.19,127.97,126.82,126.63,126.18,110.95,57.28,36.03,25.10,17.76,15.54,11.28;HRMS calcd for C23H22BrCl2N5O4[M-H]-580.015 9,found 580.015 6。
3-溴-N-(4-氯-2-甲基-6-(色氨酸-2-基氨基甲酰基)苯基)-1-(3-氯吡啶-2-基)-1H-吡唑-5-羧酰胺(l):白色固体,产率72%,熔点130~133 ℃;1H NMR (500 MHz, DMSO)δ12.72(s,1H),10.80 (d,J=1.8 Hz,1H),10.24 (s,1H),8.51 (d,J=7.5 Hz,1H),8.47 (dd,J=4.7,1.5 Hz,1H),8.11 (dd,J=8.1,1.5 Hz,1H),7.57 (m,2H),7.50 (m,1H),7.33 (m,3H),7.10 (dd,J=10.3,1.6 Hz,1H),7.07 (dd,J=8.0,1.0 Hz,1H),6.99 (m,1H),4.57(m,1H),3.23 (dd,J=14.6,5.6 Hz,1H),3.10 (dd,J=14.7,8.1 Hz,1H),2.15 (s,3H);13C NMR (126 MHz, DMSO)δ173.00,165.60,155.75,148.45,147.14,139.39,139.33,139.06,136.16,134.99,131.69,131.06,127.94,127.28,126.97,126.66,125.93,123.69,121.06,118.51,118.23,111.50,110.81,109.89,53.70,40.43,26.94,17.80;HRMS calcd for C28H21BrCl2N6O4[M-H]-653.011 2, found 653.011 1。
2.4 生物活性
所有目标化合物的测试工作均由浙江省化工研究院农药创制中心完成,如表1,2所示。测试结果表明:目标化合物对黏虫和苜蓿蚜均具有一定的杀虫活性,其中对黏虫的活性更好。在500 mg/L质量浓度下,除g以外的所有目标化合物对黏虫的杀虫活性均为100%,目标化合物f对苜蓿蚜的杀虫活性达到90%,化合物j,l对苜蓿蚜的杀虫活性为60%,但所有化合物对朱砂叶螨均没有表现出活性。当测试质量浓度为100 mg/L时,化合物b,f,j,k,l对黏虫的杀虫活性仍为100%,化合物c,e,h对黏虫的杀虫活性为90%,化合物a,d对黏虫的杀虫活性为80%,化合物i对黏虫的杀虫活性为70%。当测试质量浓度为20 mg/L时,化合物b对黏虫的杀虫活性为90%,化合物c,f,j对黏虫的杀虫活性达80%。当测试质量浓度降为4 mg/L时,化合物b对黏虫的杀虫活性为80%,化合物f对黏虫的杀虫活性为70%。
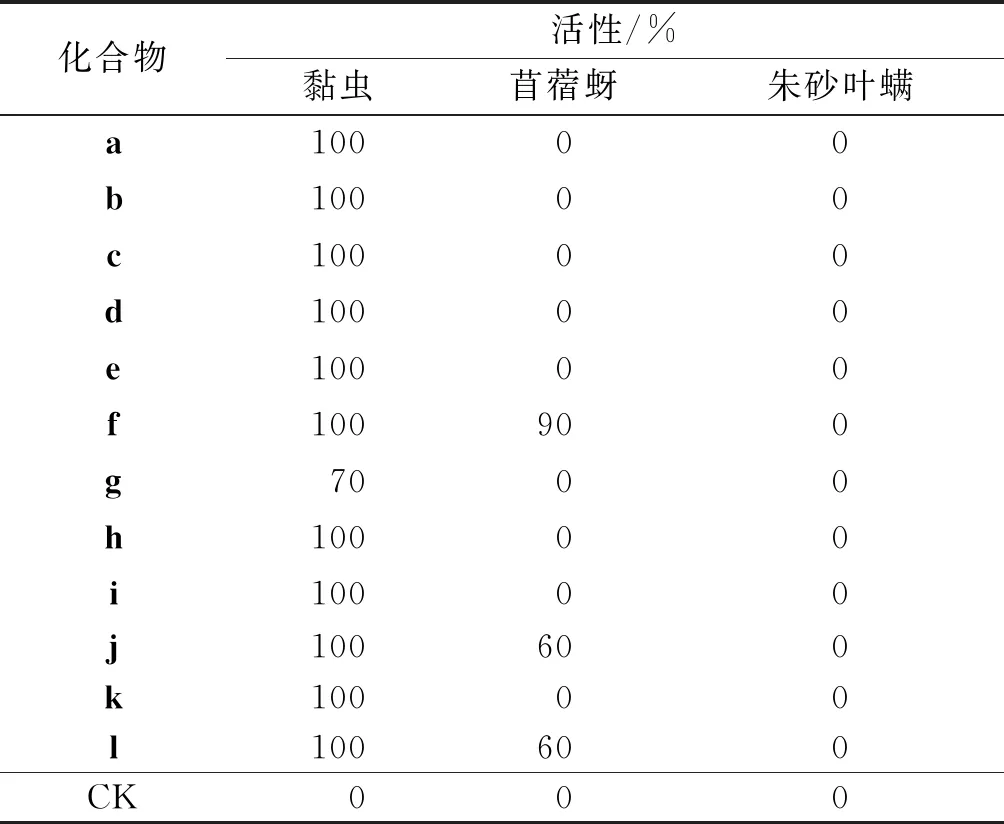
表1 目标化合物的杀虫活性(普筛)Table 1 Insecticidal activity of target compounds (general sieve)
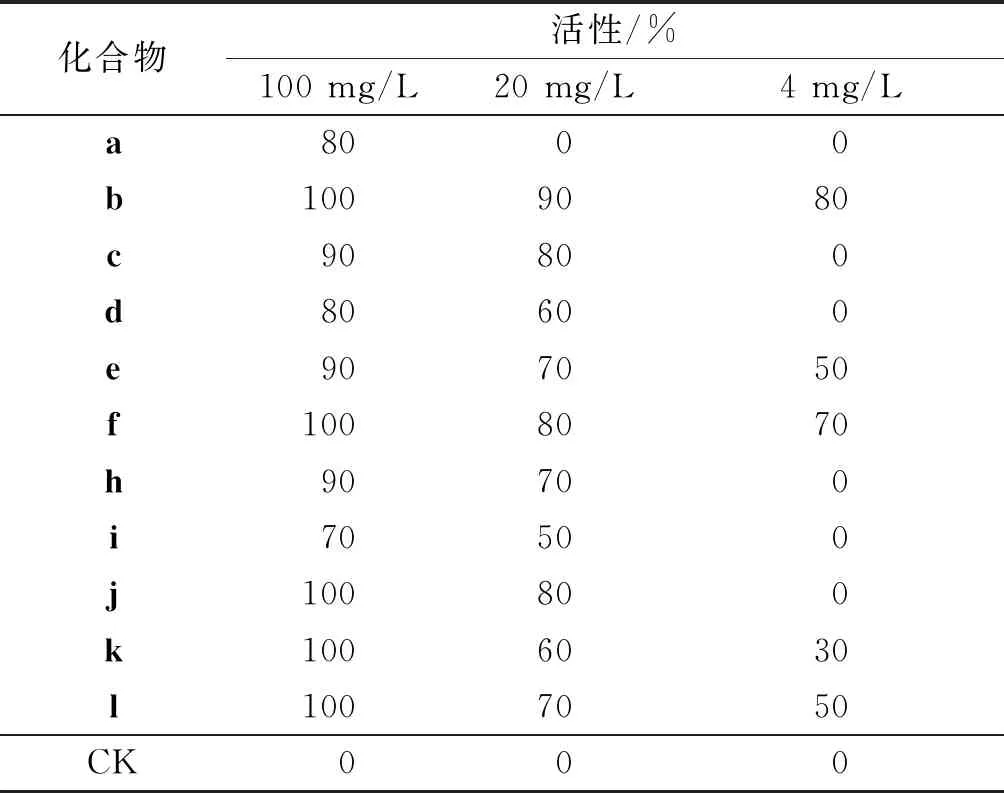
表2 目标化合物的杀虫活性(初筛)
初步的结构与活性关系分析发现:当引入的氨基酸碳链较长时,目标化合物的杀虫活性相对较好,表明目标化合物的杀虫活性与碳链的长短有一定关系,具体表现为:—CH2CH(CH3)2>—CH(CH3)2>—H。同时引入带有芳环的氨基酸比烷烃的杀虫活性相对较好,具体表现为目标化合物b(R=4-OH—PhCH2-)对黏虫的杀虫活性高于其他化合物,具有进一步研究的价值。
3 结 论
以氯虫苯甲酰胺为先导,通过引入氨基酸片段合成了12 个新化合物,初步的生物活性测试结果表明:在500 mg/L测试质量浓度下,多数目标化合物对黏虫有着较高的杀虫活性,其中化合物b在20,4 mg/L质量浓度下对黏虫分别有90%和80%的杀虫活性,化合物f在20,4 mg/L质量浓度下对黏虫分别有80%和70%的杀虫活性,需要对其进行结构优化,后续可进一步对具有氯虫苯甲酰胺抗性的害虫进行生物活性测试。
