肥厚型梗阻性心肌病外科治疗的疗效分析
2022-01-23陈奇童肖红艳宋来春
陈奇童,龚 臣,肖红艳,宋来春,陶 凉
(武汉科技大学附属武汉亚洲心脏病医院心脏外科,武汉 430022)
肥厚型梗阻性心肌病(hypertrophic obstructive cardiomyopathy,HOCM)在临床上是一种常见的常染色体显性遗传病,并且是青少年及运动员猝死的重要原因之一[1]。其临床症状差异较大,但主要表现为劳力性呼吸困难、胸痛,心慌、心悸,晕厥甚至心源性猝死(sudden cardiac death,SCD),因此,早诊断、早治疗对其预后至关重要。目前,外科手术仍然是治疗HOCM 的“金标准”[2]。本文回顾性分析武汉科技大学附属武汉亚洲心脏病医院84 例HOCM 患者行改良扩大Morrow 术后的临床资料,以探讨外科治疗肥厚型梗阻性心肌病的疗效。
1 资料与方法
1.1 一般资料
回顾性分析2016~2018年期间于武汉科技大学附属武汉亚洲心脏病医院行改良扩大Morrow 术的84例患者临床资料,年龄(51.05±11.93)岁,其中男性52例(61.90%)。入选标准:(1)静息状态下有症状且左心室流出道峰值压差(left ventricular outflow tract pressure gradient,LVOT-PG)>50 mmHg(1 mmHg=0.133 kPa),和无症状LVOT-PG>100 mmHg[3];(2)药物治疗下症状仍无法得到缓解者;(3)自愿选择行改良扩大Morrow 术治疗,并签署知情同意书。84 例HOCM 患者中,年龄为(51.05±11.93)岁,其中男性52(61.90%)例,体表面积(body surface area,BSA)为(1.67±0.16)kg/m2,心胸比值C/T 为(0.56±0.05)。症状表现为胸闷59 例(71.08%),黑矇或晕厥史17例(20.48%),心慌或心悸14例(16.87%),喘气12 例(14.46%),乏力4 例(4.82%)。合并原发性高血压(高血压)20 例(20.81%),冠状动脉粥样硬化性心脏病(冠心病)14 例(16.87%),糖尿病6 例(7.23%)。
1.2 手术方式
手术均由经验丰富的高年资医师完成,均采用改良扩大Morrow 手术方式(见图1),即在全身麻醉低温体外循环下进行,常规建立体外循环,通过右上肺静脉放左心引流。降温,阻断升主动脉,经根部灌注含血停搏液,心脏停搏满意。通过主动脉瓣口切除肥厚的室间隔左心室面心肌组织。切除范围:自主动脉右冠瓣瓣环下方3 mm 左右,开始切除,保护主动脉瓣;切除膜部室间隔的后方以左约5 mm 至二尖瓣前交界之间的肥厚心肌组织,主要保护膜部,特别是膜部后下方,以免房室传导阻滞的发生;纵向切除范围至心尖延伸至、并超越左心室流出道梗阻的部位后达到二尖瓣乳头肌腱索和肌束,如术中发现二尖瓣乳头肌黏连挛缩则同时行乳头肌松解术;术前充分评估影像学参数,术中切除范围的厚度尽可能控制在室间隔厚度的50%,宽度为35 mm,长度为50~70 mm。切除心尖部室间隔肌肉时,心脏后以纱布垫抬高,心脏外压迫右心室流出道便于流出道显露;将左心室前壁推向右侧有助于心尖部分室间隔的显露,多方位暴露,以便流出道梗阻有效解除。术前、术中均常规经胸超声心动图,如提示疏通效果不满意,则二次转机。术前检查提示合并有其他心脏疾病,则同期行复合手术治疗。本组同期合并处理其他类型心脏手术共30 例(35.71%),其中二尖瓣置换术(mitral valve replacement,MVR)7 例,二尖瓣成形术(mitral valvuloplasty,MVP)11 例,三尖瓣成形(tricuspid valvuloplasty,TVP)3 例,主动脉瓣置换术(aortic valve replacement,AVR)2 例,主动脉瓣成形(aortic valvuloplasty,AVP)3 例,卵圆孔修补术1例,经胸心脏射频改良迷宫术(MAZE)2 例,行右心房粘液瘤切除术1 例。

图1 改良扩大Morrow 手术视野过程(白色箭头所示为被切除的肥厚的室间隔肌肉)
1.3 统计学分析
数据应用SPSS 25.0 统计分析。计量资料用()表示;计量资料先判断是否符合正态分布,若符合则用t检验,不符合则用Wilcoxon符号秩和检验。计数资料以频数(率)表示,用卡方检验。以P<0.05 为差异有统计学意义。

图2 手术示意图
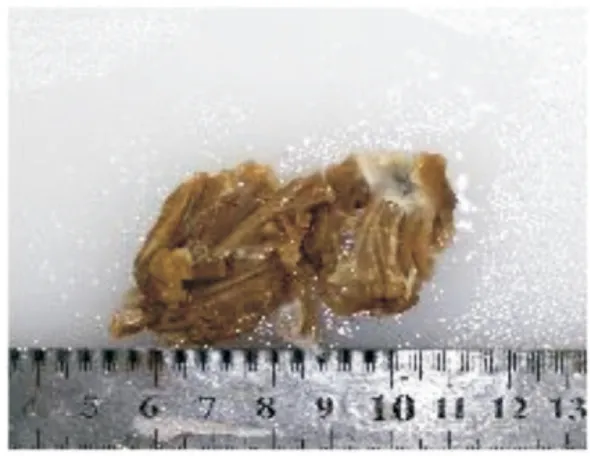
图3 切下的室间隔肌肉标本

图4 术后病理切片所见[心内膜轻度纤维化增厚,心肌细胞肥大,排列走向不规则,间质中度纤维化(HE 染色:10×10)]
2 结果
2.1 患者的治疗效果
2 例患者术后早期死于多器官衰竭,其余患者均康复出院。术中主动脉阻断时间为(49.73±22.74)min;体外循环时间为(103.39±39.98)min;术后住重症监护室(ICU)时间为(158.24±42.60)h;术后住院时间为(12.24±2.62)d。收集术前、术后一周复查超声心动图参数并进行对比(见表1)。由于流出道梗阻的解除,左心室前负荷减小,术后左心房内径、室间隔厚度及峰值压差均有减小(P<0.05),流出道的宽度增大(P<0.05),同时收缩期前向运动征明显较少(P<0.05)。HOCM 患者心肌收缩能力通常未受影响,因此左心室射血分数变化差异无明显变化(P>0.05)。心功能情况较术前明显好转(P<0.05)(见表2)。
表1 84 例患者手术前后经胸超声心动图参数结果对比[]

表1 84 例患者手术前后经胸超声心动图参数结果对比[]
注:LA=左心房;IVS=室间隔;LVOT=左心室流出道;EF=射血分数

表2 手术前后心功能分级对比(n)
2.2 患者随访情况
所有患者由专业人员定期电话随访,时间跨度为6~36 个月。大部分患者胸痛、胸闷等不适消失,心功能分级(NYHA)为Ⅰ~Ⅱ级,其余部分患者轻微症状,但可耐受或服用药物即可改善。
3 讨论
对于HOCM 治疗主要取决于左心室流出道压力,流出道的压差是发生心源性猝死(sudden car⁃diac death,SCD)风险的一个重要预后因素[5],当压差≥30 mmHg 时即可对血流动力学产生影响,SCD 风险相应增加2.4 倍[6-7]。国外曾报道采用左心室流出道疏通术后,流出道压力即可减小,通过远期随访发现患者的症状明显改善,生活质量得到提高,晕厥或猝死等不良事件明显下降,而未行手术治疗的HOCM 患者年病死率可达1%~4%[8]。回顾性分析报道证实,手术干预可提高患者生活质量[9],改善预后,本中心报道与其一致。但对于HOCM 而言,手术只解决室间隔段肥厚区域,改善流出道压差,缓解左心室前负荷,减少不良事件的发生,但心脏其他部位肥厚心肌仍存在,心脏仍然面临着缺血的局面,术后长期药物治疗仍是基石。
由于传导束经过室间隔后分支至左、右心室,心律失常仍然是术后最常见的并发症,国内有报道Morrow 术后Ⅲ度房室传导阻滞的发生率可达7.4%[10]。本组术后各种心率失常类型:房性期前收缩38 例,心房颤动15 例,室内阻滞18 例,预激综合征2 例,Ⅱ度Ⅰ型房室传导阻滞1 例。本组中2 例患者曾因晕厥于外院植入过植入式心脏复律除颤器(implantable cardioverter-defibrillators,ICD),目前普遍认为ICD 能有效减少各种恶性心律失常事件的发生,是预防HCM 患者心源性猝死的有效手段之一[2,11]。Morrow 术后死亡的主要原因包括各种严重心律失常、心力衰竭等。本次研究有2 例(2.38%)由于多器官衰竭而死亡,远低于之前报道单纯的室间隔心肌切除术的死亡率(约4%)。
HOCM 患者常常合并其他心脏疾病,因大部分存在二尖瓣解剖结构异常[12-13],二尖瓣关闭不全者占大多数,本组患者中合并二尖瓣轻-中度关闭不全有48/84 例(57.14%),与报道结果一致。术前超声心动图提示存在二尖瓣轻-中度反流者,术后经胸超声心动图提示二尖瓣反流情况明显改善,且大部分不需额外处理二尖瓣[14],而同期需处理的多数合并二尖瓣自身病变,包括感染性内膜炎、退行性瓣膜病和乳头肌或腱索结构变异等[15-16]。Minami 等[17]报道行左心室流出道疏通术同期行其他心脏手术并不影响患者远期预后。既往单纯Morrow 术后患者仍然发现有二尖瓣前叶移位,直接导致二尖瓣的关闭不全甚至加重左心室流出道梗阻现象[15],因此改良扩大的Morrow 术在切除室间隔肥厚心肌同时需对异常的乳头肌等结构进行松解、恢复,将整个左心室流出道结构范围重建延伸至心尖[18-19],以便获得更好的手术效果。
综上,通过本中心回顾性分析,对于药物难治性HOCM,改良扩大Morrow 术仍是首要选择,术后即可解除左心室流出道梗阻现象,临床症状及预后得到改善,如同时合并冠状动脉狭窄、瓣膜疾病等,同期一并处理则获益最大。
