绿色合成载银壳聚糖及其等温线、动力学及抑菌性
2022-01-14王祖华杨瑞先陈华军
王祖华,刘 萍,杨瑞先,陈华军
(洛阳理工学院环境工程与化学学院,洛阳 471023)
0 引 言
腐败菌和致病菌广泛存在于人们的日常生活中,它严重影响着人类的健康,为了防治有害微生物,人类研究出各种各样的抗菌剂。随着抗性菌株和超级细菌的出现,人类面临的健康安全问题更加严峻。因此,制备出广谱、高效、生物安全且无耐药性的抗菌剂非常重要。
壳聚糖是一种天然高分子化合物,是天然生物抑菌剂的典型代表。它由甲壳素脱乙酰基所得,具有活性氨基和羟基,因此壳聚糖具有可降解性、生物相容性、成膜性和安全无毒等良好的生物学特性[1-3],已应用在美容[4-6]、医药、食品、纺织等多领域中[7-11]。但由于其抑菌有效时间不长,耐热性不足,导致其应用范围受到了极大限制。而在有机材料壳聚糖中引入具有抑菌作用的金属离子可弥补其耐热性能不足和易洗脱的缺陷[12]。银离子作为抗菌金属离子具有广谱抗菌性,杀菌效果好,且不易使微生物产生抗药性。当银离子从抗菌剂中释放后,它可以迅速与菌株蛋白酶上的巯基结合,使蛋白酶失活从而起到杀菌作用[13],且银离子不会对活的哺乳动物细胞产生不利的影响[14]。但是由于银离子易迁移至皮肤造成重金属中毒,通常不能单独使用,利用它与其他材料结合、固载,从而发挥其抑菌作用,蔡波等[15]通过自由基接枝共聚法制备出改性壳聚糖,后经原位法合成壳聚糖基纳米银复合材料,该材料的抑菌性能良好。安静等[16]采用微波辐射法和香草醛还原,制备载银壳聚糖接枝香草醛复合胶乳,在紫外光下对大肠杆菌和枯草杆菌的抗菌效果要优于可见光下的抗菌效果。可见,利用壳聚糖和银离子所具有的不同特性,将银与壳聚糖结合,既能增强壳聚糖的稳定性,二者又能协同抑菌,提高复合材料的抑菌效果,这种复合抑菌剂逐渐引起了人们的重视,现已被用于各种不同的材料中,如医用敷料、涂布液等[17-19]。然而,采用绿色化学工艺制备载银壳聚糖,鲜有报道。
本研究通过绿色吸附法制备载银壳聚糖,采用X射线衍射(XRD)、场发射扫描电子显微镜(SEM)和热重分析(TG)分析其微观结构和热稳定性,以大肠杆菌和金黄色葡萄球菌作为试验指示菌种,测定最大银含量的载银壳聚糖的抗菌性能,并确定其最小抑菌浓度(MIC)。
1 实 验
1.1 材 料
壳聚糖(纯度99.99%)、硝酸银(纯度99.99%)购自上海阿拉丁生化科技股份有限公司。硫氰酸铵(NH4SCN,纯度99.99%)、十二水硫酸亚铁铵[NH4Fe(SO4)2,纯度99.99%]购自天津科邦化学试剂有限公司。所有试剂均为分析纯,实验用水均为去离子水。指示菌株为大肠杆菌(Escherichiacoli[ATCC 25922]),金黄色葡萄球菌(Staphylococcusaureus[ATCC 25923])
1.2 吸附等温线和动力学研究
将准确称取的1.500 0 g壳聚糖放于锥形瓶中,并加入50 mL已知浓度的pH=7的硝酸银水溶液。当吸附温度为298 K时,硝酸银水溶液的浓度会随吸附时间发生变化。混合物在25 ℃,150 r/min条件下振荡约300 min,离心分离壳聚糖,以硫酸铁铵为指示剂,用佛尔哈德法测定滤液中硝酸银的浓度,用公式(1)计算壳聚糖的吸附容量。
(1)
式中:qe为平衡吸附量(mg/g);c0为硝酸银的初浓度(mg/L);ce为硝酸银的平衡浓度(mg/L);V为硝酸银溶液的体积(L);m为壳聚糖的质量(g)。相同条件下重复所有实验并计算平均值。通过硝酸银溶液初始浓度的变化研究其对壳聚糖吸附容量的影响和达到吸附平衡时所需要的时间,并且研究硝酸银对壳聚糖的吸附动力学。
1.3 载银壳聚糖材料表征
采用X射线衍射仪(D8 Focus型X射线衍射仪,德国布鲁克公司,扫描步长0.02°,扫描范围2θ=10°~70°,持续时间0.5 s)和热重分析仪(日本津岛DTG-60H)测定载银壳聚糖的组分与热重,并运用EVA软件(布鲁克公司)中的国际衍射数据中心(ICDD)分析所获得的衍射图谱。用场发射扫描电子显微镜(FE-SEM,Sigma HD 德国蔡司)观测载银壳聚糖的微观结构。
1.4 抗菌活性试验
用革兰氏阴性菌(大肠杆菌)和革兰氏阳性菌(金黄色葡萄球菌)对吸附量最大的载银壳聚糖进行抗菌活性评价。最小抑菌浓度(MIC)的测定采用液体稀释法。在培养基中加入载银壳聚糖,使其浓度分别为50 μg/mL、60 μg/mL、70 μg/mL、80 μg/mL,在另外的培养基中加入壳聚糖,使其浓度为110 μg/mL,倒平板前使其均匀分散,以未添加二者的平板为空白对照。将指示菌株过夜培养,并稀释为10-5、10-6、10-7,分别取100 μL稀释菌液涂平板,37 ℃过夜培养。不同稀释度下不同样品重复三次。对培养后的菌落数进行计数,计算抑菌率C。
C=(A-B)/A×100%
(2)
式中:A为对照菌落数;B为样品菌落数。
2 结果与讨论
2.1 X射线衍射分析
有研究表明壳聚糖的晶体形态有两种,分别为Form Ⅰ(2θ≈10°)和Form Ⅱ(2θ≈20°)[20]。通过载银壳聚糖和壳聚糖的XRD图谱(见图1)可以看出在2θ=20.15°中出现的衍射峰对应的是晶体形态Ⅱ。壳聚糖分子间和分子内的氢键以及空间结构的规整性都有利于结晶性的增加,而银离子的引入使壳聚糖在20.15°衍射峰的相对强度明显减弱,减弱的原因在于壳聚糖中氨基基团与银配位后,使分子内结晶区减少从而降低了壳聚糖的结晶度[20]。
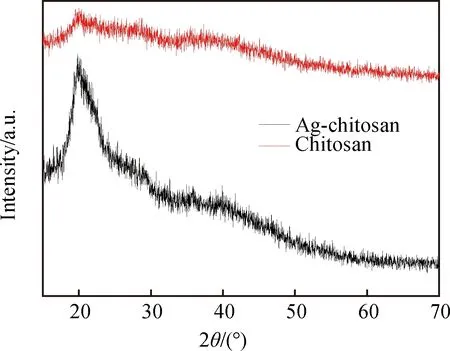
图1 壳聚糖和载银壳聚糖的XRD图谱Fig.1 XRD patterns of chitosan and Ag-chitosan
2.2 FESEM分析
分别用场扫描电镜(FESEM)和能量抑制能谱仪(EDS)对壳聚糖和载银壳聚糖的微观形貌和化学成分进行分析。壳聚糖吸附银离子后,壳聚糖的颗粒形貌并没有发生变化(见图2(a)、2(b))。EDS能谱仪分析表明,壳聚糖所吸附的银离子在壳聚糖分子中的分布并非对称均匀的。壳聚糖的外部元素组成包括碳、氮、氢、氧(见图2(c)),载银壳聚糖的外部元素由碳、氮、氢、氧和银组成(见图2(d))。通过对EDS的点分析(见图3)进一步验证了载银壳聚糖的外部元素组成,包括碳、氮、氢、氧和银。此外,由表1可以看出载银壳聚糖的化学元素(碳、氮、氢、氧)成分比例与壳聚糖一致,说明载银壳聚糖的制备并不改变壳聚糖本身的生物性能及其他理化性质。

图2 壳聚糖和壳聚糖的FESEM照片和EDS分析。(a)壳聚糖的FESEM照片;(b)载银壳聚糖的FESEM照片;(c)壳聚糖的EDS表面分析;(d)载银壳聚糖的EDS表面分析Fig.2 FESEM images and EDS analysis of chitosan and Ag-chitosan.(a)FESEM image of chitosan;(b)FESEM image of Ag-chitosan;(c)EDS surface analysis of chitosan;(d)EDS surface analysis of Ag-chitosan
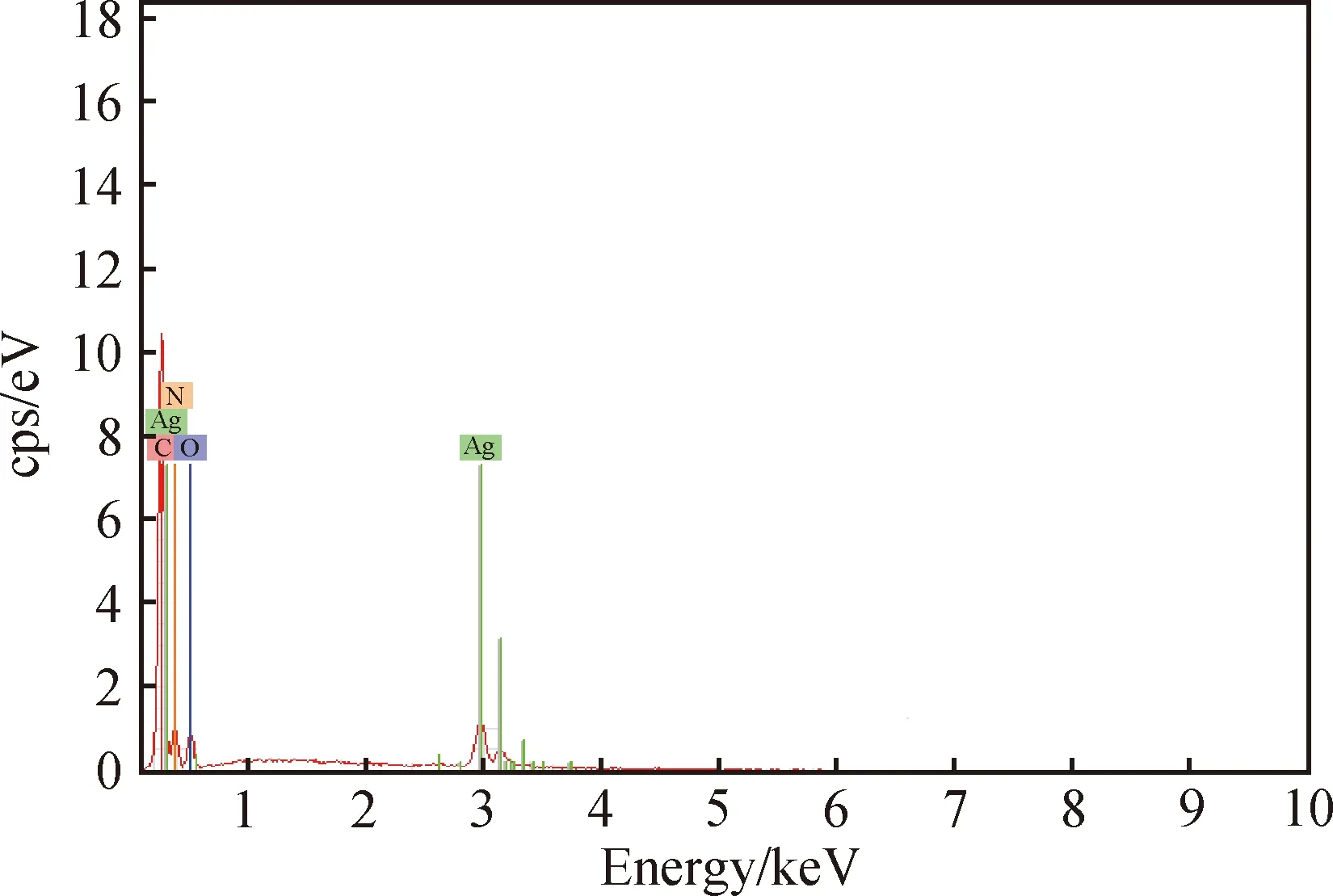
图3 载银壳聚糖的EDS谱图Fig.3 EDS spectrum of Ag-chitosan
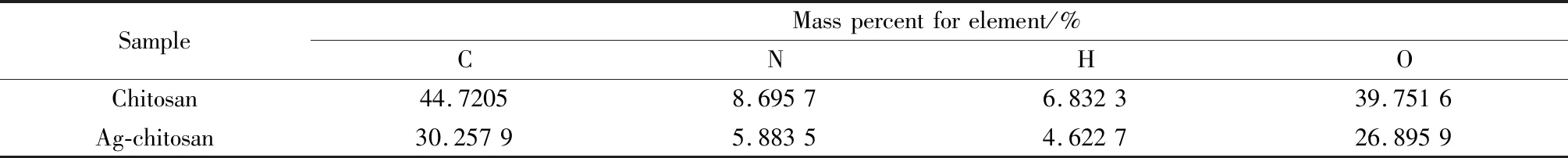
表1 载银壳聚糖与壳聚糖中各元素的含量Table 1 Concentration for elements in Ag-chitosan and chitosan
2.3 TG-DTA分析
通过载银壳聚糖和壳聚糖的TG-DTA曲线(见图4)可以看出,载银壳聚糖的热降解温度稍高于壳聚糖。将取代基引入多糖结构会一定程度地破坏壳聚糖的晶体结构,在热降解范围内载银壳聚糖的TG曲线中出现了快速失重过程。这表明银离子与分子内的氧或氮配位后使载银壳聚糖的热性能更稳定,从而使载银壳聚糖相对于壳聚糖的热稳定性有一定的提高。

图4 壳聚糖和载银壳聚糖的TG曲线Fig.4 TG curves of chitosan and Ag-chitosan
2.4 等温线和吸附机理分析
通过调整硝酸银的浓度,研究其初始浓度对壳聚糖吸附性能的影响。将壳聚糖(30 g/L)和硝酸银(其浓度范围在6~26 g/L)混合均匀,25 ℃、150 r/min振荡约300 min,结果如图5所示。从图5可以看出:硝酸银初始浓度为6 g/L到18 g/L时,在达到平衡时硝酸银的吸附量增加较为明显;当硝酸银初始浓度大于18 g/L时吸附量的增加较为缓慢。
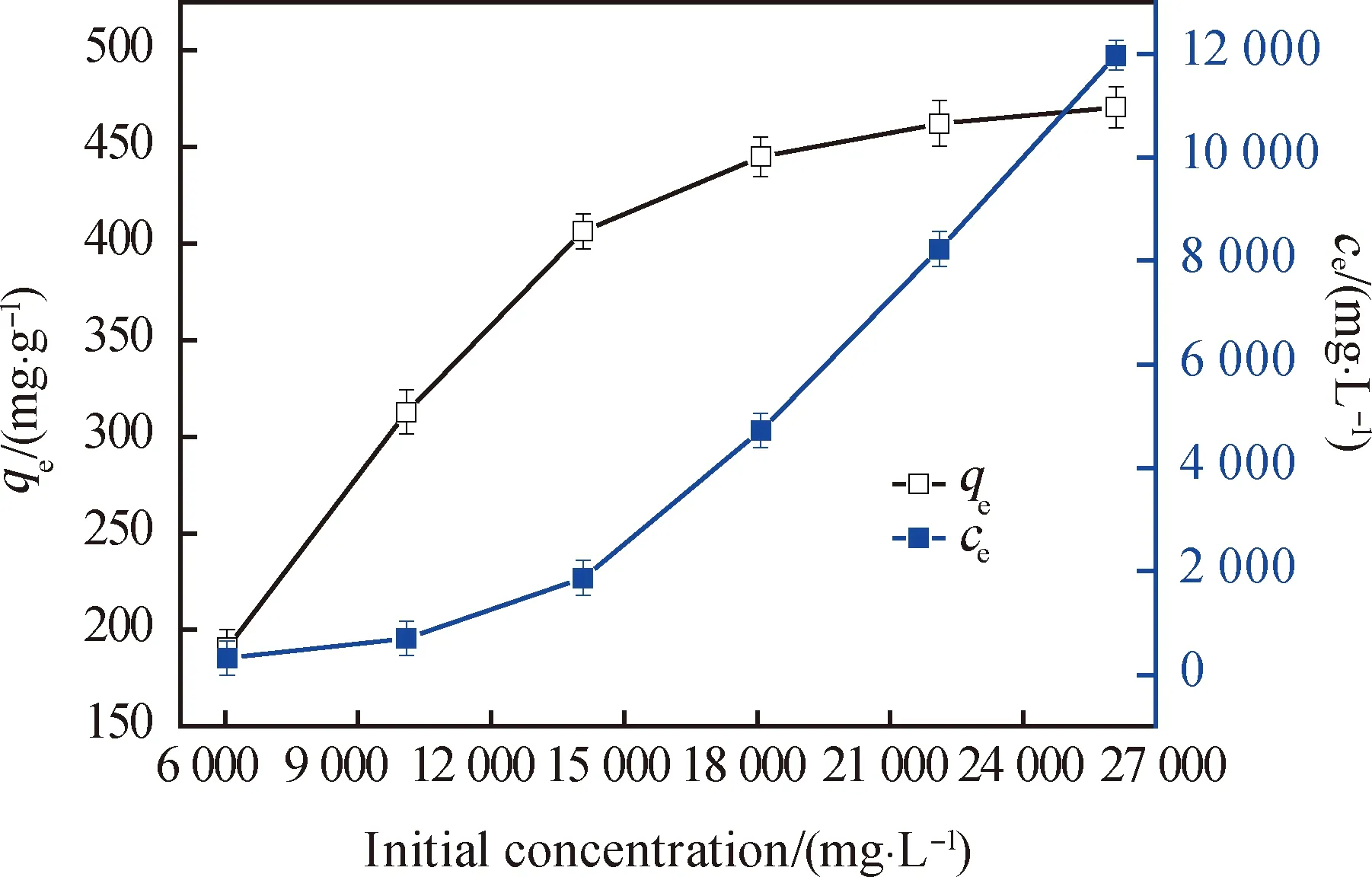
图5 硝酸银浓度对吸附量和硝酸银残留浓度的影响Fig.5 Influence of silver nitrate concentration on adsorption quantity and residual concentration of silver nitrate
用于吸附系统的平衡建模模型:Langmuir模型(3)和Dubinin-Radushkevich模型(4)。
(3)
(4)
式中:qe为平衡吸附量(mg/g);ce为平衡浓度(mL/L);qm为饱和吸附量(mg/g);b为吸附常数;R为气体常数(8.314 kJ/mol·K);T为温度(K);BD为每摩尔硝酸银吸附到壳聚糖表面所需最大的吸附能。公式(4)的线性形式如下:
(5)
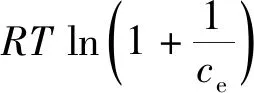
(6)
Langmuir模型的吸附等温线如图6(a)所示,结果表明壳聚糖对硝酸银的吸附等温线与Langmuir方程相一致,说明壳聚糖对硝酸银的吸附原理为单层吸附。由公式(3)可得,其饱和吸附量为469.48 mg/g,表明壳聚糖容易吸附硝酸银,比蒋卫娟等[21]研究的载银壳聚糖微球中256 mg/g的银含量高出近1倍。在图6(b)中壳聚糖对硝酸银的吸附等温线也与Dubinin-Radushkevich模型的线性图相一致,E被估计为16.61 kJ/mol,说明壳聚糖对硝酸银的吸附为化学吸附。根据公式(5)可知其饱和吸附量为478.09 mg/g,含银量为32.34%,与公式(3)的计算结果较一致。吸附机理如图7所示。
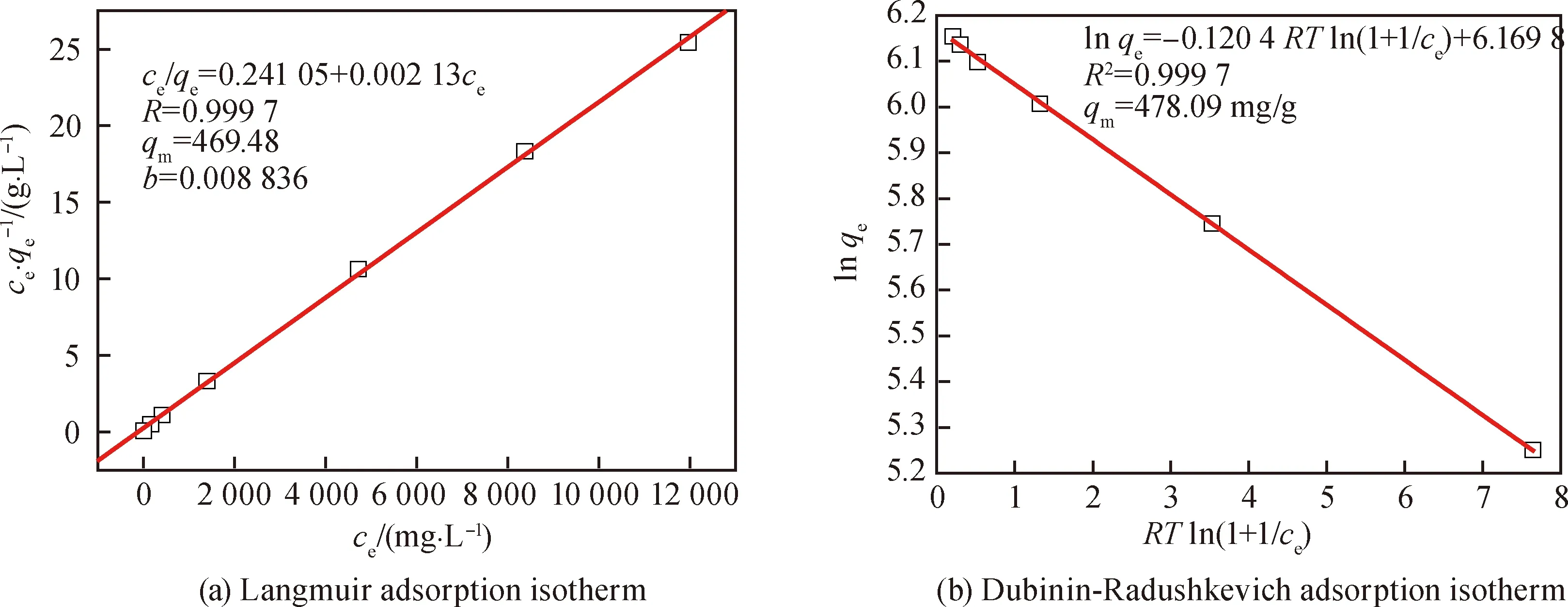
图6 壳聚糖吸附银离子的(a)Langmuir和(b)Dubinin-Radushkevich模型Fig.6 (a)Langmuir and (b)Dubinin-Radushkevich adsorption isotherms of Ag-chitosan

图7 壳聚糖对硝酸银的吸附机理Fig.7 Adsorption mechanisms of silver nitrate on chitosan
2.5 吸附动力学分析
当硝酸银浓度为12 000 mg/L,壳聚糖的含量为1.500 0 g/L时,壳聚糖吸附银离子的量随时间的不同而变化,其结果如图8所示。由图可以看出,在开始100 min内处于快速吸附阶段,之后吸附速率逐渐趋于平缓。
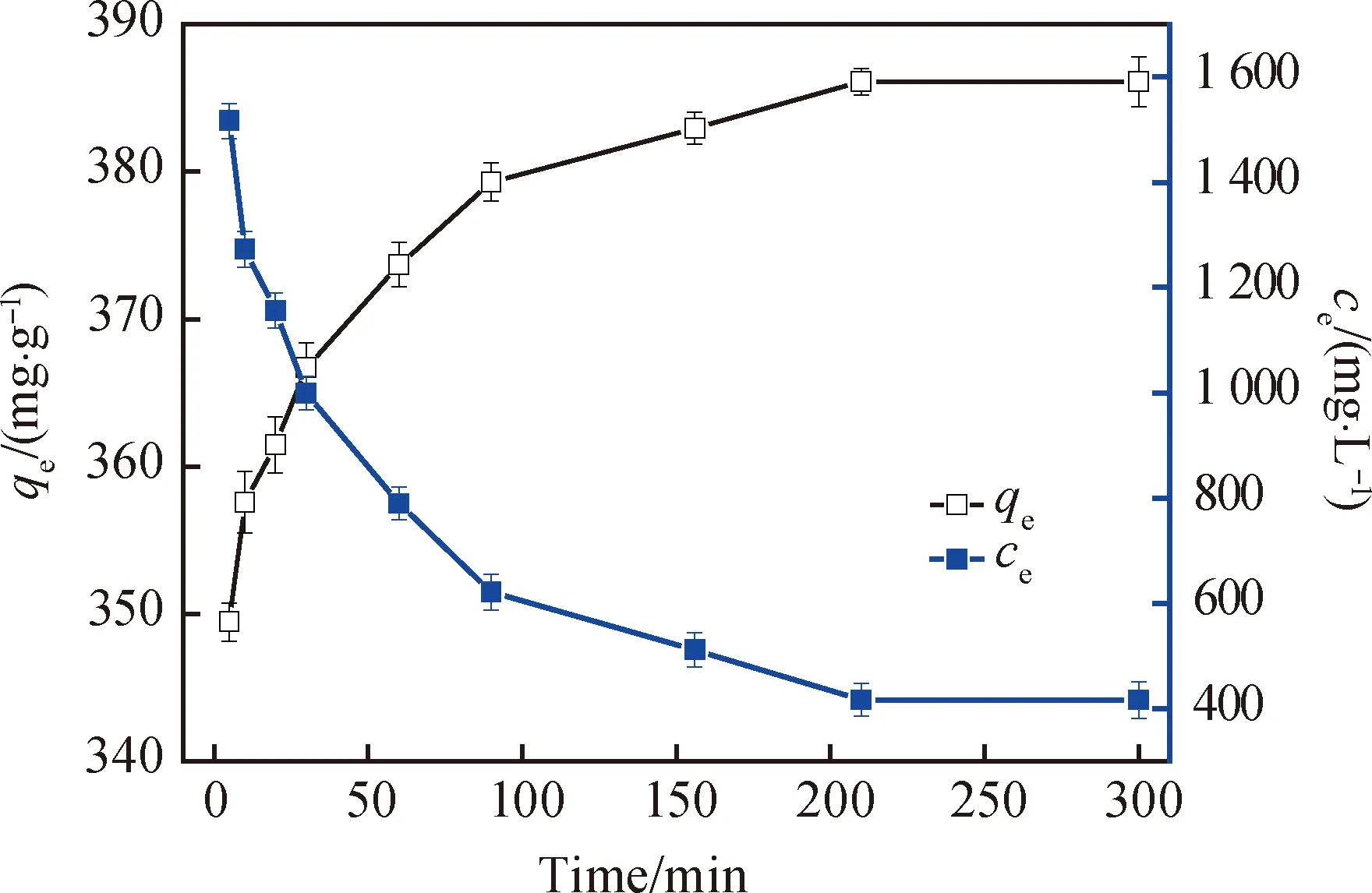
图8 吸附时间对壳聚糖银离子吸附量和硝酸银残留浓度的影响Fig.8 Influence of adsorption time on adsorption quantity of Ag+ ions on chitosan and residual concentration of silver nitrate
本文采用了颗粒内扩散方程(7)、准一级吸附动力学方程(8)、准二级吸附动力学方程(9)、修正伪一级动力学方程(10)、二级动力学方程(11)和二阶反应模型方程(12)来描述吸附过程。
qt=k·t0.5
(7)
ln(qm-qt)=lnqm-k1t
(8)
(9)
(10)
(11)
(12)

由图9可以看出,壳聚糖吸附硝酸银的动力学过程与准二级吸附过程密切相关。准二级吸附动力学模型是基于吸附速率受化学吸附控制的假设。通过动力学分析,表明化学吸附控制吸附过程,并与Dubinin-Radushkevich模型的分析结论一致。
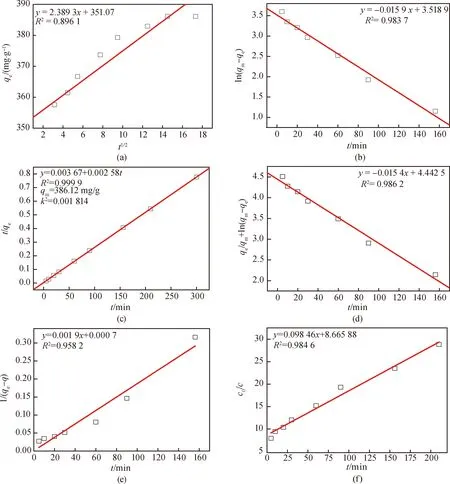
图9 壳聚糖对硝酸银的吸附动力学。(a)颗粒内扩散方程;(b)准一级吸附动力学方程;(c)准二级吸附动力学方程;(d)修正伪一级动力学方程;(e)二级动力学方程;(f)二阶反应模型方程Fig.9 Adsorption kinetic of silver nitrate by chitosan.(a)Intraparticle diffusion equation;(b)pseudo-first-order rate constant of adsorption equation;(c)pseudo-second-order kinetics equation;(d)modified pseudo-first-order equation; (e)second-order kinetics equation;(f)second-order reaction model equation
2.6 抗菌活性分析
大肠杆菌和金黄色葡萄球菌是最常见的导致院内感染和术后伤口感染的生物。抗菌试验结果表明,载银壳聚糖对大肠杆菌和金黄色葡萄球菌均有明显的抑制作用。通过图10可以看出添加壳聚糖的培养基中细菌菌落的数量明显减少(见图10(b)、(e))。对照组的大肠杆菌和黄金葡萄球菌初始数量浓度分别为5.68×107cfu/mL(见图10(a))和6.50×107cfu/mL(见图10(d)),而在添加载银壳聚糖的培养基中细菌菌落数基本为零(见图10(c)、图10(f))。

图10 壳聚糖、载银壳聚糖对大肠杆菌和金黄色葡萄球菌的抗菌活性。(a)对大肠杆菌的空白对照;(b)壳聚糖对大肠杆菌的抗菌活性;(c)载银壳聚糖对大肠杆菌的抗菌活性;(d)对金黄色葡萄球菌的空白对照;(e)壳聚糖对金黄色葡萄球菌的抗菌活性;(f)含载银壳聚糖对金黄色葡萄球菌的抗菌活性Fig.10 Antibacterial activity of chitosan and Ag-chitosan against Escherichia coli and Staphylococcus aureus. (a)Blank at Escherichia coli;(b)chitosan at Escherichia coli;(c)Ag-chitosan at Escherichia coli;(d)blank at Staphylococcus aureus;(e)chitosan at Staphylococcus aureus;(f)Ag-chitosan at Staphylococcus aureus
采用活细胞计数法测定了壳聚糖和载银壳聚糖对大肠杆菌和金黄色葡萄球菌的抗菌活性。由图11可知,载银壳聚糖添加量为50 μg/mL时对两种菌的抑菌率达到了60%以上,当添加量为80 μg/mL时其抑菌率均为99%以上,随着载银壳聚糖的含量的增加,对两种菌的抑菌率也不断上升,而壳聚糖添加量为110 μg/mL时其抑菌率只有40%左右,其抑菌率明显低于载银壳聚糖。由此表明,银离子的加入极大地增强了壳聚糖的抑菌性,即载银壳聚糖的抗菌性明显优于壳聚糖。此外,还可以看出载银壳聚糖对两种菌的抑制并没有明显的差异性,说明载银壳聚糖抑制细菌并没有选择性,并且浓度为80 μg/mL时对两种细菌的抑菌率均达到了99%以上,说明其最小抑菌浓度为80 μg/mL。与牛梅等[22]研究的载银壳聚糖复合物对大肠杆菌和金黄色葡萄球菌的最小抑菌浓度相比降低4倍左右。
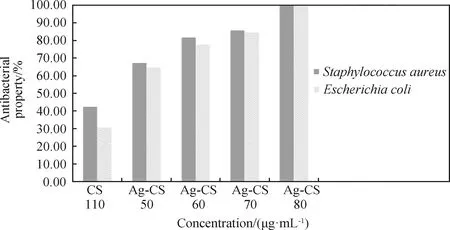
图11 载银壳聚糖和壳聚糖对大肠杆菌和金黄色葡萄球菌的抑菌效果Fig.11 Antibacterial effect of Ag-chitosan and chitosan against Escherichia coli and Staphylococcus aureus
在银离子和壳聚糖结合的情况下,产生抑菌的机制有两个方面:一是壳聚糖的抗菌活性是基于多阳离子(protonated氨基基团)与带负电的细菌表面相互作用,导致细胞膜通透性丧失、细胞液渗漏,最终使细胞死亡[23-24]。另一方面,银离子具有较强的抗菌性能,由于银离子附着在细胞壁上,干扰了细胞壁的渗透性和细胞的呼吸作用[25-26]。
3 结 论
本研究以壳聚糖为载体用绿色的方法成功合成了银含量为32.34%的载银壳聚糖。由于银离子的引入,破坏了壳聚糖的晶体结构,提高了载银壳聚糖的热稳定性和抗菌性质。壳聚糖对硝酸银的吸附等温线符合Langmiur和Dubinin-Radushkevich方程,表明吸附机制是单层和化学吸附。在琼脂平板内壳聚糖表面银离子的单层吸附有利于银离子释放,更易破坏细菌的细胞膜。通过Langmiur方程计算qm的结果为478.09 mg/g,与运用Dubinin-Radushkevich方程计算的结果相对一致,载银壳聚糖中银离子的最大含量为32.34%。其抗菌试验结果表明随着载银壳聚糖的增加,对两种菌的抑菌率也不断上升,当载银壳聚糖含量达到80 μg/mL时其抑菌率达到99%以上,而对照纯壳聚糖含量为110 μg/mL时其抑菌率只有40%左右,因此载银壳聚糖对大肠杆菌和金黄色葡萄球菌具有良好的抗菌性能,其最小抑菌浓度80 μg/mL。
