高压氧治疗一氧化碳中毒迟发脑病的疗效分析及其机制研究
2022-01-13万琛宜黄招君杨乐
万琛宜,黄招君,杨乐
(南昌大学第一附属医院 神经内科,江西 南昌330006)
碳物质燃烧时会生成无色、无臭、无刺激性气体一氧化碳CO,其吸入人体后易引起中毒并对大脑造成损伤,从而导致头晕、恶心、全身无力、昏迷。虽然治疗后上述症状发生好转,但有研究表明,0.2%~47.0%患者在经历2~60 d 的“假愈期”后会出现失语、认知障碍、急性痴呆等症状,这一系列综合表现被称作CO 中毒迟发性脑病(delayed encephalopathy after CO poisoning, DEACMP)[1]。DEACMP 的发病机制被认为是CO 由呼吸道进入人体后与血红蛋白发生反应,生成碳氧血红蛋白(carbonyl hemoglobin, CoHb),从而导致机体缺氧,给人体中枢神经系统带来严重影响。
高压氧治疗CO 中毒是国内外推荐的方法之一,虽然频率、疗程尚无统一标准,但应用较广泛,但是高压氧治疗DEACMP 的疗效是非确定性的[2]。信号通路作为一种细胞发生某种反应的传递信息,近年来在多种疾病中报道,可能有助于研究高压氧治疗DEACMP 的发生机制[3]。本研究对90 例DEACMP 患者进行临床调查,探讨高压氧对DEACMP 患者Toll样受体4(Toll-like receptor 4,TLR4)/核转录因子-κB(nuclear factor-κB, NF-κB)信号通路及后续疗效的作用,并报道如下。
1 资料与方法
1.1 研究对象
选取2018年10月—2019年10月在南昌大学第一附属医院神经内科就诊的DEACMP 患者90 例。根据抽中奇偶数的结果将患者分成两组,偶数患者作为实验组,奇数患者作为对照组,每组45 例。实验组男性26 例,女性19 例;年龄58~75 岁,平均(62.31±4.31)岁;CO 中毒时昏迷时间2~48 h,平均(18.64±3.15)h;假愈期2~60 d,平均(32.54±5.14)d;病程3~70 h,平均(32.15±4.67)h;对照组男性24 例,女性21 例;年龄56~73 岁,平均(61.85±4.26)岁;CO 中毒时昏迷时间2~46 h,平均(18.20±3.01)h;假愈期2~60 d,平均(33.68±5.36)d;病程3~72 h,平均(31.89±4.54)h;两组上述指标比较,差异无统计学意义(P>0.05),具有可比性。本研究经医院伦理委员会审批通过,患者及其家属均知情同意。
1.2 纳入与排除标准
1.2.1 纳入标准 ①参照DEACMP 诊断标准,有CO 中毒史和明确的假愈期[4];②年龄56~75 岁;③DEACMP 病程≤72 h,格拉斯哥昏迷评分[5]>8 分。
1.2.2 排除标准 ①伴有帕金森症、阿尔茨海默症、反应性精神病等认知障碍性疾病;②预计生存期≤6 个月;③心、肝、肾功能异常;④合并感染患者;⑤合并脑卒中等其他影响脑器官及日常活动能力的疾病。
1.3 治疗方法
1.3.1 对照组 采取常规治疗,在发病早期促进患者脑细胞营养代谢,予以改善脑血液循环药物[血塞通(广西梧州制药集团股份有限公司,国药准字Z20025652)500 mg/次,1 次/d];静脉滴注地塞米松(武汉久安药业有限公司,国药准字H42020896)10 mg/d,持续1 个月以上;静脉注射银杏叶提取物注射液(中豪国际有限公司,国药准字H20181022)1 次/d。15 d 后根据患者恢复情况调整用药方案。恢复期给予针灸、按摩,肢体功能锻炼等。
1.3.2 实验组 在对照组基础上使用高压氧治疗,压力0.2 MPa,持续20 min,稳压后吸100%纯氧约80 min,稳压吸氧期间休息2 次,约5 min/次,然后持续减压约20 min,1 次/d。采用烟台宏远氧业公司生产的GY3400 型高压氧舱,10 d 为1 个疗程,1 个疗程后根据患者恢复情况再调整。
1.4 观察指标
1.4.1 临床疗效 比较两组患者治疗3 个月后的临床疗效。将临床疗效分为:①痊愈,患者临床体征消失,脑电图检查显示正常,生活可以自理;②好转,患者部分症状体征消失或减轻,脑电图检查显示轻度异常或中度正常,部分活动需要照顾者帮助);③无效,患者病情无好转,脑电图检查显示重度异常,生活无法自理)[6]。总有效率(%)=(痊愈例数+好转例数)/总例数×100%。
1.4.2 TLR4/NF-κB 信号通路 比较两组患者治疗前后TLR4/NF-κB 信号通路的表达,分别采集患者治疗前及治疗3 个月后空腹静脉血10 ml,2 000 r/min 离心后进行细胞培养,采用实时荧光定量聚合酶链反应(quantitative real-time polymerase chain reaction, qRT-PCR)检测TLR4 mRNA 的表达。TLR4 mRNA 相对表达量为TLR4 与β-action 条带灰度值的比值。采用Western blotting 检测NF-κB p65蛋白的表达。兔抗人磷酸化NF-κB p65 抗体、β-action 抗体购自美国Abcam 公司,TLR4 单克隆抗体购自美国Biolegend 公司。
1.4.3 洛文斯顿作业治疗用认知评定量表(Lovins cognitive rating scale for occupational therapy,LOTCA)、日常生活能力量表(activity of daily living scale, ADL)、Wahlund 改良脑白质疏松分级量表(Wahlund modified leukoaraiosis rating scalem ARWMC)评分 比较两组患者治疗前后LOTCA[7]、ADL[8]、ARWMC[9]评分的变化。LOTCA 评分分别从定向力、知觉、视组织运动、思维运作及注意力5 个方面进行评定,共21 个测评项。除思维运作有3 项满分为5 分,余者每项满分皆为4 分,分数越低表示其认知障碍越严重。ADL 评分从进食、入厕、大小便控制、修饰、洗澡、转椅床椅、步行、洗澡、上下楼梯10 个项目进行评定,每项满分10 分,总分越高其生活自理能力越好。ARWMC 评分可依照不同时间点获取的影像图像进行判定,分别从两侧脑组织重要组成部分的局部破坏情况进行分析,满分30 分,总分>10 分时为严重的脑白质疏松,总分越低其脑白质疏松程度越轻微。本研究均由专业医师(对本研究不知情)于治疗前及治疗3 个月后对患者进行评估。
1.4.4 预后评分 比较两组患者治疗后3 个月、6 个月和12 个月预后评分的变化。预后评分采用改良Rankin(improved Rankin, mRS)评分[10],mRS 评分依照患者病后生活状态来计算分数,0 分表示无明显障碍;1 分为有轻微症状但无明显功能障碍;6 分表示患者已无生命体征。mRS ≤2 分表示预后良好。
1.5 统计学方法
数据分析采用Epi Data 3.1 和SPSS 17.0 统计软件。计量资料以均数±标准差(±s)表示,用t检验或重复测量设计的方差分析,进一步两两比较用LSD-t检验;计数资料以率(%)表示,用χ2检验。P<0.05 为差异有统计学意义。
2 结果
2.1 两组临床疗效比较
两组总有效率比较,经χ2检验,差异有统计学意义(χ2=5.000,P=0.025),观察组高于对照组。见表1。
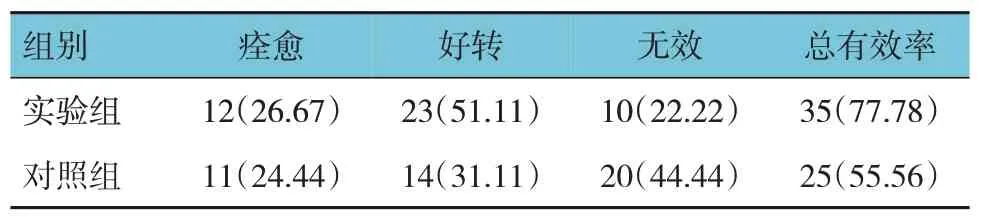
表1 两组临床疗效比较 [n=45,例(%)]
2.2 两组患者治疗前后TLR4 mRNA、NF-κB p65相对表达量的变化
两组患者治疗前后TLR4 mRNA、NF-κB p65 相对表达量的差值比较,经t检验,差异有统计学意义(P<0.05),实验组大于对照组。见表2。
表2 两组患者治疗前后TLR4 mRNA、NF-κB p65相对表达量的差值比较 (n=45,±s)
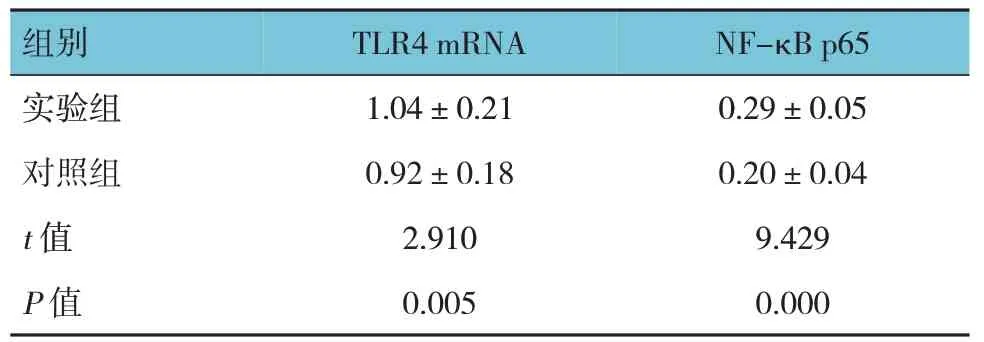
表2 两组患者治疗前后TLR4 mRNA、NF-κB p65相对表达量的差值比较 (n=45,±s)
组别实验组对照组t 值P 值TLR4 mRNA 1.04±0.21 0.92±0.18 2.910 0.005 NF-κB p65 0.29±0.05 0.20±0.04 9.429 0.000
2.3 两组患者治疗前后各项评分的变化
两组患者治疗前后LOTCA、ADL 及ARWMC 的差值比较,经t检验,差异有统计学意义(P<0.05),实验组治疗前后LOTCA、ADL 的差值大于对照组,ARWMC 的差值小于对照组。见表3。
表3 两组治疗前后各项评分的差值比较(n=45,分,±s)
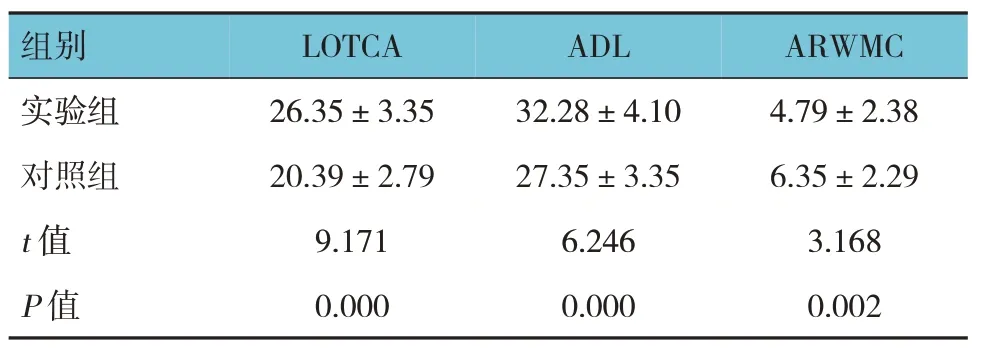
表3 两组治疗前后各项评分的差值比较(n=45,分,±s)
组别实验组对照组t 值P 值LOTCA 26.35±3.35 20.39±2.79 9.171 0.000 ADL 32.28±4.10 27.35±3.35 6.246 0.000 ARWMC 4.79±2.38 6.35±2.29 3.168 0.002
2.4 两组患者不同时间点mRS评分的变化
实验组与对照组患者治疗后3 个月、6 个月、12 个月mRS 评分比较,采用重复测量设计的方差分析,结果:①不同时间点mRS 评分有差异(F=122.783,P=0.000);②实验组与对照组mRS 评分有差异(F=43.885,P=0.000);③两组mRS 评分变化趋势有差异(F=66.939,P=0.000)。见表4。
表4 两组患者不同时间点mRS评分比较(n=45,分,±s)
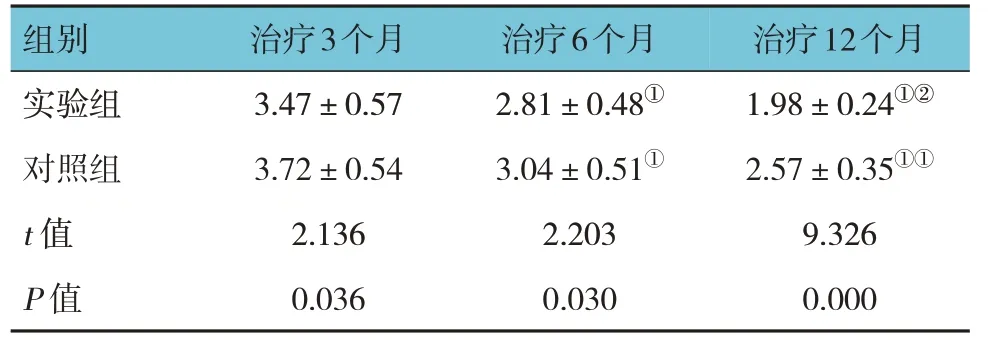
表4 两组患者不同时间点mRS评分比较(n=45,分,±s)
注:①与治疗后3个月比较,P <0.05;②与治疗后6个月比较,P <0.05。
组别实验组对照组t 值P 值治疗3个月3.47±0.57 3.72±0.54 2.136 0.036治疗6个月2.81±0.48①3.04±0.51①2.203 0.030治疗12个月1.98±0.24①②2.57±0.35①①9.326 0.000
3 讨论
CO 中毒后,脑组织自由基生成增加,脂质过氧化,从而损伤线粒体;大量生成的自由基引起髓鞘碱蛋白的修饰,激活自身免疫系统,导致髓鞘脱失,T 淋巴细胞活化,释放炎症因子,最终引起脑血管病变[11]。TLR4 作为人类发现的第1 个TLR 蛋白,与临床上许多炎症性疾病关系密切,其受体与病原相关分子模式结合,利用信号传导激活NF-κB,调控下游炎症基因,增强机体炎症因子的表达,促进机体多种器官炎症性疾病的发生、发展[12]。
本研究中观察组总有效率高于对照组,提示高压氧治疗DEACMP 临床疗效更好。李哲等[13]研究高压氧改善患者临床疗效的机制,认为高压氧治疗能增加血氧分压,改善大脑缺氧症状,减轻脑水肿的恶性循环,相同时间内增快神经纤维髓鞘活性,使血管因缺氧而造成的损伤得到修复,并成功形成侧支循环,增强微血栓生成的抑制效果,激活中枢神经生化过程。这也证实了高压氧可增强生命体抗氧化能力,尽快恢复大脑功能,减少神经细胞的变质及凋亡,改善患者症状。
本研究中实验组治疗前后TLR4 mRNA、NF-κB p65 相对表达量的差值大于对照组,提示高压氧可能通过改善TLR4/NF-κB 信号通路来提高治疗效果。DEACMP 患者大脑通常存在微循环功能障碍,神经细胞凋亡及氧化应激等病理生理改变,引起炎症级联反应,而TLR4/NF-κB 信号通路也参与了免疫信号传递和炎症因子释放的过程[14]。TLR4 主要在抗原呈递细胞及一些实质细胞中表达。在中枢神经系统中,TLR4 主要分布在小胶质细胞和神经元表面,可在一系列反应下激活NF-κB 并暴露核定位信号,促使NF-κB 活化并进入细胞核启动转录,诱导产生肿瘤坏死因子α(Tumor necrosis factor alpha,TNF-α)、白细胞介素1β(interleukin-1β, IL-1β)、IL-6、IL-8、IL-12,从而促进外周炎症细胞向缺血脑组织移动、黏附和浸润,加重组织损伤。高压氧通过提高脑组织氧含量和氧分压,增加脑组织毛细血管的弥散距离,减少细胞变性坏死,提高超氧化物歧化酶活性,加强清除自由基和抗氧化能力,纠正因无氧酵解产生的酸中毒,从而逆转神经细胞损伤,降低炎症因子水平,实现对TLR4/NF-κB 信号通路的调控[15]。
本研究中实验组治疗前后LOTCA、ADL 的差值大于对照组,ARWMC 的差值小于对照组,提示高压氧治疗可显著减轻患者认知障碍,提高生活自理能力,且可以逆转脑组织损伤。CO 中毒后,血脑屏障呈非特异性炎症状态,高压氧治疗可明显增强其通透性,降低由氧成分不足而对脑神经器官产生的破坏,促进脑功能逐渐恢复,改善认知功能[16]。
本研究中实验组与对照组治疗后3 个月、6 个月和12 个月mRS 评分有差异,提示高压氧治疗可显著改善患者预后。方建飞等[17]研究证实,较长时间的高压氧治疗能使病情得到较有效恢复,远期预后良好,与本研究结果相符。
综上所述,高压氧可改善DEACMP 患者TLR4/NF-κB 信号表达,同时缓解其大脑缺氧状态,提高临床疗效,且远期预后良好,值得临床推广。
