改良一片式可折叠后房型人工晶体睫状体平坦部缝线固定术的效果
2022-01-13刁志玮童念庭周占宇
刁志玮,童念庭,周占宇
(青岛大学第三临床医学院(青岛市市立医院)眼科,山东 青岛 266011)
后房型人工晶体缝线固定术也叫做人工晶体悬吊术,最早由MALBRAN在1986年提出,是治疗无囊袋支持的无晶状体眼的重要方法[1]。根据晶体襻在眼内固定位置的不同,后房型人工晶状体固定分为睫状沟固定、虹膜固定和睫状体平坦部固定3种方法,目前国内外以睫状沟处缝线固定最为常用。然而有学者提出,在睫状沟处固定会使得人工晶状体位置偏前,其襻及光学部可以直接触及虹膜后表面及睫状突,引起虹膜的炎症反应,影响血-房水屏障功能,术后色素播散综合征(PDS)以及色素性青光眼(PG)等并发症的发生率较高[2]。本研究对该术式进行了改良,将一片式可折叠后房型人工晶体(SPIOLs)的固定位置从传统的角巩膜缘后1.5 mm改变为角巩膜缘后3.0 mm,即从传统的睫状沟处固定调整为睫状体平坦部固定。本文研究比较改良SPIOLs睫状体平坦部缝线固定术与传统术式术后并发症的发生情况,为临床手术医生选取人工晶体悬吊位置提供依据。
1 资料和方法
1.1 一般资料
收集2011年3月—2016年4月在青岛市市立医院眼科中心行人工晶体缝线固定术、术后随访至少6个月病人的临床资料,其中合并有角膜病变、内皮细胞计数低、青光眼、葡萄膜炎、增生性糖尿病性视网膜病变、年龄相关性黄斑变性、既往眼部手术史、术前瞳孔直径>6 mm的病人被排除在外。依据人工晶体缝线固定部位的不同分成睫状沟(角巩膜缘后1.5 mm)固定组(A组)和睫状体平坦部(角巩膜缘后3.0 mm)固定组(B组)。
1.2 手术方法
两组晶状体囊袋支撑不足的病人,在人工晶状体(IOL)缝线固定术前均先行晶状体切除术和玻璃体切除术。本研究对经典的SPIOLs经巩膜缝线固定术进行了轻微的改进:在12点钟靠近角巩膜缘部位作3.0 mm透明角膜切口,采用外路法(ab externo)[3],将2根10-0双针聚丙烯悬吊线(TG140-8 plus;Alcon Laboratories,USA)的引导针依次在2点钟、8点钟角巩膜缘后1.5 mm(睫状沟固定组)或3.0 mm(睫状体平坦部固定组)进针,进入虹膜后面,让针尖在瞳孔区出现,并用1.0 mL注射器(针头稍扭弯)自12点钟角膜缘切口进入前房,将长针套入注射器针管内,并随注射器针头退出眼外。剪断角膜缘切口侧的缝针线,其中一根在人工晶状体一支襻尾打结系紧,使得人工晶状体置入前房,保留另一只襻暴露在角膜切口部位;预置的另一根悬吊线于该襻尾端打结系紧。收紧悬吊线调整人工晶状体位置至虹膜后,拉紧2点钟及8点钟的悬吊线,调整人工晶状体居中,分别于2点钟及8点钟处将悬吊线缝合于巩膜表面并打结固定,并应用晶体调位钩将留长的线结埋于相应位置的Tenon囊下。手术由同一名经验丰富的手术医生进行。术中选用的晶体均为一片式丙烯酸可折叠后房型人工晶体(ZCB00,Abbott Medical Optics,Santa Ana,CA,USA),总长度为13.0 mm,其中光学部的直径为6.0 mm,人工晶体光学部和襻之间的夹角为0°。
1.3 术后用药
术眼手术后第1天换药后开始给予5 g/L左氧氟沙星(可乐必妥)滴眼液、10 g/L醋酸泼尼松龙(百力特)滴眼液外用,每天4次,至术后1月停用。对于术后高眼压病人根据病情及个体差异,酌情选用200 g/L甘露醇、10 g/L布林佐胺(派立明)滴眼液、2 g/L酒石酸溴莫尼定(阿法根)滴眼液、20 g/L盐酸卡替洛尔(美开朗)滴眼液治疗。
1.4 观察指标
所有病人术前和每次随访时均接受了详细的眼科检查,包括最佳矫正视力(BCVA)、裂隙灯检查、前房角镜检查、间接检眼镜检查和非接触式眼压(IOP)测量等,其中裂隙灯检查用于观察病人前房炎症反应和色素弥散情况[4],前房角镜检查用于查看病人前房角的色素沉积。同时,应用超声生物显微镜(UBM)测量虹膜平面与人工晶体之间的位置关系。观察两组病人术后并发症,包括PDS、PG、反向瞳孔阻滞(RPB)、虹膜夹持(IC)、IOL并发症(脱位、倾斜、偏心)、玻璃体积血、缝线暴露、低眼压、视网膜脱离、黄斑水肿等发生情况。
1.5 统计学方法

2 结 果
2.1 两组基线资料比较
纳入研究病人共56例59眼,其中睫状体平坦部固定组35例36只眼,睫状沟固定组21例23只眼,两组基线资料包括年龄、性别、随访时间及术前BCVA、IOP等差异无显著性(P>0.05)。见表1。
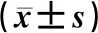
表1 两组基线资料比较
2.2 两组术后并发症比较
随访期间,睫状沟固定组的BCVA为(0.62±0.51)logMAR,而睫状体平坦部固定组为(0.57±0.44)logMAR,两组比较差异无统计学意义(P>0.05)。睫状沟固定组术后PDS、PG、RPB、IC等的发生率均高于睫状体平坦部固定组,差异有统计学意义(χ2=3.864~43.382,P<0.01)。两组其他术后并发症相比较,差异无统计学意义(P>0.05)。见表2。两组随访均未见缝线暴露、低眼压、黄斑水肿及视网膜脱离等发生。

表2 两组术后主要并发症比较(例(χ/%))
3 讨 论
既往所使用的专门为人工晶体缝线固定术设计的人工晶体由一片式聚甲基丙烯酸甲酯(PMMA)制成,植入时术中切口需要>7 mm[5]。大的切口意味着术中前房稳定性下降,眼压波动大,术后易发生低眼压,进而导致玻璃体积血、视网膜脱离等并发症发生的风险增大;并且大的手术切口需要缝线缝合,由此导致的术后散光问题显著影响了病人术后的早期恢复。随着人工晶状体材料和手术技术的进步,在人工晶体缝线固定术中逐渐摒弃了不可折叠的PMMA人工晶体,转而使用折叠晶体并通过小切口置入眼内,术后早期病人视觉质量提高明显,并且术后并发症的发生也减少[6-8]。与三片式可折叠后房型人工晶体(TPIOLs)相比,SPIOLs更适合于经巩膜缝线固定,因为SPIOLs襻材料的硬度更低,更容易在襻环上打结,并且SPIOLs襻末端的膨大使得线结更容易在该处固定[9]。据统计,在美国的白内障手术中,半数以上使用的是SPIOLs[10]。白内障术中如果发现悬韧带断裂范围超过两个象限,原有囊袋支持不足,尤其是人工晶状体已置入眼内时,我们希望使用已经置入的人工晶状体进行经虹膜缝线固定。本研究中5例人工晶状体脱位的病人使用的人工晶状体都是SPIOLs,手术中并未将原来的人工晶状体取出,而是直接行经巩膜的缝线固定术。
PDS是虹膜色素上皮受损后以色素颗粒播散并沉积到眼前段为特征的一种疾病[11]。可见于各种人工晶状体置入术后[12-15]。前房角的色素沉积可阻塞小梁网,增加房水流出阻力,最终造成眼压升高而导致PG[16-17]。本研究显示,睫状沟固定组术后PDS和PG的发生率分别为91.3%和34.8%,其原因可能与睫状沟固定后人工晶状体的光学部和襻与虹膜后表面之间的间隙过小有关;并且由于该类型人工晶体襻为直角方边设计,人工晶体的襻和光学部之间的夹角为0°,造成襻和虹膜后表面反复摩擦,这也会增加术后PDS和PG的发生率。此外,SPIOLs光学部与虹膜后表面的过于贴近也导致RPB、IC等一系列并发症的发生率增高[18-19]。
睫状体平坦部没有重要的结构,没有粗大的血管,切割玻璃体时常常在该部位做通道。选择睫状体平坦部行人工晶体缝线固定时,由于人工晶体平面较睫状沟固定更为靠后,术后病人前房深度更接近于人工晶体囊袋内固定的状态,人工晶体与虹膜后表面距离增加,因而较睫状沟固定的病人发生PDS和PG等术后并发症的概率显著降低,RPB和IC的发生率也更低[3]。本文研究结果显示,与睫状沟固定组相比,睫状体平坦部固定组术后玻璃体积血和视网膜脱离的发生率并没有增加,说明在睫状体平坦部行SPIOLs经巩膜缝线固定是安全有效的。另外,两组病人均未发生眼内炎、视网膜脉络膜脱离及黄斑部病变等,考虑可能与本文研究病例数较少、随访时间较短有关。后续研究中我们将增加病人数量、延长随访时间。
