后尿道瓣膜症患儿术后排尿功能的影响因素分析
2022-01-12虞莹璐
虞莹璐
(南京医科大学附属儿童医院泌尿外科,南京 210000)
后尿道瓣膜症(PUV)表现为尿流排出障碍,常见于男童下尿路梗阻。患儿排尿困难及反复尿路感染,严重梗阻可引起肾积水、膀胱功能障碍[1]。临床上通常进行膀胱尿道造影,可见明显的后尿道延长和扩张,对于PUV 的诊断准确度较高[2]。膀胱镜瓣膜电切术治疗PUV 微创安全,有效改善梗阻性尿路病变。但术后部分患儿仍会存在排尿异常,尿路感染复发,影响生活质量,处理较为棘手[3]。目前,国内关于PUV 术后排尿异常影响因素研究尚不充分,故本研究探讨引起PUV 术后排尿异常的危险因素,报道如下。
1 资料与方法
1.1 一般资料 回顾性分析本院2015 年1 月~2019年1 月收治的60 例PUV 患儿临床资料,均为男童,年龄1 d~6 岁,平均(2.19±1.23)岁。根据术后6 个月患儿术后尿动力学检查结果、临床症状将60 例患儿分为排尿正常组(n=11)和排尿异常组(n=49)。排尿正常组患儿年龄1d~5 岁,平均(1.85±0.68)岁,排尿异常组患儿年龄3 d~6 岁,平均(2.27±1.19)岁,两组年龄比较,差异无统计学意义(P>0.05)。纳入标准:确诊PUV,明显排尿困难症状,行膀胱经瓣膜电切术,患儿年龄≤6岁。排除先天性疾病、既往泌尿手术史。
1.2 手术方法 根据患儿年龄选择合适型号的膀胱镜,婴幼儿选择8F 膀胱镜,大龄儿选择12 F 膀胱镜,均购自德国Karl-Storz 公司。患儿取截石位,行膀胱镜瓣膜电切术,将电极插入尿道,并使之贴近瓣膜,于瓣膜5点、7 点、12 点处短时间电灼瓣膜(功率约为10 W)。确定无明显渗血后,将膀胱镜退出,按压膀胱可见尿程变远,尿线增粗,提示排尿功能已改善。术后常规留置导尿管,给予抗生素抗感染。
1.3 术后随访 所有患儿术后3 个月、6 个月来院复查,检查内容包括血常规、泌尿系彩超、尿流动力学检查,了解排尿情况,必要时进行排尿性膀胱尿道造影检查。
1.4 统计学分析 采用SPSS 20.0 软件。计量资料以mean±SD 表示,计数资料以例表示,进行t 检验、χ2检验。术后排尿异常的多因素分析采用Logistic 分析。P<0.05 为差异有统计学意义。
2 结果
2.1 术后随访 彩超和排尿结果显示,术前14 例单侧输尿管扩张合并同侧肾积水,其中3 例术后加重,5 例术后好转,术前46 例双侧输尿管扩张合双并肾积水,其中20 例术后好转,12 例术后加重;术前21 例单侧膀胱输尿管返流,其中8 例术后加重,7 例术后好转,术前32 例双侧膀胱输尿管返流,其中7 例术后加重,19 例术后好转。
2.2 术后排尿正常组和排尿异常组尿动力参数比较术后6 个月,排尿正常组逼尿肌漏尿点压力及残余尿量小于排尿异常组,膀胱顺应性及尿流率大于排尿异常组,差异有统计学意义(P<0.05),见表1。
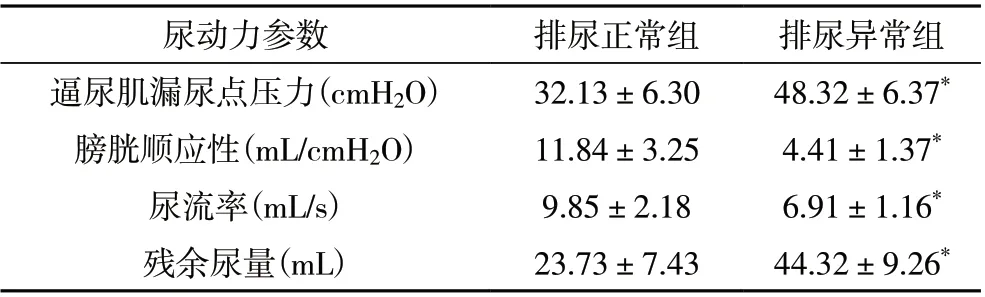
表1 术后排尿正常组和排尿异常组尿动力参数比较
2.3 术后排尿异常的单因素分析 排尿正常组和排尿异常组在诊断时间、术前膀胱壁增厚和小梁增生方面,差异有统计学意义(P<0.05)。见表2。
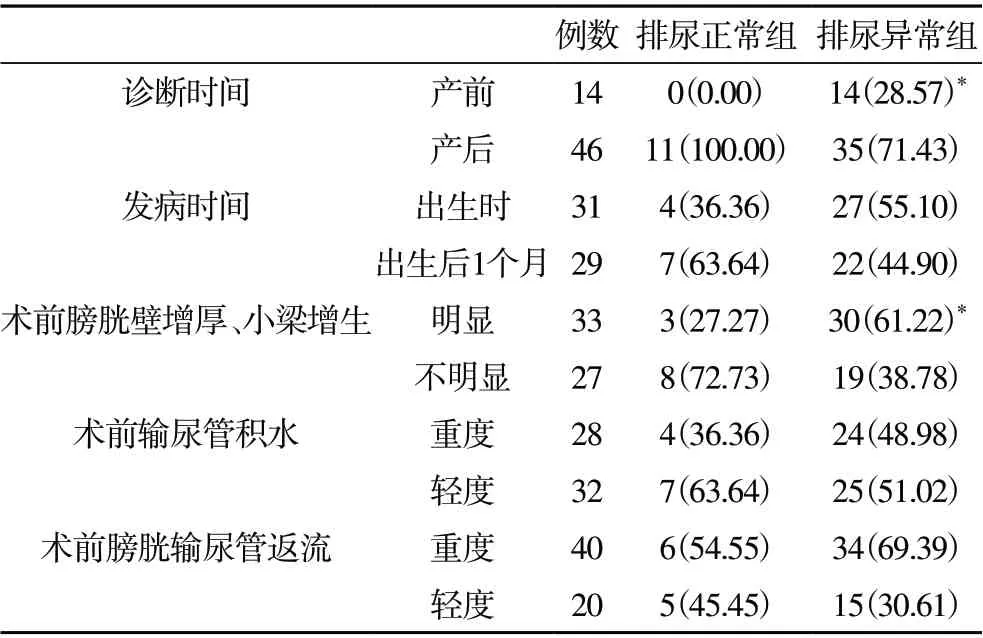
表2 术后排尿异常的单因素分析[n(%)]
2.4 术后排尿异常的多因素分析 产前诊断、术前膀胱壁增厚和小梁增生是影响术后排尿异常的独立危险因素(P<0.05),见表3。
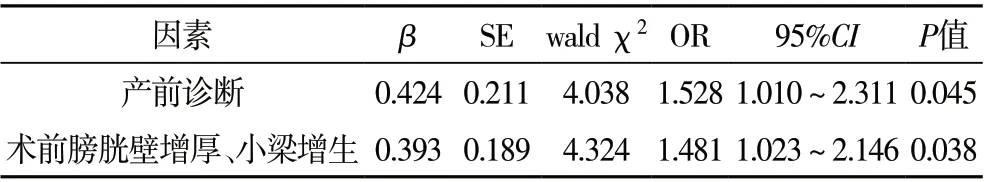
表3 术后排尿异常的多因素分析
3 讨论
PUV 是男孩最常见的下尿路先天性异常,发生率为1:5000 - 1:8000[4]。病因尚不明确,一般认为是胚胎发育时期肾管或尿生殖窦发育异常所致,中肾管插入尿生殖窦,影响尿生殖窦融合,形成隔膜,使膀胱排尿受阻。该疾病是导致男性儿童膀胱出口梗阻和肾功能不全的主要原因。PUV 患儿由于膀胱压力持续存在,排尿梗阻引起膀胱局部向外膨出,膀胱憩室导致尿液不能排出,长期严重梗阻可引起肾盂积水,持续损害肾功能,进展为慢性肾病。膀胱镜下瓣膜电切术通常能改善梗阻性尿路病变,但即使术后尿路梗阻解除后,仍有70%~80%儿童存在持续性膀胱功能障碍、排尿异常现象,慢性肾病及终末期肾病加重[5,6]。
PUV 患儿治疗后,术后随访发现部分患儿仍存在输尿管扩张、肾积水现象,甚至有加重趋势。术前14例单侧输尿管扩张合并同侧肾积水,其中3 例术后加重,5 例术后好转,术前46 例双侧输尿管扩张合双并肾积水,其中20 例术后好转,12 例术后加重;术前21 例单侧膀胱输尿管返流,其中8 例术后加重,7 例术后好转,术前32 例双侧膀胱输尿管返流,其中7 例术后加重,19 例术后好转。81.67%的患儿术后表现为排尿异常,与既往研究相似[7]。分析原因,平滑肌细胞增生是PUV 发生下尿路阻塞的早期变化,后期则出现逼尿肌纤维化、胶原沉积。而膀胱镜下瓣膜电切术无法逆转膀胱组织学的改变,所以术后常合并膀胱功能障碍,排尿异常。本研究结果显示,排尿正常组逼尿肌漏尿点压力及残余尿量显著小于排尿异常组,膀胱顺应性及尿流率显著大于排尿异常组,提示患儿膀胱功能异常。
本研究发现,产前诊断、术前膀胱壁增厚和小梁增生是影响术后排尿异常的独立危险因素。产前超声检查可用于下尿路梗阻诊断,PUV 超声表现为膀胱增大、尿道扩张、膀胱壁颈部增厚、“钥匙孔”征、羊水少、双肾积水等征象,诊断灵敏度高达90%以上[8,9]。胚胎形成早期就出现PUV 会引起胎儿泌尿系统发育异常,表现为肾功能障碍,与儿童相比,胎儿期PUV 所致的上尿路功能损伤、膀胱功能损伤、肾损伤更为严重,所以产前诊断患儿术后排尿异常发生风险较大。一项meta 分析显示,妊娠24 周内产前诊断预后较差,24 周内无明显尿路异常者预后较好[10]。对于产前诊断PUV 者,有学者认为可进行宫内干预,但宫内干预远期效果尚不清楚,且会导致流产,所以需谨慎进行[11,12]。另外,本研究结果显示,术前膀胱壁增厚和小梁增生是影响术后排尿异常的独立危险因素,术后排尿异常发生风险越高。PUV 所致的下尿路梗阻会使膀胱内压上升,残余尿量增多,引起尿路感染反复,膀胱形态发生变化,最终引起膀胱功能障碍、排尿异常,且膀胱形态改变无法通过手术改善,所以术前膀胱壁增厚、小梁增生程度是影响术后排尿异常的关键因素。在术中若发患儿膀胱壁增厚、小梁增生明显,应及时进行膀胱造口、清洁间歇导尿、尿路感染控制等措施干预,以减少术后排尿异常发生,提高治疗效果[13,14]。
综上所述,PUV 虽然发病率低,但其所致的尿道梗阻对患儿泌尿系统影响较大,应当做到早诊断早治疗,术后定期复查。术后排尿异常者膀胱功能及上尿路情况明显较差,产前诊断、术前膀胱壁增厚和小梁增生是影响术后排尿异常的独立危险因素,可为临床诊治提供参考。
