和厚朴酚衍生物的合成及防治结肠癌作用机制的预测
2022-01-12何明会党笑笑董登祥
何明会, 党笑笑, 李 军, 董登祥*
(1. 贵州中医药大学 药学院,贵州 贵阳 550000; 2. 西安解码生物科技有限公司,陕西 西安 710000)
结肠癌是一种发生于结肠部位的消化道恶性肿瘤,随着人民生活水平的提高,我国结肠癌患者在急速上升,发病率和死亡率也越来越高,严重威胁到患者的生活质量[1]。目前常规化疗药物的治疗,常因选择性不高,产生一系列的不良反应,包括腹泻、中性粒细胞减少、恶心呕吐、胃肠道毒性和肝毒性等[2-3]。而中药及单体化合物在治疗结肠癌上取得了一定的成果,可以减轻化疗带来的不良反应和结肠癌患者术后的痛苦,提高患者免疫力,降低复发率及提高结肠癌患者在预后的生活质量方面发挥了重要作用[4-6]。因此,寻找安全性高、效果好的抗结肠癌药物是当前医务工作者们迫切需要解决的科学问题。
厚朴(MagnoliaofficinalisRehdetWils)为木兰科、木兰属的植物,主要以干燥皮、根皮及枝皮入药[7]。近年来,厚朴药材中所含天然化合物的研究已经取得了较大的成果[8],发现其主要含有苯丙素类、生物碱类、挥发油类等化合物,而苯丙素类成分是厚朴主要有效成分之一,如厚朴酚、和厚朴酚、苯乙醇苷等[9]。厚朴酚与和厚朴酚的药理活性与厚朴的传统功效密切相关。近年来,国内外学者们研究发现[10-14],和厚朴酚具有抗肿瘤、抗菌、抗炎、抗氧化等广泛的药理活性,尤其在抗肿瘤作用上疗效显著[15-18],有学者研究证实了[19-20]和厚朴酚在结肠癌细胞中具有明显的抗增殖活性,和厚朴酚可能是一种可开发的结肠癌候选药物。和厚朴酚最初是由Obovata等从厚朴药材中提取分离得到的一种白色粉末状酚类化合物(Chart 1)。但其难溶于水,易溶于极性较大或中极性的有机溶剂,稳定性差等理化性质,使其研究开发及临床应用受到了极大的限制[21]。因此,解决和厚朴酚水溶性低、稳定性差的缺陷是当前医务工作者研究的热点领域。

Chart 1
糖是为人类提供能量的三大物质之一,是生命体存活的必须物质。在十九世纪二十年代初期,国外科学家研究发现了六碳糖的结构,之后科学技术越来越先进,人们借助各种技术和仪器对其进行了深入的研究[22]。迎来了糖化学的热潮,糖化学也得到了迅猛发展。研究发现[23]细胞膜糖蛋白,糖脂是由碳水化合物基团和蛋白质,脂质,磷脂组成。同时还发现其可参与细胞的识别和增殖,组织器官的形成,胚胎发育,激素调节等多种生命过程。另外有研究表明[24]糖基化结构改造可以提高药物的水溶性,使其与原苷元结合后水溶性、稳定性、活性均有所提高。虽然已有学者[25-27]对和厚朴酚进行了结构的改造及修饰,但和厚朴酚糖基化结构改造及修饰的文献报道较少。基于此,本文在和厚朴酚结构的基础上,引入简单的糖基结构,合成和厚朴酚的糖苷化合物,以达到提高其水溶性和稳定性的目的,进而提高其生物利用度[28-29]。
近些年,网络药理学和分子对接技术为中药及单体化合物作用机制的研究提供了思路。网络药理学主要是通过构建和整合“成分-靶标-通路-疾病”多层次网络,分析特定信号节点之间的相互作用关系,从系统、整体角度探索药物与机体相互作用的一门新学科[30]。网络药理学被认为是一种提高新药临床试验成功率和节省药物研发费用的新方法[31-32]。
综上所述,本文以和厚朴酚为先导化合物,以D-半乳糖、D-葡萄糖、α-乳糖等为起始原料,通过对糖羟基保护与去保护,得到一系列单糖、二糖片段、三糖片段(Scheme 1),再与和厚朴酚上的4′-OH结合,得到和厚朴酚的单糖、二糖、三糖衍生物(Scheme 2)。再将得到的目标化合物通过1H NMR、13C NMR等方法进行结构鉴定。同时,通过网络药理学和分子对接技术,初步揭示和厚朴酚衍生物防治结肠癌的作用机制,以期为和厚朴酚类药物及衍生物的深入研究及开发利用提供参考依据。
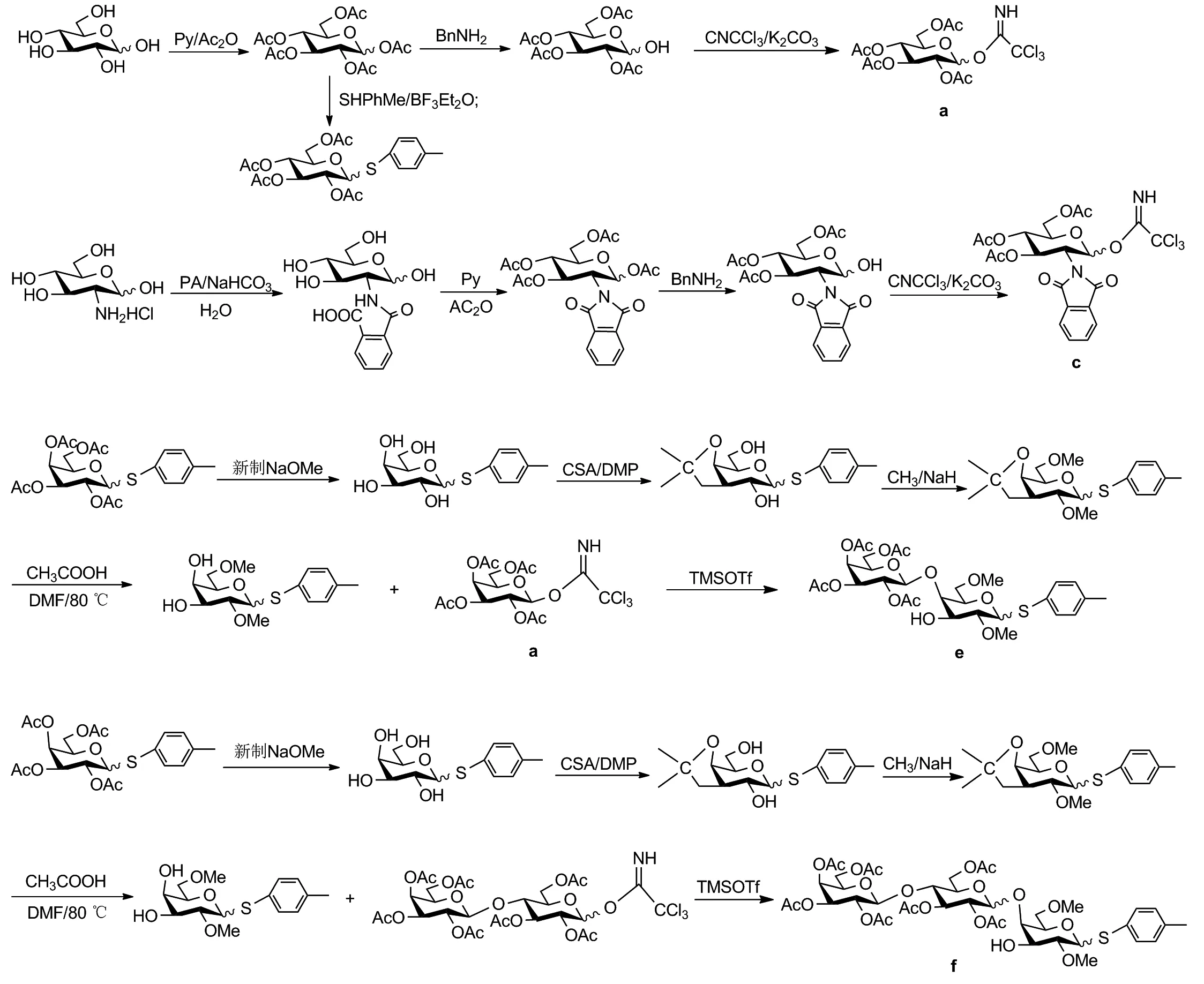
Scheme 1
1 实验部分
1.1 仪器与试剂
WFH-203B型三用紫外分析仪;INOVA-600 MHz型核磁共振仪(DMSO、 D2O或CDCl3为溶剂,TMS为内标)。
D-半乳糖、D-葡萄糖、α-乳糖、D-氨基葡萄糖盐酸盐,国药集团化学试剂有限公司;和厚朴酚,西安开来生物工程有限公司;2,3,4,6-四-O-乙酰基-D-吡喃葡萄糖亚胺脂(a), 3,4,6-三-O-乙酰基2-去氧-2-苯甲酰亚胺基-D-吡喃葡萄糖亚胺脂(c),对甲基-苯基-S-(2,3,4,6-四-O-乙酰基-β-D-吡喃葡萄糖基)-(1→4)-2,6-O-甲基-β-D吡喃半乳糖苷(e),对甲基-苯基-S-[(2′,3′,4′,6′-四-O-乙酰基-β-D-吡喃半乳糖基)-(1→4)-2,3,6-三-O-乙酰基-β-D-吡喃葡萄糖基]-(1→4)-2,6-二-O-甲基-β-D-吡喃半乳糖苷(f),其中,a,c,e,f的合成见Scheme 1;其余所用试剂均为分析纯。

Scheme 2
1.2 合成
(1)2的合成
称取化合物10.1g(0.37 mmol和a0.05 g(0.07 mmol)放置反应瓶中,量取适量DCM溶解底物,用N2保护反应体系,将反应瓶置于0 ℃平衡10 min后,取3 μL TMhof加入,0 ℃搅拌反应,每隔10 min用TLC监测反应体系(展开剂:Cy/EtOAc=2/1,V/V),反应30 min后完成(计算得Rf=0.64)。加入1 mL TEA,调节反应体系的pH至中性,终止反应。DCM萃取,收集有机相,除水,过滤,减压浓缩得粗产物。用200~300目硅胶填充硅胶柱后纯化粗产物(洗脱剂:Cy/EtOAc=5/1或Cy/EtOAc=8/1,V/V)得淡黄色固体b0.062 g,产率65.6%。
将精密称量的化合物b0.05 g置于反应瓶中,加适量MeOH溶解底物,加入10 mL新制甲醇钠(NaOMe),常温搅拌反应。每隔30 min用TLC监测反应体系(展开剂:Cy/EtOAc=2/1,V/V),反应1 h后完成(Rf=0)。加入阴离子交换树脂,调节反应体系至中性,终止反应。萃取,除水,收集有机相,减压蒸馏干燥,得到粗产物。用凝胶柱纯化粗产物(洗脱剂:甲醇),得和厚朴酚-4′-O-2,3,4,6-四-O-乙酰基-β-D-吡喃葡萄糖苷(2) 0.51 g,白色固体粉末,收率99.8%, m.p.88~89 ℃;1H NMR(600 MHz, DMSO)δ: 7.91(d,J=14.5 Hz, 1H, Ar-6′), 7.37(dd,J=13.7 Hz, 8.1 Hz, 1H, Ar-4), 7.31(s, 1H, Ar-6), 7.20(dd,J=15.2 Hz, 8.1 Hz, 1H, Ar-3), 7.11(d,J=8.0 Hz, 1H, Ar-5′), 7.06(m, 2H, 8,8′-H), 6.78(s, 1H, Ar-3′), 5.42(d,J=10.5 Hz, 1H, Glu-1-H), 4.90(dd,J=9.0 Hz, 3.4 Hz, 2H, 9′-H), 4.48(d,J=9.5 Hz, 2H, 9-H), 4.21(d,J=6.9 Hz, 4H, 7,7′-H), 4.08~4.02(m, 5H, Glu-2,3,5,6-H), 3.08(m, 1H, Glu-4-H);13C NMR(151 MHz, DMSO)δ: 167.8(Ar-C4′), 162.8(Ar-C2), 137.9(Ar-C2′), 137.3(C8′, C8), 135.2(Ar-C4), 133.0(Ar-C5), 131.9(Ar-C6), 131.4(Ar-C1′), 130.6(Ar-C1), 130.1(Ar-C4), 129.8(Ar-C6), 128.6(C9, C9′), 123.8(Ar-C3), 123.5(Ar-C3′), 102.1(Glu-C1), 97.9(C9’, C9), 75.1 (Glu-C2), 73.4(C5), 73.0(C3), 69.1(C4), 68.6(C6), 29.9(C7’, C7)。
(2)3的合成
称取化合物10.1 g(0.37 mmol)和c0.05 g放置反应瓶中,取适量DCM溶解底物,用N2保护反应体系,将反应瓶置于0 ℃平衡10 min后,量取3 μL TMSoTf加入,0 ℃搅拌反应,每10 min用TLC监测反应体系(展开剂:Cy/EtOAc=2/1,V/V),反应30 min后完成(计算得Rf=0.39)。加适量TEA,调节反应体系的pH至中性,终止反应。DCM萃取,收集有机相,干燥,过滤,减压浓缩,得粗产物。用200~300目硅胶填充硅胶柱后纯化粗产物(洗脱剂:Cy/EtOAc=5/1或Cy/EtOAc=8/1,V/V),得淡黄色固体d0.056 g,产率59.7%。
将精密称量的化合物d0.05 g,置于反应瓶中,加适量MeOH溶解底物,加入10 mL新制甲醇钠(NaOMe)(称取Na粒100 mg置于10 mL MeOH调至PH=11~12),常温搅拌反应。每30 min用TLC监测反应体系(展开剂为:Cy/EtOAc=2/1,V/V),反应1 h后完成(Rf=0)。加入阴离子交换树脂,调节反应体系至中性,终止反应。萃取,除水,收集有机相,减压蒸馏干燥,得到粗产物。用凝胶柱纯化粗产物(洗脱剂:甲醇)。得和厚朴酚-4′-O-2-邻苯二甲酰亚胺基-β-D-吡喃氨基葡萄糖苷(3)0.045 g,白色固体粉末,收率为90.5%, m.p.90~92 ℃;1H NMR(600 MHz, D2O)δ: 7.67(dd,J=5.7 Hz, 3.3 Hz, 1H, Ar-6′), 7.54(dd,J=5.7 Hz, 3.3 Hz, 1H, Ar-4), 7.38(t,J=7.8 Hz, 1H, Ar-3), 7.30(s, 2H, Ar-3′,6), 7.24(d,J=8.1 Hz, 1H, Ar-5′), 7.15(d,J=6.8 Hz, 2H, 8,8′-H), 7.10(d,J=7.9 Hz, 2H, N-Ar-H), 7.04(d,J=7.9 Hz, 2H, N-Ar-H), 5.74(m, 1H, Glu-1), 4.14(m, 4H, 9,9′-H), 3.98(t,J=10.3 Hz, 4H, 7,7′-H), 3.82(d,J=6.4 Hz, 4H, N-CH2), 3.76(m, 1H, Glu-2), 3.66(m, 2H, Glu-6), 3.64(m, 1H, Glu-3), 3.40(m, 1H, Glu-4), 3.31(m, 1H, Glu-5);13C NMR(151 MHz, D2O)δ: 168.6(Ar-C4′), 167.6(Ar-C2), 133.9 (Ar-C2′), 132.6(C8′, C8), 131.4(Ar-C5), 130.9(Ar-C1′), 129.5(Ar-C1), 129.2(C9′, C9) , 129.1(Ar-C6’), 129.0(Ar-C5′), 128.1(Ar-C4), 127.9(Ar-C6), 122.6(Ar-C3), 120.6(Ar-C3′), 118.2(Glu-C1), 117.2(C9′, C9), 74.8(Glu-C2), 69.5(Glu-C3), 69.4(Glu-C5), 67.8(Glu-C4), 60.9(N-C), 60.4(N-C), 54.1(Glu-C6), 39.9(C7′, C7)。
(3)4的合成
称取化合物10.1 g(0.37 mmol)、0.05 ge和0.1 g NBS放置反应瓶中,量取适量DCM溶解底物,用N2保护反应体系,将反应瓶置于0 ℃平衡10 min后,取3 μL TfoH加入,0 ℃搅拌反应,每10 min用TLC监测反应体系(展开剂:Cy/EtOAc=2/1,V/V),反应30 min完成(计算得Rf=0.41)。先加入饱和的硫代硫酸钠至无色,再加入饱和碳酸钠,调节反应体系的pH至中性,终止反应。DCM萃取,收集有机相,干燥,过滤,减压浓缩得粗产物。用200-300目硅胶填充硅胶柱后纯化粗产物(洗脱剂:Cy/EtOAc=5/1或Cy/EtOAc=8/1,V/V),得和厚朴酚-4′-O-(2′,3′,4′,6′-四-O-乙酰基-β-D-吡喃葡萄糖基)-(1→4)-2,6-二-O-甲基-β-D-吡喃半乳糖苷(4)0.058 g,淡黄色固体,产率59.1%, m.p.119~122 ℃;1H NMR(600 MHz, CDCl3)δ: 7.60(d,J=1.9 Hz, 1H, Ar-6′), 7.41(d,J=8.2 Hz, 1H, Ar-4), 7.29(s, 2H, Ar-3′,6), 7.13(d,J=8.1 Hz, 2H, Ar-3,5′), 7.05(d,J=1.9 Hz, 2H, 8,8′-H), 5.98~5.91(m, 2H, Glu-1,1′-H), 5.20~5.06(m, 7H, Glu-2′,3′,4′,5′,6′-H), 4.33(t,J=6.7 Hz, 4H, 9,9′-H), 3.35(d,J=6.7 Hz, 4H, 7,7′-H), 2.37~2.31(m, 7H, Glu-2,3,5,6-H), 2.26(s, 3H, Glu-2-OCH3), 1.28(s, 3H, Glu-6-OCH3);13C NMR(151 MHz, CDCl3)δ:172.2(Glu-3′-C=O), 170.4(Glu-2′-C=O), 170.1(Glu-4′-C=O), 167.4(Glu-6′-C=O), 153.2(Ar-C4′), 150.0(Ar-C2), 138.7(Ar-C2′), 137.4(Ar-C3), 136.7(Ar-C5), 133.9(C8′, C8), 132.0(Ar-C4), 129.8(Ar-C6, C6′), 128.5(Ar-C1, C1′), 124.4(Ar-C3′), 116.51(C9′, C9), 86.5(Glu-C1, C1′), 77.2(Glu-C2), 76.2(Glu-C5), 71.4(Glu-C5′), 69.5(Glu-C3′), 69.4(Glu-C2′), 68.6(Glu-C3), 66.6(Glu-C4′), 65.3(Glu-C4), 64.2(Glu-2-OCH3), 38.77(C7′, C7), 29.7(Glu-4-OCH3)。
(4)5的合成
称取化合物10.1 g(0.37 mmol)、f0.05 g(0.07 mmol)和0.1 g NBS放置反应瓶中,加适量DCM溶解底物,用N2保护反应体系,将反应瓶置于0 ℃平衡10 min后,量取3 μL TfoH加入,0 ℃搅拌反应,每10 min用TLC监测反应体系(展开剂:Cy/EtOAc=2/1),反应1.5 h完成(计算得Rf=0.34)。先加入饱和的硫代硫酸钠至无色,再加入饱和碳酸钠,调节反应体系的pH至中性,终止反应。DCM萃取,收集有机相,干燥,过滤,减压浓缩得粗产物。用200~300目硅胶填充硅胶柱后纯化粗产物(洗脱剂:Cy/EtOAc=5/1或Cy/EtOAc=8/1,V/V),得和厚朴酚-4′-O-[(2′,3′,4′,6′-四-O-乙酰基-β-D-吡喃半乳糖基)-(1→4)-2,3,6-三-O-乙酰基-β-D-吡喃葡萄糖基]-(1→4)-2,6-二-O-甲基-β-D-吡喃半乳糖苷(5)0.055 g,淡黄色固体,产率为58.3%, m.p.131~132 ℃;1H NMR(600 MHz, CDCl3)δ: 7.39(d,J=1.9 Hz, 1H, Ar-6’), 7.29(s, 2H, Ar-3′,6), 7.23(dd,J=8.2 Hz, 2.0 Hz, 1H, Ar-5′), 7.14(d,J=1.9 Hz, 2H, 8,8′-H), 6.03~5.91(m, 3H, Glu-1,1′,1″-H), 5.51~5.45(m, 4H, Glu-3′5′,3″, 5″-H), 5.18~5.08(m, 7H, Glu-2,2′,2″,4′,4″,6″-H), 4.94(dd,J=10.3 Hz, 3.6 Hz, 1H, 9-H), 4.76(d,J=8.0 Hz, 1H, 9′-H), 4.29~4.24(m, 7H, Glu-3,4,5,6,6′-H), 4.16(d,J=12.1 Hz, 2H, 7-H), 3.43(d,J=6.7 Hz, 2H, 7′-H), 2.98(s, 3H, Glu-2-OCH3)), 2.91(s, 3H, Glu-2-OCH3);13C NMR(151 MHz, CDCl3)δ:171.1(Glu-2′-C=O), 170.4(Glu-2″-C=O), 170.0(Glu-3-C=O), 169.5(Glu-3″-C=O), 169.3(Glu-4″-C=O), 169.1(Glu-6′-C=O), 168.50(Glu-6″-C=O), 146.3(Ar-C4′), 137.7(Ar-C2), 136.9(Ar-C3), 136.7(Ar-C5), 133.9(Ar-C2′), 132.2(C8′, C8), 131.2(Ar-C4), 131.1(Ar-C1′), 130.2(Ar-C1), 128.9(Ar-C6), 125.4(Ar-C6′), 122.4(Ar-C3′), 116.5(C9, C9′), 116.2(Glu-C1, C1′), 111.2(Glu-C1″), 77.2~76.8 (Glu-C2, C3, C4, C5, C6, C2′, C3′, C4′, C5′, C6′, C2″, C3″, C4″, C5″, C6″), 53.4(Glu-2-OCH3), 39.55(C7′, C7), 29.7(Glu-4-CH3)。
2 网络药理学预测和厚朴酚衍生物防治结肠癌的作用机制
2.1 和厚朴酚衍生物作用靶点的预测
运用Swiss TargetPrediction数据库,预测和厚朴酚衍生物的作用靶点,整合所有靶点,删除重复靶点,建立和厚朴酚衍生物靶点数据集。最后,利用UniProt数据库将上述筛选得到的所有靶点均转化成UniProt ID格式。
2.2 结肠癌靶点的建立
利用GEO DataSets 以“colon cancer”为关键词,检索“结肠癌”相关的文献,以“Series,Expression profiling by array和Homo sapiens”为筛选条件,选择基因芯片数据(Platform): GSE74604/GPL6104和GSE44076/GPL13667。利用GeneCards数据库以“colon cancer”为关键词,检索“结肠癌”相关的基因。整合所有基因,删除重复基因,建立结肠癌靶点数据集。
2.3 核心靶基因的筛选及PPI网络的构建
将和厚朴酚衍生物防治结肠癌的主要调控靶点导入String数据库中构建蛋白相互作用网络(PPI network, protein protein interaction network),并根据Degree值大小筛选和厚朴酚衍生物治疗结肠癌的核心靶基因。
2.4 和厚朴酚衍生物防治结肠癌网络的构建
利用cytoscape 3.6.1 软件构建“成分-靶点-疾病”和“靶点-通路”网络。
2.5 GO富集分析与KEGG通路富集分析
首先,将核心靶基因的Gene Symbol名转化entrez ID。然后使用R语言BiocManager“ClusterProfiler”中的enrichGO和enrichKEG函数,进行GO生物学过程和KEGG通路富集分析。
2.6 分子对接
首先,利用PDB数据库下载Degree值排名最前的8个核心靶基因的晶体结构。将晶体结果导入DS软件中,除去水分子、加极性氢原子及构象优化等处理后,确定活性结合位点;同时使用Prepare Ligands模块对小分子化合物进行配体预处理。然后,使用AutoDock进行分子对接,得到每个化合物与核心靶基因的对接结合亲和力(Affinity, kcal/mol),以Affinity作为评价指标。Affinity绝对值越大,配体与受体之间的结合能力越稳定。
3 结果与讨论
3.1 合成
本文共合成4个和厚朴酚糖苷衍生物,其中3~5未见文献报道。和厚朴酚为新型木质素,其结构中含有两个酚羟基,将其长时间暴露在空气当中容易发生氧化,造成和厚朴酚苷元的损失;或者反应产物不宜与其氧化物分离。因此,在保存和厚朴酚苷元时,应避光密封低温条件下保存,且经过糖修饰后其稳定性得到了相应的提高。
在合成化合物4、5两个糖苷衍生物时,产率较低。猜测可能是由于其原料糖是合成糖,合成糖存在大量的乙酰基结构,因此其结构较大难与苷元上的酚羟基相结合。同时合成糖的端羟基是用离去基团对甲苯硫酚修饰的,导致产率较低。
合成的二糖、三糖与和厚朴酚合成后,将得到的衍生物的糖上羟基采用新制Na(MeOH)强碱法还原,发现用甲氧基保护的糖羟基无法正常还原,因此该问题仍需要探索解决。
3.2 和厚朴酚衍生物防治结肠癌的作用机制
预测得到723个和厚朴酚衍生物的作用靶点和20249个与“结肠癌”相关的靶点,通过Swiss TargetPrediction、GEO DataSets和GeneCards的作用靶点绘制韦恩图(见图1,图2),筛选得到36个核心靶点。

图1 和厚朴酚合成产物治疗结肠癌主要调控靶点韦恩图

图2 和厚朴酚衍生物治疗结肠癌核心靶基因PPI网络图
软件构建“核心靶点-信号通路”网络(图3,图4)。

图3 和厚朴酚衍生物治疗结肠癌“成分-核心靶点-结肠癌”网络图(紫色六边形代表结肠癌,绿色三角形代表和厚朴酚衍生物,红色四边形代表核心靶基因)
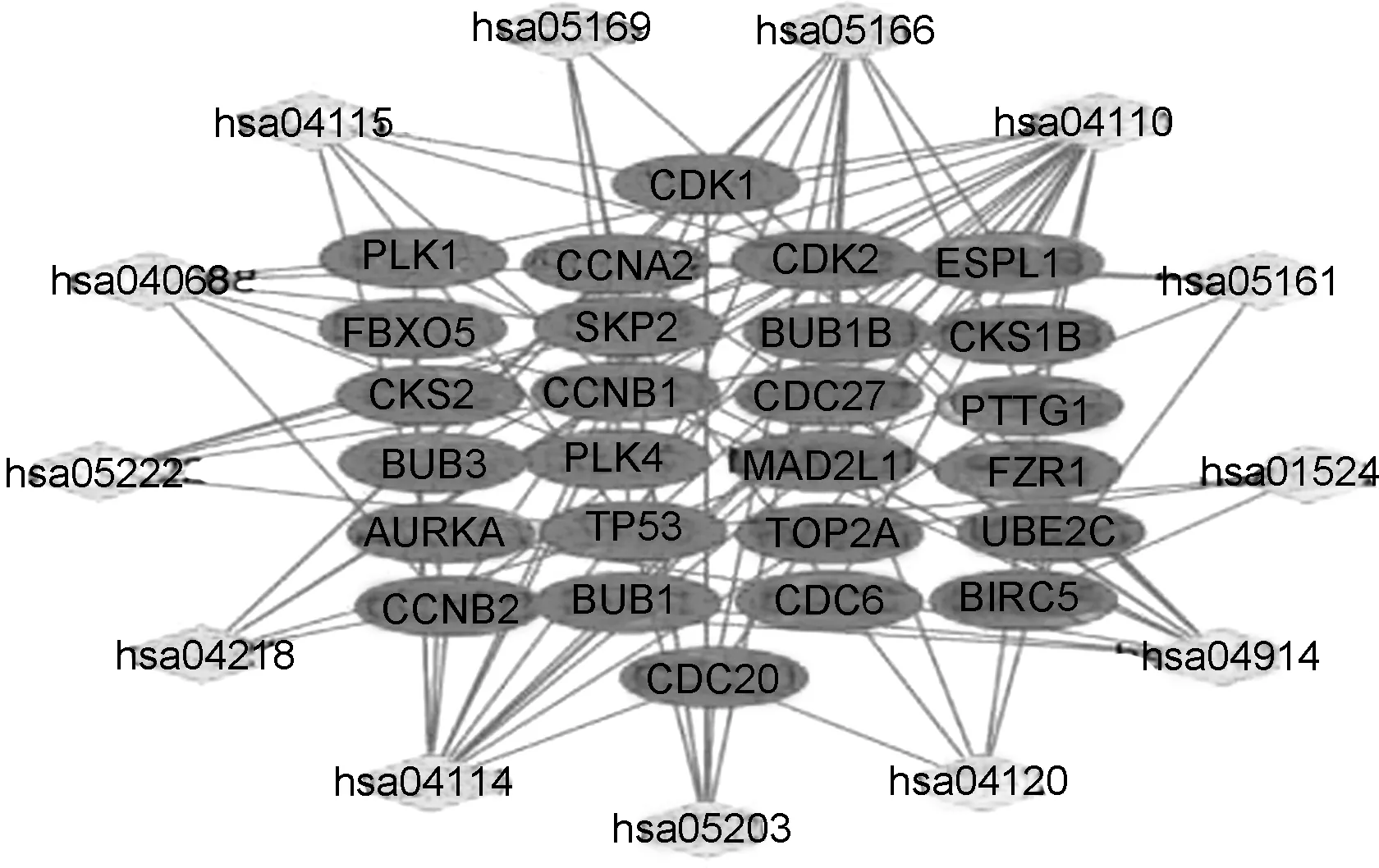
图4 和厚朴酚衍生物治疗结肠癌“核心靶点-信号通路”网络图
将36个核心靶点进行GO富集分析,保留P≤0.05的结果。结果共富集得到323条生物过程,36条细胞组成和21条分子功能,根据P-value越小,列举了显著性排名前20的生物过程进行可视化分析。结果表明,和厚朴酚衍生物治疗结肠癌涉及的主要生物过程包括有丝分裂核分裂、染色体分离的调控、细胞周期相变的调控、细胞周期G2/M相变、减数分裂细胞周期、、蛋白酶体介导的泛素依赖性蛋白分解过程、G2/M过渡有丝分裂细胞周期的调控、细胞器组织的负调控、泛素蛋白连接酶活性的调节、DNA完整性检查点涉及的信号转导、组蛋白磷酸化、膜拆卸、DNA代谢过程的调控等。这些生物过程既可能彼此调节配合,又可能相互制约,共同达到防治结肠癌的目的。
将36个核心靶点进行KEGG通路富集分析,保留P≤0.05的结果,并对信号通路行进行可视化分析。结果共富集得到13条信号通路,分别为细胞周期、卵母细胞减数分裂、孕激素介导的卵母细胞成熟、人T细胞白血病病毒1感染、p53信号通路、FoxO信号通路、小细胞肺癌、细胞衰老、病毒致癌、泛素介导的蛋白水解、铂耐药、乙型肝炎、EB病毒感染。
使用Docking模块进行分子对接,得到8个和厚朴酚衍生物与核心靶基因的对接结合亲和力,结果表明,这8个核心靶基因与和厚朴酚衍生物的亲和力在-10.1~-6.2 kcal/mol,两者结合相对较稳定,与网络拓扑参数的筛选结果基本一致,结果见表1。

表1 核心靶点与和厚朴酚合成产物分子对接结果(kcal/mol)a
研究已证实,和厚朴酚具有治疗结肠癌的作用。通过网络药理学分析,结果表明AURKB、CDK1、CCNB1、PLK1、AURKA为和厚朴酚糖苷衍生物防治结肠癌的主要核心靶点。PLK1基因编码的ser/thr蛋白激酶在有丝分裂过程中高度表达,并且在许多不同类型的癌症中都有升高的水平,其在癌细胞中的缺失显著地抑制了细胞增殖和诱导凋亡,为癌症治疗的靶点[33]。
基于网络药理学方法,构建了“和厚朴酚糖苷衍生物-核心靶点-疾病”、“靶点-通路”网络,发现和厚朴酚糖苷衍生物抗结肠癌的作用机制涉及多个生物过程、多条通路。提示和厚朴酚糖苷衍生物抗结肠癌的作用机制可能是上述靶点和信号通路共同作用的结果。课题组下一步,将对预测结果进行动物实验加以验证。
本文报道的方法不仅改善和厚朴酚稳定性差及水溶性低的问题,还丰富了和厚朴酚衍生物的种类,为和厚朴酚类药物及其衍生物的开发奠定基础。采用网络药理学的方法,通过数据挖掘和筛选,分别构建和厚朴酚糖苷衍生物防治结肠癌的“成分-核心靶点-疾病”、“靶点-通路”和PPI网络,筛选得到了核心靶基因,并对核心靶基因进行GO和KEGG富集分析,通过分子对接初步探讨了和厚朴酚衍生物防治结肠癌的分子机制,体现出和厚朴酚衍生物多靶点、多通路的特点,但需进一步通过动物及细胞实验对预测结果进行验证。
