基于G E 混合规则的SRK-CPA 状态方程预测CO2 在地层水中的溶解度
2022-01-11周建堂康丽侠杨立国卞小强
周建堂,康丽侠,杨立国,张 维,熊 伟,卞小强
(1. 中国石油 长庆油田分公司 第四采油厂,宁夏 银川 750005;2. 西南石油大学 石油与天然气工程学院,四川 成都 610500)
注CO2是提高原油采收率的重要方式之一,CO2易溶于地层水,利用效率并不高,高含NaCl地层水和CO2之间的相互作用规律目前仍未十分清晰[1-2]。Dindoruk 等[3]利用Peng-Robinson 状态方程,结合GE(Huron-Vidal,HV)混合规则,建立了酸气-水体系(CO2,H2S,CH4,H2O)的状态方程模型,预测了体系中CO2的溶解度。基于改进的缔合流体理论(SAFT)模型,卞小强等[4]提出了SRKCPA-Huron-Vidal 模型,预测了在278 ~573 K、0.1 ~140 MPa 下,CO2在H2O 中的溶解度。Sun等[5]使用SAFT-LJ 模型预测了573 K 以下NaCl溶液中CO2的溶解度。Dubacq 等[6]构建了H2OCO2-NaCl体系相平衡在283 ~653 K 和0.1~350.0 MPa 范围内的活度组分模型。Nomeli 等[7]通过计算溶解CO2的局部摩尔体积,提出了一个新的模型来表征温度、压力和盐度对CO2封存过程中浮力驱动对流开始的影响。Mao 等[8]利用亥姆霍兹自由能模型预测了273 ~1 273 K、0 ~500 MPa下,NaCl 溶液中CO2的溶解度。然而,这些模型要么非常复杂,有太多的可调参数;要么预测精度相对偏低。Kontogeorgis 等[9]提出了立方型结合缔合流体理论状态方程(CPA EoS)。Jia 等[10]利用CPA EoS 研究了水/含沥青质稠油混合物的复杂多相行为。郭平等[11]利用考虑分子间物理和缔合相互作用的CPA EoS,计算了水在饱和/非饱和状态下的热力学性质,得到了令人满意的结果。Jia 等[12]建立了CPA-HV 模型,预测了CH4在纯水和NaCl水溶液中的溶解度,预测精度较高。然而,这些CPA 模型针对NaCl 盐溶液的研究相对偏少,同时考虑盐溶液中H2O-H2O 之间的自缔合和CO2-H2O的交互缔合较少。
本工作将SRK-CPA 状态方程与GE混合规则相结合,建立了一个能够描述CO2-H2O-NaCl 混合溶液体系的热力学行为,并能预测地层水中CO2溶解度的新热力学模型(iCPA-HV)。该模型既考虑了H2O-H2O 之间的自缔合,又考虑了CO2-H2O 之间的交互缔合,并在实验条件(T=303 ~523 K,p=0.1 ~130.0 MPa)下,利用最小二乘法对模型的拟合参数(Ei j,Ej i,F)进行了回归。最后,与SRK-HV 模型[13]进行了对比分析。
1 热力学模型
1.1 状态方程
SRK-CPA EoS 的表达式见式(1)。
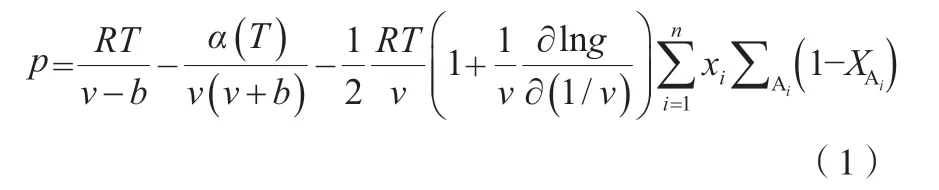
式中,p为体系压力,MPa;R为通用气体常数,8.314 J/(mol·K);T为体系温度,K;ν为摩尔体积,cm3/mol;g为径向分布函数;xi为给定组分i的摩尔分数;XAi为在缔合位A 未发生缔合的组分i的摩尔分数;a为能量参数,(MPa·cm6)/mol2;b为体积参数,cm3/mol。
引力参数(α)的表达式见式(2)。

式中,a0,c1为系数;Tr为对比温度,无因次。
径向分布函数(g (ρ))的近似表达式见式(3)。

式中,ρ为摩尔密度,mol/cm3;η为对比密度,无因次。
未缔合分子的摩尔分数(X)与混合体系的摩尔密度和缔合强度有关,按式(5)计算。

式中,X为在缔合点处未缔合分子的摩尔分数,表示在此分子上对所有缔合点的加和,上标A,B 表示缔合点;N为极性组分的数量;ΔAB为缔合点A和缔合点B 处的综合缔合强度,与摩尔内能和缔合体积有关,可由式(6)计算。
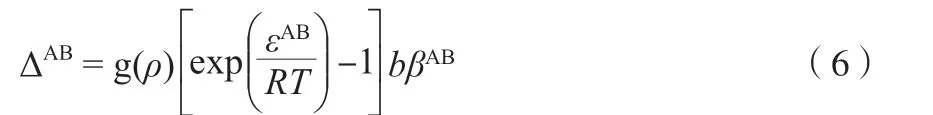
式中,εAB为缔合能量,(MPa·cm3)/mol;βAB为交互作用体积,无因次。
为提高高温、高压下模型的预测精度,选用了HV 混合规则替代CPA 方程中的vdW 混合规则。同时,假设CPA 方程中的交叉缔合作用只与水的缔合作用强度有关,引入二元交互作用参数(F)来描述二者之间的关系,缔合强度(ΔAiBj)可由式(7)估算。

式中,i代表H2O;j代表CO2。
受篇幅所限,SRK 状态方程的具体表达式不再展开叙述,可参考文献[13]。
1.2 基于活度系数的混合规则
HV 混合规则见式(8)和式(9)。
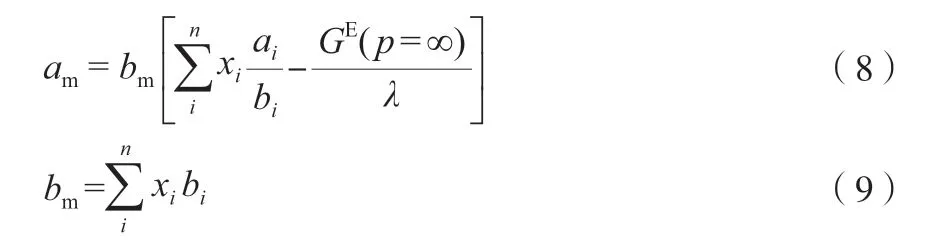
式中,n为组分的总个数;下角标m,i分别为混合物和组分i;λ为ln2;GE为p=∞时的超额Gibbs 能量,可利用HV 混合规则修正后的NRTL 模型[14]计算,见式(10)~(12)。

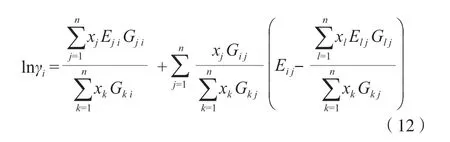
式中,θ为非无规参数;E为交互作用参数;G为Gibbs 自由能,J;γ为活度系数,无因次;j,k分别为组分j、组分k。
1.3 CO2 在水中的溶解度模型
iCPA-HV 模型(式(1)~(12))有4 个拟合参数(α,Ei j,Ej i,Fi j),这4 个拟合参数采用最小二乘法拟合大量文献实验数据(见表1)得到,拟合的目标函数(OF)计算公式见式(13)。

式中,xexp,xcal分别为CO2在水中溶解度的实验值和计算值;i为溶解度的第i个数据点数;n为溶解度数据总的个数。
H2O-NaCl 和CO2-NaCl 体系之间不存在缔合作用,纯组分NaCl 的参数可由SRK 模型计算。对于H2O-CO2,H2O-NaCl,CO2-NaCl 体系,α与温度无关,最优化表1 中的实验数据后分别取α=0.10,-0.78,0.02。由于H2O-NaCl 和CO2-NaCl体系不存在缔合作用,故1-F=0。其余7 个可调节参数见表2(CO2为惰性组分,只接受一个电子与H2O 形成氢键,H2O 的缔合结构为4C)。平均绝对相对误差(AARD)按式(14)计算。

表1 CO2 在水中溶解度数据Table 1 Experimental data for the solubility of CO2 in aqueous solution

由表2 可知,H2O-CO2两组分的交互作用参数(Ei j,Ej i,F)随温度升高而降低,说明高温下水与CO2分子间的交叉缔合作用强度减弱;而H2ONaCl 和CO2-NaCl 体系之间不存在缔合作用,交互作用参数(Ei j,Ej i)与温度之间无明显的变化规律。
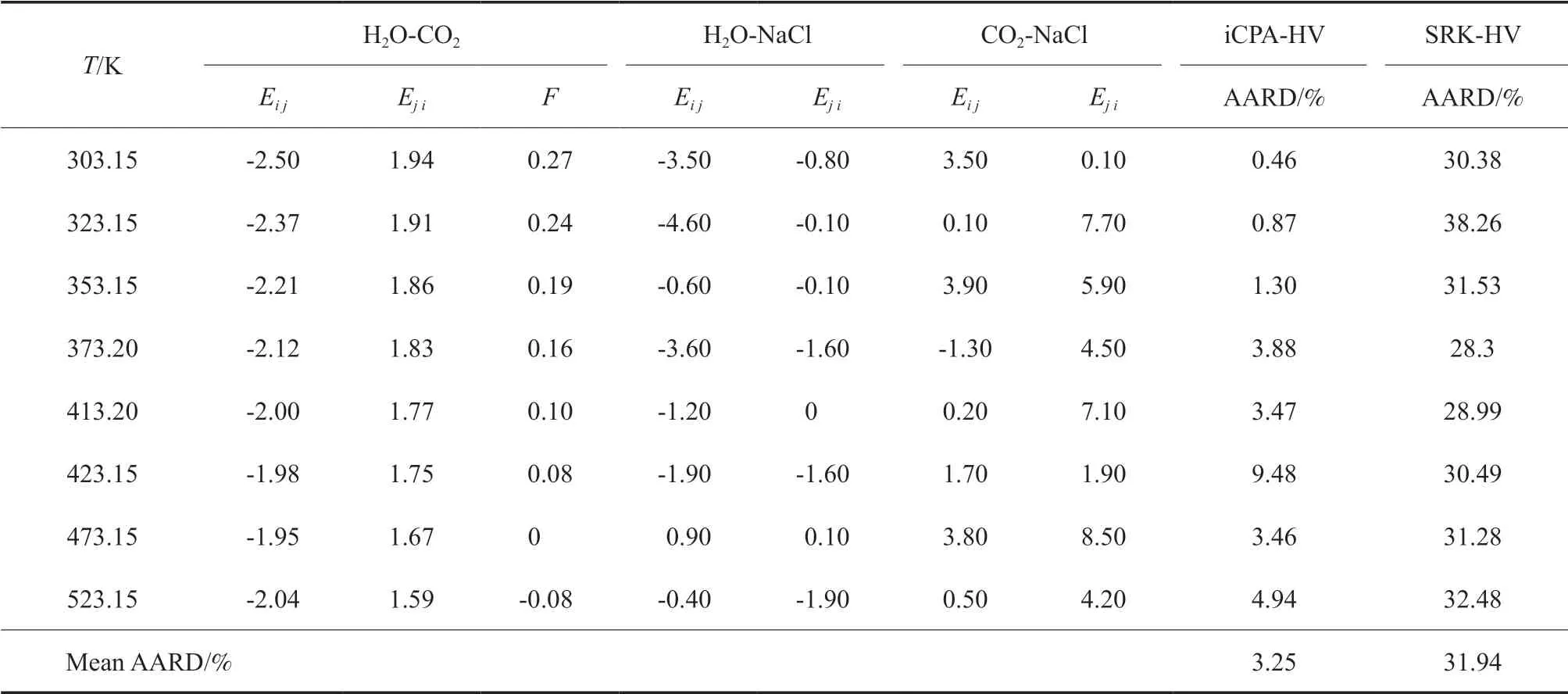
表2 CO2-H2O-NaCl 体系iCPA-HV 模型拟合参数与NaCl 溶液中CO2 溶解度的AARDTable 2 Tuned parameters of iCPA-HV model for the CO2-H2O-NaCl system and average absolute relative error(AARD) of the calculated CO2 solubility in the aqueous NaCl solutions
2 结果与讨论
为验证iCPA-HV 模型的精确性,任选取353 K 下实验数据与模型计算结果进行对比,结果见图1。由图1 可知,该模型能够很好地预测不同压力、不同矿化度下CO2在CO2-H2O-NaCl 体系中的溶解度,AARD 为1.30%。

图1 CO2 在NaCl 溶液中的溶解度(x(CO2))模型预测结果对比(353 K)Fig.1 Comparison of the calculated CO2 solubility in aqueous NaCl solutions(353 K).
不同压力-温度-质量摩尔浓度(M)条件下,iCPA-HV 和SRK-HV 模型预测在不同浓度NaCl 水溶液中CO2溶解度的模型计算结果对比如图2 所示。由图2 可知,在实验数据范围内,整个过程中考虑了H2O-H2O 和H2O-CO2分子之间缔合作用的iCPA-HV 模型的整体预测效果较好(整体AARD为3.25%),相比只考虑了Gibbs 自由能的SRKHV 模型预测结果(AARD 为31.94%),该模型能够准确地预测CO2在不同矿化度的地层水中溶解度。结合表2 可知,在303 ~523 K 范围内,随着温度的升高,iCPA-HV 模型计算结果偏离实验数据增大,说明温度对CO2在NaCl 水溶液中的溶解度影响较大。仔细分析模型计算结果可知,温度、压力相同时,低温低压(T=303 ~413 K,p=0.1 ~15.0 MPa)条件下,随着水溶液中NaCl 的M的增加,iCPA-HV 模型计算结果与实验数据的偏差减小,预测精度提高;高温高压(T=423 ~523 K,p=20 ~130 MPa)条件下,随着水溶液中NaCl 的M增加,iCPA-HV 模型计算结果与实验数据的偏差增大,预测精度减小。温度、M相同时,低温、低浓度(T=303 ~323 K,M=0.170 ~1.091 mol/kg)条件下,iCPA-HV 模型模拟精度变化无明显规律;高温、高浓度(T=353 ~523 K,M=2.50 ~5.99mol/kg)条件下,iCPA-HV 模型预测精度随压力增大而提高。
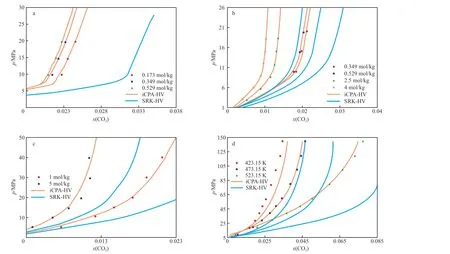
图2 CO2 在NaCl 溶液中的溶解度模型预测结果对比Fig.2 Comparison of the calculated CO2 solubility in aqueous NaCl solutions.
3 结论
1)基于改进的SAFT 模型,利用CPA-SRK状态方程结合GE混合规则,建立了一个能够描述CO2-H2O-NaCl 混合溶液体系的热力学行为,并能够预测CO2在地层水中溶解度的新热力学模型。
2)此模型中含有7 个可调节参数(Ei j,Ej i,F),并考虑了水的自缔合和CO2-H2O 的相互缔合。与SRK-HV 模型对比表明,在较宽泛的温压(303 ~523 K,0.1 ~130.0 MPa)范 围 内,该模型(AARD 为3.25%)相比只考虑了超额Gibbs自由能的SRK-HV 模型(AARD 为31.94%)预测精度较高,能够准确预测CO2-NaCl-H2O 三元混合体系的热力学相平衡计算,为精确描述CO2-NaCl-H2O 体系气体溶解作用提供了一种新思路。

符 号 说 明

η 对比密度,无因次ΔAB 缔合点A和缔合点B处的综合缔合强度,是摩尔体积和缔合能量的函数εAB 缔合能量,(MPa·cm3)/mol θ 非无规参数下角标i,j,k,l 不同的化学组分m 混合组分
