评估前列腺癌患者的前列腺动脉造影表现
2022-01-11田伟徐忠伟周春高冷斌施海彬刘圣
田伟 徐忠伟 周春高 冷斌 施海彬 刘圣
前列腺癌是男性第二大常见的恶性肿瘤,也是全世界癌症相关死亡率的第五大病因[1]。中晚期及转移性前列腺癌患者常合并血尿或下尿路梗阻症状[2]。目前前列腺动脉栓塞术(prostatic artery embolization,PAE)已广泛用于前列腺增生患者下尿路梗阻症、血尿及急性尿潴留的治疗[3-4]。国内外少数研究探索性报道了PAE以及前列腺动脉化疗栓塞术作为前列腺癌姑息性治疗的一种方式[5-6],但这些研究对前列腺癌的血管造影表现却鲜有涉及。本研究旨在探讨前列腺癌患者的前列腺动脉造影表现及造影过程中是否存在异常表现,同时评估异常造影患者PAE治疗下尿路梗阻症状或血尿的疗效情况。
资料与方法
一、研究对象
本研究回顾性分析2014年10月至2019年12月经活检证实为前列腺癌并接受PAE治疗的患者病例资料。通过泌尿外科、介入放射科等多学科评估,将PAE联合近距离放射治疗或化疗作为一种姑息性治疗手段用于前列腺癌患者下尿路梗阻症状、血尿及尿潴留的治疗,同时改善生活质量。入选标准为:(1)存在中重度下尿路症状(症状国际前列腺症状评分(international prostate symptom score,IPSS)≥13和生活质量评分(quality of life,QoL)≥ 3)、血尿或者尿潴留;(2)不适合或拒绝行前列腺根治切除术。排除标准为:全身严重感染、对比剂过敏、凝血功能差、严重肾功能不全、急性前列腺炎、巨大的膀胱憩室、膀胱结石以及随访资料缺失。本研究已经医院伦理委员会批准,并获得患者及家属的知情同意。
共计61例患者纳入研究,平均年龄为(74.7 ±8.2)岁,平均前列腺特异抗原(prostate specific antigen,PSA)为(338.6 ± 145.5)ng/mL。前列腺穿刺活检提示Gleason评分7~10分。所有患者术前接受CT或者MRI检查以评估前列腺情况并依据影像学表现进行TNM肿瘤分期,分期均超过T2aN0M0。经过泌尿外科、介入科等多学科会诊后,一致同意行PAE治疗患者下尿路梗阻或血尿症状。术前48例患者曾接受碘粒子植入治疗,粒子植入与PAE的间隔时间为1~5 d。所有患者在PAE治疗前均签署了手术知情同意书。
二、造影评估及前列腺动脉栓塞
所有患者术前常规留置导尿管,30%~50%浓度对比剂(碘克沙醇,江苏恒瑞)10 mL充盈导尿管球囊,以此作为术中前列腺的解剖定位标志。1%利多卡因局部浸润麻醉下采用改良Seldinger技术穿刺右侧股动脉,导入5 F动脉鞘(Terumo,日本),在DSA透视下引入5 F Cobra 导管(COOK,美国)至左侧髂内动脉造影,造影角度采用同侧斜位35°~55°、头侧10°,以清晰显示前列腺动脉的起源。若髂内动脉造影未发现闭孔动脉及前列腺动脉,则行同侧髂外动脉造影。造影过程中,如果发现肿瘤染色或者动静脉瘘等异常表现,则超选择插管至责任血管进一步造影评估。随后,采用同轴插管方法,在路径图导引下将2.7F Progreat微导管(Terumo,日本)超选择插管至前列腺动脉,造影明确前列腺动脉。根据前列腺动脉造影表现以及与邻近血管的吻合情况,选择合适的栓塞材料。若存在动静脉瘘异常造影表现,则栓塞直径较大的聚乙烯醇(polyvinyl alcohol,PVA,COOK,美国)颗粒(直径 300~500 µm),以避免发生急性肺栓塞等严重并发症。若前列腺动脉与邻近血管存在吻合,则经微导管缓慢注入直径为180~300 μm PVA颗粒栓塞至前列腺动脉完全闭塞;若不存在吻合,则选择直径为90~180 μm PVA颗粒以达到精准栓塞效果。栓塞终点定义为前列腺实质不显影,靶血管内血流淤滞。同理,通过Cobra导管成襻插入右侧髂内动脉,相同的方法栓塞右侧前列腺动脉。
三、术后随访
所有患者术后住院观察3~5 d,记录是否发生并发症及其相关处理措施。同时术后3个月、12个月通过电话或门诊随访患者情况,复查前列腺体积、PSA,评估IPSS及QoL。对于动静脉瘘的患者密切关注PAE的疗效变化及可能发生的并发症。
四、统计学方法
采用SPSS 22.0统计软件进行数据分析。计量资料以平均值±标准差(± s )表示。通过改良Fisher精确检验比较125I粒子植入患者与未植入患者动静脉瘘的发生率。通过配对t检验比较动静脉瘘患者术前及术后各随访时间点IPSS、QoL的变化情况。P < 0.05为差异有统计学意义。
结 果
一、前列腺动脉起源
61例患者完成121侧盆腔造影(1侧盆腔因髂内动脉主干闭塞未造影) (见表1),共显示147支前列腺动脉。95侧(95/121,78.5%)盆腔侧仅有1支前列腺动脉;26侧(26/121,21.5%)盆腔侧存在2支独立的前列腺动脉。前列腺动脉起源包括阴部内动脉(46例,31.3%);膀胱 动脉(40例,27.3%);闭孔动脉(31例,21.1%);臀-阴动脉干(23例,15.7%);臀下动脉(3例,2.0%);阴部副动脉(3例,2.0%);臀上动脉(1例,0.6%)。61例患者中,17例(17/61,27.9%)患者的前列腺动脉起源呈左右对称的特点。此外,前列腺动脉还存在一些非典型起源。2支(2/147,1.4%)前列腺动脉起源于阴部内动脉末端(见图1),并斜行向上供血前列腺。3例髂内动脉造影未发现闭孔动脉及前列腺动脉,通过进一步的同侧髂外动脉造影,发现3支(3/147,2.0%)前列腺动脉起源于髂外动脉的闭孔动脉。
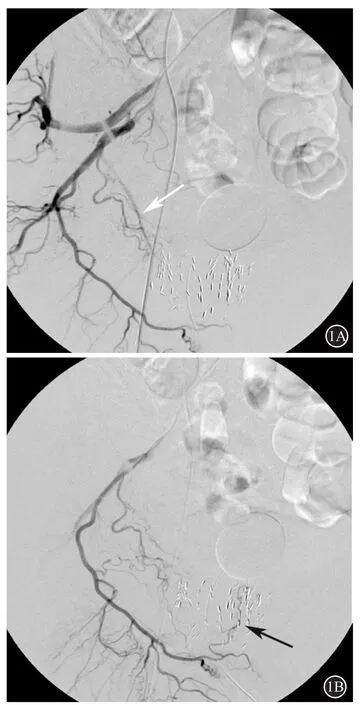
图1 65岁男性,前列腺癌,右侧髂内动脉造影显示两支前列腺动脉(分别起自右侧阴部内动脉的近端和远端)
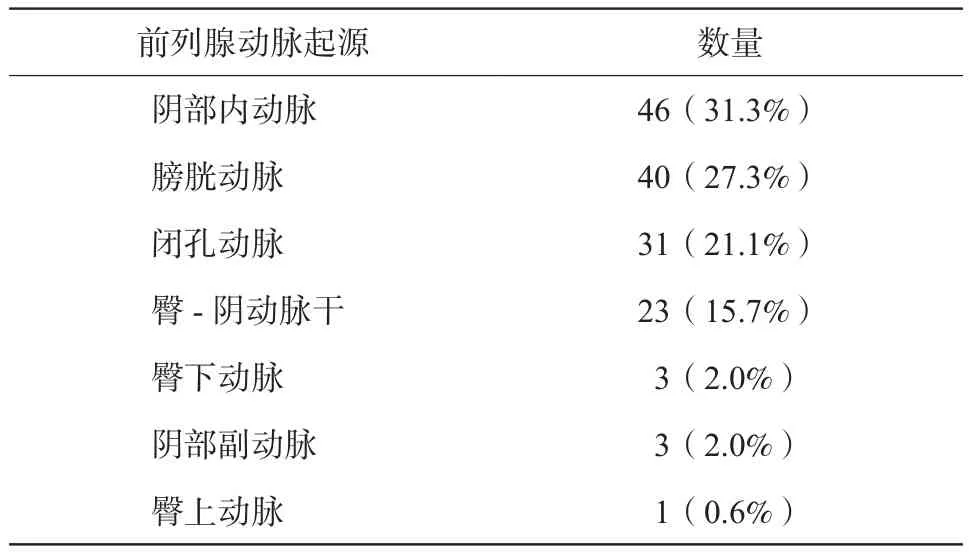
表1 61例患者髂动脉造影前列腺动脉起源分布(n = 61,%)
二、动静脉瘘
有6例患者造影发现存在动静脉瘘(5例发生于125I粒子植入患者,1例发生于未植入125I粒子患者)。造影表现为动脉早期前列腺动脉增粗,远端分支增多、紊乱,其引流静脉早显,且部分动静脉瘘呈弥漫性分布特点(见图2)。当微导管超选择插管至动静脉瘘所累及的动脉造影,其引流静脉充盈、早显更加明显。125I粒子植入患者与未植入患者动静脉瘘发生率对比显示,结果无统计学差异[(10.4%,5/48) vs(7.7%,1/13);P> 0.05]。
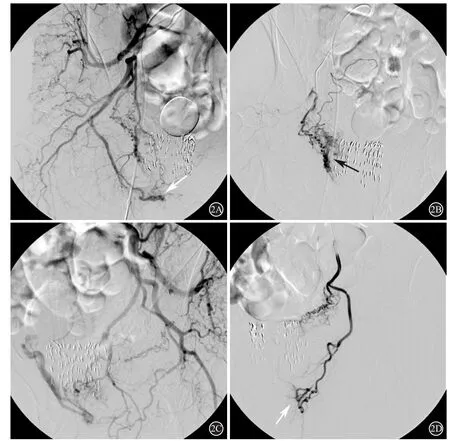
图2 72岁男性,前列腺癌,DSA造影可见动静脉瘘征象
6例动静脉瘘患者临床症状及术前术后IPSS、QoL评分见表2。其中,2例术前血尿患者PAE术后3 d内血尿自发性消失,且12个月内血尿未复发。所有患者术后3、12个月IPSS、QoL均有改善,IPSS由术前(18.2 ± 8.4)改善至术后3个月(9.0 ± 4.1)(P= 0.005),到术后12个月(8.0 ± 4.1) (P=0.006);QoL由术前(4.0 ± 1.7)改善至术后3个月(2.0 ± 1.1) (P= 0.003),到术后12个月(1.7 ±1.0) (P= 0.005),均存在统计学差异。所有患者术后均未出现盆腔脏器缺血坏死等严重并发症。
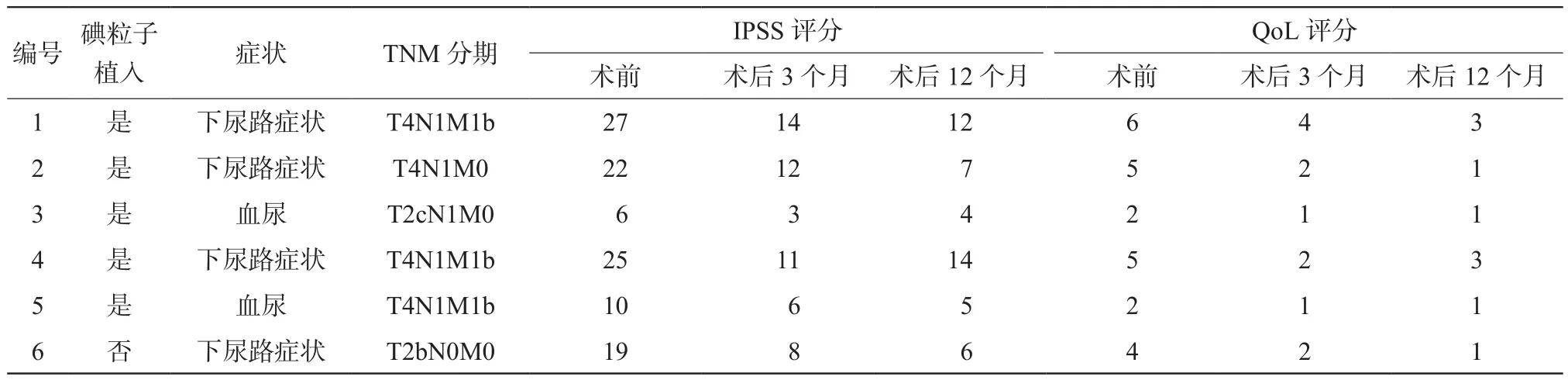
表2 6例动静脉瘘患者术前情况及术后3、12个月IPSS、QoL评分
讨 论
PAE成功的前提是正确识别盆腔内血管及前列腺动脉的解剖。然而,由于盆腔内血管及前列腺动脉存在解剖学变异、动脉粥样硬化、局部血管迂曲闭塞等特征,使得前列腺动脉识别与插管变得复杂且困难[8]。尽管许多研究已经报道了前列腺动脉的造影表现,但大多局限于尸体解剖或前列腺增生患者[9-14],前列腺癌患者的动脉造影表现鲜有涉及。本研究结果显示,前列腺癌患者的血管形态较前列腺增生患者略有不同,前列腺癌患者前列腺动脉管径增粗,远端分支增多、紊乱,肿瘤血管细小杂乱,而增生患者前列腺动脉大多呈现螺旋状结构,较为规则、粗细均一[15]。但前列腺癌患者前列腺动脉主要起源与前列腺增生基本相似,包括阴部内动脉、膀胱动脉、闭孔动脉、臀-阴动脉干。同时,我们发现部分前列腺动脉起源于阴部内动脉末端和闭孔动脉(髂外动脉发出),这与Bhatia等[16]的研究结果类似。在本研究成功造影的121侧盆腔中,95侧(95/121,78.5%)盆腔侧只有1支前列腺动脉,26侧(26/121,21.5%)盆腔侧存在2支独立的前列腺动脉。这项结果与既往文献中的结果存在差异。Bilhim等[17]在2010年通过50例盆腔造影发现24%的单侧盆腔存在两支前列腺动脉;随着时间的推移,样本量逐渐扩大,2012年Bilhim等[9]在150例盆腔造影中发现单侧盆腔存在两支前列腺动脉的比例达43%。随后Zhang[11]和Wang[10]在DSA的基础上结合锥体束CT发现单侧盆腔存在两支前列腺动脉的比例分别为3.6%和7.4%。这在一定程度上印证了DeMerit等[18]的研究结果,即前列腺内部可能存在多个血管室间隔,需要多支前列腺动脉参与供血。但各研究间比例又不尽相同,这可能与研究人群、检查手段及认知差异有关。
本组病例中,6例患者行髂内动脉造影可见动静脉瘘。这种动静脉瘘的形成是盆腔内动脉与周围静脉之间的异常沟通所致,究其原因,我们推测存在以下原因:(1)前列腺活检或者125I粒子植入所致的医源性动静脉瘘。尽管统计学结果提示动静脉瘘的发生率在125I粒子植入与未植入人群中无显著差异,但是由于纳入样本量较小,存在选择偏倚等因素的影响,不能否认125I粒子植入会造成医源性动静脉瘘的可能。另外,PAE术前前列腺穿刺活检可能与动静脉瘘的产生也存在一定的相关性。(2)肿瘤侵犯邻近血管导致动静脉瘘。6例动静脉瘘患者中有4例TNM分期超过T4N0M0;MRI提示前列腺肿瘤巨大且形态不规则,已侵犯膀胱、直肠或精囊,而前列腺周围还存在着丰富血管,当多处静脉血管壁被肿瘤侵蚀时,可出现弥漫性分布的动静脉瘘。因此,医生栓塞过程中需要留意动静脉瘘,避免非靶器官异位栓塞不良事件的发生。本组6例动静脉瘘患者,术中均先用大颗粒PVA(300~500 μm)栓塞动静脉瘘,然后根据周围血管的吻合情况选择合适的PVA颗粒(90~180 μm或180~300 μm)栓塞前列腺动脉,术后短中期内取得了较好的疗效,同时住院期间及随访期内未出现盆腔脏器缺血坏死等严重并发症。
本研究也存在一些不足:本研究是单中心、回顾性研究,观察样本量偏小,研究结果存在局限性;本研究中前列腺动脉评估单纯使用DSA,术前缺乏CTA、MRA或锥体束CT等检查进一步分析,然而DSA对部分微小供血动脉显影不如锥体束CT以及MRA灵敏;未评估前列腺穿刺活检与动静脉瘘的关系。
综上所述,前列腺癌患者的前列腺动脉起源主要有阴部内动脉、膀胱上动脉、闭孔动脉、臀-阴动脉干,与前列腺增生患者基本相似。此外,部分前列腺癌患者存在动静脉瘘这一异常造影表现,但只要术中选择合适栓塞材料,PAE治疗前列腺癌源性下尿路梗阻及血尿症状仍然是安全、有效的。
