腹腔镜卵巢巧克力囊肿剥除术后应用GnRH-a对患者残留卵巢储备功能及复发率的影响因素分析
2022-01-08林丽张汉英张利
林丽,张汉英,张利
(深圳市龙华区人民医院 妇科,广东 深圳 518109)
卵巢巧克力囊肿为子宫内膜异位症常见的疾病类型,多见于25~45 岁育龄妇女[1]。流行病学统计显示,不孕症患者中约有20%~35%患者伴发卵巢巧克力囊肿,严重影响了育龄妇女的生活质量及家庭和谐[2]。腹腔镜卵巢巧克力囊肿剥除术作为临床治疗卵巢巧克力囊肿的首选方法,但有较多研究报道指出,该术式会降低患者卵巢储备功能,导致患者术后自然妊娠率低,且患者术后复发率仍较高[3-4]。有研究表明,术后应用促性腺激素释放激素激动剂(GnRH-a)能够促使残留病灶处于较低的雌激素环境,从而改善患者的卵巢功能[5]。但较多研究采用测定基础性激素评估术后卵巢储备功能,由于性激素容易受到诸多因素影响而产生较大波动,对卵巢功能的评估容易造成偏差。本研究选用卵巢功能评价敏感指标,用以评估腹腔镜卵巢巧克力囊肿剥除术后应用GnRH-a 对年轻患者残留卵巢储备功能的影响,现报道如下。
1 资料与方法
1.1 一般资料
选取2016 年1 月至2017 年12 月深圳市龙华区人民医院妇科收治的120 例育龄妇女卵巢巧克力囊肿患者作为研究对象,根据患者术后是否接受GnRH-a 治疗将其分为对照组和观察组,每组60 例。对照组年龄20~35 岁,平均(28.5±4.2)岁;病程6~18 个月,平均(14.6±3.5)个月;囊肿直径4.3~10.8,平均(7.5±1.5)cm;参照美国生育协会分期标准(r-AFS)[6]:Ⅰ期10 例,Ⅱ期23 例,Ⅲ期18 例,Ⅳ期9 例;观察组年龄20~35岁,平均(28.8±4.0)岁;病程6~18 个月,平均(14.2±3.9)个月;囊肿直径4.2~10.6 cm,平均(7.4±1.2)cm;r-AFS 分期:Ⅰ期11 例,Ⅱ期21例,Ⅲ期18,Ⅳ期10 例。纳入标准:①术前经超声检查、血清肿瘤标志物(癌抗原125、甲胎蛋白、癌胚抗原)检查及临床症状诊断为卵巢巧克力囊肿,且经术后标本病理检查证实;②卵巢巧克力囊肿且为初次入院接受治疗;③年龄20~35 岁,已婚;④有明确的生育需求,性生活正常,患者双侧输卵管通畅,卵巢功能正常,男方精液正常;⑤患者及其家属知情同意。排除标准:①合并腹腔镜手术及GnRH-a 使用禁忌症;②近6 个月接受过激素类药物治疗;③怀疑或确诊恶性肿瘤;④内分泌疾病、血液系统疾病及严重的肝、肾功能障碍;⑤精神性疾病、认知功能障碍;⑥随访困难。本研究通过医院伦理委员会批准。两组年龄、病程等基线资料比较,差异无统计学意义(P>0.05)。
1.2 方法
两组患者均行卵巢巧克力囊肿腹腔镜剥除术:术前常规禁食8 h,禁饮4 h,取膀胱截石位,气管插管全身麻醉,于脐上缘作约1 cm 切口并穿刺10 mm Trocar、建立气腹,维持压力12~15 mmHg,并置入腹腔镜;分别于右下腹、左下腹麦氏点、左上腹穿刺5 mm Trocar 作操作孔;腹腔镜下仔细探查囊肿具体情况,常规分离盆腔粘连组织后,于囊肿无血管部位以单极电凝作约1 cm 切口。采用负压吸引装置吸出囊液,同时以生理盐水反复冲洗囊腔至囊液清澈;而后剪开囊肿壁,明确正常皮质与囊肿壁界限后行剥除术,同时在生理盐水冲洗下明确出血点,明显出血点行点状电凝止血,并用可吸收缝线缝合卵巢皮质重塑卵巢,将剥除囊壁取出后立即置入标本袋送病理活检;术中注意对双侧输卵管的保护,并置入宫腔管,行美兰通液;术毕以大量生理盐水灌洗腹腔,常规放置引流管。观察组术后于月经来潮次日肌肉注射醋酸曲普瑞林(法国Ipsen Pharma Biotech 公司,注册证号H20140298)3.75 mg,间隔28 d 注射1次,共3 次;对照组术后不给于任何激素药物治疗。
1.3 观察指标
1.3.1 卵巢储备功能 分别于术前月经第2、3 天和术后第3 次月经的第2、3 天采集两组患者静脉血液5 mL、肝素钠抗凝;以5 000 r/min 离心取血清,-20℃保存待测。采用酶联免疫法检测血清样品中抗缪勒管激素(AMH)、抑制素B(INHB),使用仪器为全自动酶免分析仪(意大利Adaltis 公司,型号:Nexgen Four),检测试剂盒均购自美国RD 公司;采用化学发光法检测血清中促卵泡激素(FSH)水平,使用仪器为全自动化学发光免疫分析仪(美国贝克曼库尔特公司,型号:DxI800),试剂盒购置瑞士罗氏公司。分别于术前和术后6个月患者月经周期结束后第3~7 天行阴道彩色超声计数窦状卵泡计数(AFC),超声仪为荷兰飞利浦公司HDI5000,探头频率为5~9 MHz。
1.3.2 骨密度及骨代谢 于治疗前和术后3 个月采用双能X 射线吸收骨密度仪(美国GE 公司,型号:Prodigy)测定患者腰椎(L1~L4)骨密度(L-BMD),并采集患者清晨静脉血液采用铜蓝比色法检测血钙、血磷等骨生化代谢指标。
1.3.3 临床疗效 于术后6 个月评定临床疗效:①显效为疼痛等临床症状(痛经、腹痛、性交痛)消失,病灶完全消失;②有效为疼痛症状明显减轻,盆腔病灶缩小;③无效为疼痛症状未见明显改善或加重,盆腔病灶未缩小或增大。总有效率=(显效+有效)例数/总病例数×100%。
1.3.4 随访 患者出院后第3、6、12、18、24 个月采用电话或门诊等方式随访,记录患者自然妊娠情况及术后复发情况。术后>2 次月经周期后超声检查提示盆腔卵巢囊肿病灶原有疼痛症状复发或盆腔结节触痛加重、或血清癌抗原125>35 IU/mL均判定为复发;
1.4 统计学方法
数据分析采用SPSS 20.0 统计软件。计量资料以均值±标准差(±s)表示,比较用t检验;计数资料以率(%)表示,比较用χ2检验,等级资料比较用秩和检验,P<0.05 为差异有统计学意义。
2 结果
2.1 两组手术前后残留卵巢储备功能比较
两组术前血清AMH、INHB、FSH 及AFC 比较,差异无统计学意义(P>0.05)。两组术后3 个月血清AMH、INHB、AFC 均较术前降低,而FSH较术前增高,差异有统计学意义(P<0.05)。见表1。
表1 两组手术前后残留卵巢储备功能比较(n=60,±s)
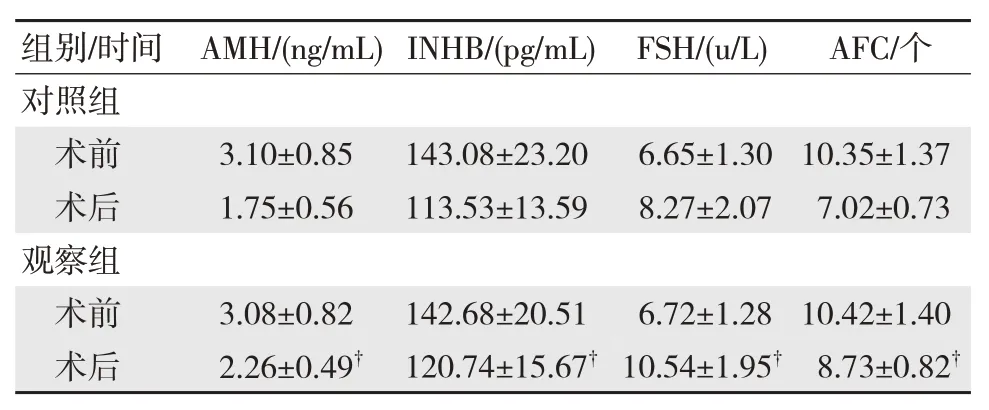
表1 两组手术前后残留卵巢储备功能比较(n=60,±s)
注:†与同期对照组比较,P<0.05。
2.2 两组手术前后骨密度及骨代谢变化水平比较
两组术前L-BMD 和钙、磷水平比较,差异无统计学意义(P>0.05)。两组术后3 个月L-BMD 和钙、磷水平较术前无明显变化,差异无统计学意义(P>0.05)。见表2。
表2 两组手术前后骨密度及骨代谢变化水平比较(n=60,±s)
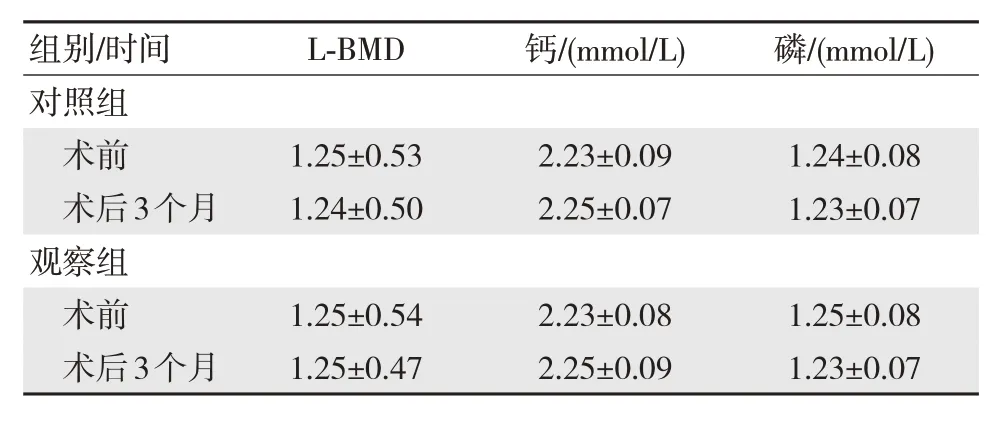
表2 两组手术前后骨密度及骨代谢变化水平比较(n=60,±s)
2.3 两组治疗后临床疗效比较
观察组术后6 个月临床疗效优于对照组,差异有统计学意义(P<0.05)。见表3。

表3 两组治疗后临床疗效比较 [n=60,n(%)]
2.4 两组术后妊娠终局及复发情况比较
两组r-AFS 分期Ⅰ~Ⅱ期妊娠率比较,差异无统计学意义(P>0.05)。两组r-AFS 分期Ⅲ~Ⅳ期妊娠率比较,差异有统计学意义(P<0.05)。观察组总妊娠率优于对照组,而复发率低于对照组,且复发时间较对照组延长,差异有统计学意义(P<0.05)。见表4。

表4 两组术后妊娠及复发情况比较(n=60)
3 讨论
卵巢巧克力囊肿为年轻育龄妇女常见的疾病,该病症存在较高的恶变性,随着病情的进展会累及单侧或双侧卵巢,患者常表现为慢性盆腔疼痛、痛经、性交痛、月经不调、不孕等症状。腹腔镜剥除术能够迅速去除病灶、控制病情,其具有切口小、出血少、恢复快等优势。但对术者操作技术要求较高,容易残留病灶,尤其术中囊壁破裂导致囊液外溢,会增加病灶细胞扩散风险;同时该术式容易损伤正常卵巢组织,造成性激素紊乱,从而降低患者术后妊娠率[7]。术后应用3~6 个周期GnRH-a 已成为减小腹腔镜剥除术对卵巢功能的影响和提高患者术后妊娠率的常用方法。目前,GnRH-a 为公认的治疗卵巢巧克力囊肿的有效药物,该药物能够高效结合垂体内促性腺激素释放激素受体,抑制垂体促性腺激素分泌功能,从而促进卵巢排卵,加速分泌促性腺激素,通过负反馈引起雌激素降低[8]。有研究显示,GnRH-a 还能抑制囊肿周围组织炎症反应,减缓炎症介质对卵巢的刺激作用[9]。目前已有较多研究显示,腹腔镜术后给予GnRH-a 治疗能够有效保护卵巢功能,但大多以性激素水平评定卵巢功能的变化,并未对卵巢储备功能作出评价,且机体性激素水平容易受到年龄、饮食、基础疾病等多方面因素影响,对卵巢功能的评估可能产生偏倚。AMH 为公认的卵巢储备功能评价指标,其能敏感地反应卵巢储备功能变化[10];而INHB 能够反馈性抑制FSH 分泌,同时FSH 能够促进颗粒细胞分泌INHB,其为评估卵巢储备功能直接而有效的指标[11]。顾媚等[12]研究认为,AMH、INHB 水平与卵巢储备功能呈正比关系,两者联合检测能够提高卵巢储备功能评估准确性。
本研究结果显示,两组术后3 个月血清AMH、INHB 均较术前降低,而观察组AMH、INHB 降低幅度小于对照组,同时结合FSH 及AFC 分析,观察组FSH 增高幅度大于对照组,而AFC 较低幅度小于对照,进一步证实了术后应用GnRH-a 能够改善患者卵巢储备功能,为术后自然妊娠提供良好的条件。本研究6 个月临床疗效评价结果显示,观察组临床总有效率较对照组明显提升,且观察组总妊娠率显著优于对照组,比较有差异,与文献报道结果基本一致[13-14]。提示腹腔镜术后应用GnRH-a 较单纯腹腔镜手术治疗卵巢巧克力囊肿能够获得更佳的临床疗效,且能显著提升患者术后自然妊娠率。卵巢巧克力囊壁与卵巢皮质界限不清导致手术在切除病灶的同时,损伤大量正常卵巢滤泡,同时术中电凝止血容易对卵巢供血产生影响,降低卵巢的反应性,引起储备能力下降[15];而术后应用GnRH-a 能够较长时间促使卵巢处于低雌激素状态,致使残留病灶细胞饥饿死亡,保护卵巢功能;同时GnRH-a 对炎症反应的抑制作用能够促进卵巢功能迅速恢复,改善子宫内膜容受性,改善临床症状,提高术后自然妊娠率。值得注意的是,两组r-AFS 分期Ⅰ~Ⅱ期妊娠率比较无差异,而r-AFS 分期Ⅲ~Ⅳ期妊娠率比较有差异,其原因可能为r-AFS 分期Ⅰ~Ⅱ期患者盘腔内粘连不严重,腹腔镜手术能较好分离病灶,对卵巢储备功能影响较小;而r-AFS 分期Ⅲ~Ⅳ期患者盆腔粘连相对严重,腹腔镜手术清除病灶难度大,且易切除正常卵巢组织,而术后GnRH-a 治疗对残留病灶发挥治疗作用,最大限度的保留卵巢储备功能,从而提高了术后妊娠率。
另外本研究结果还显示,观察组复发时间较对照组明显延长,观察组复发率显著低于对照组,比较有差异,与文献报道结果相符[16]。提示腹腔镜术后应用GnRH-a 能有效延长患者复发时间,降低复发率。有研究显示,病灶组织残留和激素持续刺激是卵巢巧克力囊肿复发的高风险因素[17]。GnRH-a 能维持患者术后低雌性激素水平,从而促进异位内膜萎缩和退化,使残留病灶细胞发生缺血、坏死,从而降低术后复发率;而复发时间的延长能为患者提供充足的备孕时间,尤其对高龄妇女具有重要的意义。同时本研究发现,GnRH-a应用后观察组骨密度及骨代谢指标均无明显变化,表明本研究治疗方案未对患者骨密度及骨代谢产生影响。雌激素能对抗甲状旁腺素的骨吸收作用,维持正常骨代谢,并能促进消化道及肾对钙的吸收及钙盐、磷盐在骨质中沉积。而GnRH-a 所致的低雌激素水平,可能会引起骨丢失。本研究术后应用3个周期的GnRH-a 后未发现患者出现骨代谢改变,分析其原因可能为虽GnRH-a 应用后雌激素水平降低,但仍使其维持在治疗窗浓度(110~146 pmol/L)[18],其既有效抑制了病灶细胞增殖和浸润,又避免了副作用的发生。当然,指导推荐GnRH-a 治疗不应>6 个月,延长治疗周期后是否有利于提高妊娠率,是否会产生副作用仍有待进一步研究。
综上所述,腹腔镜卵巢巧克力囊肿剥除术后应用GnRH-a 能够有效保护育龄患者残留卵巢储备功能,提高术后自然妊娠率、降低复发率,并对骨代谢无影响,尤其有利于r-AFS 分期Ⅲ~Ⅳ期患者,值得临床推广应用。
