血清sST2、PCⅢ、LN及HA诊断老年高血压合并心肌肥厚的临床价值
2022-01-07白洁,朵杰,周茜
白 洁,朵 杰,周 茜
据统计,我国原发性高血压病人超过2亿人,成年人高血压患病率在20%以上,高血压已被证实为诱发心脑血管疾病的重要病因[1]。心室是高血压常累及的靶器官,左心室肥厚(心肌肥厚)可能增加心血管不良事件发生率及死亡率,故对高血压合并心肌肥厚的诊断极为重要,采取积极的治疗措施可改善病人预后。影像学手段诊断心肌肥厚均有一定的局限性,各种血清学指标可辅助应用于心肌肥厚的诊断[2]。相关研究显示,血清可溶性ST2(sST2)、Ⅲ型前胶原(PCⅢ)、层黏连蛋白(LN)、透明质酸(HA)与心肌肥厚进程相关[3-5]。本研究分析血清sST2、PCⅢ、LN及HA诊断老年高血压合并心肌肥厚的临床价值。
1 资料与方法
1.1 病例选择标准
1.1.1 诊断标准 高血压诊断参照中国高血压指南推荐的诊断标准[6];左心室肥厚诊断参照《亚洲高血压合并左室肥厚诊治专家共识》[7]中相关标准。
1.1.2 纳入标准 年龄≥60岁;原发性高血压,符合相关诊断标准;正在口服降压药治疗。
1.1.3 排除标准 继发性高血压;参与研究前6个月有急性心肌梗死、不稳定型心绞痛、慢性心力衰竭急性加重史;合并扩张型心肌病、肥厚性心肌病、先天性心脏病等其他类型心脏疾病人;糖尿病血糖控制不佳;合并外周血管疾病、恶性肿瘤、自身免疫性疾病、肝胆疾病等。
1.2 一般资料 选取2017年1月—2020年1月我院收治的133例老年高血压病人为研究对象,所有病人均行心脏彩超检查,获得相关指标后计算左室质量指数(LVMI),根据《亚洲高血压合并左心室肥厚诊治专家共识》相关标准将病人分为高血压组(96例)与高血压合并心肌肥厚组(37例),同时选取同期健康体检者为对照组(50名)。
1.3 方法
1.3.1 一般资料收集 病人一般资料包括入院时体质指数(BMI)、空腹血糖、收缩压(SBP)、舒张压(DBP)、总胆固醇(TC)、三酰甘油(TG)、高密度脂蛋白胆固醇(HDL-C)、低密度脂蛋白胆固醇(LDL-C)。
1.3.2 心脏彩超检查 心脏彩超均由专业心脏彩超医生进行。检查前病人休息15 min,保持呼吸平稳,检查时病人取仰卧位,按照美国心脏彩超协会推荐的方法进行检查,收集室间隔舒张末期厚度(IVSTD)、左室后壁舒张末期厚度(LVPWTD)、左室舒张末期内径(LVEDD)、左室质量(LVM)等参数,计算LVMI,LVMI=LVM/体表面积(BSA)。男性LVMI>125 g/m2,女性>120 g/m2时,即诊断为左心室肥厚。
1.3.3 血清生化指标 采集所有研究对象空腹静脉血10 mL,注入含EDTA无菌试管,以3 000 r/min离心10 min,分离上层血清,置于-80 ℃冰箱保存待用。将待测血清样本取出,逐渐解冻至-20 ℃、4 ℃至最终平衡至室温后,采用酶联免疫吸附法测定血清sST2水平,试剂盒由Abclonal公司提供;放射免疫法检测PCⅢ水平,试剂盒由北京京华英生物制品研究所提供;LN、HA均采用放射免疫法检测,试剂盒均由上海海军医学研究所生物技术中心提供。
1.4 观察指标 ①比较对照组、高血压组及高血压合并心肌肥厚组临床资料。②比较对照组、高血压组与高血压合并心肌肥厚组血清sST2、PCⅢ、LN及HA水平。③分析高血压合并心肌肥厚组LVMI与血清sST2、PCⅢ、LN及HA水平之间的相关性。④绘制受试者工作特征(ROC)曲线,分析血清sST2、PCⅢ、LN及HA诊断高血压合并心肌肥厚的临床价值。
2 结 果
2.1 3组临床资料比较(见表1)
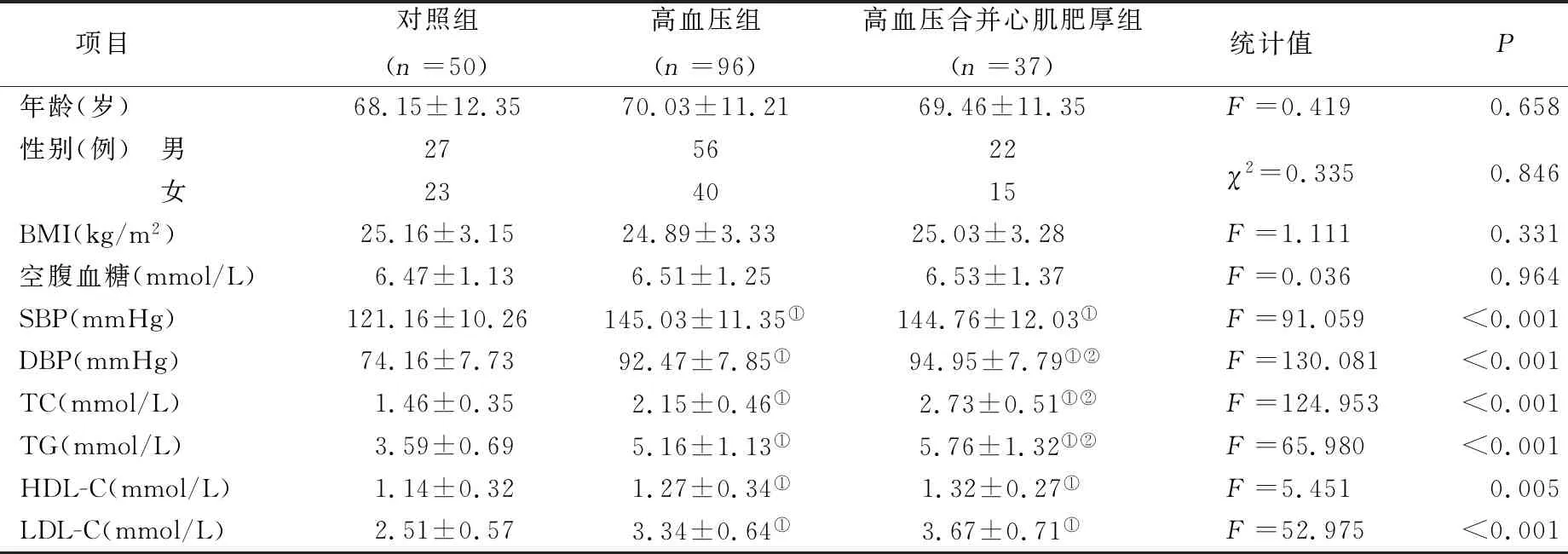
表1 3组临床资料比较
2.2 3组血清sST2、PCⅢ、LN及HA水平比较 对照组及高血压组血清sST2、PCⅢ、LN及HA水平均低于高血压组合并心肌肥厚组(P<0.05)。详见表2。

表2 3组血清sST2、PCⅢ、LN及HA水平比较(±s)
2.3 高血压合并心肌肥厚病人LVMI与血清sST2、PCⅢ、LN及HA水平的相关性 相关性分析结果显示,高血压合并心肌肥厚病人血清sST2、PCⅢ、LN及HA水平均与LVMI呈正相关(P<0.05)。详见表3。
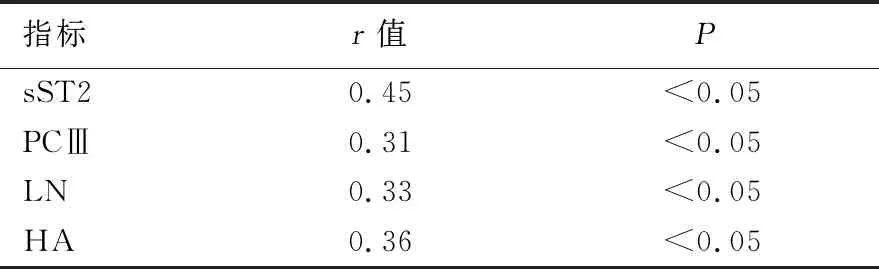
表3 高血压合并心肌肥厚病人LVMI与血清sST2、PCⅢ、LN及HA水平的相关性分析
2.4 血清sST2、PCⅢ、LN及HA诊断高血压合并心肌肥厚的临床价值 血清sST2诊断高血压合并心肌肥厚的ROC曲线下面积(AUC)为0.751[95%CI(0.640,0.861)],灵敏度、特异度分别为70.30%和80.00%。详见表4、图1。
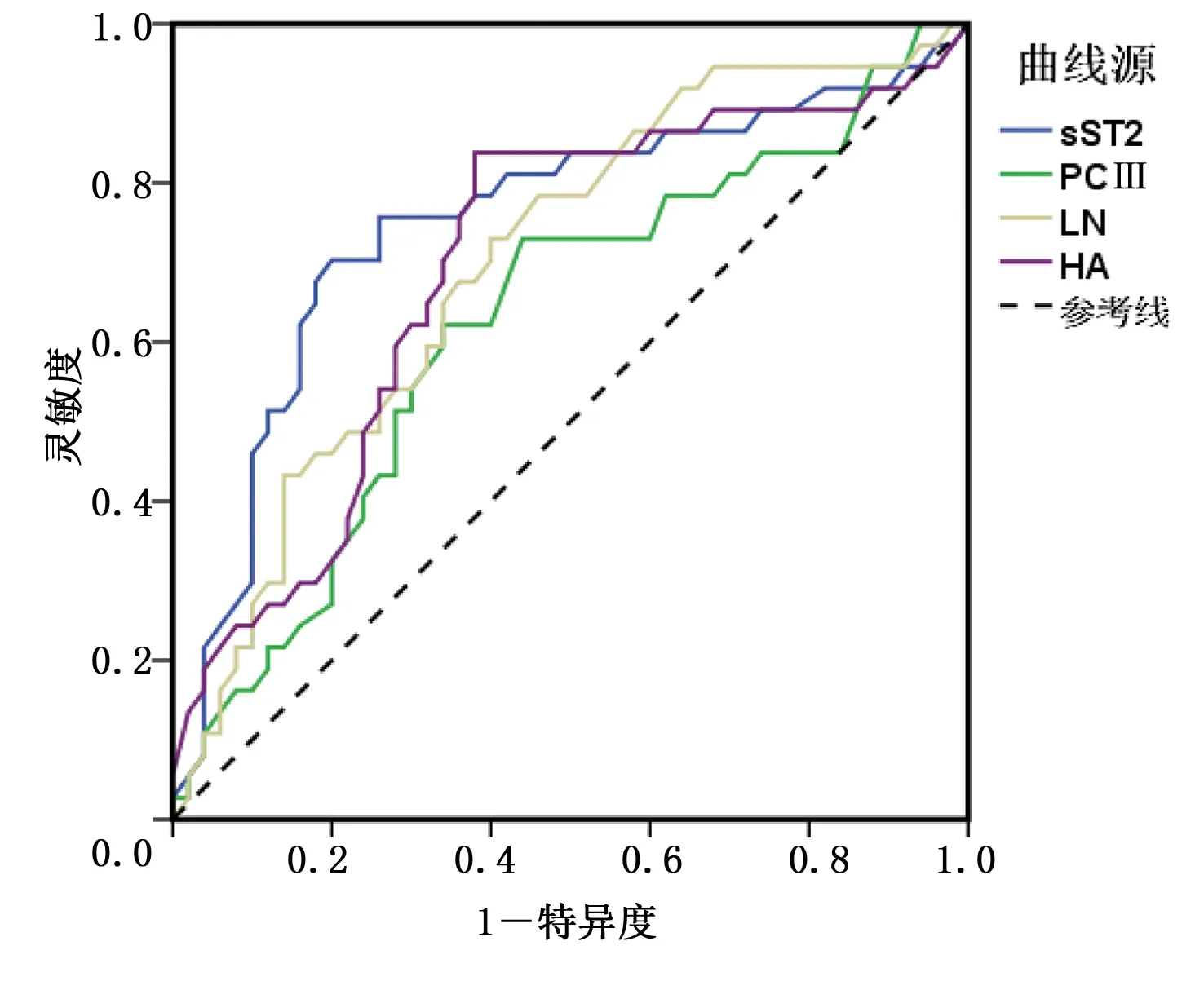
图1 血清sST2、PCⅢ、LN及HA诊断高血压合并心肌肥厚的ROC曲线

表4 血清sST2、PCⅢ、LN及HA诊断高血压合并心肌肥厚的临床价值
3 讨 论
目前,诊断高血压合并心肌肥厚主要依靠心电图、心脏彩超、心脏磁共振成像等影像学手段,其中心电图检查价格低廉、操作简单,是基层医院诊断高血压合并心肌肥厚的主要方式,但其诊断敏感度较低[8]。心脏彩超诊断敏感度较高,但受到超声波投照方向、检查者手法等因素影响,其诊断效能受到限制[9]。心脏磁共振成像检查具有可重复性高、敏感度高等优势,但病人体位运动可能产生明显伪影,对诊断造成干扰,且心脏磁共振成像检查费用高,不适于临床推广[10]。高血压合并心肌肥厚的病理及生理机制尚不明确,可能与血流动力学及神经体液因素密切相关,故血清学指标逐渐应用于高血压合并心肌肥厚的诊断。
人ST2基因属于白细胞介素(IL)-1R/Toll样受体(TLR)超家族的一员,sST2是ST2基因编码的主要成员,当外界因素刺激肌细胞或成纤维细胞时,引起IL-33/ST2信号通路高表达,导致IL-33与受体ST2L相互作用,保护心肌细胞。有研究显示,sST2与心肌肥厚、纤维化及心室功能障碍等密切相关,血清sST2升高时可预测心肌梗死病人不良预后、急诊胸痛病人预后及心力衰竭[11]。本研究结果显示,对照组与高血压组血清sST2水平比较,差异无统计学意义;高血压合并心肌肥厚组血清sST2水平高于对照组与高血压组。相关性分析结果显示,高血压合并心肌肥厚病人血清sST2水平与LVMI呈正相关;绘制ROC曲线,血清sST2水平>22.31 ng/mL,诊断高血压合并心肌肥厚的AUC为0.751,95%CI[0.640,0.861],灵敏度、特异度分别为70.30%和80.00%。推测sST2水平不仅与急性心血管事件相关,还可反映左室肥厚,与心室心肌重构密切相关,可用于预测心脏结构与功能改变[12]。
随着分子细胞生物学不断发展,有研究显示,组织神经内分泌激素在高血压合并心肌肥厚中发挥着重要作用,PCⅢ等生物活性物质进入组织间隙,促进成纤维细胞合成胶原及心肌细胞肥大[13]。Ⅲ型胶原有优良的伸展回弹性,形成纤维网,与Ⅰ型胶原纤维共同维持心脏结构与功能完整性。PCⅢ是Ⅲ型前胶原氨基肽(PⅢP)前体,在心肌细胞中PCⅢ分子量大,血清含量受炎症影响小,血清PCⅢ可作为心肌纤维化无创及特异性生化检测指标。本研究结果显示,高血压组和高血压合并心肌肥厚组血清PCⅢ水平均高于对照组,提示PCⅢ参与高血压及高血压合并心肌肥厚的发生与发展;高血压合并心肌肥厚组血清PCⅢ水平高于高血压组,提示PCⅢ可反映心肌肥厚[14]。本研究结果显示,高血压合并心肌肥厚病人血清PCⅢ水平与LVMI呈正相关,绘制ROC曲线,血清PCⅢ水平>104.35 μg/L时诊断高血压合并心肌肥厚的AUC为0.626,95%CI[0.506,0.746],灵敏度、特异度分别为73.00%和56.00%,说明PCⅢ是反映高血压病人心肌胶原合成活跃程度与心肌纤维化的敏感指标。
心肌肥厚过程中,除胶原纤维大量合成聚集外,其他成分在间质的积累也影响心肌肥厚进程。LN属于非胶原糖蛋白,促进成纤维细胞增生,是心肌纤维化的重要标志物[15]。HA是亲水性糖胺多糖,是真皮成纤维细胞的分泌产物,引起间质水肿,形成血管周围间质纤维化[16]。LN及HA均参与心肌纤维化进程,是纤维化的常见血清标志物。本研究结果显示,与对照组及高血压组比较,高血压合并心肌肥厚组血清LN及HA水平升高,且血清LN及HA水平与LVMI呈正相关,绘制ROC曲线,血清LN水平>135.92 μg/L时诊断高血压合并心肌肥厚的AUC为0.701,95%CI[0.590,0.811],灵敏度、特异度分别为73.00%和60.00%;血清HA水平>102.00 μg/L时,诊断高血压合并心肌肥厚中的AUC为0.696,95%CI[0.581,0.811],灵敏度、特异度分别为83.80%和62.00%,两者诊断效能相似。
综上所述,血清sST2、PCⅢ、LN及HA均可用于诊断高血压合并心肌肥厚,其中血清sST2诊断价值最高。
