川崎病合并冠状动脉损害的研究进展
2022-01-07李建泳吴雅娟
李建泳 吴雅娟
528200 佛山,广东省人民医院南海医院儿科
川崎病(Kawasaki disease,KD)是一种通常发生在婴幼儿童的、未知病因的血管炎症,尽管病因不明,但普遍认为自身免疫、感染及遗传易感性是该病的重要参与因素[1]。KD很少发生于成人,病程以自限性为主,发热和急性炎症表现多见,病程平均持续12 d而无须特殊治疗[2]。
然而,患有KD的儿童有严重的心血管并发症的风险。患者的预后与冠状动脉瘤(coranary artery aneurysm,CAA)瘤体的大小和持续时间等均密切相关,病变严重的患者管腔内可见血栓形成或内膜增厚,可导致冠状动脉狭窄,造成心肌缺血、梗死,甚至猝死[3]。日本循环学会(JCS)联合日本心脏外科学会(JSCS)2020年共同发布了《川崎病心血管后遗症的诊断和管理指南(JCS/JSCS 2020)》,系统介绍了KD心血管后遗症的诊疗和管理新进展[4]。本文总结性回顾了KD合并冠状动脉损害(coronary artery damage,CAD)的评估、诊断、治疗和远期管理及随访等方面的临床研究进展,以期为改善患者预后提供更多资料。
1 定义和流行病学
早期KD主要表现为无动脉粥样硬化性的坏死性全动脉炎,炎性细胞的浸润冠状动脉可导致动脉中膜和内膜弹性层的破裂及坏死[5]。尽管目前静脉应用人免疫球蛋白(intravenous immunoglobulin,IVIG)治疗KD已经较为广泛,但我国KD急性期发生CAD的发生率仍较高。近期的一项流行病学调查,纳入2013—2017年上海地区的50家医院确诊的4 452例KD患儿,结果提示IVIG的应用率高达97.0%,8.4%患者表现为IVIG抵抗,9.1%患者表现为CAD,2.7%表现为CAA,0.7%表现为巨大冠状动脉瘤(giant CAA,GCAA)[6]。
2 CAD表现
研究发现,CAD多位于心外膜冠状动脉中,最常见于左前降支近端和右冠状近端,其次为左主干冠状动脉、回旋支冠状动脉和右冠状动脉远端[7]。CAA的形状可以是囊状、梭状或直肠(扩散性扩张、无节段性动脉瘤),并且其形状和大小可随时间而变化。例如,最初看起来是直肠的动脉瘤可能会在数周内演变为分段或串珠状[8](图1)。

图1 一例5岁男患儿入院时(A)和随访1年时(B)的右冠状动脉情况
3 CAD的检查和诊断
主要包括血液心肌损伤标记物检查(肌酸激酶同工酶、肌钙蛋白、B型利钠肽)、心电图(静息心电图、动态心电图和运动心电图)、超声心动图(静息超声心动图、负荷超声心动图)、冠状动脉造影和其他影像学检查(心肌灌注成像、CT血管成像或MRI等)。其中,冠状动脉造影主要适用于有诱发性心肌缺血表现(Ⅰ类推荐,A级证据)、急性期中度至GCAA表现(Ⅱa类推荐,C级证据)和明显冠脉狭窄表现(Ⅱa类推荐,C级证据)的患者[4]。
4 CAD严重程度评估
从KD冠状动脉损害的长期管理的角度来看,我们推荐用超声心动图测得冠状动脉内径和体表面积计算的Z值评估冠状动脉损害严重程度为标准方法,测量部位为左回旋支和右冠状动脉主干近段、中段和远段。具体分为(1)无病变:Z值始终<2;(2)仅冠状动脉扩张:2≤Z值<2.5;或最初Z值<2,随访期间Z值下降>1;(3)小型CAA:2.5≤Z值<5;(4)中型CAA:5≤Z值<10,或绝对值内径<8 mm;(5)GCAA:Z值≥10,或绝对值内径≥8 mm。目前,将Z值≥2.5定义为长期显著的CAD表现(Ⅱa类推荐,B级证据)[9]。
5 CAD的进展
CAD的自然过程在很大程度上取决于KD急性期冠状动脉疾病的严重程度。疾病发作后的4~6周内,CAD的大小可能会增加。达到峰值直径后,约有50%~75%的CAD恢复至正常管腔直径[9-10]。通常发生在KD初发后的2年内恢复正常。在这段时间之后,进一步增大的可能性不大。CAD消退至正常管腔直径的可能性与其最大直径密切相关。GCAA最不可能消退。在较年幼的孩子,更远端的位置或形状呈梭形的情况下,CAD也更有可能消退。
在患有持续性CAD的患者中,CAD入口或出口处的肌内膜增生随时间持续进展。在一项研究中,通过15年的随访,大约有一半的最大直径≥6 mm的CAA发展为狭窄。动脉瘤动脉段也容易出现曲折,钙化和血栓闭塞。由于动脉壁会随着时间的推移而钙化,因此非常罕见的CAA破裂事件通常仅限于发病后的最初几个月[11]。
6 CAD进展的相关因素[12-15]
包括(1)晚期诊断和延迟治疗。研究发现,在疾病的前10 d进行IVIG治疗可将CAA的患病率降低五倍。(2)年龄:年龄<1岁和>9岁。研究发现,即使迅速进行IVIG治疗,婴儿,尤其是6个月以下的婴儿,发生CAA的风险最高[12-13]。此外,由于许多婴儿患有非典型疾病,因此可能会延迟诊断和治疗。但是,>9岁的儿童发生CAA的风险也增加,可能与对冠状动脉扩张易感性增加和(或)IVIG给药延迟有关;(3)男性;(4)发烧时间长(即≥14 d);(5)初始IVIG治疗无效,表现为持续性和复发性发热;(6)实验室检查结果异常,包括:低血细胞比容(即<35%)、低血清白蛋白、低血清钠、谷丙转氨酶升高、C反应蛋白和红细胞沉降率升高、白细胞计数升高和低基线血清免疫球蛋白G;(7)遗传多态性,包括但不限于基质金属蛋白酶单倍型、内皮生长因子及其受体、钙信号通路和转化生长因子β信号通路[16-17]。
7 CAD的治疗
对于合并CAD的KD患者,缺血性心脏病的治疗是改善预后的关键。KD引起的心肌缺血主要与血栓性堵塞和内膜增厚导致管腔狭窄等有关。常见的治疗方案包括[18-24]:
7.1 药物治疗
包括(1)抗血小板治疗:对于持续性CAA的患者常用阿司匹林进行抗血小板治疗,预防血栓形成和缺血性心脏病发生(Ⅰ类推荐,C级证据)。(2)抗凝治疗:常用华法林抗凝,治疗KD的指征为合并GCAA、或合并血栓形成、或既往有心肌梗死病史(Ⅱa类推荐,C级证据)。(3)肾素血管紧张素转换酶抑制剂或肾素血管紧张素多体拮抗剂:一些观察性研究发现,肾素血管紧张素转换酶抑制剂或肾素血管紧张素多体拮抗剂有助于降低GCAA或冠脉狭窄的发生风险(Ⅱa类推荐,C级证据)。对于合并缺血性心脏病的患者,应用ACEI/ARB可显著改善心脏重构,改善预后(Ⅰ类推荐,A级证据)。(4)他汀:一些小样本研究结果提示,他汀可对CAD起到修复作用,JCS/JSCS 2020指南建议,对于CAA的KD患者,可给予经验性使用他汀治疗(Ⅱb类推荐,C级证据)。(5)溶栓:KD患者,特别是合并GCAA患者,发生血栓性冠脉闭塞的风险高,血栓多位于动脉瘤的入口或出口。对于合并急性冠状动脉综合征的KD患儿推荐溶栓治疗(Ⅰ类推荐,C级证据)。
7.2 非药物治疗
对于合并急性心肌梗死的KD患者,建议由技术熟练的介入医师进行介入治疗(Ⅰ类推荐,C级证据)[25]。
8 CAD的长期管理
对合并CAD的患者进行临床风险分级,共分为5级:(1)Ⅰ级:冠状动脉无扩张;(2)Ⅱ级:急性期短暂扩张,表现为轻微的一过性扩张,发病1个月后可恢复正常;(3)Ⅲ级:发病1个月后仍合并CAD改变,常在长期随访中恢复正常;(4)Ⅳ级:冠状动脉造影显示持续存在双侧或单侧CAA改变,但无缺血性结果;(5)Ⅴ级:造影显示冠状动脉狭窄病变,有或无缺血性表现[26-28]。
根据CAD的严重程度和临床风险分级对KD患者进行远期管理和随访(表1)。
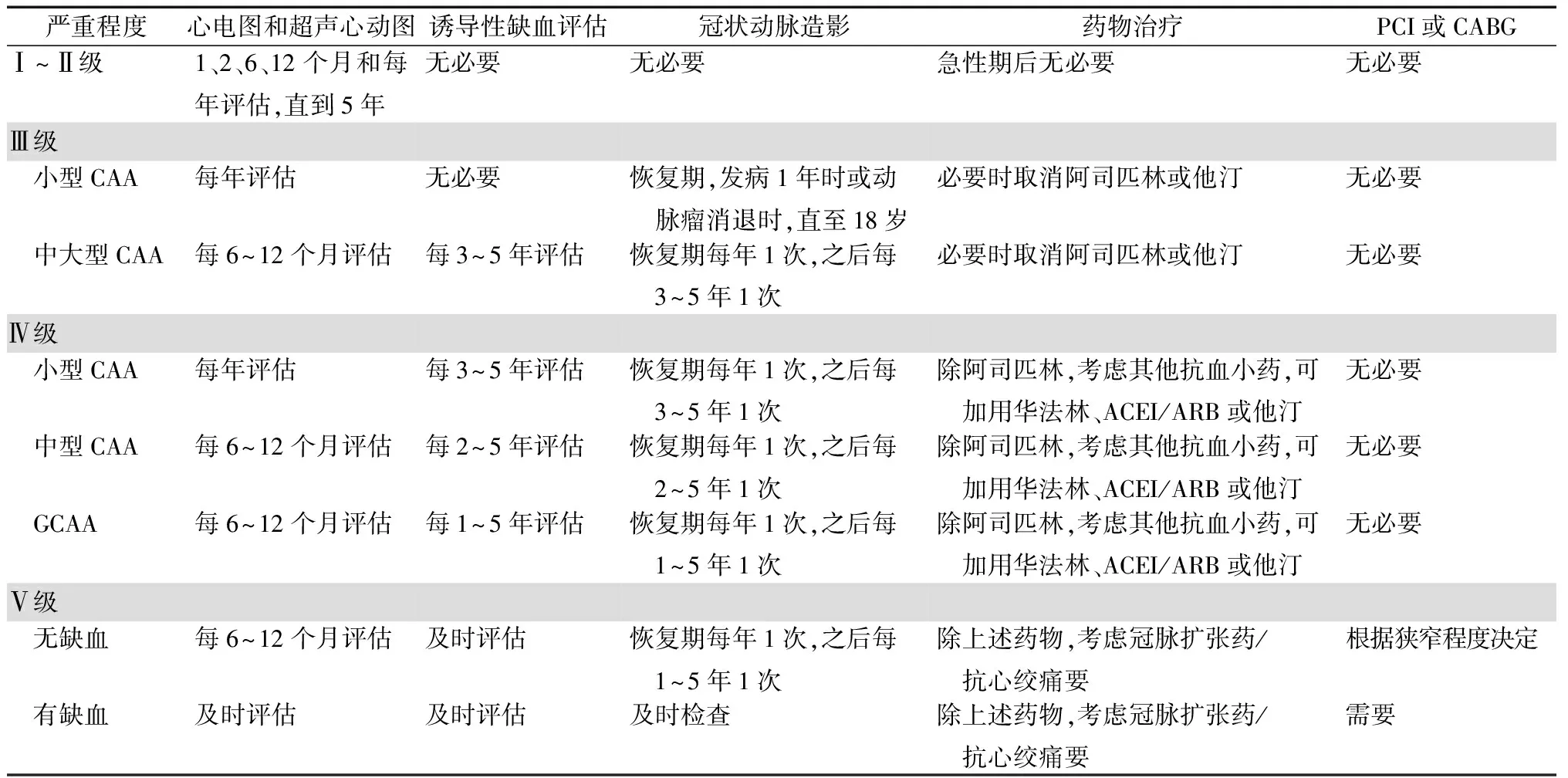
表1 KD相关CAD的长期管理方案[29]
9 小结
KD患者可出现严重的心血管并发症,最常见的是CAD,预后不良,特别是合并GCAA患者,可出现心肌缺血、梗死,甚至猝死[30]。需注意高危患者,及时评估、诊断和早期治疗,并对合并CAD的患者进行远期管理和随访,以改善患者的预后。