橘皮中可溶性膳食纤维理化性质的研究
2021-12-30郝晓华罗晓敏罗淑政
郝晓华, 罗晓敏, 罗淑政, 宿 婧
(忻州师范学院生物系,山西忻州 034300)
我国南方盛产柑橘,果肉可食用或生产橘汁,但是橘皮多数作为废弃物丢掉。 橘皮经微生物分解后腐烂发臭, 柑橘果皮渣的污染情况愈加严重(臧玉红,2006),资源无法充分利用,橘皮的处理成为困扰生产厂家的一大难题。
膳食纤维(DF)是以多糖为主体的物质,但不能被肠胃消化吸收, 摄入一定的膳食纤维不仅能有效刺激肠道蠕动, 还能清除肠道内对身体有害的物质(马昱阳等,2020),预防胆结石、便秘、直肠癌、冠心病等疾病的发生。橘皮中含有许多的膳食纤维,分为不可溶性和可溶性(王海娟等,2020)。可溶性膳食纤维(SDF)是指不能被人体消化酶所分解的多糖类物质。 不可溶性膳食纤维(IDF)是指不溶于水且不易被人体所消化的一类膳食纤维(宋康等,2020)。本试验通过碱法提取干燥橘皮中含有的可溶性膳食纤维, 研究碱液浓度、 浸提时间、浸提温度、料液比对SDF 提取率的影响,选择出最佳条件碱法提取橘皮SDF,并对其持水力、溶胀性、脂肪结合能力、还原力这些理化性质进行测定,旨在为充分开发利用橘皮资源提供理论基础。
1 材料与方法
1.1 试验材料 本研究所用橘子购买于超市,试验前事先用蒸馏水对橘皮进行清洗并晾干, 再用粉碎机粉碎成粉末。
1.2 试验试剂及仪器 氢氧化钠、 磷酸二氢钠、磷酸氢二钠、铁氰化钾、氯化钠、无水乙醇、磷酸二氢钾、三氯乙酸、醋酸、盐酸、蒸馏水、植物油(非转基因玉米胚芽油, 食品级); 酚酞指示剂;pH 6.6的磷酸盐缓冲剂;维生素(Vc)。 所有化学试剂均为常规且为分析纯。
万分之一电子天平、电热恒温振荡水槽、低速离心机、调温电热套、密封型手提式粉碎机、紫外可见分光光度计、数显鼓风干燥箱。
1.3 橘皮碱法提取工艺流程 清洁橘皮-干燥橘皮-粉碎-碱法提取 (单因素试验)-收集滤液-酸中和-醇沉淀干燥沉淀物-烘干-称重-橘皮SDF-正交试验,验证正交试验结果,得到最佳提取条件,然后按照试验步骤对其各项理化性质进行研究。
准确称取2 g 橘皮粉,料液比为1:10 ~1:70,将其和质量浓度为20 ~50 mg/mL 的NaOH 溶液混合,进行水浴加热,加热温度为30 ~90 ℃,水浴加热时间为1 ~7 h, 对上清液中和 (使用醋酸),使用电热套将其减压浓缩,直至其液体呈黏稠状,将其冷却,直至其温度到室温。 再加入无水乙醇(10 倍体积)后静置,使用离心机将其进行分离。分离成功后干燥,进行称量,干燥再称量,直至其恒重为止,就可得到可溶性膳食纤维(SDF)(郭艳峰等,2017;戴余军等,2014),此时为固体状态。
1.4 橘皮SDF 提取率的计算及数据处理

1.5 橘皮SDF 提取的单因素试验 试验选取浸提温度、浸提橘皮时碱液的浓度、料液比、浸提橘皮的时间4 个因素对可溶性膳食纤维提取率的影响进行研究。
1.5.1 料液比对提取率的影响 准备7 份粉碎好的橘皮粉, 每份 2 g, 根据料液比为 1:10、1:20、1:30、1:40、1:50、1:60、1:70(g/mL)的比例分别加入质量浓度为20 mg/mL 的NaOH 溶液, 充分搅拌,于事先准备好50 ℃水浴槽中水浴1 h。 再4200 r/min离心分离3 min,对上清液中和(使用醋酸),使用电热套将其浓缩, 直至其液体呈黏稠状, 将其冷却,直至其温度到室温。 样品:无水乙醇按照1:10的比例,充分静置,使用离心机将其进行分离,将上清液舍弃,将下层沉淀物置于干燥箱中干燥后,得到可溶性膳食纤维(SDF),分别称取不同比例的料液比所制得的SDF 质量,比较不同料液比对于SDF 提取率的影响。
1.5.2 碱液浓度对提取率的影响 称取粉碎好的橘皮粉 7 份,每份 2 g,按照料液比 1:40(g/mL)分别加入质量浓度 20、25、30、35、40、45、50 mg/mL的NaOH 溶液,充分搅拌,于事先准备好50 ℃水浴槽中水浴1 h。 其余步骤参照上述料液比对提取率影响方法进行操作。 最后再分别称取不同碱液浓度所制得的SDF 质量,考察不同碱液浓度对于SDF 提取率的影响。
1.5.3 浸提温度对提取率的影响 称取粉碎好的橘皮粉 7 份,每份 2 g,按照料液比 1:40(g/mL)分别加入质量浓度20 mg/mL 的NaOH 溶液,充分搅拌,溶液分别置于 30、40、50、60、70、80、90 ℃的恒温水浴槽条件下水浴1 h。 其余步骤参照上述料液比对提取率影响的方法进行操作。 最后再分别称取不同浸提温度所制得的SDF 质量,比较不同浸提温度对SDF 提取率的影响。
1.5.4 浸提时间对提取率的影响: 称取粉碎好的橘皮粉 7 份,每份 2 g,按照料液比 1:40(g/mL)分别加入质量浓度20 mg/mL 的NaOH 溶液,充分搅拌,将溶液置于事先准备好50 ℃恒温水浴槽中分别水浴 1、2、3、4、5、6、7 h, 其余步骤参照上述料液比对提取率影响的方法进行操作。 最后再分别称取不同浸提时间所制得的SDF 质量,比较不同浸提时间对SDF 提取率的影响。
1.6 橘皮可溶性膳食纤维(SDF)的理化性质测定
1.6.1 持水力测定 参考周淑仪等(2019)、李伟伟等(2018)的方法略做修改,取0.5 g 已粉碎好的可溶性膳食纤维,放入到15 mL 离心管中,并加入蒸馏水7.5 mL,将其充分混合均匀,放入恒温水浴槽中(37 ℃)水浴,水浴时间为 12 h,再 4000 r/min离心15 min,小心倒出上清液,用滤纸上干燥剩余部分并称重。
持水力/(g/g)=(样品湿重-样品干重)/样品干重。
1.6.2 脂肪结合能力测定 参考仝文玲等(2019)、王彩虹(2018)的方法略做修改,称取 0.5 g的可溶性膳食纤维(m0),加入 HCl 溶液(0.1 mol/L)100 mL,充分溶解,再加10 g 植物油,再将其充分混匀,于事先准备好的37 ℃恒温水浴槽分别振荡水浴 0、30、60 min,4000 r/min 离心 15 min, 小心除去上层未结合的油,去除游离的植物油,称重得出 m1、m2、m3,做平行的试验 3 次。
脂肪吸附量/(g/g)=(mn-m0)/m0。
1.6.3 溶胀力测定 参考徐守梁等(2020)的方法略做修改,准备10 mL 的量筒,放入提取的膳食纤维1.5 g 并记录体积,再加入蒸馏水5 mL,浸泡12 h,记录体积。 设浸泡后的体积为V1,浸泡前干品体积为V2,干品质量为m3。
溶胀力/(mL/g)=(V1-V2)/m3。
1.6.4 还原力测定 参考蒋纬等(2019)的方法略做修改。 试验组: 将提取的可溶性膳食纤维加蒸馏水充分混匀,配制成5 mg/mL SDF 溶液,在试管中依次加入样品溶液2 mL, 铁氰化钾溶液(1%)2.5 mL、磷酸盐缓冲液(pH=6.6)2.5 mL 并充分混和均匀,置于事先准备好的50 ℃恒温水浴槽中水浴20 min。随后加入三氯乙酸(0.1%)2 mL 充分混和均匀,将其静置5 min 后,测定吸光度(紫外分光光度计的波长为700 nm)。
阳性对照组:移取 Vc 溶液(5 mg/mL)2 mL 于试管中,加入铁氰化钾溶液(1%)2.5 mL、磷酸盐缓冲液(pH=6.6)2.5 mL,并将其充分混和均匀,置于事先准备好的50 ℃恒温水浴槽中水浴20 min。再加入2 mL 0.1%三氯乙酸, 并将其充分混和均匀,静置5 min,测定吸光度(设置波长为700 nm)。
阴性对照组: 试验基本流程和阳性对照组相同,但Vc 被等体积蒸馏水替换。 用其在分光光度计调零调百,测定阴性和阳性对照组的吸光度值。
2 试验结果
2.1 单因素试验结果
2.1.1 料液比试验结果 由图1 可知,当料液比增大时,橘皮SDF 的提取率先上升后下降。 主要原因是当料液比增大时,细胞壁内侧和外侧的渗透压随之不断升高,这是橘皮SDF 浸出的有利条件。 当料液比大于1:40 后,提取率开始下降,可能是因为当料液比逐渐增大时,杂质浸出增多,提取率下降。综合考虑溶剂损耗量,进行正交试验时取1:20、1:30、1:40 这三个水平。
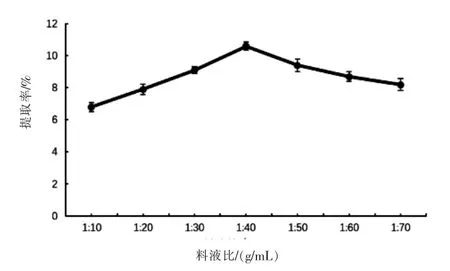
图1 料液比对橘皮SDF 提取率的影响
2.1.2 浸提温度试验结果 如图2 所示, 当浸提温度增加时,橘皮SDF 提取率先增加后下降。 当温度由30 ℃升温至70 ℃时,橘皮SDF 提取率在不断地增大,是因为分子的运动受温度的影响,温度升高,分子运动速率加快,因此SDF 的提取率得以提高。但温度大于70 ℃后,SDF 提取率并没有继续增高反而降低,可能因为过高的温度,降解了橘皮SDF 中的部分成分,所以提取率下降。 正交试验时选取浸提的温度为60、70 、80 ℃这三个水平。
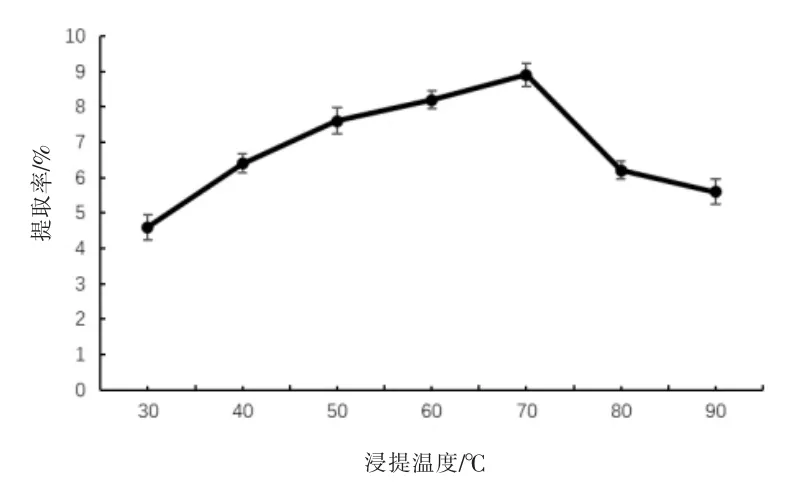
图2 浸提温度对橘皮SDF 提取率的影响
2.1.3 浸提时间试验结果 如图3 所示, 当浸提橘皮的时间增加时,橘皮SDF 提取率是先升高后下降。可能是因为随着浸提时间的增加,橘皮SDF逐渐浸出,在4 h 时达到最大。 超过4 h 后提取量减小, 推测浸提橘皮的时间过长造成了已经浸出的橘皮SDF 分子结构发生改变或被破坏,且时间过长容易造成杂质成分的析出, 造成提取液黏稠度增大,杂质过多,使得抽取难度增加,降低了提取率。综合考虑后续提取工作量等方面,选择浸提时间为3、4、5 h 作为正交试验的三个水平。
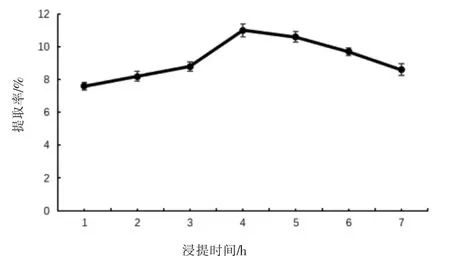
图3 浸提时间对橘皮SDF 提取率的影响
2.1.4 碱液浓度试验结果 由图4 可知, 在试验范围内,随着碱液浓度的增加,橘皮SDF 提取率呈先增后减的变化趋势。 当低于35 mg/mL 时,橘皮SDF 提取率随着碱液浓度的增加而增大; 当高于35 mg/mL 时,橘皮SDF 提取率随着碱液浓度的增加而减少。当橘皮SDF 提取率达到最大值时,碱液浓度为35 mg/mL。在碱液浓度35 mg/mL 之前其细胞解离程度随着碱液浓度的增大而升高, 其产出的SDF 也就越多。 但当浓度高于35 mg/mL 时,会导致已析出来的SDF 发生降解,进而导致提取率下降。 因此做正交试验的三个NaOH 碱液浓度水平为 30、35、40 mg/mL。
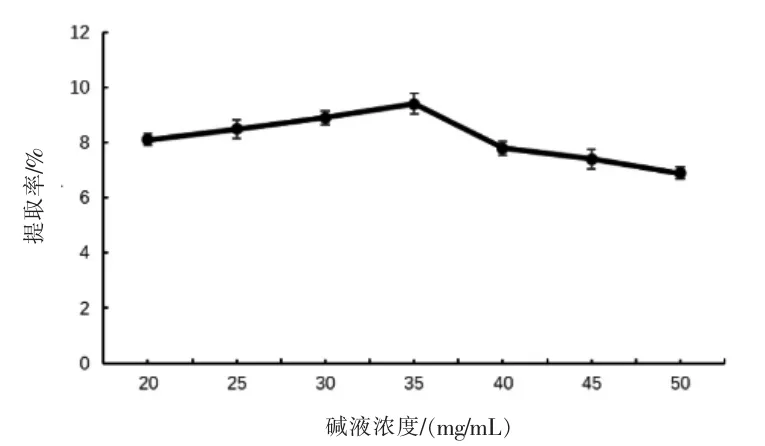
图4 碱液浓度对橘皮SDF 提取率的影响
2.2 橘皮SDF 提取工艺的正交设计及结果 由单因素试验结果可知,不同因素对橘皮SDF 提取率的影响有所不同。 为了考察试验因素对试验结果的综合影响,选取料液比(A)、浸提橘皮的时间(B)、浸提橘皮所用碱液的浓度(C)、浸提橘皮的温度(D)为考察因素,用 SPSS 20.0 设计 L9(34)正交试验(表1),通过比较橘皮SDF 的提取率,得出提取橘皮可溶性膳食纤维最好的条件。
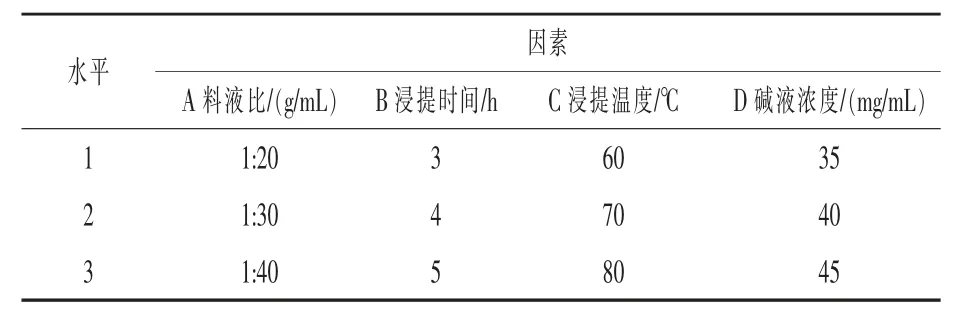
表1 橘皮SDF 提取工艺L9(34)因素水平
由表2 可知,橘皮SDF 最低提取率为3.7%,最高提取率为9.1%,相差2.5 倍,说明各种因素的组合对提取结果影响很大。 因素D 的极差(R)在4 个因素中最大,说明其对橘皮SDF 提取率影响最明显。 根据R 值,得到影响提取率的因素为D>A>B=C。
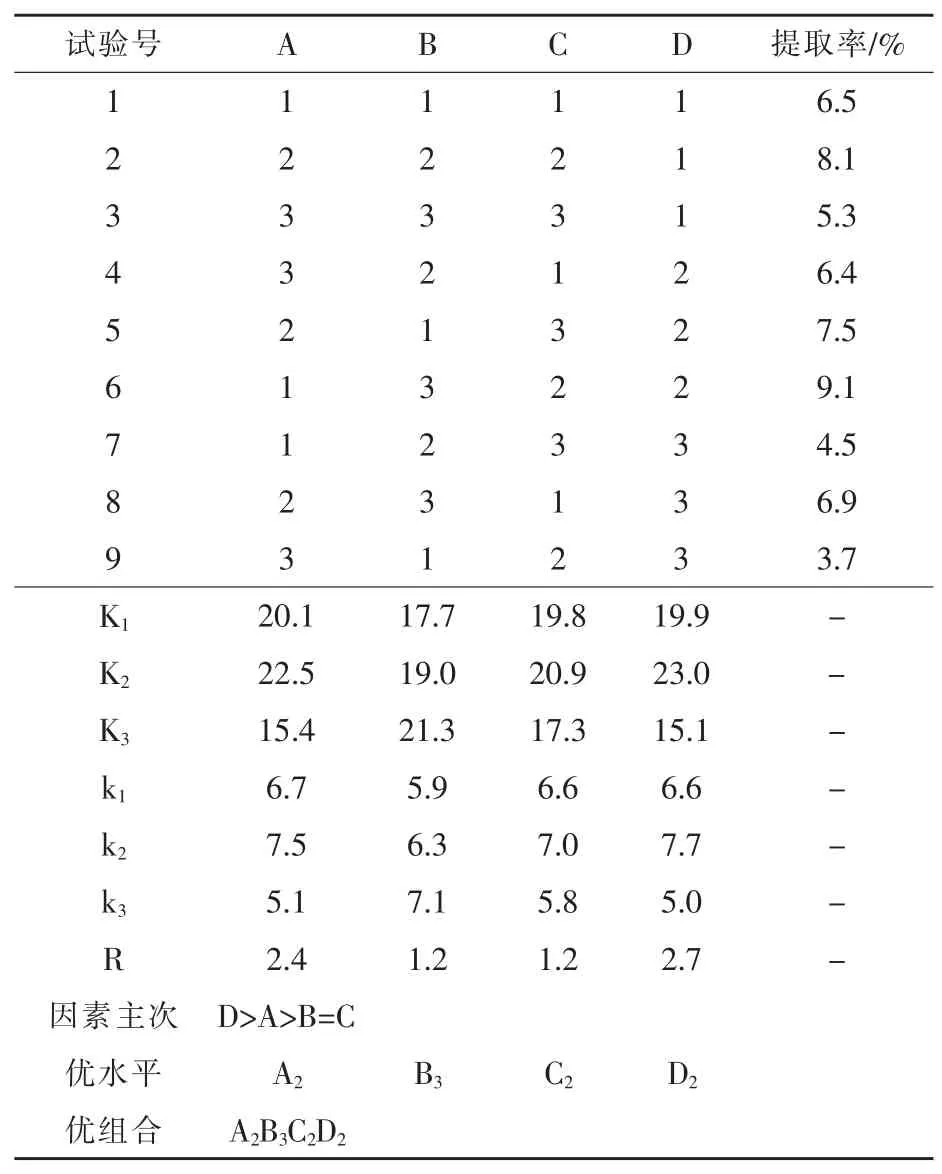
表2 橘皮SDF 碱法提取工艺正交试验结果
综上所述,可确定橘皮SDF 提取的最佳条件为A2B3C2D2, 即橘皮中提取SDF 最好的条件为料液比 1:30(g/mL)、浸提时间 5 h、浸提温度 70 ℃、碱液浓度35 mg/mL。为了进一步考察该工艺是否可作为最优选择,进行验证试验。
2.3 验证试验 准确称取橘皮粉3 份,每份各2 g,根据上述提取最佳条件(A2B3C2D2)进行重复性验证试验, 测得提取率分别为9.13%、9.31%、9.25%,平均提取率为9.23%,三次重复试验SDF 提取率较接近,没有明显差异,且得到平均提取率高于正交设计表中的最高值,说明该提取工艺可靠。
2.4 橘皮可溶性膳食纤维(SDF)的理化性质测定结果
2.4.1 持水力和溶胀性的测定结果与分析 可溶性膳食纤维来源和制备形式不同, 持水力及溶胀性会有所差异, 其范围大致在纤维自重的1.5 ~2.5 倍。 由测定可得,橘皮 SDF 持水力为 1.21 g/g,溶胀性为2.32 mL/g, 持水力为纤维自重的1.2倍,溶胀力为纤维自重的2.3 倍。
2.4.2 脂肪结合能力的测定结果与分析 由表3可知,在0 ~30 min 橘皮SDF 脂肪吸附量增加的幅度较大,在 30 ~ 60 min 未增加,0.5 h 后吸附平衡。脂肪结合能力会受时间的影响,脂肪吸附量达到饱和也就意味着反应到达平衡。

表3 橘皮SDF 脂肪结合能力测定结果
2.4.3 还原力的测定结果与分析 铁氰化钾的三价铁被抗氧化剂还原成二价铁, 二价铁进一步再和三氯化铁反应生成墨绿色的普鲁士蓝, 该颜色在波长为700 nm 时有最大吸光度, 使用此性质可以间接反映抗氧化剂的还原能力, 即吸光度越大表示还原能力越强。由表4 可得,橘皮可溶性膳食纤维具备一定的还原能力, 但还原能力小于Vc,是Vc 还原力的53.06%。
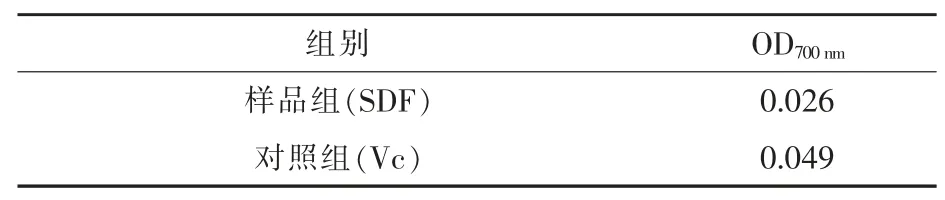
表4 橘皮SDF 还原力的测定结果
3 结论
本试验采用碱法提取橘皮中的SDF, 运用单因素试验结合正交试验, 测定橘皮中SDF 的提取率,确定最好的提取SDF 的条件。且对SDF 的持水力、溶胀性、脂肪结合能力、还原力这些理化性质进行测定。本研究最终结果表明,橘皮中提取可溶性纤维最好的条件为料液比(1:30) g/mL、浸提时间5 h、浸提温度70 ℃、碱液浓度35 mg/mL,在该条件下,平均提取率高达9.23%。
在理化性质试验中, 橘皮SDF 的持水力为0.91 g/g; 橘皮脂肪结合量在 0 ~ 30 min 增幅较大,在 30 ~ 60 min 几乎未增加,表明 30 min 已达到吸附平衡;溶胀性为2.32 mL/g,还原力测定中橘皮可溶性膳食纤维具备一定的还原能力,为Vc还原力的53.06%。
目前, 橘皮膳食纤维的主要提取方法为酶解法、固态发酵法等,关于橘皮可溶性膳食纤维碱法提取工艺及其性质研究还鲜有报道。 研究碱法提取橘皮中的可溶性膳食纤维含量及其理化性质,为橘子果皮的综合开发利用提供理论支持和技术指导作用。
