Ag/Ag2O/g-C3N4/BiVO4复合光催化体系降解盐酸四环素机理研究
2021-12-21蒲生彦季雯雯
许 洋, 蒲生彦*, 季雯雯, 杨 曾
1.成都理工大学, 地质灾害防治与地质环境保护国家重点实验室, 四川 成都 610059 2.成都理工大学生态环境学院, 国家环境保护水土污染协同控制与联合修复重点实验室, 四川 成都 610059
四环素类抗生素是目前使用最广泛、用量最大的抗生素种类之一[1],其中盐酸四环素(TC-HCl)是一种广泛应用的光谱抗生素,主要用于医疗及畜牧行业,但由于人类和动物的吸收率低[2],大量TC-HCl未被吸收利用,直接以原液形式随排泄物进入环境中,导致微生物耐药性不断增强[3-5]. 自然生态系统中的生物降解难以将TC-HCl有效去除[6-8],因此高效处理水环境中的TC-HCl已成为当前研究热点.
目前降解TC-HCl的主要方法包括生物处理法[9]、Fenton试剂法[10]、电化学氧化法[11]、光催化法[12]和吸附法[13],其中,光催化法具有氧化能力强、降解效率高、能耗少且无二次污染等优点,是抗生素处理的理想方法[14-16]. 但常规的光催化剂带隙宽、光能利用率低、去除效果差,因此开发一种高效稳定降解TC-HCl的光催化剂具有一定的研究意义[17-19]. 钒酸铋(BiVO4)作为一种环境友好型光催化剂,具有低带隙能、光利用率高、无毒、耐腐蚀等优点. BiVO4的吸收率可达标准AM 1.5太阳光谱的11%,最大光电流密度为7.6 mA/cm2[20],具有出色的光催化活性,是降解TC-HCl的理想材料[21-22]. 但BiVO4的光电荷载流子转移慢、光生电子-空穴对复合速率快等问题,限制了其光催化性能,难以被实际推广应用[23].
为克服上述问题,该研究以TC-HCl为目标降解物,用银基材料(Ag/Ag2O)和石墨相氮化碳(g-C3N4)对BiVO4进行改性,成功制备了Ag纳米粒子修饰的Ag/Ag2O/g-C3N4/BiVO4四元复合材料;使用XRD、SEM及XPS等方法对复合材料的晶体形态、结构、元素组成和光学性质进行了表征,通过降解水溶液中的TC-HCl来考察复合材料的光催化性能,同时对光催化机理进行了探讨,以期为高效降解抗生素的光催化剂开发及推广应用提供参考.
1 材料与方法
1.1 主要试剂与材料
五水硝酸铋〔Bi(NO3)3·5H2O〕、钒酸铵(NH4VO3)、硝酸银(AgNO3)、尿素(CH4N2O)均购自成都科龙化学试剂厂;盐酸四环素(C22H24N2O8)购自上海阿拉丁试剂厂. 试剂纯度均为分析纯.
1.2 主要仪器
扫描电子显微镜(Sigma 300,德国卡尔蔡司公司);X射线衍射仪(DX-2700,丹东浩元仪器有限公司);紫外-可见-近红外分光光度计(UV-2450,日本岛津公司).
1.3 研究方法
1.3.1BiVO4的制备
取5 mmol Bi(NO3)3·5H2O加入10 mL冰醋酸中,搅拌至分散均匀得到A液;取5 mmol NH4VO3溶解于60 mL热水中得到B液.
用胶头滴管将B液缓慢滴加至A液中,混合溶液超声处理20 min后室温搅拌30 min,加入2 mol/L氢氧化钠溶液调节pH至9,使用高压反应釜在40 ℃下反应20 h,洗涤烘干后300 ℃下煅烧2 h,得到BiVO4,存储备用.
1.3.2g-C3N4的制备
取尿素置于坩埚中加热,以5 ℃/min的升温速率加热至500 ℃,持续2 h,冷却至室温后得到g-C3N4,储存备用.
1.3.3g-C3N4/BiVO4的制备
称取0.5 g g-C3N4置于100 mL CH3OH溶液中,超声2 h使其分散均匀,再加入0.5 g BiVO4,先超声1 h,再连续搅拌24 h. 使用马弗炉将样品于300 ℃下煅烧2 h,得到g-C3N4/BiVO4复合材料,储存备用.
1.3.4Ag/Ag2O/g-C3N4/BiVO4的制备
称取0.4 g g-C3N4/BiVO4置于100 mL去离子水中,搅拌30 min,称取0.02 g AgNO3溶解于上述溶液,加入2 mol/L氢氧化钠溶液,调整溶液pH至14;所得悬浮液连续搅拌24 h. 将析出沉淀洗涤后置于70 ℃干燥箱中干燥,热分解得到Ag/Ag2O/g-C3N4/BiVO4四元复合材料,存储备用.
1.3.5光催化性能的研究
称取0.05 g Ag/Ag2O/g-C3N4/BiVO4四元复合材料均匀分散在50 mL 10 mg/L的TC-HCl溶液中,于暗条件下搅拌30 min至吸附解吸平衡,加载420 nm截止过滤器,打开300 W Xe灯,进行光催化;由固定时间点从悬浮液中进行取样分析,以 10 000 r/min的速率进行两次离心,每次5 min,使复合材料得以完全分离. 通过紫外分光光度计测量λ=357 nm处的吸收强度,得到TC-HCl的浓度. 降解率(η)按式(1)计算:
η=(C0-Ct)/C0×100%
(1)
式中:C0为降解前TC-HCl的浓度,mg/L;Ct为降解t时间(min)后的TC-HCl浓度,mg/L.
2 结果与讨论
2.1 X-射线衍射分析
通过X射线衍射(XRD)表征,得到Ag/Ag2O/g-C3N4/BiVO4、g-C3N4/BiVO4、g-C3N4和BiVO4材料的XRD图谱. 如图1所示,纯BiVO4属于单斜白钨矿型BiVO4(JCPDS14-0688),在可见光下表现出极强的光学活性[24]. 纯g-C3N4在13.32°和27.63°处的衍射峰分别对应g-C3N4的(100)面和(002)面,即面内结构峰与芳香环的层间堆积[25]. g-C3N4的特征峰(27.63°)在g-C3N4/BiVO4和Ag/Ag2O/g-C3N4/BiVO4二者的XRD图谱中均有显现. 此外,在Ag/Ag2O/g-C3N4/BiVO4的XRD图谱中,未观察到Ag和Ag2O粒子的特征衍射峰,这是因为Ag/Ag2O粒子含量低、粒径小且分散造成的. XRD图谱中未观察到BiVO4晶体及结构改变,样品中不存在其他衍射峰,证明g-C3N4与BiVO4存在于复合材料中,且制备过程中无其他杂质生成.
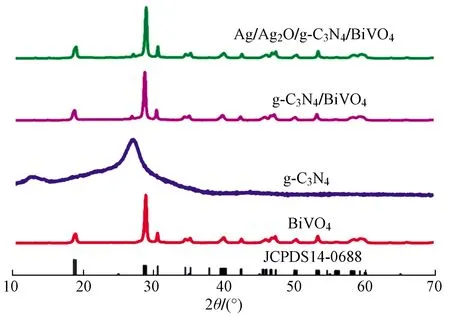
图1 制备样品的XRD图谱Fig.1 XRD pattern of the prepared samples
2.2 扫描电子显微镜分析
扫描电子显微镜分析(SEM)表征结果显示:纯BiVO4在SEM图谱下表现为球体,是由多个微球堆积而成的大球体〔见图2(a)〕;g-C3N4是由纳米片堆叠而成的多层结构〔见图2(b)〕;Ag/Ag2O/g-C3N4/BiVO4的形态则是一种复杂且不规则的微结构,复合材料以g-C3N4为底物,空隙中包裹着球体BiVO4,整体表现为堆叠形状,其表层附着细小的Ag/Ag2O粒子〔见图2(c)〕,这种结构有利于增加复合材料的比表面积. 为研究复合材料的组成成分,通过元素映射(见图3)和EDS能谱图(见图4)对材料进行分析,证明复合材料是由Bi、N、C、O、V和Ag这6种元素组成,其中Ag含量约为6%,且各元素分散性良好. 以上结果表明,Ag/Ag2O/g-C3N4/BiVO4复合材料合成成功.

图2 BiVO4、g-C3N4和Ag/Ag2O/g-C3N4/BiVO4复合材料的SEM图像Fig.2 SEM images of BiVO4, g-C3N4, and Ag/Ag2O/g-C3N4/BiVO4 composites
2.3 X-射线光电子能谱分析
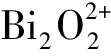
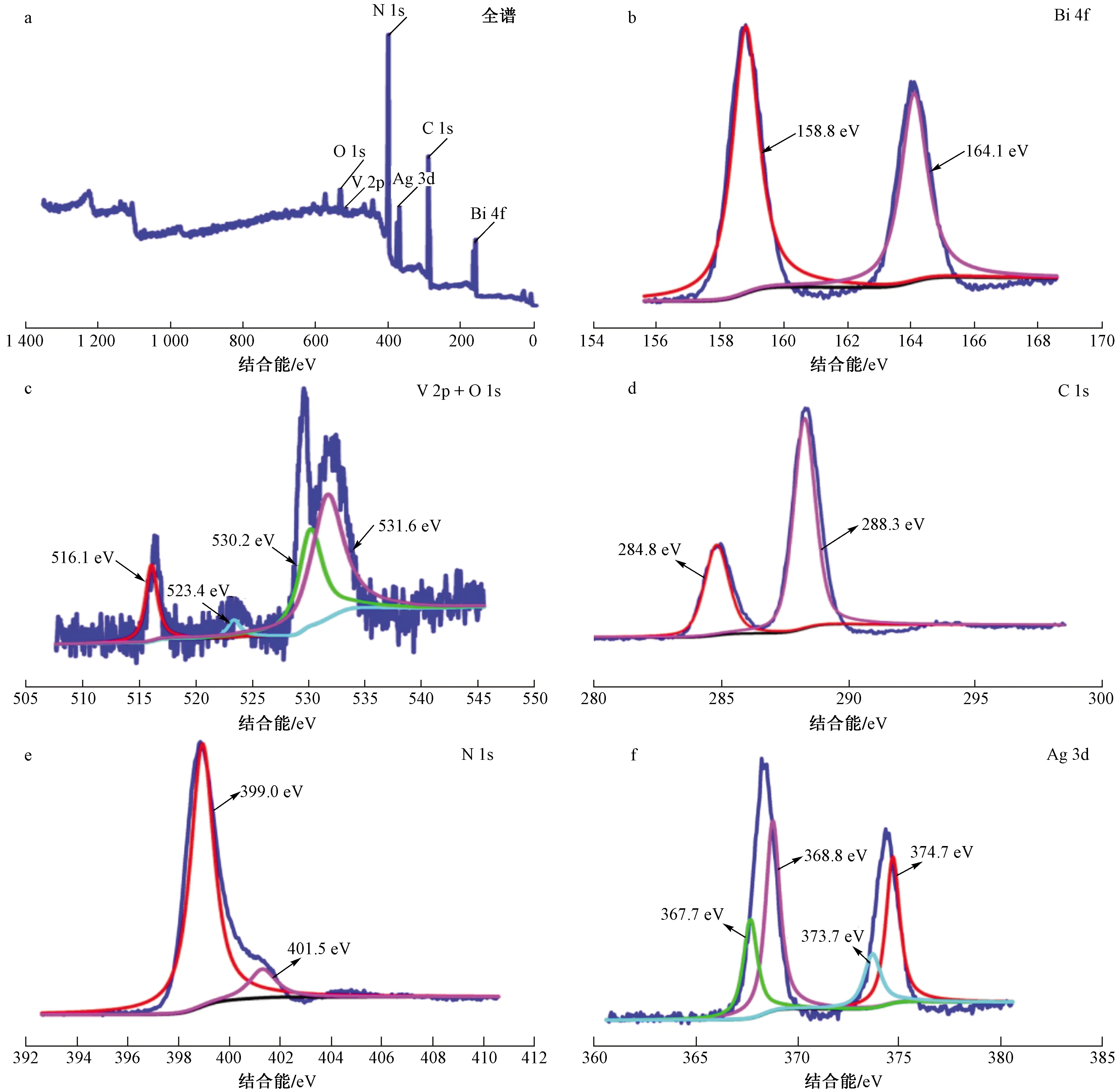
图5 Ag/Ag2O/g-C3N4/BiVO4复合材料XPS图谱Fig.5 XPS spectra of Ag/Ag2O/g-C3N4/BiVO4 composite
2.4 紫外可见漫反射吸收光谱分析
通过紫外-可见漫反射光谱法(UV-vis DRS)对复合材料进行表征,如图6(a)所示,将银基材料(Ag/Ag2O)沉积在BiVO4上之后,对可见光范围内复合材料的光吸收效果有一定的提高,BiVO4的吸收阈值约为538 nm,g-C3N4的吸收阈值约为459 nm,Ag/Ag2O/g-C3N4/BiVO4的吸收阈值约为548 nm. 这表明该复合材料可在一定程度上提升对可见光的吸收率,激发更多光生电子-空穴对[30]. 同时,BiVO4和g-C3N4的带隙宽度(eV)可以通过Kubelka-Munk公式[31]计算:
R∞=10-A
(2)
F(R∞)=(1-R∞)2/2R∞
(3)
F(R∞)hv=C1(hv-Eg)
(4)
式中:R∞为相对漫反射率;A为吸光度;hv为带隙能量;C1为比例常数;Eg为禁带宽度,eV.
由图6(b)可知,BiVO4和g-C3N4的禁带宽度分别为2.4和2.7 eV.
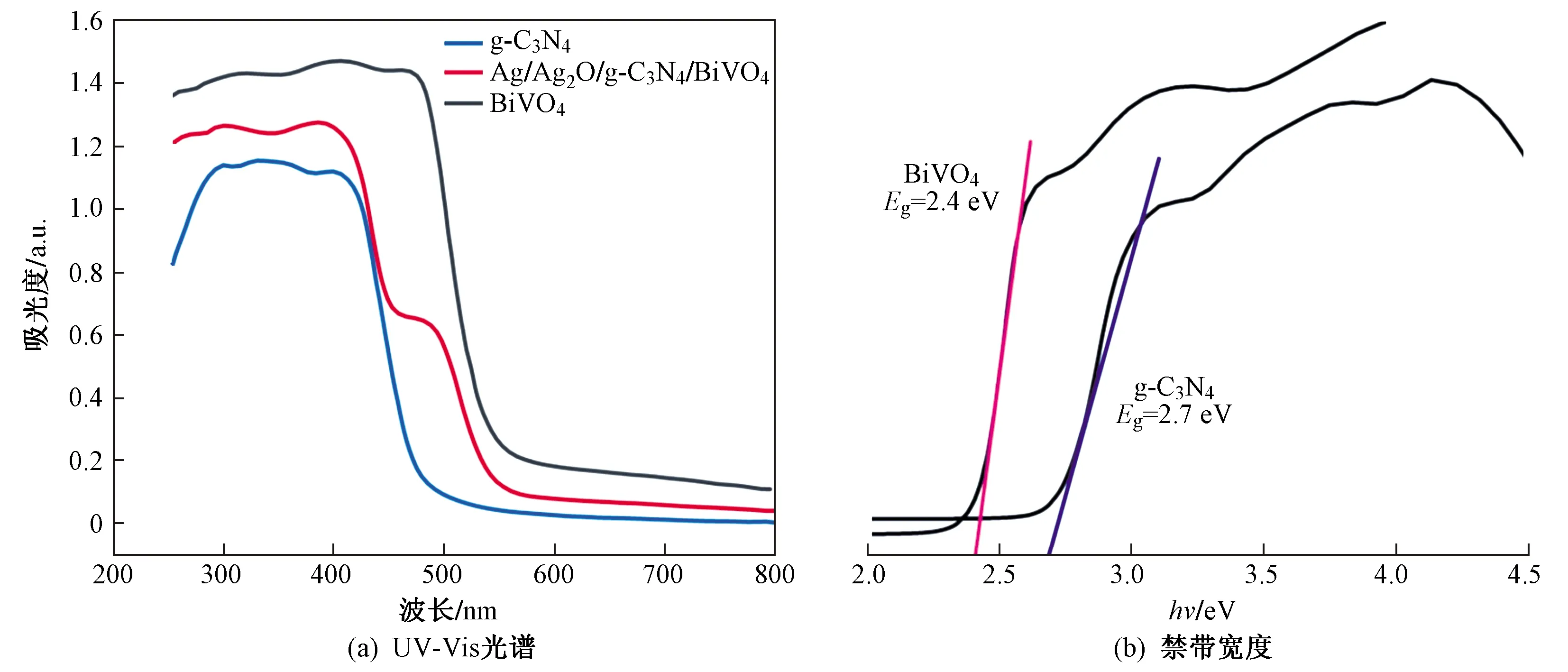
图6 BiVO4、g-C3N4、Ag/Ag2O/g-C3N4/BiVO4的UV-Vis光谱以及BiVO4和g-C3N4的禁带宽度Fig.6 UV-Vis spectra of BiVO4, g-C3N4, Ag/Ag2O/g-C3N4/BiVO4 and forbidden band widths of BiVO4 and g-C3N4
2.5 Ag/Ag2O/g-C3N4/BiVO4复合材料对TC-HCl的降解
通过复合材料光催化TC-HCl的试验,测定制备的BiVO4、g-C3N4、g-C3N4/BiVO4及Ag/Ag2O/g-C3N4/BiVO4的催化性能. 不同光催化剂对TC-HCl降解效果的时间变化曲线如图7所示. 所有材料在黑暗条件下进行30 min的吸附试验,相较于纯BiVO4、纯g-C3N4及g-C3N4/BiVO4,Ag/Ag2O/g-C3N4/BiVO4对TC-HCl的吸附效果显著提高,原因可能是沉积的Ag/Ag2O粒子增加了材料的比表面积,进而更易吸附污染物[32].
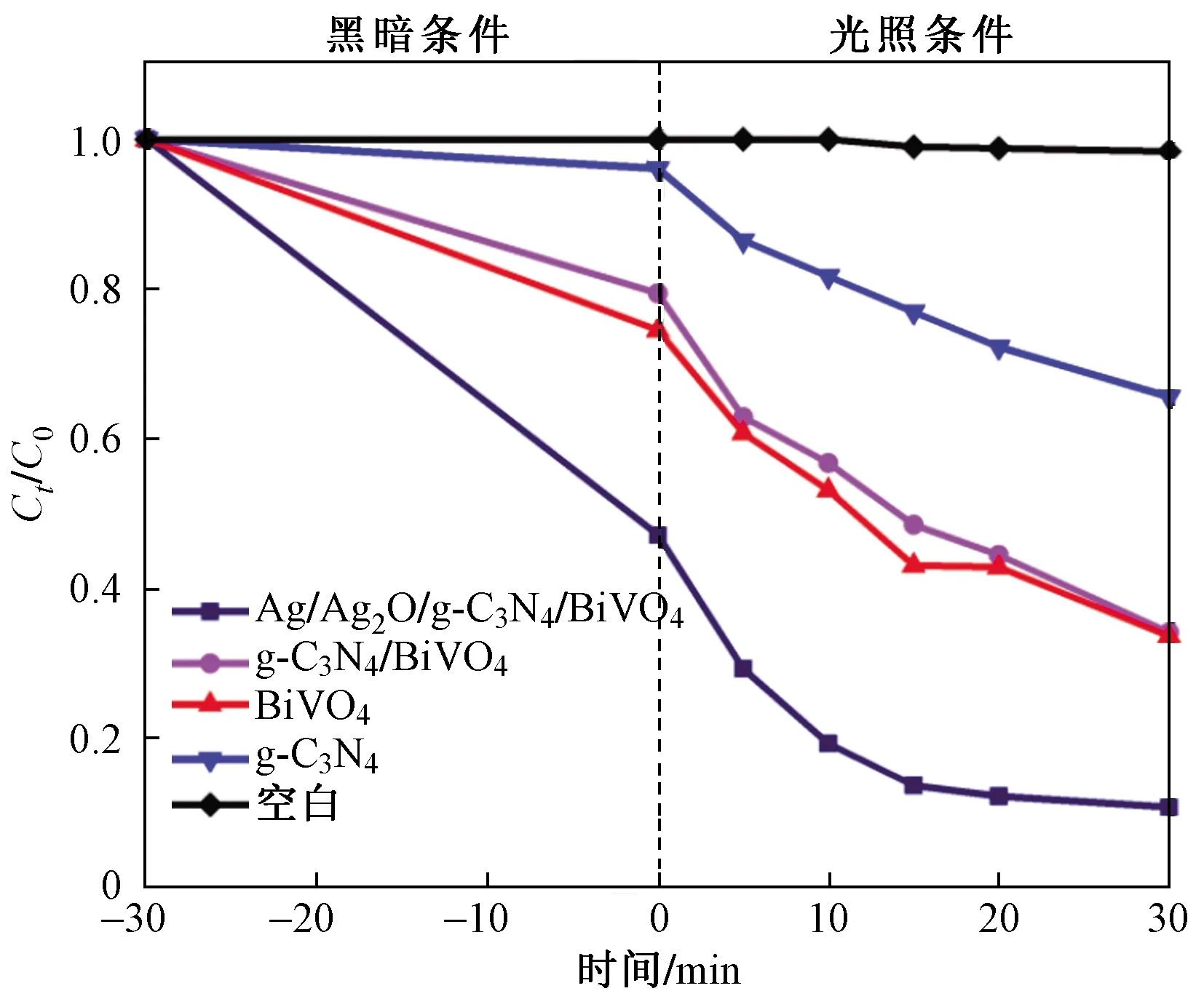
图7 不同光催化剂对TC-HCl降解效果的 时间变化曲线Fig.7 Degradation curves of TC-HCl by different photocatalysts
进入光催化阶段,TC-HCl在自然状态下几乎不发生自降解;Ag/Ag2O/g-C3N4/BiVO4对TC-HCl的光催化降解效果显著强于BiVO4、g-C3N4及g-C3N4/BiVO4,最终降解率达到89.19%,远高于BiVO4的66.34%和g-C3N4/BiVO4的65.86%. 这是因为,纳米Ag粒子产生的表面等离子体共振效应(SPR)[33],拓宽了光响应范围,有效促进了光生电子转移,从而增强了复合材料的光催化性能.
为进一步研究复合材料对TC-HCl的吸附动力学特性,通过拟一级动力学模型[34]对所得数据进行模型拟合.
-ln(CT/C0)=kapT
(5)
式中:CT为不同光催化时间后TC-HCl的浓度,mg/L;kap为反应速率常数;T为光催化时间,min.
由表1可见,拟一级动力学模型拟合结果中R2

表1 不同光催化材料对TC-HCl光催化降解的拟一级动力学参数
整体大于0.93,拟合度较高. 反应速率常数(kap)从小到大依次为g-C3N4、g-C3N4/BiVO4、BiVO4、Ag/Ag2O/g-C3N4/BiVO4. 其中,Ag/Ag2O/g-C3N4/BiVO4的kap最高,达到 0.070 3 min-1,是g-C3N4/BiVO4(kap为 0.030 3 min-1)的2.32倍,是BiVO4(kap为 0.032 0 min-1)的2.20倍,是g-C3N4(kap为 0.014 8 min-1)的4.75倍.
综上,复合了银基材料(Ag/Ag2O)及g-C3N4后的BiVO4光催化剂,其光催化效果显著增强,试验表明,Ag/Ag2O粒子可以有效提高复合材料对TC-HCl的吸附效果,同时Ag粒子的表面等离子体共振效应以及Ag2O与g-C3N4/BiVO4之间形成的异质结,可以抑制光生电子-空穴的快速复合,提高能量转移效率,从而有效促进光催化效率.
2.6 Ag/Ag2O/g-C3N4/BiVO4四元复合材料机理探究
2.6.1稳定性研究
为探究Ag/Ag2O/g-C3N4/BiVO4复合材料的稳定性,对TC-HCl的光催化降解进行了4次重复试验. 如图8所示,经过4次循环后,复合材料对TC-HCl的降解率仍能达到74.8%,证明该光催化剂具有较稳定的降解性能.

图8 Ag/Ag2O/g-C3N4/BiVO4的稳定性试验Fig.8 Experiment of Ag/Ag2O/g-C3N4/BiVO4 stability
2.6.2自由基捕获试验
为检测Ag/Ag2O/g-C3N4/BiVO4在光催化降解过程中产生作用的活性基团,使用乙二胺四乙酸二钠盐(edetate disodium, EDTA-2Na)、异丙醇(iso-propyl alcohol, IPA)、对苯醌(benzoquinone, BQ)分别作为TC-HCl降解反应中的h+,·OH、·O2-作为捕获剂[35-37]. 如图9所示,加入EDTA-2Na后,对光催化效果影响极大,TC-HCl的降解率骤降到11.63%;加入BQ后,对光催化效果影响较大,TC-HCl的降解率降至26.47%;相较之下,加入IPA对复合材料的光催化效果影响较小,TC-HCl降解率达69.56%,仅受到轻微光催化抑制. 捕获试验可证明,在Ag/Ag2O/g-C3N4/BiVO4光催化过程中,h+和·O2-是主要的活性基团,·OH基团同样参与光催化TC-HCl的降解过程,但影响较小. 3种活性基团对光催化降解的影响顺序为h+>·O2->·OH.
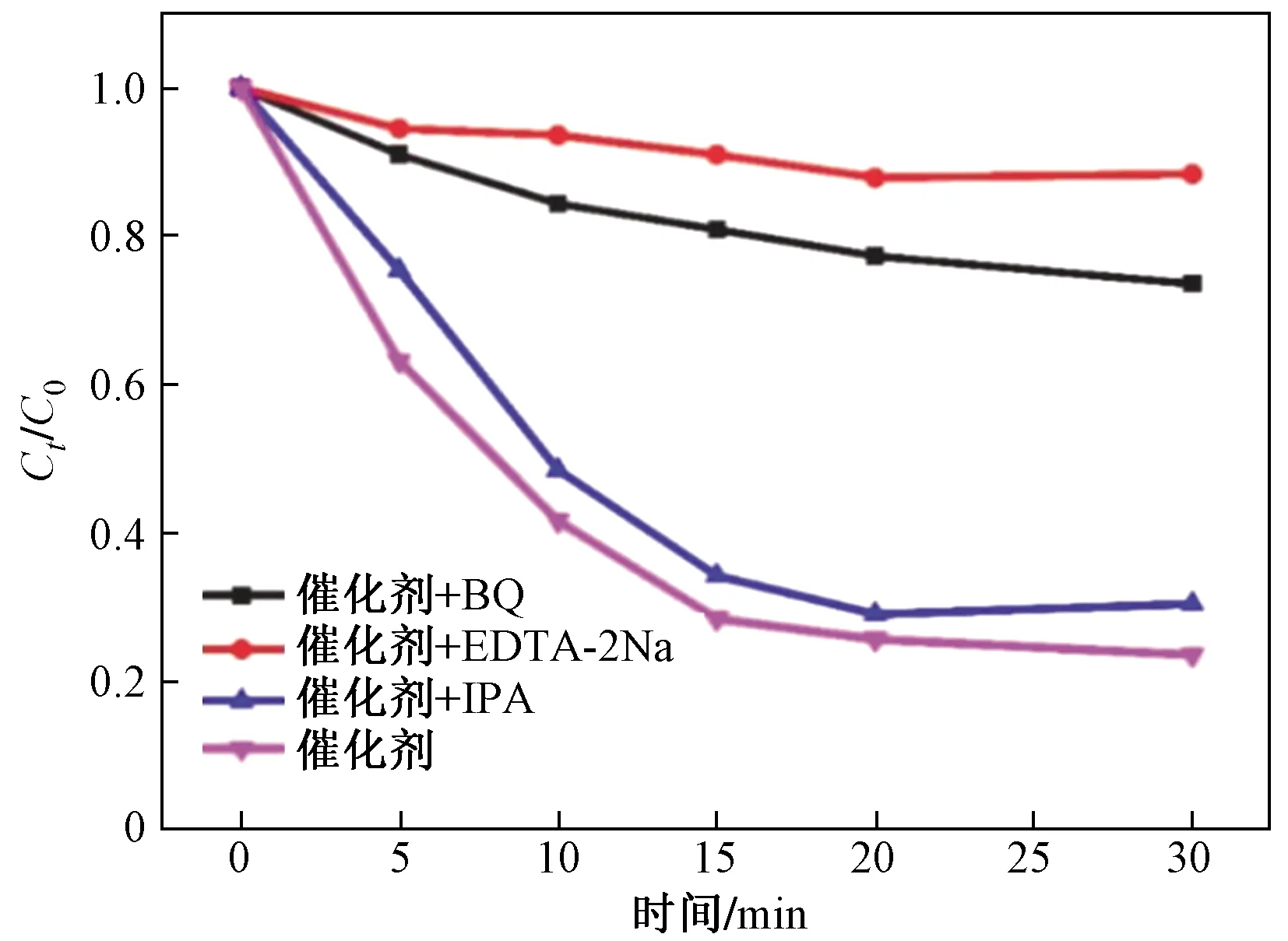
图9 Ag/Ag2O/g-C3N4/BiVO4光催化降解 TC-HCl的捕获试验Fig.9 Capture experiments of Ag/Ag2O/g-C3N4/BiVO4 photocatalytic degradation of TC-HCl
2.6.3光催化降解机理
基于上述表征结果与分析,对Ag/Ag2O/g-C3N4/BiVO4复合材料降解TC-HCl的机理进行分析(见图10). 在可见光照射时,电子因光电功函数差的缘故,会从导带能量高的半导体向能量低的半导体转移,因此g-C3N4导带上被激发的电子会迅速扩散到Ag2O及BiVO4的导带,同时BiVO4价带上的空穴也会迁移到g-C3N4及Ag2O的价带,以平衡费米能级,而在金属Ag粒子和Ag2O之间会形成内部电场,使得Ag2O存在一些带负电区域,Ag和Ag2O之间的强界面静电相互作用会有效抑制光生电子-空穴对的复合,光催化效率得以提高. 电子在内部电场作用下转移到导带上,最终在材料表面被O2所捕获生成·O2-,处于价带的空穴会与材料外部的H2O和OH-发生反应,生成·OH. 这些活性基团(h+、·O2-、·OH)具有强氧化性,使得Ag/Ag2O/g-C3N4/BiVO4复合材料的光催化性能增强.
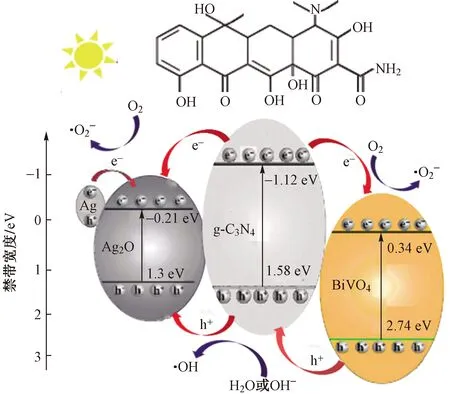
图10 Ag/Ag2O/g-C3N4/BiVO4复合材料的 光催化机理示意Fig.10 Schematic diagram of the possible photocatalytic mechanism of Ag/Ag2O/g-C3N4/BiVO4 composites
3 结论
a) 通过水热法、煅烧法、湿浸渍法、沉淀和热分解法分步制备了Ag/Ag2O/g-C3N4/BiVO4光催化剂,使用XRD、SEM和XPS等表征分析,证明了Ag/Ag2O/g-C3N4/BiVO4复合材料合成成功,沉积Ag/Ag2O 粒子后,复合材料对TC-HCl的吸附能力显著提高;纳米Ag粒子的表面等离子体共振效应(SPR)以及g-C3N4的协同作用拓宽了光响应范围,表现出更好的光催化性能.
b) Ag/Ag2O/g-C3N4/BiVO4四元复合材料对TC-HCl 具有较好的去除效率,最终降解率可达89.19%,相较于BiVO4、g-C3N4及g-C3N4/BiVO4等合成光催化剂,该材料表现出更强的光催化活性,且在4次循环后仍能保持74.8%的降解率.
c) 通过紫外可见漫反射吸收光谱以及X-射线能谱确定了Ag/Ag2O/g-C3N4/BiVO4的可见光响应拓展至548 nm,可激发更多光生电子-空穴对.
d) 通过体系自由基捕获试验证明,在Ag/Ag2O/g-C3N4/BiVO4光催化TC-HCl降解体系中主要的活性物种为h+与·O2-,且h+的影响大于·O2-.
