间歇超声波强化ZVI/PS体系氧化降解磺胺抗生素
2021-12-21崔皓,田禹*,张军
崔 皓, 田 禹*, 张 军
1.哈尔滨工业大学, 城市水资源与水环境国家重点实验室, 黑龙江 哈尔滨 150090 2.哈尔滨工业大学环境学院, 黑龙江 哈尔滨 150090
磺胺类抗生素(SAs)作为一类人工合成的广谱抑菌药,具有合成简单、抗菌谱广、产量大的特点,广泛应用于农业、畜牧业和人类医疗领域[1]. 据统计,2013年我国SAs的总使用量达 7 920 t[2]. 秦延文等[3]研究发现,我国每年排放进入水环境中的抗生素超过5×104t,水环境中抗生素的残留问题引起广泛关注. 长期暴露在SAs环境中,动植物体内会对SAs产生抗性基因[4],通过食物链传播,最终到达人体内,引发人类造血系统紊乱[5]、降低生殖能力[6],甚至引发致畸、致癌、致突变等病变[7],严重威胁人类健康. 因此,亟待开发SAs高效去除技术,减少水环境中SAs的残留[8-9].
利用过硫酸盐(PS)氧化体系去除水中难降解污染物是近年来的研究热点. 与传统的羟基自由基(·OH)相比,PS活化产生的硫酸根自由基(SO4·-)的氧化还原电位更高、半衰期更长,而且在pH为3~11的范围内都有较好的降解效果[10-11]. PS的活化方式有过渡金属活化[12-13]、碱活化[14]、电活化[15]、热活化[16]、光活化[17]、超声波活化[18]等,其中零价铁(ZVI)具有价格低廉、催化效果好等优点,在PS活化领域得到广泛应用[19]. 但是ZVI表面容易生成氧化膜,降低ZVI对PS的活化性能,从而影响污染物降解效率[20]. 而超声波(US)能通过空化作用提高非均相体系的化学反应效率,因此有学者提出将US与ZVI/PS技术联用来处理难降解污染物. Gao等[21]构建US-nZVI/PS体系处理普萘洛尔(PRO),30 min内PRO去除率达到94.2%. 有学者对US-ZVI/PS体系降解二恶烷、三氯甲烷、柠檬酸镍、三氯酚、酸性橙染料等污染物进行研究,证明了US-ZVI/PS体系能够实现多种有机污染物的高效降解[22-26].
综上,US-ZVI/PS体系是一项具有应用潜力的难降解污染物去除技术,但是目前利用US-ZVI/PS体系降解多种SAs的对比研究较少,SAs在该体系中的反应路径也不明晰. 因此,该文将利用US-ZVI/PS体系氧化降解5种典型SAs,检测SAs降解中间产物,总结不同结构SAs的反应路径,以期为水中SAs的高效去除提供理论依据和技术支持.
1 材料与方法
1.1 试验试剂
该研究中使用的主要试剂为ZVI、PS和5种典型SAs(见表1),均购于美国Sigma公司,纯度为分析纯;甲醇和甲酸为色谱纯,购于韩国SK Chemicals公司;氢氧化钠、浓硫酸等为分析纯,购于天津致远化学试剂有限公司.
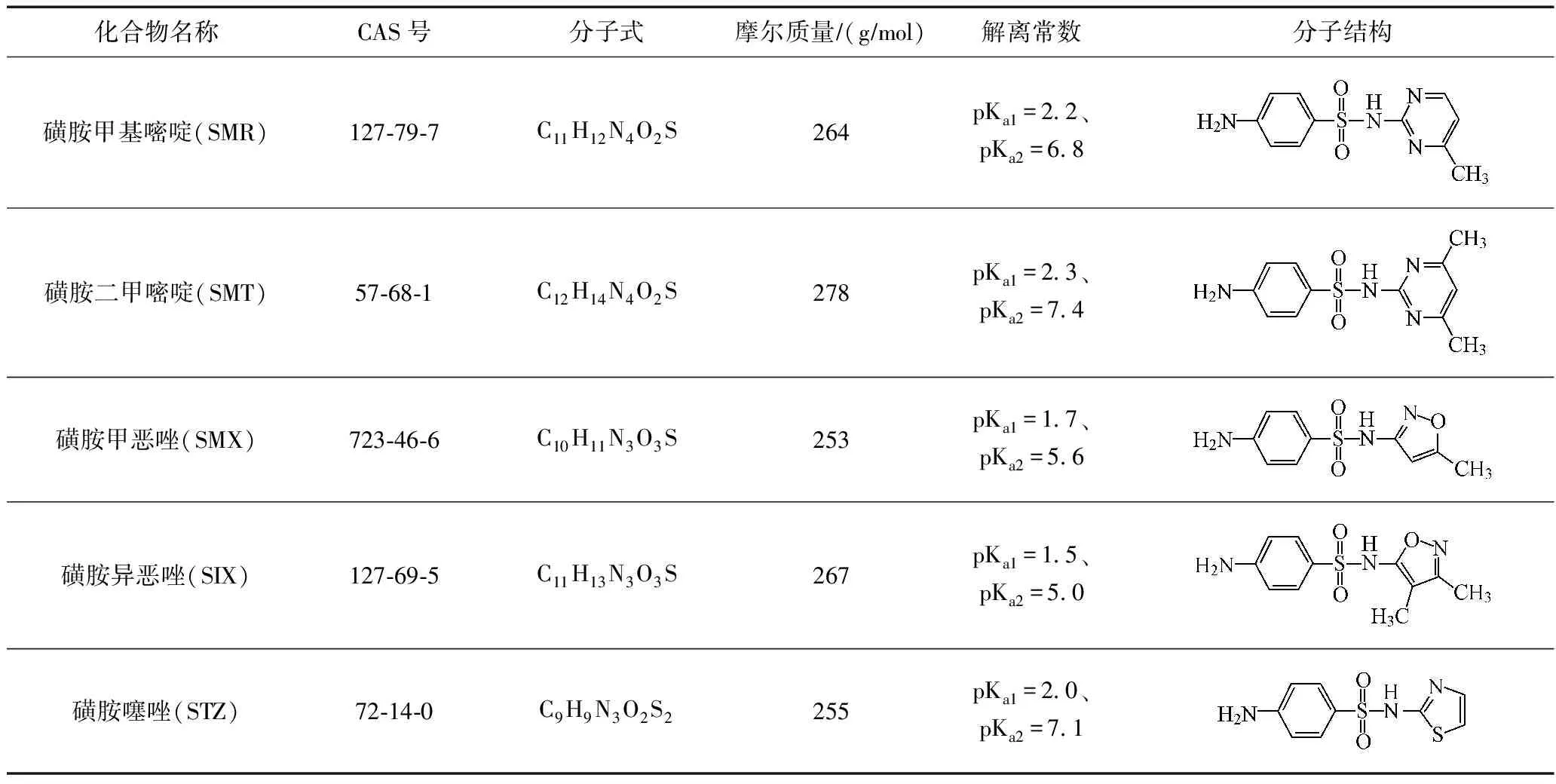
表1 5种典型SAs的性质
1.2 试验方法
Cui等[27]研发了超声波间歇作用的新模式,得到了US-ZVI/PS体系作用的最佳试验条件,超声波强度、pH、ZVI浓度和PS浓度分别为0.25 W/cm3、6.0、0.6 mmol/L和1.4 mmol/L,实现了磺胺嘧啶(SDZ)的高效去除(去除率为97.4%)[27]. 因此,笔者研究沿用该试验条件,若无其他特殊说明,文中所有试验将按照以下步骤进行:①配制200 mg/L的SAs储备液;②将 50 mL SAs储备液移入500 mL容量瓶中,得到初始浓度为20 mg/L的目标污染物溶液,移取400 mL该溶液于反应容器(锥形瓶)中;③初始pH调节为6.0;④向溶液中投加13.41 mg ZVI和133.34 mg PS,并开始反应计时;⑤反应开始2 min后,开启超声中央控制器,按照设定好的超声操作条件运行;⑥取样检测.
US-ZVI/PS体系降解SAs的试验中所使用的超声破碎仪(JY92-IIDN型,宁波新芝生物科技股份有限公司)由超声探头和中央控制器组成,反应开始前,将配有20 mg/L SAs的锥形瓶移入超声反应装置中,将超声探头插入溶液中,距离液面55 mm,超声破碎仪开启60 s后,关闭60 s,循环进行. 反应开始2 min 后,点击中央控制器的启动按钮,按照设定好的程序进行超声破碎. 该试验中采用恒温器和循环水浴,将溶液温度控制在室温.
1.3 分析方法
该研究中,采用高效液相色谱仪(Agilent 1100型,美国Agilent公司)检测SAs的浓度. 按1.2节中试验步骤进行试验,用注射器取样后立即加入500 mmol/L的甲醇终止反应,然后用0.22 μm聚四氟乙烯过滤膜过滤,加入到棕色液相小瓶中. 将液相小瓶放入高效液相色谱仪的进样室内,自动采样器将样品采集进入C18色谱柱(420 mm×250 mm, 5 μm, 美国Agilent公司),然后经过流动相的洗脱作用,最后流入PDA检测器进行定量分析. 该文采用的5种抗生素SMR、SMT、SMX、SIX、STZ的检测波长分别为258、266、270、275和284 nm,具体条件:进样体积10 μL;流动相为乙腈和0.1%甲酸水溶液,体积比依次为15∶85、30∶70、30∶70、15∶85和20∶80,流速为0.2 mL/min;箱体内温度为30 ℃.
SAs降解过程中产生的中间产物由高效液相色谱质谱串联仪测定. 液相色谱柱为C18色谱柱,进样量为10 μL,流动相为乙腈和0.1%的甲酸水溶液(体积比为20∶80),流速为0.2 mL/min,质谱检测器的离子源为电喷雾电离源(ESI),离子电压为80 V,采用正、负离子模式分别进行全扫描,质荷比(m/z)范围设置为50~600. 随后用正离子模式(ESI-MS+)对中间产物进行鉴定,毛细管电压为4.0 kV,锥孔电压为30 V,源温度为600 ℃,脱溶剂温度为900 ℃,碰撞电压为2 kV.
2 结果与讨论
2.1 US-ZVI/PS体系降解5种特征SAs的效能
该研究选取5种特征磺胺抗生素SMR、SMT、SMX、STZ和SIX作为研究对象,探究US-ZVI/PS体系对不同SAs的处理效果,并同时以PS体系和ZVI/PS 体系作为空白组和对照组. 由图1可见,在PS体系中,5种SAs的浓度均没有发生明显变化,反应30 min后,5种SAs的去除率均小于5%,说明未活化PS的氧化性能较差,对SAs几乎没有降解作用. ZVI/PS 体系对5种SAs均有不同程度的去除,说明催化剂ZVI的加入能够提高PS的氧化性能,促进5种SAs的去除. ZVI/PS体系对SMR去除效果最好,去除率为45.5%;对STZ的去除效果最差,去除率为20.5%. ZVI/PS体系的氧化性能虽然高于PS体系,但是对SAs的去除率都小于50%,难以实现SAs的有效去除. 在US-ZVI/PS体系中,5种SAs均得到有效去除,最终去除率均大于95%;同时,达到95%的去除率时,SMX和SIX需要的反应时间较长,猜测可能是由于五元杂环SAs的开环需要更大的能量,因此需要的反应时间较长. 综上,US-ZVI/PS体系能够实现5种典型SAs的高效去除,而且对不同结构的SAs有不同的降解效果.

图1 US-ZVI/PS、ZVI/PS和PS体系降解SMR、SMT、SMX、SIX和STZ的效能Fig.1 The degradation of SMR, SMT, SMX, SIX, and STZ by US-ZVI/PS, ZVI/PS and PS system
2.2 US-ZVI/PS体系降解5种SAs的动力学方程
该研究对US-ZVI/PS体系降解5种SAs的过程进行动力学方程拟合(见图2). SAs在US-ZVI/PS体系中的降解均符合拟一级反应动力学〔见式(1)〕,直线斜率为该SAs的拟一级表观速率常数kobs(单位为min-1). 所有拟合过程R2均大于0.900,证明US-ZVI/PS 体系降解SAs的过程符合拟一级反应动力学.

图2 US-ZVI/PS体系氧化降解5种特征 磺胺抗生素的拟一级动力学曲线Fig.2 The pseudo-first order fitting curves of five SAs degradation by US-ZVI/PS system
ln(Ct/C0)=-kobs
(1)
式中:C0和Ct分别为反应时间为0和t时刻污染物浓度,mg/L;kobs为拟一级反应的表观速率常数,min-1;t为反应时间,min.
根据拟合曲线进行计算,得出SMR、SMT、STZ、SIX和SMX 的kobs分别为0.223、0.215、0.203、0.181和0.119 min-1. 根据5种SAs的结构,US-ZVI/PS体系对六元环SAs (SMR和SMT)的降解速率明显大于五元环SAs (SMX、SIX和STZ). 这说明分子结构对于SAs在US-ZVI/PS体系中降解有重要影响. 因此,有必要检测SAs降解过程的中间产物,从反应路径方向解析SAs结构对于降解效能的影响.
2.3 US-ZVI/PS体系降解5种SAs中间产物分析
利用高效液相色谱质谱串联仪(UPLC-MS-MS)高效分析SAs中间产物有以下步骤:①在正离子模式下,对样品进行全扫描,从色谱图中可知,在不同的停留时间处有不同强度的峰出现,这代表了不同的中间产物;②选择质谱图中某一质核比,再打质谱,如果仍有峰形,说明该质核比下的中间产物可能存在;③对所有峰的特征质核比进行分析,与磺胺母体质核比进行比较,通过加减原子种类和数量,推测可能的断键部位和中间产物的分子结构. 由于篇幅所限,该节内容不赘述中间产物的具体检测和分析过程,而将中间产物的结构和性质通过列表的方式给出.
2.3.1六元环磺胺抗生素(SMR和SMT)降解的中间产物
2.3.1.1SMR降解的中间产物
利用UPLC-MS-MS对US-ZVI/PS体系降解SMR产生的中间产物进行了鉴定. 首先对样品进行正离子模式下的全扫描,检测到了7种主要中间产物的峰,选择其中一个峰进行质谱分析,在一级质谱图上得到该产物对应的质子化离子(用[M+H]+表征),由此可以推断出该产物的分子量;在二级质谱上得到碎片离子(用m/z表征),由此可以推断出该产物的断键部位和分子结构. 该研究中所有SAs产物均采用上述方法进行数据分析. 在SMR降解样品的色谱图中,检测到了7种主要中间产物. 在一级质谱图中得到这7种产物对应的质子化离子分别为[M+H]+295、[M+H]+281、[M+H]+201、[M+H]+174、[M+H]+151、[M+H]+139和[M+H]+124(见表2). [M+H]+295对应的二级质谱碎片离子为m/z197和m/z123,推测其为嘧啶环上甲基的氧化作用,记为产物SMR 294. [M+H]+281对应的二级质谱碎片离子为m/z254和m/z236,根据结构推测为7号N原子受到攻击生成的产物,记为产物SMR 280,与Deng等[28]研究结果相同. 根据二级质谱信息,推测[M+H]+140为嘧啶环的开环产物. [M+H]+201和母体质核比相差64,推测为结构上缺失了1个SO2基团,将此产物记为SMR 200,推测其为“SO2提取”的产物. 根据二级质谱碎片离子m/z110和m/z92,推测[M+H]+174是S—N键断键的产物,记为产物SMR 173,另外一个S—N键断键产物为SMR 150. [M+H]+124的碎片离子为m/z78,为硝基苯,记为产物SMR 123.

表2 SMR降解的中间产物的分子结构式和质谱碎片离子分布
2.3.1.2SMT降解的中间产物


表3 SMT降解中间产物的分子结构式和质谱碎片离子分布
2.3.2五元环磺胺抗生素(SMX、SIX和STZ)降解的中间产物
2.3.2.1SMX降解的中间产物


表4 SMX降解中间产物的分子结构式和质谱碎片离子分布
2.3.2.2SIX降解的中间产物
在SIX降解过程中,检测到了7种主要中间产物,在一级质谱图中得到这7种中间产物对应的质子化离子分别为[M+H]+298、[M+H]+228、[M+H]+201、[M+H]+174、[M+H]+113、[M+H]+98和[M+H]+94(见表5). [M+H]+298对应的二级质谱碎片离子为m/z252、m/z116和m/z96,根据结构推测为7号N原子受到攻击生成的产物,记作产物SIX 297. [M+H]+213的二级质谱碎片离子为m/z116和m/z92,根据结构推测其为异恶唑五元环的开环产物,记为产物SIX 227,其攻击位点为13号碳原子. SO4·-能使五元杂环直接被打开,形成产物SIX 200. [M+H]+174为S—N键断裂的产物,是SAs降解过程中的常见产物——对氨基苯磺酸,记为产物SIX 173. 根据二级质谱碎片离子m/z93、m/z80和m/z65,推测[M+H]+113是S—N断键的另一个产物,记为产物SIX 112,在Liu等[31]研究中也有检出. 而[M+H]+98与[M+H]+113相差15,说明二者分子结构相差1个 —NH2基团,推测[M+H]+98为产物SIX 112的去氨基化产物,记为产物SIX 97. [M+H]+94的碎片离子为m/z77,为产物SIX 173的进一步降解产物,记为产物SIX 93.

表5 SIX降解中间产物的分子结构式和质谱碎片离子分布
2.3.2.3STZ降解的中间产物
在STZ降解过程中,检测到了7种主要的中间产物,在一级质谱图中得到这7种中间产物对应的质子化离子分别为[M+H]+290、[M+H]+286、[M+H]+219、[M+H]+174、[M+H]+140、[M+H]+135和[M+H]+101(见表6). [M+H]+290对应的二级质谱碎片离子为m/z156、m/z108和m/z92,根据结构推测其为羟基加成的产物,记为产物STZ 289. [M+H]+286的二级质谱碎片离子为m/z241、m/z162和m/z92,根据结构推测其为7号N原子的氧化产物,记为产物STZ 285. [M+H]+174为S—N键断裂的产物,是SAs降解过程中的常见产物——对氨基苯磺酸,记为产物STZ 173. [M+H]+140的二级质谱碎片离子为m/z110、m/z81和m/z54,根据结构推测其为S—N键断裂的产物,记为产物STZ 139. 根据二级质谱离子m/z74和m/z59,推测[M+H]+101为S—N断键的另一个产物,记为产物STZ 100. 而[M+H]+135与[M+H]+101相差34,分子结构相差2个—OH基团,推测[M+H]+135为产物STZ 100的氧化产物,记为产物STZ 134.

表6 STZ降解中间产物的分子结构式和质谱碎片离子分布
2.4 US-ZVI/PS体系降解5种SAs的反应路径
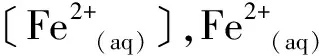

图3 US-ZVI/PS体系降解5种SAs的反应路径Fig.3 The degradation pathways of SAs by US-ZVI/PS system
3 结论
a) PS体系对5种SAs几乎没有降解作用,虽然ZVI/PS体系的氧化性能高于PS体系,但是对5种SAs的去除率也均小于50%,难以实现SAs的有效去除. 而在US-ZVI/PS体系下,5种SAs得到有效去除,最终去除率均大于95%;同时,5种SAs去除率达95%时,SMX和SIX需要的反应时间较长.
b) US-ZVI/PS体系降解SMR、SMT、SMX、SIX和STZ过程均符合拟一级反应动力学,其表观速率常数(kobs)大小依次为SMR(0.223)>SMT(0.215)>STZ(0.203)>SIX(0.181)>SMX(0.119),六元环SAs的反应速率明显高于五元环SAs.
c) 5种SAs共同的反应路径包括S—N键断裂、C—N键断裂、苯环羟基化、苯胺氧化和R取代基氧化过程,而六元环SAs反应路径多一个N—N重排过程. 2种六元环SAs分子结构的区别在于R取代环上的甲基取代基的数量和位置不同,由此影响到R取代环的整体电子云密度分布,从而导致不同的初级氧化产物的生成,对后续降解过程产生影响.
