对燃烧法测定氧气含量实验的再认识
2021-12-19陆伟生
陆伟生


[摘 要]在燃烧法测定空气中氧气含量的实验中,我们经常会分析哪些因素会导致氧气测量结果偏小。其实,还存在着一个导致氧气测量结果偏大的因素,那就是将燃烧物的火焰移入集气瓶时,火焰的上方存在一定量的“热空气团”,这些“热空气团”处于高温膨胀状态,当火焰移入容器熄灭后,这部分“热空气团”就会冷却收缩,造成瓶内气压变小,导致氧气含量的测量结果偏大。这个因素比较隐蔽,很多时候会被忽略或误判。
[关键词]热空气团;燃烧法;氧气含量;测量结果;偏大
[中图分类号] G633.8 [文献标识码] A [文章编号] 1674-6058(2021)35-0086-02
一、问题的来源
2020年上海市“空中课堂”六年级科学第五单元《空气的组成②》一课中,教师在讲授空气中氧气的比例时,播放了一个演示实验(下称实验一):将一支小蜡烛置于一小盘中,小盘浮于盛有水的大盘中央。点燃蜡烛后,用一个玻璃杯倒扣蜡烛,一会儿后,蜡烛的火焰熄灭了,随后有较多的水进入玻璃杯(如图1)。
接着,教师讲道:蜡烛燃烧消耗掉杯中氧气,水面上升的体积大致相当于杯中原有氧气的体积。
但这样的结论从化学原理来分析是不被认可的。具体分析如下:蜡烛的主要成分是石蜡,石蜡是从石油的含蜡馏分经冷榨或溶剂脱蜡而制得的,是几种高级烷烃的混合物,主要是正二十二烷(C22H46)和正二十八烷(C28H58),含碳元素约85%,含氢元素约14%。根据反应原理,少部分氧气与氢元素结合生成水,大部分氧气与碳元素结合生成二氧化碳,这会补充氧气所消耗的体积,杯子内的气压是不会明显变小的,也就是火焰熄灭后,按理水是不会进入杯子内的。但事实胜于雄辩,火焰熄灭后,几乎是同时,水确实进入了杯子内,而且量也不少,约占杯子容积的五分之一,这到底是什么原因呢?
笔者当时猜想的原因是,反应生成的二氧化碳溶于水中,造成杯子内气压减少。但笔者用石灰水替代水重复该实验时,火焰熄灭后,石灰水几乎不变浑浊,水进入杯子的现象也不变。从现象来分析,火焰熄灭的同时,水就立即进入杯子,这么短的时间内,杯内的二氧化碳是来不及溶解于水中的。
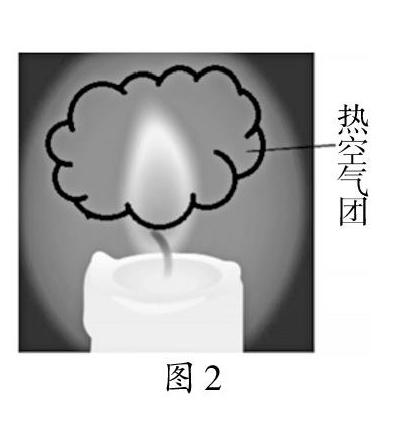
经过更多的思考與分析,笔者认为,蜡烛火焰熄灭后,水进入杯中的真正原因是蜡烛火焰上方的“热空气团”(如图2)造成的。这一团热空气温度较高,当玻璃杯扣到蜡烛火焰上方导致火焰熄灭后,它就会冷却收缩,造成杯子内气压变小,因而导致水进入杯中。因此,水不是因为氧气的减少而进入杯中的。
以上的分析只是推理,可不可以通过实验来证明呢?
二、实验与探究
笔者做了探究实验二,具体如下:
采用教材中的经典装置(如图3)进行实验,只是将红磷用蜡烛代替。要确保操作规范准确,特别要注意当火焰移入集气瓶时要做到迅速、准确,确保不会因为双孔塞塞入过慢而导致氧气含量的测量结果偏高。集气瓶的容积为178毫升(塞完双孔塞后集气瓶的容积为169毫升,实验用数据以此为依据)。实验时,蜡烛火焰熄灭后稍冷却,有水进入集气瓶中,倒出进入瓶内的水测其体积。实验重复三次,测得水的体积的平均值为 19毫升。而且火焰一熄灭,水马上进入瓶中,与蜡烛在盘中燃烧(实验一)的现象如出一辙。但实验二中火焰熄灭后,进入的水的体积明显不如实验一进得多。笔者以为这是因为实验一中的蜡烛火焰是静止的,上方积累的“热空气团”较多,而实验二中的蜡烛火焰是移入集气瓶中的,在移动过程中“热空气团”有散失,故火焰熄灭后进入瓶中的水不多。
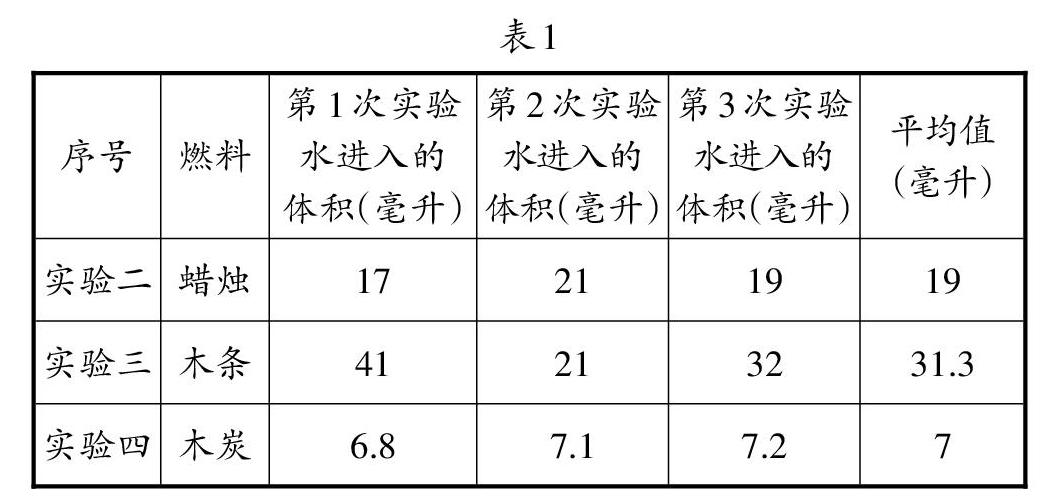
为了验证以上的推理,笔者做了探究实验三、探究实验四,分别用木条、木炭作为燃料替代红磷进行实验,装置与实验二相同,每一个实验重复三次,集气瓶(塞好双孔橡胶塞后)的容积均为169毫升。火焰熄灭后水进入的体积数据如表1所示。
附加现象一:当木条火焰较大时,进入瓶中的水要比火焰较小时量要大,两者相差较大。
附加现象二:木炭烧得红热后放入集气瓶中,立即塞紧双孔塞,一段时间内水不会进入,约3分钟后,水才缓缓地进入瓶中。
按照化学教材上的经典说法,燃烧法测量空气中氧气的比例时选用红磷的原因是,红磷燃烧后的生成物是五氧化二磷,是一种固体,故火焰熄灭后会造成集气瓶内气压变小,水在外界大气压的作用下进入集气瓶。
笔者之所以选择木条和木炭作为实验对照用燃料,是因为这两种物质根据教材实验原理,是不能用于燃烧法测量空气中的氧气含量实验的,原因是它们燃烧后会产生同体积的二氧化碳,填补了所消耗的氧气体积,瓶内气压不会变小。但事实上,火焰熄灭后,仍有一定量的水会进入集气瓶内,最多的为木条实验,会进入18%左右(31.3/169),可见确实是火焰上方的“热空气团”的作用使然。
那么使用红磷燃烧法测量空气中的氧气含量时,这种火焰上方的“热空气团”效应会存在吗?答案是肯定的。
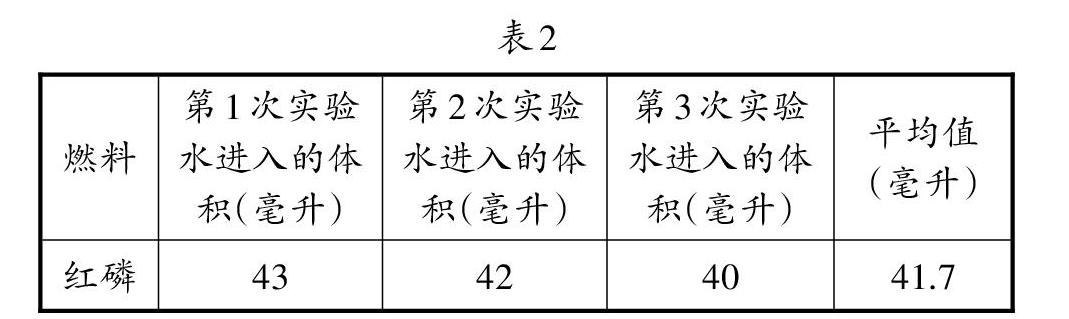
为此,笔者也精确地做了红磷燃烧实验(实验五),实验数据如表2所示。
实验分析:集气瓶容积为169毫升,其五分之一约为34毫升,但事实上进入集气瓶的水约41.7毫升,超过理论值7毫升多。由此证明,用红磷燃烧法做此实验时,确实存在“热空气团”效应,而且影响不小。我们平时实验时也有所发现,即火焰熄灭后,进入的水不是少了而是多了,常常无法解释,也容易被忽略,在此得以证明。
三、结论与应用
这样看来,燃烧法测量空气中的氧气含量时,影响实验结果的因素较多,而平时我们只分析了实验结果偏小的原因,不外乎:气密性不良、红磷不够、集气瓶未冷却、导管内留有水柱等。随着传感器在实验中的广泛应用与发展,发现红磷燃烧实验中火焰熄灭后,集气瓶中的氧气并没有完全耗尽,而实验最后剩余的氧气含量约为7%,相当于原有的氧气只消耗了67%剩下了约33%。这可是个不小的数据,但为什么我们一直没发现氧气的测量结果偏小呢?原因就在这儿,该实验还存在着氧气测量结果偏大的因素,即火焰上方的“热空气团”效应,当两者同时产生作用时,常常相互掩盖,使两者均不容易被发现。
对燃烧法测量氧气含量实验的全面认识,也有助于解答相关问题,如下面的习题:
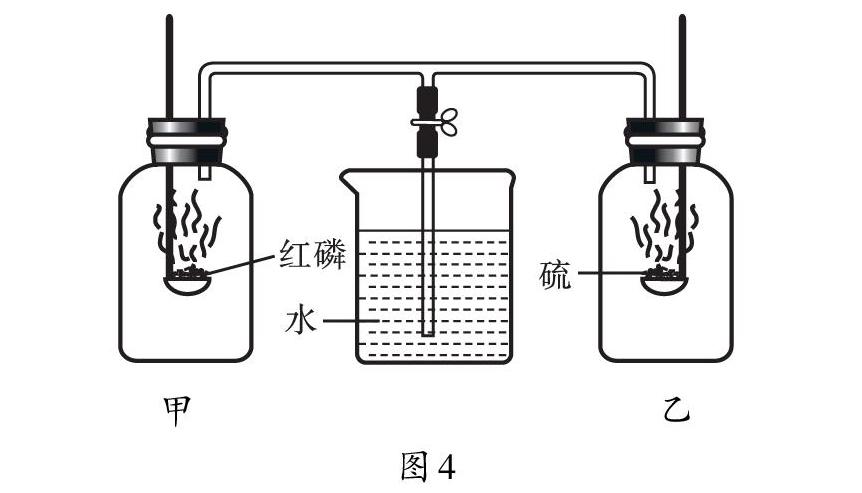
如图4所示,等体积的甲、乙两集气瓶内充满空气,燃烧匙内分别盛有过量的红磷和硫粉,点燃它们充分反应后,冷却至室温,打开弹簧夹,出现的现象是( )。
A.甲瓶中有水流入,而乙瓶中没有水流入
B.甲瓶中没有水流入,而乙瓶中有水流入
C.甲、乙瓶中均有水流入
D.甲、乙瓶中均无水流入
从以上的分析不难看出答案应该是C,但有部分教师想当然地认为答案是A。可见,有些平时想象中不可能出现的结果,有时候也会存在,只不过被我们忽略了,如果还有人将此作为结论来考学生,实在有一点误人子弟了。
真没想到,一个做了多年的经典实验,居然还有我们没有考虑到的因素,甚至还会颠覆我们对原实验的认识。正是验证了著名化学家付鹰说的话“化学是实验的科学,只有实验才是最高法庭”,可见实验可以对观点做出最公正的判决。
[ 参 考 文 献 ]
[1] 陈学东,严西平.红磷、白磷在密闭容器中燃烧的耗氧量探究[J].化学教与学,2014(7):90-91.
[2] 王祖浩,王磊.义务教育教科书化学:上册[M].上海:上海教育出版社,2013:13-14.
[3] 张贞,杨承印.空气中氧气含量测定实验原理探析[J].中学化学教学参考,2010(11):36-37.
(责任编辑 罗 艳)
