不同中药注射液联合常规治疗用于重症急性胰腺炎疗效与安全性的网状Meta分析
2021-12-16马玉景郎晓猛刘建平李佃贵
马玉景,郎晓猛,康 欣,杨 倩,刘建平*,李佃贵
·循证医学与临床用药·
不同中药注射液联合常规治疗用于重症急性胰腺炎疗效与安全性的网状Meta分析
马玉景1,郎晓猛2,康 欣2,杨 倩2,刘建平2*,李佃贵2
1. 河北中医学院第一附属医院,河北省 石家庄 050013 2. 河北省中医院,河北省 石家庄 050013
应用网状Meta分析的方法评价不同中药注射液联合常规治疗重症急性胰腺炎(severe acute pancreatitis,SAP)的疗效及安全性。计算机检索PubMed、EMbase、Cochrane、Web of Science、中国知网(CNKI)、万方(Wanfang)、维普(VIP)等数据库,检索时间为各数据库建库至2021年9月1日。根据纳入、排除标准,由2名研究者独立进行文献检索,按照Cochrane协作网制定的Cochrane风险偏倚评估工具进行质量评价,应用Stata 14.0软件进行统计分析。最终纳49项临床随机对照试验(randomized controlled trials,RCTs),涉及10种中药注射液,3820例患者。网状Meta分析结果显示,临床疗效排序从优到劣为参麦注射液、丹参川芎嗪注射液、参芎葡萄糖注射液、血必净注射液、灯盏花素注射液、川芎嗪注射液、丹红注射液、丹参注射液、复方丹参注射液分别联用常规治疗;病死率排序从低到高为丹参川芎嗪注射液、血必净注射液、灯盏花素注射液、参附注射液、复方丹参注射液、丹参注射液、丹红注射液分别联用常规治疗;血淀粉酶恢复时间排序从优到劣为参芎葡萄糖注射液、丹参注射液、丹参川芎嗪注射液、灯盏花素注射液、血必净注射液、参麦注射液、复方丹参注射液分别联用常规治疗;不良反应发生率从低到高为川芎嗪注射液、血必净注射液、复方丹参注射液、丹参川芎嗪注射液、参麦注射液、丹参注射液分别联用常规治疗。在常规治疗基础上联合不同中药注射液可提高SAP的临床疗效,降低病死率,缩短血淀粉酶恢复时间,降低不良反应发生率,但由于纳入研究的局限性,方法学质量普遍不高,应谨慎选择用药,未来仍需开展多中心、大样本、高质量的RCTs予以验证。
中药注射液;重症急性胰腺炎;网状Meta分析;随机对照试验;参麦注射液;丹参川芎嗪注射液;参芎葡萄糖注射液;血必净注射液;灯盏花素注射液;川芎嗪注射液;丹红注射液;丹参注射液;复方丹参注射液;参附注射液
重症急性胰腺炎(severe acute pancreatitis,SAP)是临床上常见且来势极为凶险的一类急腹症,起病急、进展快,临床病理变化复杂,早期即可引发全身性炎症反应综合征、急性呼吸窘迫综合征、多器官功能障碍综合征,病死率高达20%~30%[1]。如何早期发现SAP的危险因素,对症处理,控制病情发展,降低病死率是胰腺炎临床研究中关注的重点。临床上对SAP的治疗主要包括禁食、禁水、胃肠减压、液体复苏、抗感染、抑制胰酶分泌、维持水电解质平衡、纠正酸碱平衡、重要器官功能监测、营养支持、手术等,但疗效仍不理想。大量的临床随机对照试验(randomized controlled trials,RCT)显示[2-50],在常规治疗的基础上联用中药注射液能有效提高SAP临床疗效,降低病死率,缩短血淀粉酶恢复时间,且不良反应较低。市面上常见的中药注射液多达10余种,且各自有其疗效特点与优势,尚缺乏有关治疗效果的直接比较研究,给临床医生精准地用药选择造成一定的困扰,不利于最佳治疗方案的抉择。网状Meta分析作为传统Meta分析的扩展,其优势在于通过对同一疾病共同对照组之间进行间接比较,对不同干预措施进行定量化的统计分析,并可对结局指标的优劣进行排序,从而为临床用药提供证据支持[51]。本研究采用网状Meta分析的方法,比较不同中药注射液联合常规治疗SAP的疗效及安全性,以期为临床用药提供更可靠的参考证据。
1 资料和方法
1.1 纳入标准
1.1.1 研究类型 RCT,无论是否采用盲法及分配隐藏方式。
1.1.2 研究对象 (1)纳入受试者符合以下任意1项SAP诊断标准:《中国急性胰腺炎诊治指南》中有关SAP的诊断标准[52];《急性胰腺炎诊治指南》有关SAP的诊断标准[53];《重症急性胰腺炎中西医结合诊治指南》[1];2019 WSES Guidelines for the Management of Severe Acute Pancreatitis[54]。(2)同一研究不同干预措施组患者在性别、年龄、病情严重程度及病程上无明显基线失衡,二者具有可比性。
1.1.3 干预措施 治疗组为中药注射液联合常规治疗;对照组为单独常规治疗,或中药注射液联合常规治疗(中药注射液与治疗组不同)。2组的常规治疗方案相同,主要包括禁食、禁水、胃肠减压、液体复苏、抗感染、抑制胰酶分泌、维持水电解质平衡、纠正酸碱平衡、重要器官功能监测、营养支持等基础治疗。
1.1.4 结局指标 (1)主要结局指标:①临床疗效,参照《中国急性胰腺炎诊治指南》[52]。临床症状包括发热、腹痛、腹胀、恶心等基本消失;主要体征包括腹部压痛、反跳痛,腹肌紧张消失;相关检验指标包括血常规、血淀粉酶、尿淀粉酶恢复水平,按治愈、显效、有效、无效4个级别评定疗效情况。治愈:5 d内达到上述3项标准;显效:7 d内达到上述3项标准;有效:10 d内达到上述3项标准;无效:超过10 d仍未达上述3项标准。总有效率=(治愈例数+显效例数+有效例数)/总例数;②病死率。(2)次要结局指标:①血淀粉酶恢复时间;②不良反应发生率,主要包括出现恶心、呕吐、眩晕、腹压升高、肝功能异常、肾功能异常等。
1.2 排除标准
(1)研究类型非RCT,如队列研究、横断面研究、病例对照研究、综述、动物实验等。(2)干预措施受其他治疗措施干扰,如口服中药、针灸、贴敷等。(3)无法获取全文、重复发表。
1.3 数据库和检索策略
计算机检索PubMed、EMbase、Cochrane、Web of Science、中国知网(CNKI)、万方(Wanfang)、维普(VIP)数据库。检索时间自各数据库建库至2021年9月1日。采用主题词与自由词相结合的方式,每个数据库检索策略根据数据库特点做相应调整。中文数据库检索主题词为“重症急性胰腺炎”“注射”“随机对照试验”;自由词:“急性重症胰腺炎”“注射液”“注射用”“提取物”“注射剂”“分配”“随机对照试验”“对照临床试验”“临床试验”“临床研究”“RCT”。英文数据库检索MeSH为“severe acute pancreatitis“injections”“traditional Chinese medicine”;all fields:“acute severe pancreatitis”“injection”“injectables”“injectable”“Chinese traditional medicine”“zhongyi”“zhongyao”。此外,还对会议论文、学位论文、Cochranea临床对照试验数据库、NRR、CCT、Opengrey、GreyNet、DARE网站进行了灰色文献检索。
1.4 文献筛选及数据提取
2名研究者根据制定的检索策略独立筛选文献,将检索出的文献导入EndNoteX9软件,剔除重复文献;将剩余文献根据确立的纳入标准与排除标准,通过阅读题目与摘要删除不合格的文献;阅读全文做进一步的筛选,如有分歧,与第3方一起讨论,是否决定纳入相关文献。提取资料基本信息包括:第一作者、发表年份、样本量、性别、年龄、干预措施、疗程、结局指标。
1.5 偏倚风险评价
2名研究者严格遵守Cochrane协作网制定的Cochrane风险偏倚评估工具,主要从随机方法、分配方案隐藏、盲法、结果评价者盲法、结局数据的完整性、选择性报告研究结果、其他偏倚风险来源7个方面对文献进行偏倚风险评估。
1.6 GRADE证据质量评价
根据GRADE系统[55]从以下5个方面评价证据质量:偏倚风险、不直接性、不一致性、不精确性和发表偏倚,将证据质量分为高、中、低和极低4个级别。
1.7 统计分析
采用Stata14.0软件选择频率学框架随机效应模型进行网状Meta分析,本研究结局指标计数资料采用比值比(odds ratio,OR)为效应指标,计量资料采用平均差(mean deviation,MD);各效应量均以其95%置信区间(confidence interval,CI)表示。先将3臂及3臂以上研究拆分成两两对比的组合,绘制证据网络图。采用比较-校正漏斗图识别研究间的小样本效应,进行发表偏倚检验。对于每个结局指标,使用累积排名曲线下面积(surface under the cumulative ranking,SUCRA)值对干预措施的疗效进行排序。当证据网络图中存在闭环时,使用节点拆分方法来计算直接比较证据和间接比较证据之间的差异。
2 结果
2.1 文献检索结果
根据制定的检索策略,初步检索308篇文献,利用EndNote X9软件查重后获得156篇文献,通过阅读题目、摘要、全文筛查后,最终纳入49篇文献,均为中文文献。文献筛选流程见图1。
2.2 文献基本特征
共纳入49项RCTs[2-50],总样本量3820例,均为双臂研究,10种中药注射液分别为血必净注射液、参麦注射液、丹参川芎嗪注射液、复方丹参注射液、灯盏花素注射液、川芎嗪注射液、丹参注射液、丹红注射液、参附注射液、参芎葡萄糖注射液,其中36项[2,4-8,10-13,16,19,20-22,24-28,31-32,35-36,38-39,41-50]报道了临床疗效,16项[3,9,12,14-15,17-18,20-22,33-34,37,39-41]报道了病死率,16项[4,8,10-11,21-22,24,29-30,44,46]报道了血淀粉酶恢复时间,13项[4,810-11,21-22,24-24,29-30,44,46-47]报道了不良反应发生率(表1)。
2.3 质量评价
纳入的49篇文献均采用随机分组的方法,15项[4,11,17,20-21,23,27,29-30,33,36,39-40,49-50]采用随机数字表法,1项[46]采用抽签法,1项采用信封法[38],1项[41]按住院顺序随机分组,其余未说明具体随机方法;所有研究未提及具体的分配隐藏方案及盲法;总体数据完整性好;未存在选择性报告;其他偏倚情况不清楚(图2)。
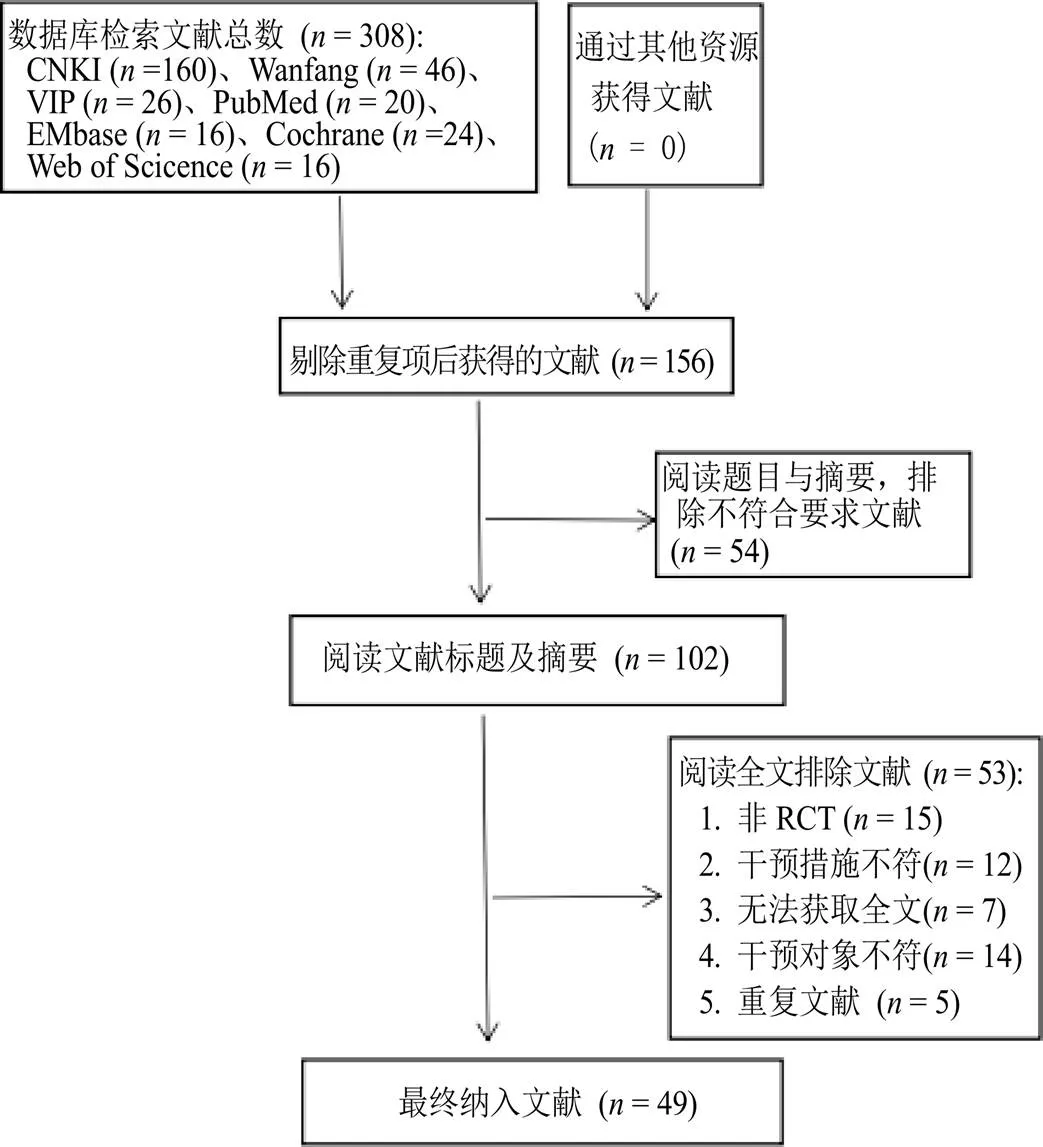
图1 文献筛选流程
2.4 临床疗效
2.4.1 证据网络图 36项研究报道了临床疗效[2,4-8,10-13,16,19,20-22,24-28,31-32,35-36,38-39,41-50],涉及9种中药注射液,9个直接比较,无闭合环形成。图中线的粗细代表研究数量的多少,圆点大小代表样本量的大小。结果显示,血必净注射液联合常规治疗的研究数量最多(13个RCTs),样本量最大(1170例)(图3)。
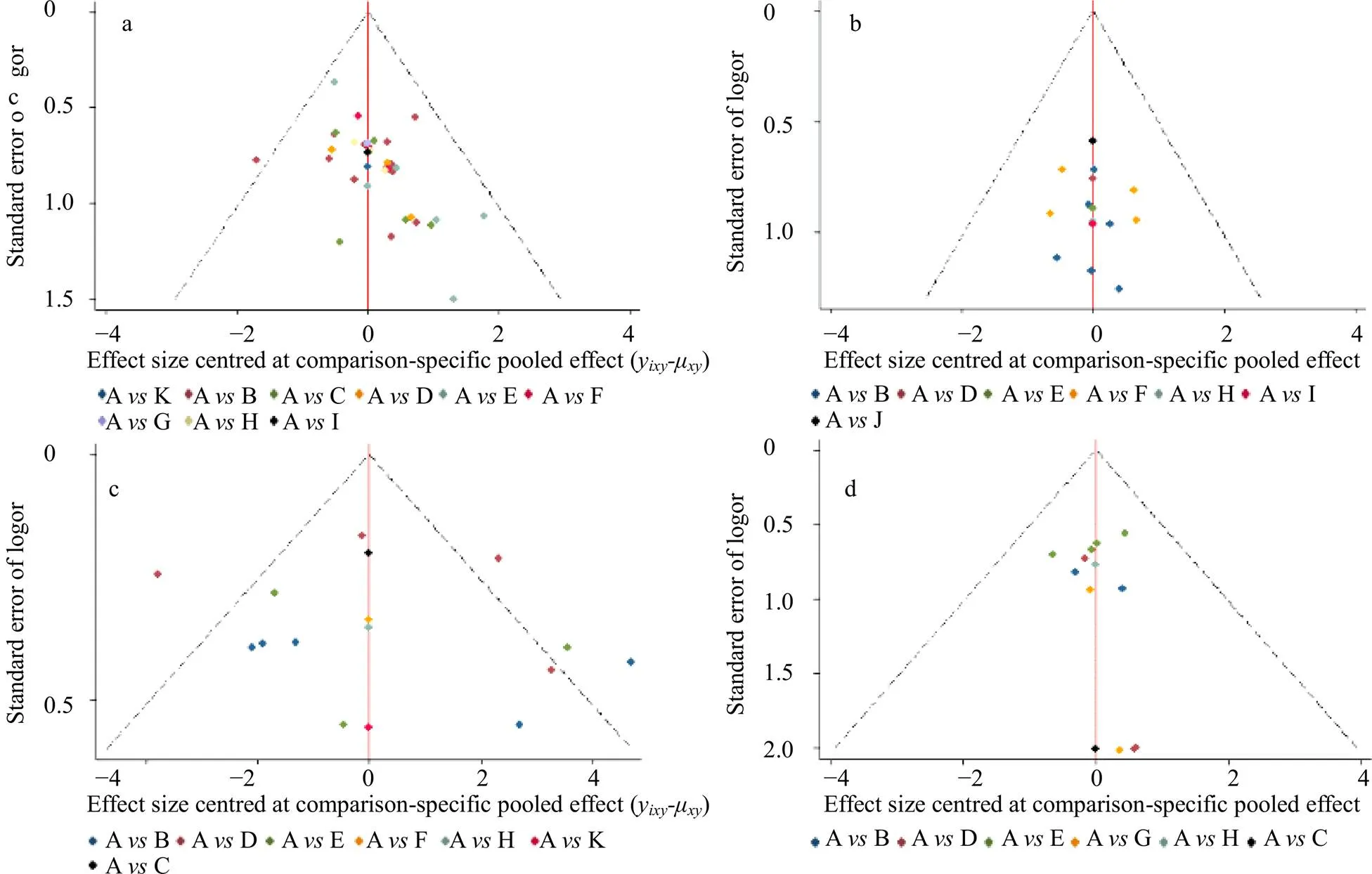
2.4.2 发表偏倚 比较-校正漏斗图结果显示研究大致分布于=0垂直线两侧,提示存在发表偏倚和小样本效应可能性较小(图4-a)。
2.4.3 网状Meta分析 网状Meta分析共产生45个两两比较,其中7个比较差异有统计学意义,与常规治疗相比,参芎葡萄糖注射液、丹参注射液、灯盏花素注射液、复方丹参注射液、丹参川芎嗪注射液、参麦注射液、血必净注射液分别联合常规治疗的临床疗效更优,差异具有统计学意义,分别为OR=5.56,95% CI [1.14,27.07];OR=3.69,95% CI [1.60,8.49];OR=4.21,95% CI [1.99,8.89];OR=3.47,95% CI [2.06,5.85];OR=5.42,95% CI [2.13,13.81];OR=5.51,95% CI [2.63,11.54];OR=4.08,95% CI [2.65,7.6.27]。其余干预措施两两比较差异均无统计学意义(表2)。

表1 纳入研究的基本特征
续表1
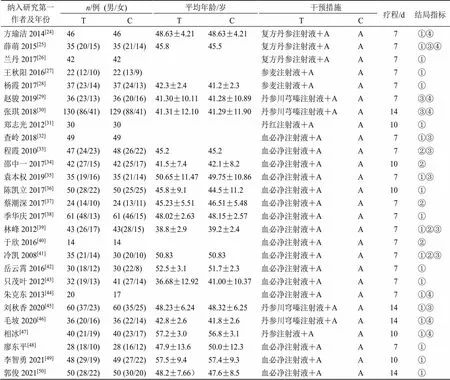
纳入研究第一作者及年份n/例(男/女)平均年龄/岁干预措施疗程/d结局指标 TCTCTC 方瑜洁2014[24]464648.63±4.2148.63±4.21复方丹参注射液+AA 7①④ 薛萌2015[25]35 (20/15)35 (21/14)45.845.5复方丹参注射液+AA 7①③④ 兰丹2017[26]4242 复方丹参注射液+AA 7① 王秋阳2016[27]22 (12/10)22 (13/9) 参麦注射液+AA 7① 杨霞2017[28]37 (23/14)37 (24/13)42.3±2.441.2±2.3参麦注射液+AA 7① 赵骏2019[29]36 (23/13)36 (20/16)41.30±10.1141.28±10.89丹参川芎嗪注射液+AA 7③④ 张琪2018[30]130 (86/41)129 (88/41)41.31±12.1041.29±11.90丹参川芎嗪注射液+AA14③④ 郑志光2012[31]3030 丹红注射液+AA10① 查岭2018[32]4949 血必净注射液+AA 7①③ 程霞2010[33]47 (24/23)48 (26/22)45.245.2血必净注射液+AA 7②③ 邵中一2017[34]42 (27/15)42 (25/17)41.5±7.442.1±8.2血必净注射液+AA10② 袁本权2019[35]35 (19/16)35 (21/14)50.65±11.4749.75±10.86血必净注射液+AA 7①③ 陈凯立2017[36]50 (28/22)50 (25/25)45.8±9.144.5±11.2血必净注射液+AA10① 蔡潮深2017[37]24 (14/10)24 (13/11)45.23±5.5146.51±5.48血必净注射液+AA 7② 季华庆2017[38]61 (48/13)61 (46/15)48.02±2.6348.15±2.57血必净注射液+AA 7① 林峰2012[39]43 (26/17)43(28/15)38.8±2.939.2±2.4血必净注射液+AA 7①②③ 于欣2016[40]1414 血必净注射液+AA 7② 冷凯2008[41]35 (21/14)30 (20/10)50.8350.83血必净注射液+AA 7①②③ 岳云霄2016[42]30 (18/12)30 (22/8)52.5±3.151.7±2.3血必净注射液+AA 7① 只茂叶2012[43]32 (19/13)41 (27/14)36.68±12.9241.00±10.37血必净注射液+AA 7① 朱克东2013[44]2017 血必净注射液+AA 7①④ 刘秋香2020[45]60 (37/23)60 (35/25)48.23±6.2448.32±6.25丹参川穹嗪注射液+AA14①③ 毛坡2020[46]36 (20/16)36 (22/14)42.8±2.641.8±2.6丹参川穹嗪注射液+AA14①④ 相冰[47]40 (21/19)40 (23/17)57.2±3.056.8±3.1丹参注射液+AA10①④ 廖东平[48]28 (18/10)28 (16/12)47.9±13.650.0±12.3血必净注射液+AA 7① 李智勇2021[49]48 (29/19)49 (27/22)57.5±9.457.4±9.3血必净注射液+AA10① 郭俊2021[50]50 (28/22)50 (30/20)48.2±7.66)47.6±8.5血必净注射液+AA14①
T-治疗组 C-对照组 A-常规治疗,下表及图3、5、6同 ①临床疗效 ②病死率 ③血淀粉酶恢复时间 ④不良反应发生率
T-treatment group C-control group A-conventional treatment, same as below tables and fig. 3, 5, 6 ①clinical efficacy ②case fatality rate ③blood amylase recovery time ④incidence of adverse reactions

图2 纳入研究产生偏倚风险的项目所占比例
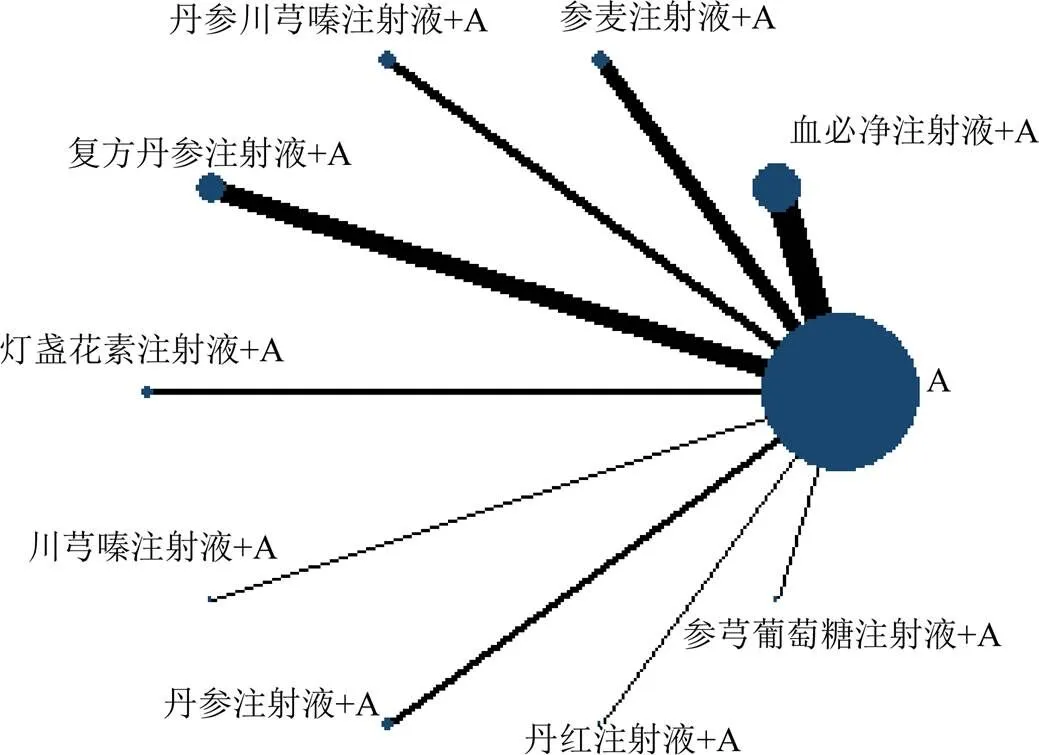
图3 临床疗效证据网络图
2.4.4 网状Meta分析结果排序 临床疗效通过排序概率表评估从优到劣为参麦注射液、丹参川芎嗪注射液、参芎葡萄糖注射液、血必净注射液、灯盏花素注射液、川芎嗪注射液、丹红注射液、丹参注射液、复方丹参注射液分别联用常规治疗(表3)。
2.5 病死率
2.5.1 证据网络图 16项[3,9,12,14-15,17-18,20-22,33-34,37,39-41]研究报道了病死率,涉及7种中药注射液,7个直接比较,无闭合环形成(图5)。结果显示,血必净注射液联合常规治疗的研究数量最多(6个RCTs),样本量最大(403例)。
A-常规治疗 B-血必净注射液 C-参麦注射液 D-丹参川芎嗪注射液 E-复方丹参注射液 F-灯盏花素注射液 G-川芎嗪注射液 H-丹参注射液 I-丹红注射液 J-参附注射液 K-参芎葡萄糖注射液
2.5.2 发表偏倚 比较-校正漏斗图结果显示,研究大致分布于垂直线(=0)两侧,提示存在发表偏倚和小样本效应可能性较小(图4-b)。
2.5.3 网状Meta分析 网状Meta分析共产生28个两两比较,其中7个比较差异有统计学意义,与常规治疗相比,灯盏花素注射液、丹参川芎嗪注射液、血必净注射液分别联合常规治疗的病死率低,差异具有统计学意义,分别为OR=0.33,95% CI [0.15,0.75];OR=0.21,95% CI [0.05,0.94];OR=0.32,95% CI [0.15,0.70]。其余干预措施两两比较差异均无统计学意义(表4)。

表2 临床疗效的网状Meta分析
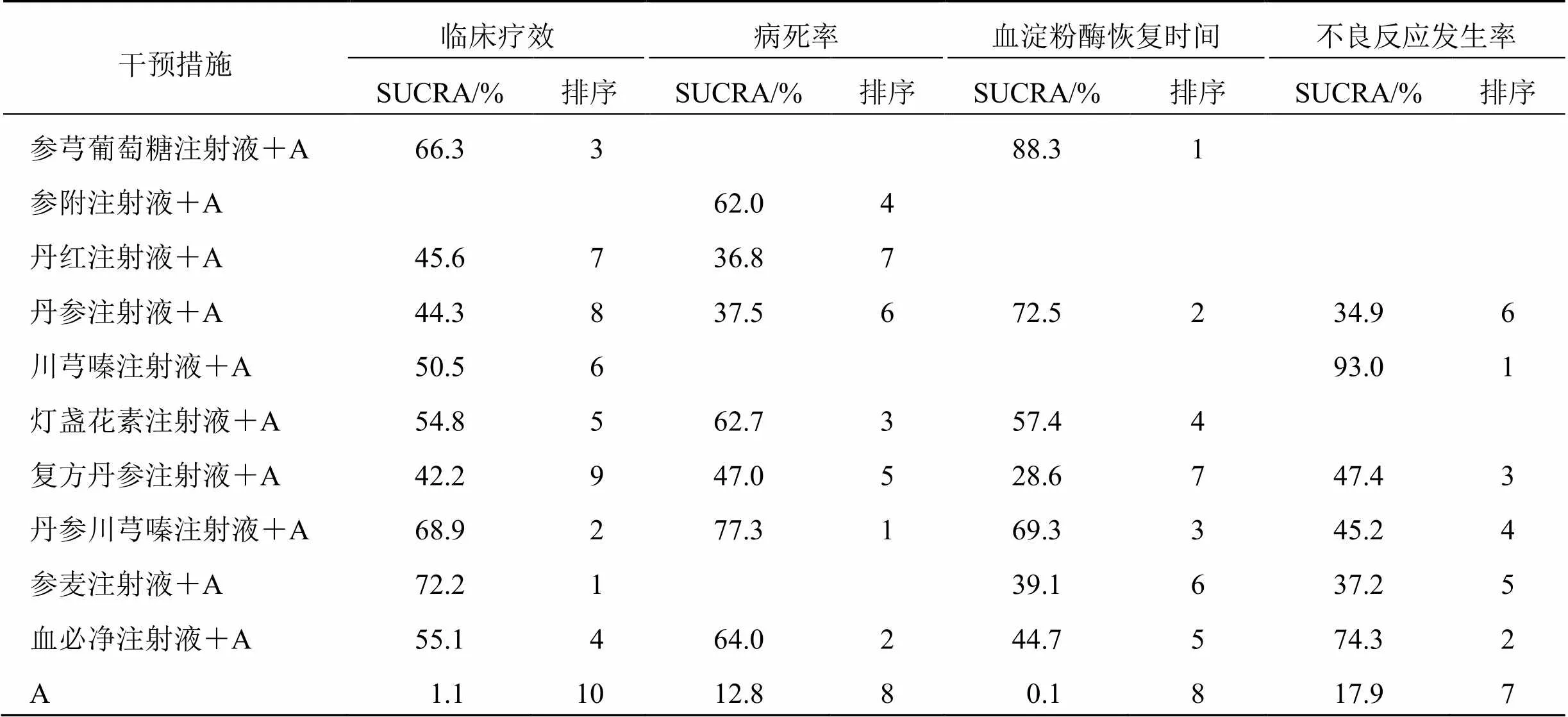
表3 中药注射液改善结局指标SUCRA排序

图5 病死率证据网络图
2.5.4 网状Meta分析结果排序 病死率通过排序概率表评估从低到高为丹参川芎嗪注射液、血必净注射液、灯盏花素注射液、参附注射液、复方丹参注射液、丹参注射液、丹红注射液分别联用常规治疗(表3)。
2.6 血淀粉酶恢复时间
2.6.1 证据网络图 16项[4,7,9,12,15,20,22,25,29-30,32-33,35,39,41,45]研究报道了血淀粉酶恢复时间,涉及7种中药注射液,7个直接比较,无闭合环形成(图6)。结果显示,血必净注射液联合常规治疗的研究数量最多(5个RCTs),样本量最大(414例)。
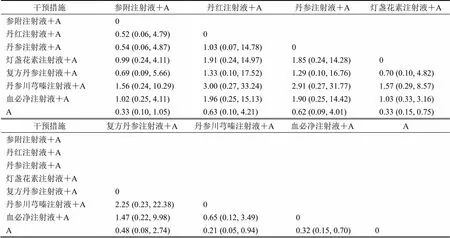
表4 病死率的网状Meta分析
2.6.2 发表偏倚 比较-校正漏斗图结果显示研究不对称分布于垂直线(=0)两侧,提示存在发表偏倚和小样本效应可能性较大(图4-c)。
2.6.3 网状Meta分析 网状Meta分析共产生28个两两比较,其中17个比较差异有统计学意义:与常规治疗相比,参芎葡萄糖注射液、丹参注射液、灯盏花素注射液、复方丹参注射液、丹参川芎嗪注射液、参麦注射液、血必净注射液分别联合常规治疗血淀粉酶恢复时间短,差异具有统计学意义,分别为MD=−3.30,95% CI [−3.99,−2.60];MD=−2.80,95%CI [−3.91,−1.69];MD=−2.30,95% CI [−2.96,−1.63];MD=−0.90,95% CI [−1.73,−0.07];MD=−2.56,95% CI [−3.52,−1.87;MD=−1.58,95% CI [−2.45,−0.72];MD=−1.80,95% CI [−2.2,−1.4]。参芎葡萄糖注射液联合常规治疗的血淀粉酶恢复时间优于灯盏花素注射液、复方丹参注射液、参麦注射液、血必净注射液分别联合常规治疗,差异具有统计学意义,分别为MD=−0.70,95% CI [−1.22,0.18];MD=−3.42,95% CI [−5.19,−1.65];MD=−3.40,95% CI [−4.22,−2.58];MD=−1.97,95%CI [−2.67,−1.26]。丹参注射液联合常规治疗的血淀粉酶恢复时间优于参麦注射液,差异具有统计学意义(MD=−0.08,95% CI [−1.40,−1.25])。灯盏花素注射液联合常规治疗的血淀粉酶恢复时间优于复方丹参注射液、参麦注射液、血必净注射液分别联合常规治疗,差异具有统计学意义,分别为MD=−2.72,95% CI [−4.50,−0.94];MD=−2.70,95% CI [−3.55,−1.85];MD=−0.89,95% CI [−1.77,0.00]。丹参川芎嗪注射液联合常规治疗的血淀粉酶恢复时间优于参麦注射液、血必净注射液分别联合常规治疗,差异具有统计学意义,分别为MD=−2.26,95% CI [−3.98,−0.53];MD=−0.99,95% CI [−1.46,−0.5]。其余干预措施两两比较差异均无统计学意义(表5)。

图6 血淀粉酶恢复时间证据网络图

表5 血淀粉酶恢复时间的网状Meta分析
2.6.4 网状Meta分析结果排序 血淀粉酶恢复时间通过排序概率表评估从优到劣为:参芎葡萄糖注射液,丹参注射液,丹参川芎嗪注射液,灯盏花素注射液,血必净注射液,参麦注射液,复方丹参注射液分别联合常规治疗(表3)。
2.7 不良反应发生率
2.7.1 证据网络图 13项[4,8,10-11,21-22,24-25,29-30,44,46-47]研究报道了不良反应发生率,涉及6种中药注射液,6个直接比较,无闭合环形成(图7)。结果显示,丹参川芎嗪注射液及复方丹参注射液分别联合常规治疗的研究数量最多(分别为4个RCTs),丹参川芎嗪注射液联合常规治疗的样本量最大(630例)。
2.7.2 发表偏倚 比较-校正漏斗图结果显示研究大致分布于垂直线(=0)两侧,提示存在发表偏倚和小样本效应可能性较小(图4-d)。
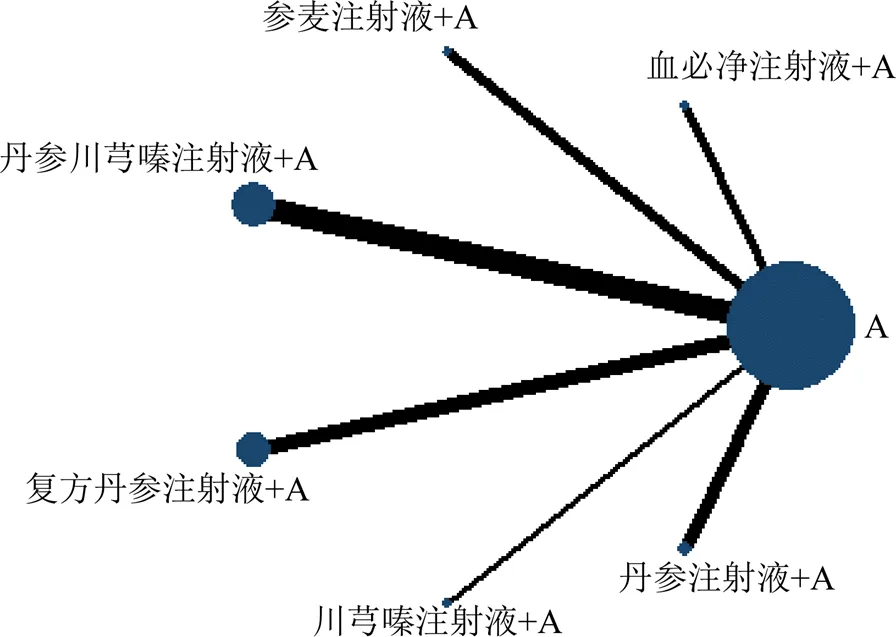
图7 不良反应发生率证据网络图
2.7.3 网状Meta分析 网状Meta分析共产生21个两两比较,其中3个比较差异有统计学意义,与常规治疗相比,川芎嗪注射液、血必净注射液分别联合常规治疗的不良反应发生率低,差异具有统计学意义,分别为OR=0.09,95%CI [0.02,0.43];OR=0.24,95% CI [0.07,0.81)。与复方丹参注射液联合常规治疗相比,川芎嗪注射液联合常规治疗的不良反应发生率低,差异具有统计学意义(OR=0.17,95%CI [0.03,0.89])。其余干预措施两两比较差异均无统计学意义(表6)。
2.7.4 网状Meta分析结果排序 不良反应发生率通过排序概率表评估从低到高为川芎嗪注射液、血必净注射液、复方丹参注射液、丹参川芎嗪注射液、参麦注射液、丹参注射液分别联用常规治疗(表3)。

表6 不良反应发生率率的网状Meta分析
2.8 GRADE证据质量评价
临床疗效、病死率、不良反应发生率为低级证据质量,血淀粉酶恢复时间为极低级证据质量(表7)。
3 讨论
SAP的发病机制尚未完全明确,多认为是由胰酶在胰腺内被异常激活,继而破坏正常的胰腺细胞,促使机体产生免疫变态反应、微循环障碍,引起胰腺组织水肿、出血、坏死,甚至其他器官合并损伤。临床特征以急性突发的上腹痛、呕吐、肠鸣音消失、血尿淀粉酶增高为主,常伴有全身炎症反应及器官功能障碍,对患者生命安全产生严重影响[56]。中医学中没有对“重症急性胰腺炎”明确的记载,但根据其临床表现,将该病归于“厥心痛”“胃脘痛”“脾脏痛”“腹痛”的范畴,病机为湿邪、痰浊、瘀血蕴结体内,致使肝失疏泄、脾胃升降失司、脏腑失调引起肝胆湿热、气滞血瘀、胃肠热结等证,不通则痛[57]。中药注射液是在中医理论指导下,应用现代药物生产工艺,对中药材提取、纯化后所制成的供人体输入的无菌制剂,但是不同中药注射液治疗SAP的疗效与安全性方面尚没有RCTs的比较结果。本研究引入网状Meta分析的方法,以常规治疗为共同干预措施,比较不同中药注射液联合常规治疗用于SAP的疗效和安全性,进而为临床治疗SAP方案提供参考指导意见。

表7 GRADE证据质量评价
本研究共纳入49项RCTs,10种中药注射液,10种干预措施。结果显示,临床疗效排序从优到劣为参麦注射液、丹参川芎嗪注射液、参芎葡萄糖注射液、血必净注射液、灯盏花素注射液、川芎嗪注射液、丹红注射液、丹参注射液、复方丹参注射液分别联合常规治疗;病死率排序从低到高为丹参川芎嗪注射液、血必净注射液、灯盏花素注射液、参附注射液、复方丹参注射液、丹参注射液、丹红注射液分别联合常规治疗;血淀粉酶恢复时间排序从优到劣为参芎葡萄糖注射液、丹参注射液、丹参川芎嗪注射液、灯盏花素注射液、血必净注射液、参麦注射液、复方丹参注射液分别联合常规治疗;不良反应发生率从低到高为川芎嗪注射液、血必净注射液、复方丹参注射液、丹参川芎嗪注射液、参麦注射液、丹参注射液分别联合常规治疗。参麦注射液是由红参和麦冬2味中药制成的纯中药复方制剂,具有益气固脱、养阴生津、温补心肾、祛瘀的功效。有研究表明参麦注射液在SAP的早期治疗可能通过提高机体免疫力,降低促炎因子水平,改善血液流变性和调节血液黏滞状态以调节胰腺的微循环[58]。丹参川芎嗪注射液主要组分为丹参和川芎嗪,丹参可以保护内皮细胞,减少氧自由基的产生,提高胰腺组织对缺氧的耐受性[59]。川芎嗪可以抗血小板聚集,改变血液流变性从而改善微循环[60]。血必净注射液的主要成分来源于清代名医王清任的“血府逐瘀汤”,具有活血化瘀、行气止痛的功效。现代研究表明,血必净注射液可以减轻肿瘤坏死因子-α(TNF-α)、白细胞介素-6(interleukin-6,IL-6)促炎因子的释放,降低内毒素水平,阻断体内炎症级联反应,抑制SAP诱发的全身炎症反应综合征。
本研究全面搜集中药注射液联合常规治疗SAP的RCTs,按照MA-PRISMA扩展声明报告,但仍存在一定局限性:①纳入的49项研究,仅有15篇文献采用正确的随机方法,均未提及具体的分配隐藏方案及是否采用盲法,影响本研究的论证等级。②GRADE质量评价等级较低,影响研究结果的可信度。③临床使用中药注射剂时应遵循中医“辨证论治”的特点,所纳入的研究均未提及中医证型。
综上,本研究应用网状Meta分析的方法分析了不同中药注射液联合常规治疗SAP的疗效及安全性,为临床治疗用药提供证据和指导。由于纳入的研究存在一定局限性,故应谨慎看待排序结果,未来仍需开展多中心、大样本、高质量的RCTs予以验证,为临床合理用药提供参考。
利益冲突 所有作者均声明不存在利益冲突
[1] 崔云峰, 屈振亮, 齐清会, 等. 重症急性胰腺炎中西医结合诊治指南(2014年, 天津) [J]. 临床肝胆病杂志, 2015, 31(3): 327-331.
[2] 赖运兴. 奥曲肽联合灯盏花素治疗急性重症胰腺炎的临床研究 [J]. 现代诊断与治疗, 2013, 24(8): 1820-1821.
[3] 杨伟钦. 参附注射液治疗重症急性胰腺炎“厥脱证”的临床及实验研究 [D]. 广州: 广州中医药大学, 2018.
[4] 王巨峰. 参麦注射液联合兰索拉唑治疗重症急性胰腺炎效果观察 [J]. 中国乡村医药, 2018, 25(22): 39-40.
[5] 王生锋. 参麦注射液与奥曲肽及乌司他丁联用对急性重症胰腺炎患者的疗效及其对炎症因子水平的影响 [J]. 抗感染药学, 2019, 16(1): 65-67.
[6] 黄超, 罗灵和, 陈军贤. 参麦注射液佐治急性重症胰腺炎20例临床观察 [J]. 浙江中医杂志, 2016, 51(5): 378.
[7] 陈健, 廖鑑能, 韦文明, 等. 参芎葡萄糖注射液辅助治疗急性重症胰腺炎疗效观察 [J]. 首都医药, 2013, 20(16): 52-53.
[8] 蔡娉娉, 钟超, 陈伟平. 川芎嗪注射液联合乌司他丁治疗重症急性胰腺炎的临床疗效及安全性研究 [J]. 中国处方药, 2021, 19(1): 102-104.
[9] 黄志辉. 丹参川芎嗪注射液治疗重度急性胰腺炎的疗效观察 [J]. 中国现代医生, 2014, 52(35): 130-132.
[10] 李聃, 刘召明, 张华, 等. 丹参川芎嗪注射液治疗重症急性胰腺炎的临床研究 [J]. 检验医学与临床, 2017, 14(20): 3035-3037.
[11] 许志伟, 秦福芳. 丹参注射液联合33%硫酸镁治疗重症急性胰腺炎的临床观察 [J]. 中国医学工程, 2015, 23(6): 95.
[12] 岳建农, 刘忠和. 丹参注射液联合33%硫酸镁治疗重症急性胰腺炎的临床观察 [J]. 中国药房, 2013, 24(36): 3430-3432.
[13] 章丽. 丹参注射液联合生长抑素治疗重症急性胰腺炎的疗效分析 [J]. 中国社区医师, 2017, 33(22): 111.
[14] 李晓龙, 陈季云, 张龙. 丹红注射液对急性重症胰腺炎患者血清TNF-α NO的影响及临床疗效观察 [J]. 辽宁中医杂志, 2010, 37(4): 669.
[15] 张彩红. 灯盏花素持续性动脉介入对老年重症急性胰腺炎的影响 [J]. 中成药, 2015, 37(8): 1669-1672.
[16] 李抗利, 王林, 王超, 等. 灯盏花素辅助治疗对重症急性胰腺炎患者炎症因子、免疫功能和血液流变学的影响 [J]. 海南医学院学报, 2016, 22(9): 876-878.
[17] 黄冬葵. 灯盏花素干预重症胰腺炎的临床研究 [J]. 中国实用医药, 2006, 1(4): 11-12.
[18] 白云, 崔冬雪, 解淑蕊, 等. 灯盏花素治疗重症急性胰腺炎临床研究 [J]. 军事医学, 2014, 38(7): 567-568.
[19] 吴亚军. 灯盏花素注射液联合杂合式血液净化治疗重症急性胰腺炎的临床效果 [J]. 河南医学研究, 2019, 28(24): 4525-4527.
[20] 高绪照, 陈功波, 熊廷刚. 复方丹参注射液联合甲泼尼龙治疗重症急性胰腺炎的疗效观察 [J]. 中国现代医生, 2013, 51(3): 142-143.
[21] 王仲征, 应武江, 孟祥娣. 复方丹参注射液联合生长抑素治疗重症急性胰腺炎患者的效果及对胃肠功能和血清TNF-α、IL-6水平的影响 [J]. 世界华人消化杂志, 2016, 24(15): 2394-2399.
[22] 吴敏助. 复方丹参注射液联合生长抑素治疗重症急性胰腺炎的疗效观察 [J]. 现代消化及介入诊疗, 2017, 22(1): 72-74.
[23] 田晓鹏, 赵慧敏, 白文元. 联用灯盏花素选择性动脉介入治疗老年重症急性胰腺炎的临床观察 [J]. 中国普通外科杂志, 2014, 23(2): 212-216.
[24] 方瑜洁, 徐俊丽. 生长抑素联合复方丹参注射液治疗重症急性胰腺炎的疗效观察 [J]. 临床和实验医学杂志, 2014, 13(10): 811-813.
[25] 薛萌, 刁云辉. 生长抑素联合复方丹参注射液治疗重症急性胰腺炎疗效研究 [J]. 中国医学工程, 2015, 23(2): 182.
[26] 兰丹, 刘龙江. 探讨生长抑素联合复方丹参注射液治疗重症急性胰腺炎的临床效果 [J]. 临床医药文献电子杂志, 2017, 4(25): 4888-4889.
[27] 王秋阳. 乌司他丁、参麦联合治疗急性重症胰腺炎疗效观察 [J]. 航空航天医学杂志, 2016, 27(2): 159-160.
[28] 杨霞. 乌司他丁+参麦注射液治疗急性重症胰腺炎的临床疗效 [J]. 临床医药文献电子杂志, 2017, 4(60): 11842.
[29] 赵骏. 乌司他丁结合丹参川芎嗪注射液在急性重症胰腺炎综合治疗中的效果分析 [J]. 海峡药学, 2019, 31(12): 193-195.
[30] 张琪, 王长友. 乌司他丁联合丹参川芎嗪注射液治疗重症急性胰腺炎疗效观察 [J]. 安徽医药, 2018, 22(12): 2441-2443.
[31] 郑志光. 乌司他丁联合丹红注射液治疗重症急性胰腺炎的疗效分析 [J]. 中国现代医生, 2012, 50(27): 75-76.
[32] 查岭, 谷玉行, 赵明. 乌司他丁联合血必净治疗重症急性胰腺炎的临床疗效观察 [J]. 重庆医学, 2018, 47(8): 1124-1125.
[33] 程霞, 王玉红. 血必净联合乌司他丁治疗重症急性胰腺炎的临床疗效观察 [J]. 中国全科医学, 2010, 13(24): 2670-2671.
[34] 邵中一, 苏赛赛, 鲍丽莎. 血必净注射液辅助治疗重症急性胰腺炎临床观察 [J]. 新中医, 2017, 49(2): 54-57.
[35] 袁本权. 血必净注射液辅助治疗重症急性胰腺炎临床价值分析 [J]. 中外医学研究, 2019, 17(5): 33-34.
[36] 陈凯立, 张汉洪, 林龙, 等. 血必净注射液联合奥曲肽、乌司他丁治疗急性重症胰腺炎的临床观察 [J]. 中国药房, 2017, 28(32): 4540-4544.
[37] 蔡潮深. 血必净注射液联合生长抑素治疗重症胰腺炎的临床观察 [J]. 中国当代医药, 2017, 24(11): 41-44.
[38] 季华庆, 杨平. 血必净注射液联合乌司他丁对重症急性胰腺炎患者临床疗效及对血清炎症因子水平的影响 [J]. 陕西中医, 2017, 38(7): 909-910.
[39] 林峰, 林艳, 洪建湘. 血必净注射液联合乌司他丁治疗重症急性胰腺炎临床观察 [J]. 内蒙古中医药, 2012, 31(15): 8-9.
[40] 于欣, 王潇然, 饶艳伟, 等. 血必净注射液治疗早期重症急性胰腺炎的临床疗效观察 [J]. 中国社区医师, 2016, 32(18): 109-110.
[41] 冷凯, 黄钲焘, 曾鹏飞. 血必净注射液治疗重症急性胰腺炎的临床疗效观察 [J]. 中国药房, 2008, 19(27): 2144-2146.
[42] 岳云霄, 余守雅. 血必净注射液治疗重症急性胰腺炎的临床效果 [J]. 当代医学, 2016, 22(29): 140-141.
[43] 只茂叶, 何若冲. 血必净注射液治疗重症急性胰腺炎临床疗效观察 [J]. 山西医科大学学报, 2012, 43(5): 386-390.
[44] 朱克东. 血必净注射液治疗重症急性胰腺炎临床疗效观察 [J]. 中华全科医学, 2013, 11(7): 1054.
[45] 刘秋香, 牛福玉, 杨思贤, 等. 重症急性胰腺炎应用乌司他丁+丹参川芎嗪注射液治疗的效果分析 [J]. 中国医药指南, 2020, 18(12): 47-48.
[46] 毛坡, 翟伟锋. 注射用乌司他丁联合丹参川芎嗪注射液治疗重症急性胰腺炎的临床疗效 [J]. 临床合理用药杂志, 2020, 13(9): 80-81.
[47] 相兵. 丹参注射液联合奥曲肽对重症急性胰腺炎的疗效及其对凝血功能、血液流变学的影响 [J]. 中国处方药, 2021, 19(8): 137-139.
[48] 廖东平, 张霓, 伍文才, 等. 低分子肝素联合血必净注射液对重症急性胰腺炎患者IL-6、P-选择素、D-二聚体的影响及临床意义 [J]. 吉林医学, 2021, 42(6): 1380-1383.
[49] 李智勇. 血必净注射液对急性重症胰腺炎患者血清AMY、WBC、TNF-α水平的影响 [J]. 航空航天医学杂志, 2021, 32(6): 668-670.
[50] 郭俊, 闵飞. 血必净注射液联合奥曲肽对重症急性胰腺炎患者胰腺血流灌注及血流动力学的影响 [J]. 天津中医药, 2021, 38(6): 732-735.
[51] 杨丰文, 田金徽, 张俊华, 等. 中医药网状meta分析方法及要点 [J]. 中医杂志, 2017, 58(10): 841-844.
[52] 中华医学会消化病学分会胰腺疾病学组. 中国急性胰腺炎诊治指南(草案) [J]. 中华消化杂志, 2004(3): 62-64.
[53] 赵玉沛, 王春友, 李非. 急性胰腺炎诊治指南(2014版) [J]. 中华消化外科杂志, 2015, 14(1): 1-5.
[54] Leppäniemi A, Tolonen M, Tarasconi A,. 2019 WSES guidelines for the management of severe acute pancreatitis [J]., 2019, 14: 27.
[55] Balshem H, Helfanda M, Schunemann H J, 等. GRADE指南: Ⅲ. 证据质量分级 [J]. 中国循证医学杂志, 2011, 11(4): 451-455.
[56] 张莉. 乌司他丁联合奥曲肽治疗重症急性胰腺炎的临床效果分析 [J]. 中外医疗, 2016, 35(8): 117-118.
[57] 史海全. 用乌司他丁与奥曲肽治疗重症急性胰腺炎的效果分析 [J]. 当代医药论丛, 2016, 14(18): 86.
[58] 刘德伟, 陈海涛, 朱腾开. 48例重症急性胰腺炎的临床分析 [J]. 当代医学, 2010, 16(30): 60-61.
[59] 万新焕, 王瑜亮, 周长征, 等. 丹参化学成分及其药理作用研究进展[J]. 中草药, 2020, 51(3): 788-798.
[60] 杨军, 顾元龙, 钱毅, 等. 丹参川芎嗪腹腔灌洗对重症急性胰腺炎大鼠血液流变学的影响 [J]. 中国中西医结合外科杂志, 2013, 19(2): 153-156.
Network Meta-analysis of efficacy and safety of different traditional Chinese medicine injections combined with conventional treatments for severe acute pancreatitis
MA Yu-jing1, LANG Xiao-meng2, KANG Xin2, YANG Qian2, LIU Jian-ping2, LI Dian-gui2
1. The First Affiliated Hospital of Hebei College of Traditional Chinese Medicine, Shijiazhuang 050013, China 2. Hebei Provincial Hospital of Traditional Chinese Medicine, Shijiazhuang 050013, China
To evaluate the efficacy and safety of different traditional Chinese medicine injections combined with conventional treatments for severe acute pancreatitis (SAP) by the method of network Meta-analysis.PubMed, EMbase, Cochrane, Web of Science, CNKI, Wanfang, VIP database were searched by computer, the search time was from the establishment of each database to September 1, 2021. According to the inclusion and exclusion criteria, two researchers conducted independent literature searches, followed the Cochrane risk bias assessment tool developed by the Cochrane Collaboration for quality evaluation, and applied Stata 14.0 software for statistical analysis.In the end, 49 randomized controlled trials (RCTs) were included, involving 10 kinds of traditional Chinese medicine injections and 3820 patients. The results of the network Meta-analysis showed that the clinical efficacy was ranked from best to worst: Shenmai Injection (参麦注射液), Danshen Ligustrazine Injection (丹参川芎嗪注射液), Shenxiong Glucose Injection (参芎葡萄糖注射液), Xuebijing Injection (血必净注射液), Breviscapine Injection (灯盏花素注射液), Ligustrazine Injection (川芎嗪注射液), Danhong Injection (丹红注射液), Danshen Injection (丹参注射液), Compound Danshen Injection (复方丹参注射液) combined with conventional treatment respectively; The case fatality rate was ranked from low to high: Danshen Ligustrazine injection, Xuebijing Injection, Breviscapine Injection, Shenfu Injection (参附注射液), Compound Danshen Injection, Danshen Injection, Danhong Injection combined with conventional treatment respectively; Blood amylase recovery time was ranked sorted from best to worst: Shenxiong Glucose Injection, Danshen Injection, Danshen Ligustrazine Injection, Breviscapine Injection, Xuebijing Injection, Shenmai Injection, Compound Danshen Injection combined with conventional treatment respectively; The incidence of adverse reactions was ranked from low to high: Ligustrazine Injection, Xuebijing Injection, Compound Danshen Injection, Danshen Ligustrazine Injection, Shenmai Injection, Danshen Injection combined with conventional treatment respectively.Combining with different traditional Chinese medicine injections on the basis of conventional treatment can improve the clinical efficacy of SAP, reduce the case fatality rate, shorten the recovery time of blood amylase, and reduce the incidence of adverse reactions. However, due to the limitations of the included studies, the methodological quality was generally not high and should be choose drugs carefully, and multi-center, large-sample, high-quality RCTs are still needed for verification in the future.
traditional Chinese medicine injection; severe acute pancreatitis; network Meta-analysis; randomized controlled trial; Shenmai Injection; Danshen Ligustrazine Injection; Shenxiong Glucose Injection; Xuebijing Injection; Breviscapine Injection; Ligustrazine Injection; Danhong Injection; Danshen Injection; Compound Danshen Injection; Shenfu Injection
R285.64
A
0253 - 2670(2021)24 - 7583 - 13
10.7501/j.issn.0253-2670.2021.24.021
2021-08-12
国家中医临床研究基地建设项目(国中医药办科技函[2018]18);国家中医药管理局第三界国医大师传承工作室及全国名老中医传承工作室建设项目(人社部发[2017]45号);国家科技部重点研发课题:基于“道术结合”思路与多元融合方法的名老中医经验传承创新研究(2018YFC1704100);东部地区名老中医学术观点、特色诊疗方法和重大疾病防治经验课题(2018YFC1704102);河北省自然基金项目(H2019423077)
马玉景(1992—),女,博士,研究方向为胃肠临床与基础的研究。E-mail: 1535392045@qq.com
刘建平,女,博士,博士生导师,研究方向为胃肠临床与基础的研究。E-mail: 13603396653@163.com
[责任编辑 潘明佳]
