MCM-41嫁接离子液体催化CO2环加成反应
2021-12-16贺润发
王 颖,贺润发,李 钢
大连理工大学化工学院精细化工国家重点实验室,辽宁 大连 116024
CO2是化石燃料燃烧的主要副产物,同时也是一种温室气体。2019年,大气中的CO2浓度已经从工业时代初期的277 mg/kg上升至410 mg/kg左右[1],CO2的大量排放产生了一系列环境问题,比如全球变暖和物种灭绝等。然而,CO2也是一种丰富、无毒、可循环利用的C1资源,可以利用其合成高附加值的化学品,其中以CO2与环氧化物为原料合成环状碳酸酯的反应工艺引起了研究者们的注意,反应式如下:

该反应满足了绿色化学和原子经济的要求。环状碳酸酯可以用作有机合成的中间体和极性非质子溶剂等[2],用途非常广泛。由于CO2存在热力学稳定和动力学惰性的问题,需要在该反应体系中加入高效的催化剂[3-7]。离子液体是一种独特的由有机阳离子和无机或有机阴离子组成的盐。按照阳离子组成可以将离子液体分为咪唑型离子液体、吡啶型离子液体、吡咯型离子液体、季铵盐型离子液体和季鏻盐型离子液体。咪唑型离子液体的碱性活性中心咪唑基团能够吸附和活化CO2,用于催化CO2与环氧化物环加成反应时具有较高的催化活性[8]。但是,由于其是液体催化剂,难以从反应体系分离和重复使用,所以咪唑型离子液体常被负载到载体上制备成负载型离子液体催化剂。介孔分子筛MCM-41表面存在大量的硅羟基可以被表面修饰锚定离子液体,而且MCM-41的介孔结构有利于催化反应中的传质,因此咪唑型离子液体/MCM-41有望成为一种高效的CO2环加成反应催化剂。Appaturi等[9-10]使用咪唑试剂直接与氯丙基修饰的MCM-41反应嫁接咪唑基团,此过程需要相对高的反应温度,之后引入卤代烷烃,在MCM-41表面逐步嫁接离子液体。
本研究使用N,N’-羰基二咪唑(CDI)替代咪唑,通过后合成修饰法,逐步将咪唑类离子液体嫁接到氨基修饰的MCM-41上,制备出一种多相催化剂MCM-41-ImBr,用于催化CO2与环氧氯丙烷(ECH)环加成反应,并进一步研究该反应的动力学特性,优化反应条件,探究该催化体系中可能存在的反应机理。
1 实验部分
1.1 催化剂制备
MCM-41的制备:准确称取4.38 g十六烷基三甲基溴化铵(CTAB),将其加入140 mL去离子水中,待其充分溶解后加入4 mL乙二胺。随后逐滴滴入12 mL正硅酸乙酯(TEOS),30 ℃下搅拌40 min。再将混合凝胶装到晶化釜中,110 ℃下晶化2 d,然后抽滤,将滤饼干燥并研磨成粉末,再于马弗炉中550 ℃下焙烧4 h,得到白色的MCM-41粉末。
MCM-41-NH2的制备:将1.50 g MCM-41分散于60 mL甲苯中,加入10.50 mL的3-氨丙基三乙氧基硅烷(APTES),将混合物在60 ℃、氮气保护条件下加热12 h,然后离心分离,用乙醇充分洗涤固体产物,干燥后得到MCM-41-NH2备用。
MCM-41-Im的制备:取1.00 g的MCM-41-NH2分散于20 mL甲苯中,加入5.20 mg的1,8-二氮杂二环[5.4.0]十一碳-7-烯(DBU),将混合物在30 ℃下搅拌1 h,再加入0.36 g的N,N’-羰基二咪唑(CDI),于30 ℃下继续反应12 h,抽滤,滤饼干燥得MCM-41-Im。
MCM-41-ImBr的制备:将上述制备的MCM-41-Im分散于20 mL甲苯中,加入98 μL溴乙烷,于70 ℃下冷凝回流24 h,抽滤,用甲苯充分洗涤滤饼,干燥得到产物MCM-41-ImBr。
催化剂的制备路线如图1所示。
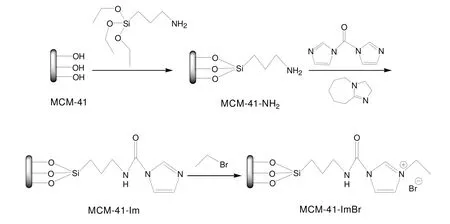
图1 MCM-41-ImBr的制备路线Fig.1 Preparation path of MCM-41-ImBr
1.2 催化剂表征
采用日本Ringku公司D/max-2400型X射线衍射仪(XRD)表征催化剂的晶体结构,靶源为Cu-Kα靶,扫描2θ为1°~5°,扫描步幅为0.02°,电压为45 kV,电流为200 mA,扫描速度为1 (°)/min。采用德国Bruker公司EQUINOX55型傅里叶变换红外光谱仪(FT-IR)对催化剂进行化学结构表征,使用KBr压片法制备样品,波数为4 000~400 cm-1。采用德国elementar公司varioELⅢ型元素分析仪(EA)测试催化剂的C,H和N元素含量。
1.3 CO2与ECH环加成反应
CO2与ECH环加成反应在间歇式不锈钢高压反应釜中进行。在高压反应釜中加入一定用量的催化剂、22 mL乙腈、1 mL甲苯(内标物)和2 mL ECH,然后将反应釜密封;在室温条件下用CO2置换釜中的空气3次,随后将反应压力升到设定值;在设定温度下反应一定时间,然后待反应釜冷却后释放出未反应的CO2。反应混合物离心后取样进行色谱分析(Agilent6890N型气相色谱仪,HP-5色谱柱,氢火焰检测器),内标法计算产物组成。氯丙烯碳酸酯选择性(SCC)定义为产物色谱分析中氯丙烯碳酸酯峰面积和所有产物峰面积之比。离心分离得到的催化剂用乙醇洗涤3次,真空干燥后可重复使用。CO2与ECH环加成反应的主副反应式如下所示。
主反应:
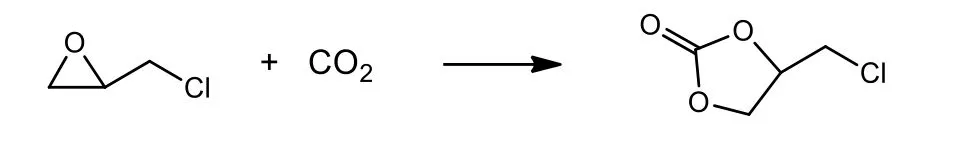
可能的副反应:
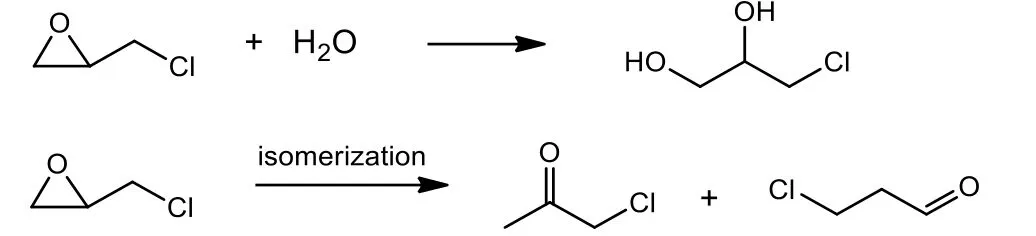
2 结果与讨论
2.1 催化剂表征结果
图2为催化剂样品的XRD图谱。由图2可知,所有的样品均呈现出有序的介孔结构,其中2.2°,3.7°和4.4°附近的特征衍射峰依次归属于MCM-41的(100),(110)和(200)晶面[11],具有典型空间群对称性(P6mm)的六方结构。随着MCM-41被有机基团修饰,这些特征衍射峰仍然存在,表明后合成修饰过程中介孔结构得到保持。但特征衍射峰的峰位置逐渐向高角度偏移,说明样品的层间距逐渐变窄[12]。
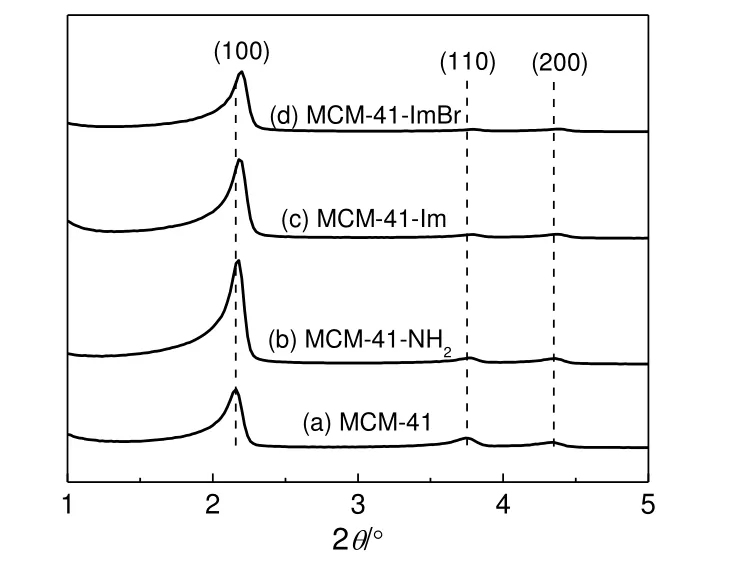
图2 催化剂样品的XRD图谱Fig.2 XRD patterns of catalyst samples
催化剂样品的红外光谱见图3。图3中3 419 cm-1附近的宽峰为Si—OH的伸缩振动峰和吸附水分子的伸缩振动峰[13],2 942 cm-1和2 882 cm-1处为丙基链上—CH2的伸缩振动峰[14],1 602 cm-1和689 cm-1处分别为对称的NH2的弯曲振动峰和N—H键的弯曲振动峰[15],这些峰的出现表明APTES成功嫁接到MCM-41上。1 631 cm-1处为MCM-41和MCM-41-NH2上吸附的水分子O—H键弯曲振动峰[16]。对于MCM-41-Im和MCM-41-ImBr而言,1 602 cm-1处—NH2的振动峰消失表明CDI与伯胺键合,1643cm-1和1 557 cm-1处咪唑环上C=N的伸缩振动峰和C=N—H的弯曲振动峰的出现表明咪唑成功嫁接到MCM-41上[17-18]。此外,1 631 cm-1处的N—H键弯曲振动峰和3 300~3 400 cm-1处—NH2的对称和不对称伸缩振动峰被样品中水分子的振动峰覆盖,1 000~1 200 cm-1处C—N键的伸缩振动峰被1 225 cm-1附近的Si—CH2—R的伸缩振动峰和1 085 cm-1附近的Si—O—Si的伸缩振动峰覆盖,因而在红外光谱图中均未检测到这些特征峰的存在[15]。
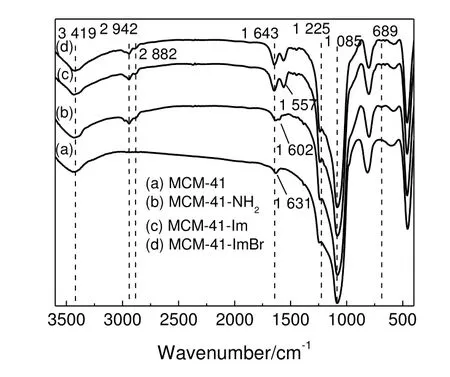
图3 催化剂样品的FT-IR图谱Fig.3 FT-IR spectra of catalyst samples
MCM-41-NH2和MCM-41-ImBr的C,H和N元素分析结果如表1所示。根据表中MCM-41-NH2和MCM-41-ImBr的N元素含量,计算得到MCM-41-ImBr中咪唑类离子液体的负载量为53.6 mmol/g。

表1 MCM-41-NH2和MCM-41-ImBr样品的元素分析结果Table 1 Elemental analysis of MCM-41-NH2 and MCM-41-ImBr
2.2 催化剂性能评价
以MCM-41-ImBr为催化剂,考察了反应温度、反应时间、催化剂用量和CO2压力对CO2与ECH环加成反应的影响,结果如图4所示。

图4 反应条件对MCM-41-ImBr催化性能的影响Fig.4 Effect of reaction conditions on the catalytic performance of MCM-41-ImBr
由图4(a)可知,随着反应温度从120 ℃增加到160 ℃,ECH转化率(XECH)从60.7%增加到100.0%,而氯丙烯碳酸酯的选择性(SCC)几乎没有改变。对于化学反应而言,升高温度会加快反应物分子运动,增加反应物之间的有效碰撞,有利于提高反应速率;而且在一定温度范围内升高温度有利于活化CO2。实验结果表明,在此反应条件下,150 ℃的反应温度即可达到完全反应。由图4(b)可知,当反应时间为2~6 h时,氯丙烯碳酸酯的选择性几乎没有变化,均在97%左右;ECH的转化率由95.2%提升到99.9%,ECH接近完全转化。由图4(c)可知,在实验条件下,催化剂用量的增加有利于ECH转化率提高,但氯丙烯碳酸酯的选择性有所降低。由图4(d)可知,CO2压力的增加有利于ECH转化率提高,因为气体压力的增加提高了气体在液相中的溶解量,有利于环加成反应的进行。由实验结果可知,150 ℃的反应温度、4 h的反应时间、0.1 g的催化剂用量和0.7 MPa的CO2压力是MCM-41-ImBr催化CO2与ECH环加成反应的较佳反应条件,在此条件下,ECH转化率高达100.0%,氯丙烯碳酸酯选择性达到98.2%。
MCM-41-ImBr催化CO2与ECH环加成反应的实验结果与文献报道结果进行了比较,结果如表2所示,其中ZnHZSM-5催化剂催化CO2与ECH环加成反应的结果是氯丙烯碳酸酯的产率,为91.0%[19]。由表2可知,MCM-41-ImBr在更短的反应时间(4 h)内即可高效催化CO2环加成反应[10,19-20]。此外,由于MCM-41-ImBr已经负载了卤素阴离子,所以在环加成反应过程中无需添加助催化剂。

表2 不同催化剂催化CO2与ECH环加成反应的性能比较Table 2 Comparison of various reported heterogenous catalysts for cycloaddition of CO2 with ECH
2.3 反应动力学研究
根据前面的研究可知,CO2与ECH环加成反应的副反应量很少,则定义反应速率如下:

式中:r为反应速率,mol/(m3·s);CECH,CCO2和Ccat.分别为ECH、CO2和催化剂的浓度,mol/L;t为反应时间,s;k是速率常数,(mol/m3)(1-a-b-c)/s;a,b和c分别为相应的反应物级数。由于反应在1.6 MPa下进行,CO2是过量的,所以CO2浓度可以认为是常数,此外催化剂用量也是定值,因此式(1)可以简化为式(2):

式中:kobs为表观速率常数,(mol/m3)(1-a)/s。根据文献报道[21],CO2与ECH的环加成反应是一级反应,则a为1。如果用ECH的转化率表示,恒温一级反应的积分式为:
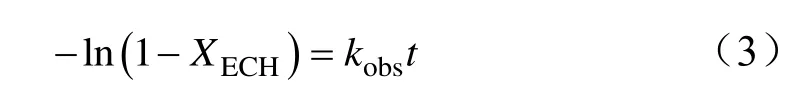
将图4(b)的实验数据按式(3)处理,得到图5所示的结果。线性拟合得到的直线斜率是1.40h-1,即为150 ℃下的kobs值。
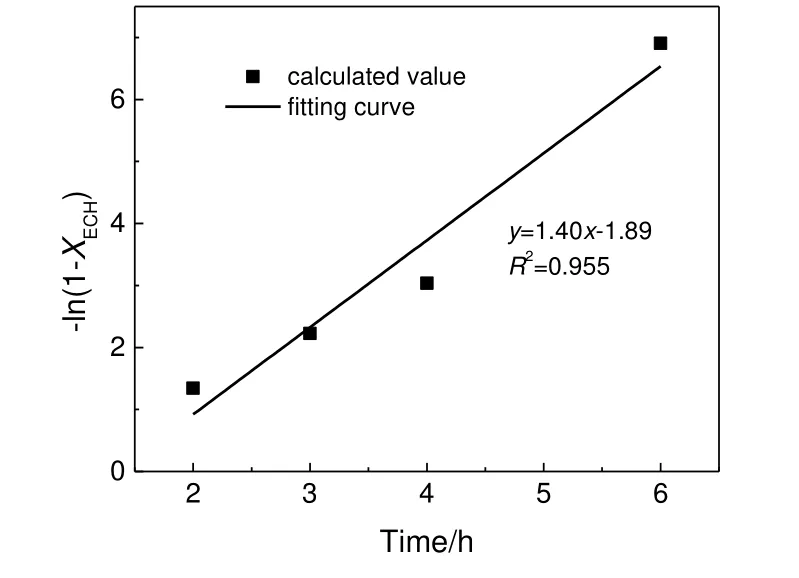
图5 -ln(1-XECH)与反应时间关系Fig.5 Plot of -ln(1-XECH) and reaction time for the cycloaddition reaction
2.4 催化剂的重复使用性
在反应温度为150 ℃、催化剂用量为0.10 g、CO2压力为0.7 MPa、反应时间为4 h的条件下,对催化剂MCM-41-ImBr的重复使用性进行了研究,结果如图6所示。由图6可知,MCM-41-ImBr重复使用时活性逐次降低,第2次使用时ECH转化率降至79.8%,第3次使用时为75.2%,这说明吸附或弱键合的活性组分在使用中有些流失。但是,催化剂在重复使用过程中,氯丙烯碳酸酯选择性几乎没有变化,均在97%左右。
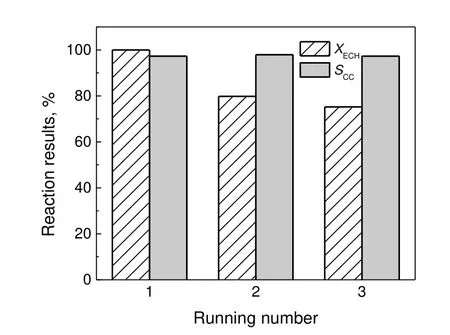
图6 MCM-41-ImBr的重复使用性Fig.6 Recycling of MCM-41-ImBr
2.5 反应机理
在上述得到的较佳反应条件下,将逐步修饰得到的催化剂分别催化CO2环加成反应,结果如表3所示。由实验结果可知,MCM-41在该反应体系中无催化活性,没有测到反应产物,但是,随着功能基团的逐步嫁接,合成催化剂的活性呈现递增趋势。由表3可知:MCM-41-NH2催化剂中存在碱性活性物种氨基,有利于吸附和活化CO2,催化性能有所提升;与MCM-41-NH2相比,MCM-41-Im催化性能显著提升,这是由于咪唑基团赋予MCM-41-Im催化剂较强的碱性位,碱性中心的存在有利于催化剂对CO2的吸附与活化,促进环加成反应的进行;MCM-41-ImBr催化剂在一系列催化剂中表现出较优的催化性能,这主要是由于最后引入的卤素阴离子作为亲核试剂具有助催化作用,与碱性中心咪唑基团协同催化ECH与环加成反应进行。

表3 不同催化剂催化CO2与ECH环加成反应性能Table 3 Catalytic performance of different catalysts for the cycloaddition of CO2 with ECH
Yang等[22]报道了含N基团可作为碱性中心与CO2作用,促进环加成反应进行。Appaturi等[9]报道了咪唑型离子液体中咪唑环可作为碱性中心与CO2作用,卤素阴离子可作为亲核试剂与环氧化物作用,促进环氧化物开环。根据表3的实验结果和参考文献,MCM-41-ImBr催化CO2与ECH环加成反应可能的机理如下所示:
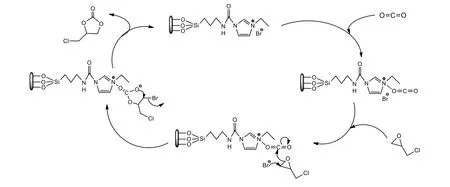
首先MCM-41-ImBr咪唑环上的季N原子与CO2产生配位键活化CO2,同时Br-亲核进攻ECH中空间位阻小的β碳原子促使ECH开环,之后上述两种活化物种相互作用产生中间产物碳酸酯,最后分子内环闭合生成产物环状碳酸酯,同时催化剂再生,完成一个催化循环过程。而MCM-41介孔结构有利于环加成反应中CO2的吸附和传质。
3 结 论
采用后合成修饰法在MCM-41表面逐步嫁接咪唑类离子液体,制备了多相催化剂MCM-41-ImBr。XRD和FT-IR表征结果说明离子液体成功负载,离子液体负载量为53.6 mmol/g。考察了MCM-41-ImBr催化CO2与ECH的环加成反应。在反应压力为0.7 MPa,反应温度为150 ℃,反应时间为4 h,催化剂用量为0.10 g且无需添加助催化剂的条件下,ECH转化率高达100.0%,氯丙烯碳酸酯选择性为98.2%。当CO2过量,反应温度为150 ℃的条件下,ECH一级反应的表观速率常数为1.40 h-1,催化剂至少可以使用3次。
