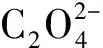草酸协同ZrO2-(NH4)3PW12O40复合催化剂降解罗丹明B及其机理
2021-12-15冯少凡李征李静
冯少凡,李征,李静
(1.河北工业大学 土木与交通学院,天津 300401;2.中国市政工程华北设计研究总院 第一设计研究院,天津 300074)
印染废水中大分子有机染料具有一定的生物毒性,难以通过常规水处理工艺去除[1]。光催化技术具有高效、反应条件温和以及绿色环保等优点。二氧化锆(ZrO2)具有热稳定性好、耐光、腐蚀性能好等优点,但是纯ZrO2材料的光生载流子分离效率低,降低其光催化活性[2]。磷钨酸铵具有稳定的化学结构及Keggin特征,可显著影响其他半导体催化剂的催化性能[3]。本文将ZrO2与(NH4)3PW12O40相复合,制备出ZrW复合型光催化剂,并应用于草酸协同光催化降解罗丹明B(RhB)体系中,考察了催化剂种类、草酸浓度、初始pH等因素对RhB降解的影响,并探讨了草酸协同ZrW光催化技术的降解作用机制。
1 实验部分
1.1 试剂与仪器
氧氯化锆、氯化铵、苯醌(BQ)、乙二胺四乙酸二钠(EDTA-2Na)、异丙醇(IPA)、氨水(25%~27%)、磷钨酸、甲基紫精(MV)、草酸、草酸铵、草酸钠均为分析纯;实验用水为超纯水。
Talos F200S场发射高分辨透射显微镜;Nova Nano SEM450场发射电子显微镜;ESCALAB 250Xi X射线电子能谱仪;Lambda 25紫外-可见漫反射光谱仪;Lambda 25 紫外可见漫反射光谱仪;CHI760E电化学工作站;UV 5800PC 紫外可见分光光度计。
1.2 ZrO2-(NH4)3PW12O40的制备
ZrO2的制备参考Cui的制备方法[4]。将ZrO2烘干后置于马弗炉中,500 ℃煅烧3 h。
将200 mg ZrO2置于40 mL超纯水中,超声分散,滴入过量的NH4Cl(按n((NH4)3PW12O40)∶n(NH4Cl)>3∶1计算),称为溶液A。将一定质量的H3PW12O40·XH2O溶于5 mL超纯水中,称为溶液B。将溶液B按照n(Zr)∶n(W)=1∶3比例缓慢滴至A中,磁力搅拌15 h。沉淀离心、清洗、烘干后,置于马弗炉中,350 ℃煅烧,退火反应2 h,冷却至室温,得到ZrO2-(NH4)3PW12O40复合材料,记为ZrW。
1.3 样品表征
采用场发射电子显微镜(SEM)、场发射高分辨透射显微镜(TEM)、X射线电子能谱(XPS)对样品的微观形貌进行表征,利用紫外可见漫反射光谱仪测定样品的紫外-可见漫反射光谱(UV-Vis DRS),利用电化学工作站测试样品的光电流响应和电化学阻抗。
1.4 光催化实验
将制备的复合催化剂加入100 mL 浓度 15 mg/L 的RhB溶液中,加入一定量的草酸,用HCl和NaOH溶液调节溶液pH,在暗环境下搅拌30 min,待催化剂表面达到吸附-脱附平衡后,用400 W汞灯照射,每隔5 min取少量水样,经离心分离后,在λ=552 nm 处测定上清液吸光度。根据朗伯-比尔定律换算成RhB浓度。
2 结果与讨论
2.1 ZrW微观形貌表征
由图1可知,ZrO2为粒径10~20 nm的粉状颗粒,出现明显团聚现象。(NH4)3PW12O40为球状颗粒,粒径为200~700 nm。

图1 ZrO2(a)和(NH4)3PW12O40(b)的SEM图Fig.1 SEM of ZrO2 (a) and (NH4)3PW12O40 (b)
由图2a可知,粉状的ZrO2分布在(NH4)3PW12O40周围,表明ZrW复合材料已经成功制备。图2b中晶格条纹间距0.31 nm和0.33 nm分别对应于ZrO2和(NH4)3PW12O40的晶面。说明具有晶体结构ZrO2和(NH4)3PW12O40之间紧密结合在一起。ZrO2和(NH4)3PW12O40复合后,对 (NH4)3PW12O40形貌基本无影响,但减少了ZrO2的团聚现象。

图2 ZrW的TEM图(a)和晶格条纹图(b)Fig.2 TEM (a)and lattice fringes (b) of ZrW
2.2 ZrW元素价态分析
对ZrW材料进行XPS表征,结果见图3。
由图3可观察到Zr、W和O的特征峰(图3a)。Zr 3d 的XPS图谱中两个特征峰分别对应Zr 3d3/2和 Zr 3d5/2(图3b),表明Zr4+存在于ZrW材料中。在W 4f的XPS谱图中(图3c),位于34.9 eV 和 37.2 eV 的W 4f7/2和W 4f5/2对应W5+[5],结合能为36.3 eV和38.5 eV的特征峰对应于W6+[6]。XPS分析说明异质结复合材料成功制备,且在复合过程中发生W的还原,生成还原态的W5+,从而为催化反应提供反应活性中心[5]。
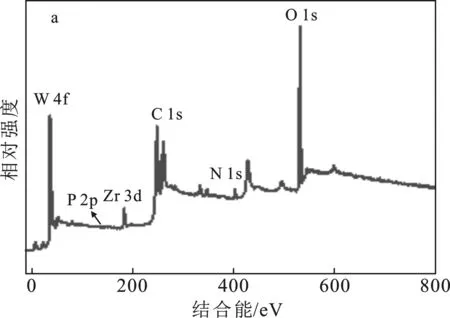
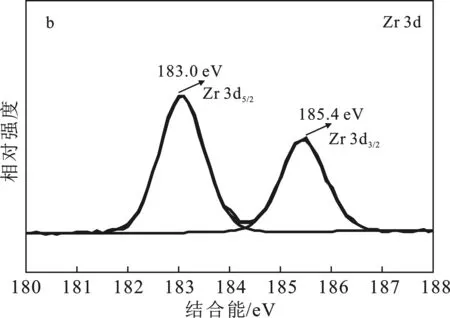
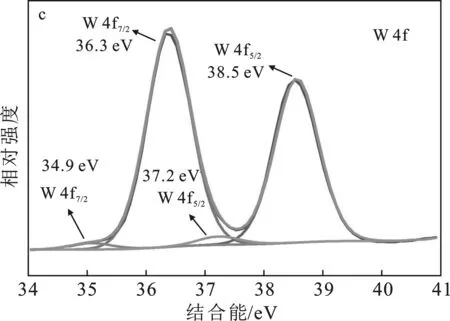
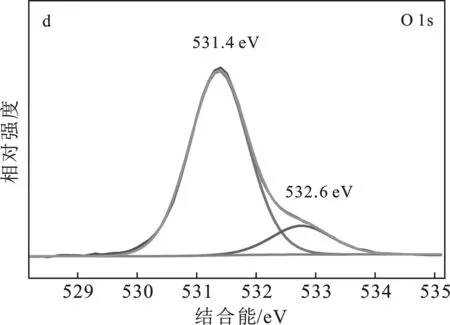
图3 ZrW的XPS能谱图Fig.3 The XPS spectra of ZrWa.全扫描;b.Zr 3d;c.W 4f;d.O 1s
2.3 ZrW光吸收性能分析
ZrO2、(NH4)3PW12O40和ZrW的UV-Vis DRS见图4。
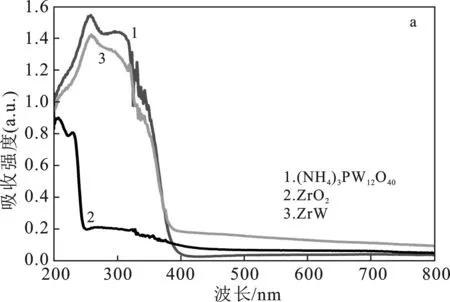
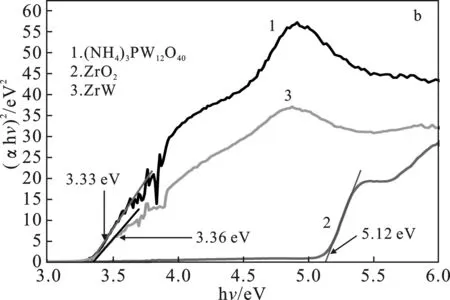
图4 样品的UV-Vis光谱图(a)和Tauc 图(b)Fig.4 UV-Vis spectra (a) and correspondingTauc spectra (b) of the samples
由图4a可知,ZrO2在紫外区有明显吸收,吸收带边为240 nm左右。(NH4)3PW12O40的吸收也主要在紫外区,吸收带边为370 nm左右。ZrW复合材料的吸收情况与(NH4)3PW12O40相似,说明与(NH4)3PW12O40复合,拓宽了ZrO2紫外光吸收阈值,ZrW在紫外光区的吸收有所增强。
通过Tauc-DavidMott公式计算样品的禁带宽度(图4b)[7],ZrO2、(NH4)3PW12O40和ZrW的禁带宽度分别为5.12,3.33,3.36 eV,ZrW的带隙宽度明显小于ZrO2,与图4a吸收曲线相一致,说明ZrW复合材料易于被激发产生光生载流子。
2.4 ZrW的光电性能测试
材料的光生载流子的分离和迁移能力,电化学工作站测试结果见图5。


图5 光电流响应图(a)和电化学阻抗图(b)Fig.5 Photocurrent response diagram(a) andelectrochemical impedance diagram(b)
由图5可知,在紫外光照射下,复合材料的光电流明显高于ZrO2和(NH4)3PW12O40的光电流。说明复合材料具有更高的载流子密度。复合材料的阻抗曲线半径小于ZrO2和(NH4)3PW12O40,说明复合材料内部光生载流子迁移速度较快[8],载流子的分离效率更高。结合图4的分析结果,表明复合材料更易于吸收紫外光,生成光生载流子,且减少载流子的无效复合,具有较高的光催化活性。
2.5 光催化评价实验
2.5.1 草酸的影响 在RhB初始浓度15 mg/L,初始pH值为2,草酸的浓度为0.1 mmol/L,在不同光催化体系中的RhB降解效果见图6。
由图6可知,紫外光照射30 min后,无催化剂、ZrO2、(NH4)3PW12O40和ZrW体系中RhB降解率为24.9%,34.5%,51.5%和73.1%。将草酸引入以上体系中,RhB降解率分别达到 69.8%,90.1%,83.7% 和 99.7%。说明在光照体系中,草酸俘获空穴(h+)和羟基自由基(·OH),生成CO2·-,降低光生电子空穴的复合率,提高光催化降解率。
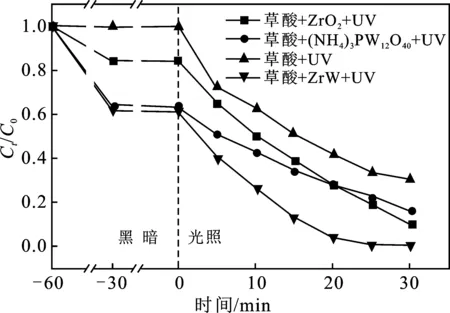
图6 草酸对光催化降解RhB的影响Fig.6 Effect of oxalic acid on photocatalyticdegradation of RhB
2.5.2 常见阳离子种类的影响 在相同反应体系中分别加入草酸、草酸铵和草酸钠,阳离子如H+、NH4+、Na+对光催化效果的影响见图7。
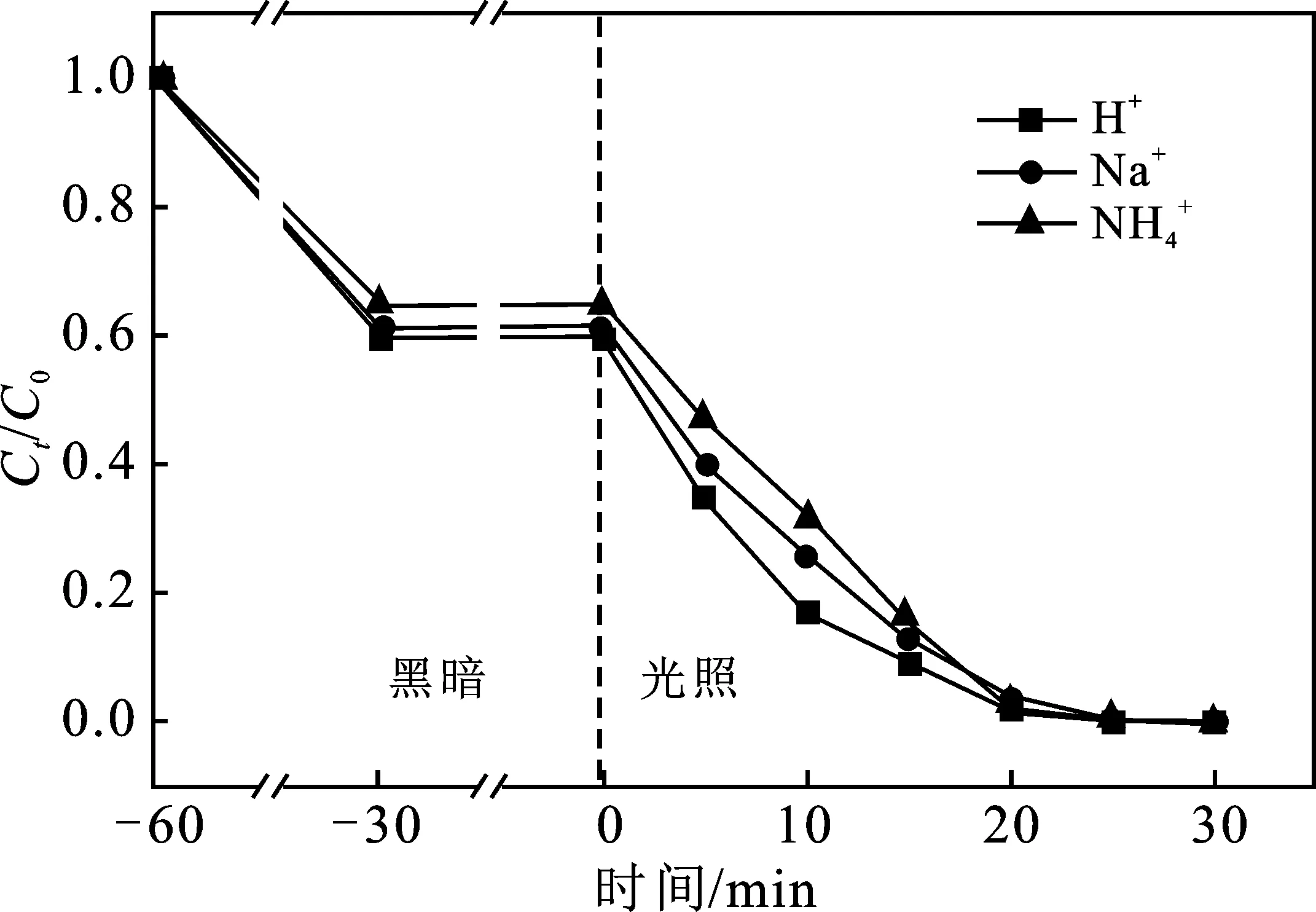
图7 H+、NH4+和Na+对光催化降解RhB的影响Fig.7 H+、NH4+ and Na+ the effect on photocatalyticdegradation of RhB
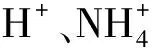
2.5.3 草酸浓度的影响 在RhB初始浓度为 15 mg/L,ZrW投加量为0.2 g/L,初始pH=2时,草酸浓度对光催化降解RhB的影响见图8。
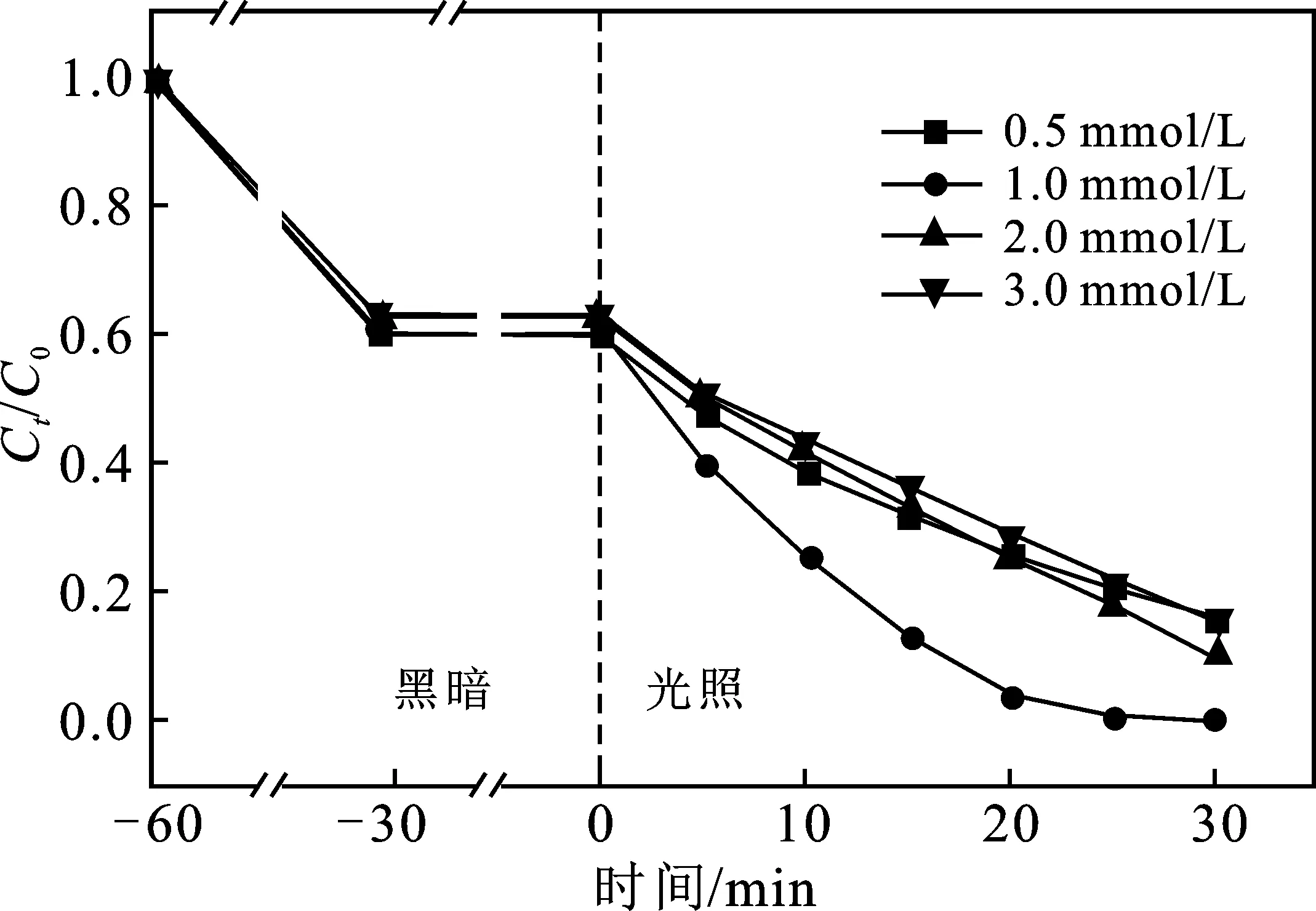
图8 草酸浓度对光催化降解RhB的影响Fig.8 Effect of oxalic acid concentration onphotocatalytic degradation of RhB
2.5.4 初始pH的影响 pH影响催化剂表面电荷及半导体表面性质。初始pH对RhB去除率的影响见图9。

图9 初始pH对光催化降解RhB的影响Fig.9 The effect of initial pH on photocatalyticdegradation of RhB
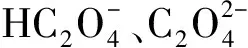
2.6 活性氧化物种分析
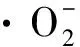
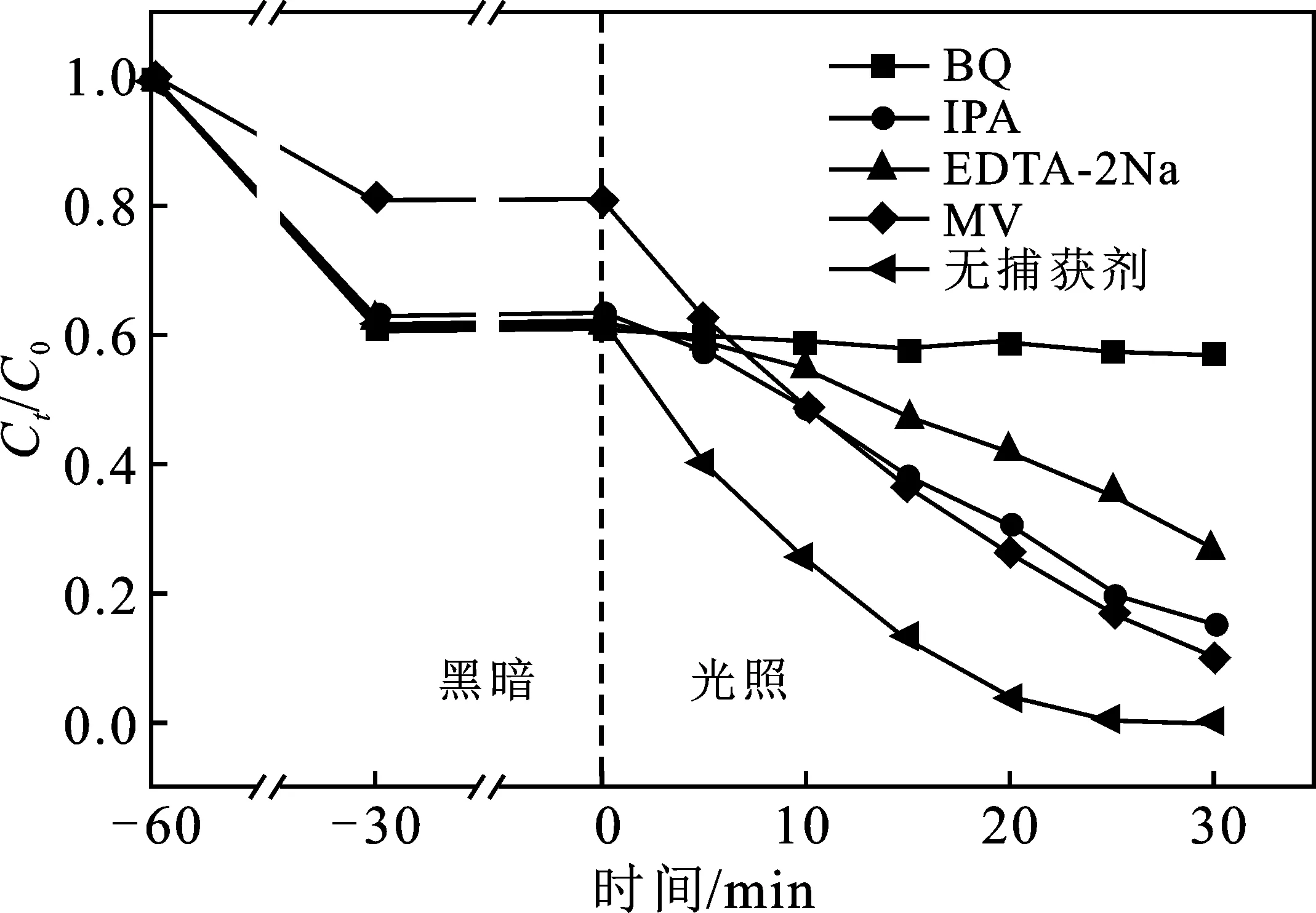
图10 酸性条件不同捕获剂对光催化降解RhB的影响Fig.10 Effect of different trapping agents on photocatalyticdegradation of RhB under acidic conditions
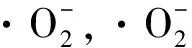
ZrO2-(NH4)3PW12O40+hv⟹
ZrO2(NH4)3PW12O40(e-+h+) (1)
(2)
(3)
h++OH-⟹·OH
(4)
(5)
(6)
(7)
h++RhB⟹CO2+H2O
(8)
3 结论