外周血免疫细胞、免疫球蛋白、补体及Gd-IgA1在儿童过敏性紫癜中的表达及意义
2021-12-15杨剑敏姜林林
杨剑敏,姜林林,高 原,马 展,张 泓
上海市儿童医院检验科,上海 200062
过敏性紫癜(HSP)是一种以小血管炎症表现为主的变态反应性疾病,在学龄儿童中的发病率较高,疾病临床表现多样,主要累及皮肤、关节、消化道及肾脏[1]。当疾病累及肾脏时,患儿有血尿、蛋白尿表现,从而发生紫癜性肾炎(HSPN),甚至可能发展为肾衰竭,是HSP最为严重的并发症[2]。目前,HSP及HSPN的致病机制尚不明确,但其与机体免疫异常密切相关,有报道声称,HSP患儿存在体液免疫功能亢进,其血清免疫球蛋白(Ig)水平升高,但并未得出一致的结论[3]。研究HSP以及HSPN患儿T淋巴细胞、血清Ig以及补体水平,有助于了解细胞免疫及体液免疫在HSP以及HSPN中的作用。此外,近年来有研究指出,HSPN患儿血清低糖化IgA1(Gd-IgA1)水平异常,Gd-IgA1的形成改变了IgA1正常生理功能,与HSPN的发病密切相关[4]。本研究分析了HSP患儿体内免疫细胞、Ig、补体及Gd-IgA1表达水平及意义,旨在探究HSP及HSPN的发生机制,现报道如下。
1 资料与方法
1.1一般资料 将上海市儿童医院2017年6月至2020年6月收治的94例HSP患儿纳入HSP组,50例健康同龄儿童纳入健康组。HSP患儿均符合文献[5]HSP的诊断标准:(1)皮肤紫癜;(2)弥漫性腹部疼痛;(3)组织病理学显示以IgA为主的免疫复合物沉积;(4)急性关节炎或关节肿痛;(5)肾脏受累。其中(1)为必要条件,加上其余条件中的任意一条即可确诊。HSP组排除标准:参与研究前2周内应用糖皮质激素、免疫抑制剂、免疫调节药物者;合并其他自身免疫性疾病、免疫缺陷性疾病、过敏性疾病、肿瘤性疾病及肾脏疾病者。根据上海医学会儿科学分会肾脏专业组制定的HSPN诊断标准[6],患儿病程中或紫癜消失后,出现血尿(肉眼或镜下)或尿蛋白即可确诊为HSPN。将HSP组患儿分为HSPN组(n=36)及非紫癜性肾炎(NHSPN)组(n=58)两个亚组。健康组近1个月内无感染,排除既往过敏性疾病、肾病史及免疫缺陷病等疾病者。HSPN组、NHSPN组及健康组年龄、性别构成差异无统计学意义(P>0.05),见表1。本研究经医院伦理委员会批准,参与研究的儿童家长知情且同意。
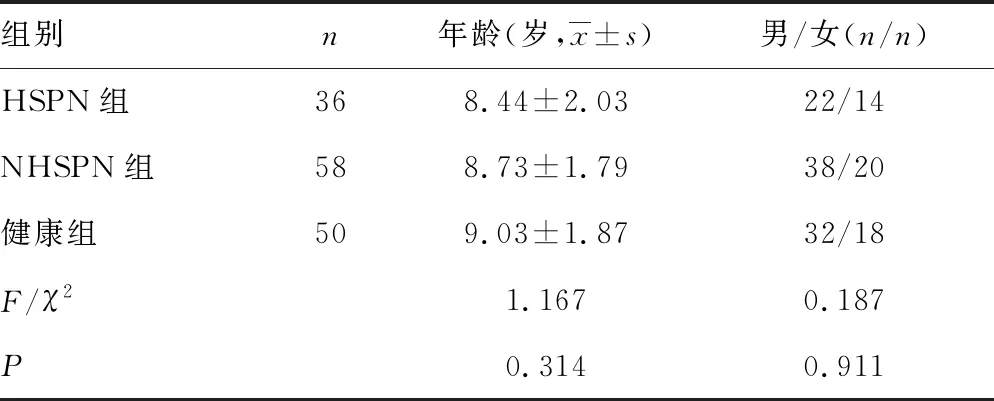
表1 3组年龄、性别分布情况
1.2方法
1.2.1外周血免疫细胞检测 检测仪器:美国BECTON DICKINSON公司FACSCalibur流式细胞仪。检测步骤:采集受试者外周静脉血3 mL,取15%的EDTA三钾抗凝外周血50 μL,分别加入相应荧光CD3+、CD4+、CD8+、CD4+/CD8+、CD19+、CD16+/CD56+单克隆抗体试管,混合均匀后放置在避光处孵育0.5 h;加入裂解液2 mL,10 min后120 r/min离心10 min,弃上清液;加入磷酸盐缓冲液(PBS)2 mL,1 000 r/min离心10 min,弃上清液;悬浮细胞加入固定液450 mL,混合均匀后放置在避光处,待上机检测。
1.2.2免疫球蛋白及补体检测 检测仪器为SIEMENS BN Ⅱ全自动蛋白分析仪。定量检测IgA、IgG、IgM水平。免疫比浊法检测补体C3、C4水平。
1.2.3Gd-IgA1水平检测 抽取受试者外周静脉血2 mL,3 000 r/min离心15 min,分离上层血清,应用上海汲泓生物科技有限公司提供的Gd-IgA1试剂盒检测血清Gd-IgA1水平,检测步骤:从冰箱中取出试剂盒,室温复温平衡30 min,将浓缩洗涤液稀释为原倍数洗涤液,加入标准品与待测标本,37 ℃水浴锅温浴30 min,洗板4次,加酶标工作溶液,37 ℃水浴锅温浴30 min,洗板4次,滴加显色剂A后加入显色剂B,平板混匀30 s,37 ℃显色15 min,终止反应,测定各孔吸光度值,计算标本中Gd-IgA1水平。
1.2.4肾功能指标的检测 采用贝克曼DXI800全自动血生化仪检测血肌酐(Cr)、尿素氮(BUN)、肾小球滤过率(GRF)水平。
1.3观察指标 (1)比较HSPN组、NHSPN组及健康组外周血免疫细胞水平。(2)比较HSPN组、NHSPN组及健康组Ig及补体水平。(3)比较HSPN组、NHSPN组及健康组血清Gd-IgA1水平。(4)分析3组血清Gd-IgA1水平与肾功能指标间的相关性。

2 结 果
2.13组外周血免疫细胞水平的比较 HSPN组与NHSPN组患者外周血CD3+、CD4+、CD4+/CD8+及CD16+/CD56+水平均较健康组显著下降(P<0.05),CD8+及CD19+水平较健康组显著上升(P<0.05),HSPN组与NHSPN组外周血免疫细胞水平差异无统计学意义(P>0.05)。见表2。

表2 3组外周血免疫细胞水平比较
2.23组Ig及补体水平比较 3组IgM及补体C4水平差异无统计学意义(P>0.05),HSPN组及NHSPN组IgA、补体C3水平均显著高于健康组(P<0.05),且HSPN组补体C3水平显著高于NHSPN组(P<0.05),HSPN组IgG水平明显低于NHSPN组与健康组,NHSPN组与健康组IgG水平差异无统计学意义(P>0.05)。见表3。
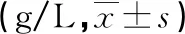
表3 3组Ig及补体水平比较
2.33组血清Gd-IgA1水平比较 HSPN组Gd-IgA1水平[(5.63±0.85)mg/L]与NHSPN组Gd-IgA1水平[(3.71±0.76)mg/L]均显著高于健康组[(2.47±0.41)mg/L],差异有统计学意义(P<0.05),且HSPN组血清Gd-IgA1水平显著高于NHSPN组(P<0.05)。
2.43组肾功能指标比较 HSPN组GRF水平显著低于NHSPN组与健康组(P<0.05),Cr及BUN水平显著高于NHSPN组与健康组(P<0.05),NHSPN组与健康组Cr、BUN及GRF水平差异无统计学意义(P>0.05)。见表4。

表4 3组肾功能指标比较
2.5HSPN组患儿血清Gd-IgA1水平与其肾功能指标间的相关性分析 相关分析显示,HSPN组患儿血清Gd-IgA1水平与其肾功能指标Cr及GRF水平呈明显正相关(P<0.05)。见表5。
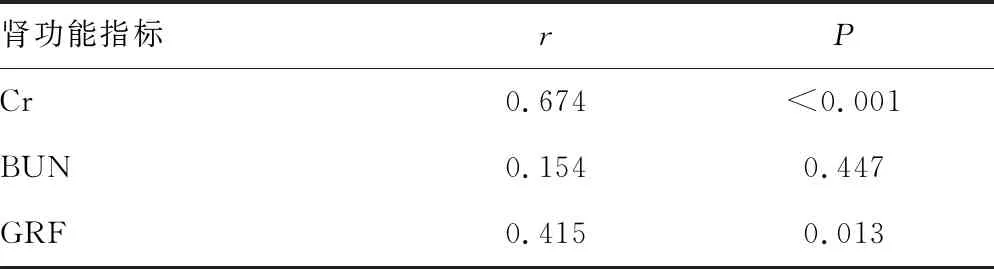
表5 HSPN组患儿血清Gd-IgA1水平与其肾功能指标间的相关性分析
3 讨 论
HSP是学龄期儿童常见的自身免疫性疾病,疾病以广泛小血管炎症为病理基础,HSP临床表现多样,主要症状有皮肤紫癜,同时合并关节疼痛、腹痛、便血及肾功能损伤等[7]。多数患儿经治疗后,病情稳定,预后良好,但临床研究数据提示,约30%的HSP患儿病情反复发作,将继发HSPN,患儿肾脏受损。HSPN最终可能发展为终末期肾病,是HSP最为严重的并发症[8-9]。
HSP的具体致病机制尚不明确,但该病属于免疫性疾病,与机体免疫功能紊乱密切相关[10]。有研究发现,HSP患者皮肤损害部位与肾小球基底膜均出现IgA免疫复合物的沉积,提示HSP与免疫失衡有关。既往关于HSP与外周血细胞免疫功能间的研究不多,机体免疫状态主要与淋巴细胞数量及功能相关,淋巴细胞是最重要的免疫细胞。本文采用流式细胞术(FCM)检测HSP患者外周血免疫细胞水平,包括T淋巴细胞(CD3+、CD4+、CD8+、CD4+/CD8+)、B淋巴细胞(CD19+)、自然杀伤细胞(CD16+/CD56+),结果提示,HSPN及NHSPN患者外周血T淋巴细胞、B淋巴细胞及自然杀伤细胞水平与健康组间差异均有统计学意义(P<0.05),其中外周血CD3+、CD4+、CD4+/CD8+及CD16+/CD56+水平均较健康组显著下降,CD8+及CD19+水平较健康组显著上升,提示HSP患儿机体T淋巴细胞总数及辅助性T淋巴细胞数量减少,B淋巴细胞数量增多。CD4+/CD8+是评价机体免疫水平与免疫调节平衡功能最具意义的指标,以上研究结果提示,HSP患者细胞免疫功能低下。
此外,本研究还通过检测血清IgA、IgG、IgM水平及补体C3、C4水平以了解B淋巴细胞功能,检测结果提示,HSPN组、NHSPN组患儿IgA水平较健康组明显上升,这提示患儿体内B淋巴细胞数量增多,产生大量Ig[11]。HSPN患儿IgG水平较NHSPN组与健康组下降,可能与HSPN患儿体内过多的免疫复合物(IgGIC)形成,耗损大量IgG有关[12]。3组IgM水平差异无统计学意义(P>0.05),与某些研究结果不一致,可能与检测方法不同有关[10]。
解剖学研究发现,HSPN患儿皮肤毛细血管、肾小球系膜区内存在补体沉积,其主要成分有补体C3c、C4+、C3+复合物,说明补体C3与HSPN的发生及发展关系密切[13]。补体C3是补体活化途径的枢纽成分,IgA循环免疫复合物沉积是诊断HSP的标志,细胞感染时,经甘露糖结合凝集素可激活补体促使补体C3水平升高。本研究发现,HSPN组、NHSPN组及健康组补体C4水平差异无统计学意义(P>0.05),而HSPN组补体C3水平明显高于健康组及NHSPN组,提示机体补体C3激活与HSP患儿肾损伤间关系密切。
有研究显示,HSP急性期儿童小血管壁内沉积大量IgA1,提示IgA1抗体是促使HSP发病的重要物质[14]。IgA1分子存在低糖基化,表现为O-N-乙酰半乳糖胺(GalNAc)半乳糖基化的程度降低,进而引起GalNAc单糖型的糖基增多,半乳糖基化或唾液酸化的糖基形式减少,半乳糖基总含量减少[15]。这种低糖基化的IgA1分子严重影响IgA1的正常功能。本研究发现,与健康组相比,HSPN组与NHSPN组患者血清Gd-IgA1水平显著升高,且HSPN组血清Gd-IgA1水平高于NHSPN组,证明HSPN及NHSPN患儿体内存在IgA1低糖基化现象,且Gd-IgA1与HSP疾病发生及发展间存在密切联系。随后行相关分析发现,HSPN组患儿血清Gd-IgA1水平与其肾功能指标GRF、Cr水平呈正相关,说明血清Gd-IgA1水平可有效提示患儿肾功能状态。
综上所述,HSP患儿细胞免疫功能下降,体液免疫功能亢进,HSPN患儿补体C3水平及血清Gd-IgA1水平均上升,且相关性分析提示Gd-IgA1水平与HSPN患儿肾功能指标GRF、Cr水平呈正相关,检测Gd-IgA1水平在辅助诊断HSP患儿肾脏病变中具有一定价值。
