氯气制备和性质检验一体化实验的新设计
2021-12-14阎润鸿冯高峰
阎润鸿 冯高峰

摘要:使用单排管和恒压滴液漏斗组合,设计并自制了中学化学“氯气的制备与性质检验”一体化实验装置。该实验装置能在密闭体系中控制反应进行,用作演示实验可使氯气性质的讲解和实验演示依次有序进行,教学效果良好。同时,该一体化实验装置可有效防止有毒气体外泄,并具有良好的普适性,可用于二氧化硫等其他气体的制备与性质检验的教学。
关键词:氯气制备; 一体化实验装置; 氯气性质; 实验探究
文章编号:10056629(2021)11006804
中图分类号:G633.8
文献标识码:B
1 问题提出
氯是高中化学阶段无机化学中重要的非金属元素,氯气的制备与性质实验是高中化学的重要实验之一。《普通高中化学课程标准(2017年版)》中将“氯气的制备及性质”写入了“常见无机物及其应用”主题学习活动建议的实验及探究活动中,要求通过实验探究,了解氯及其重要化合物的主要性质[1]。按照人教版化学必修1(新版)中氯气的实验室制法,将MnO2和浓盐酸混合加热制取氯气,能源消耗较大,检测氯气的性质实验时还需制备氯气,导致实验准备时间过长,氯气消耗量太大,造成原料浪费,不符合绿色化学思想[2]。本文将单排管和具支试管等组合起来,使氯气制备和性质检验实验一体化,并用注射器和三通阀吸收尾气[3],设计出一套适合课堂教学的实验装置。
2 研究现状
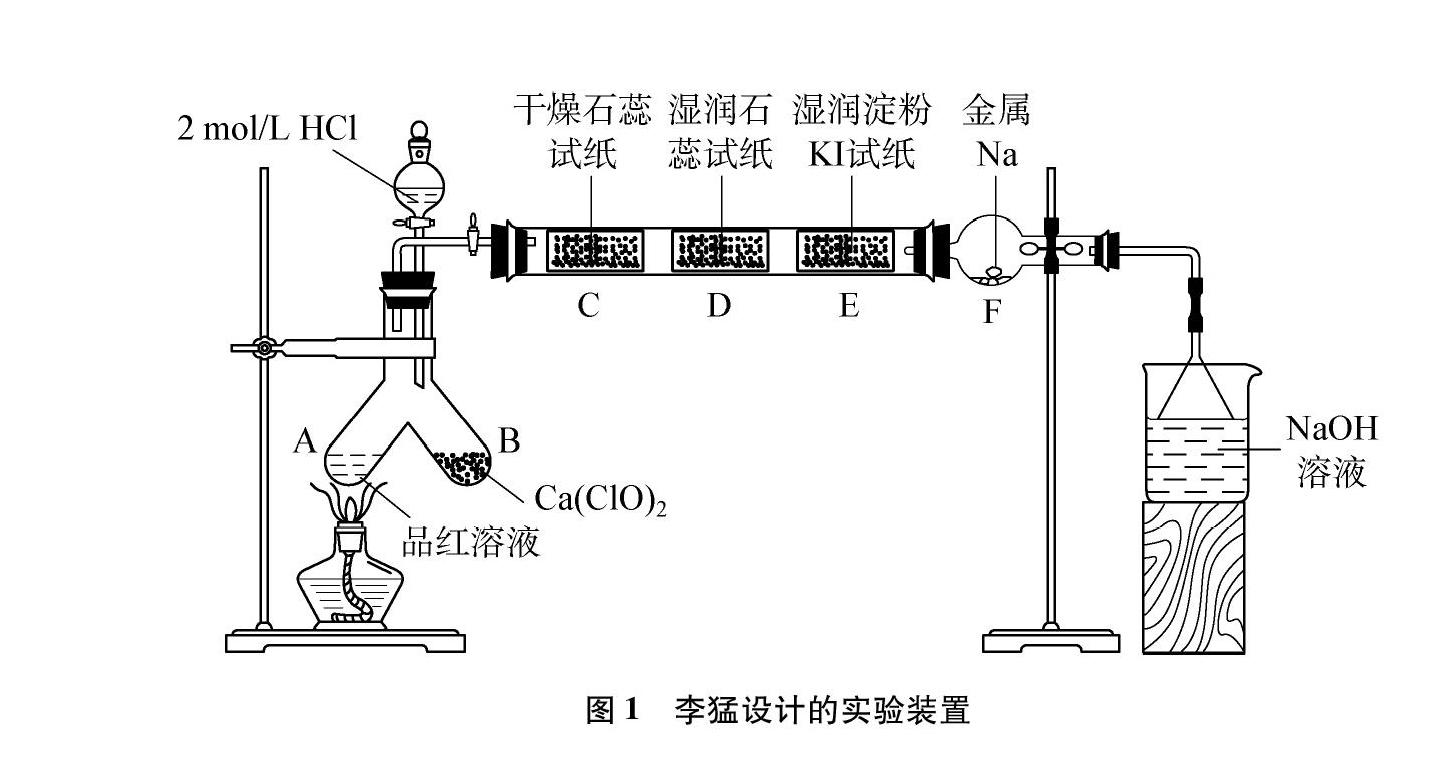
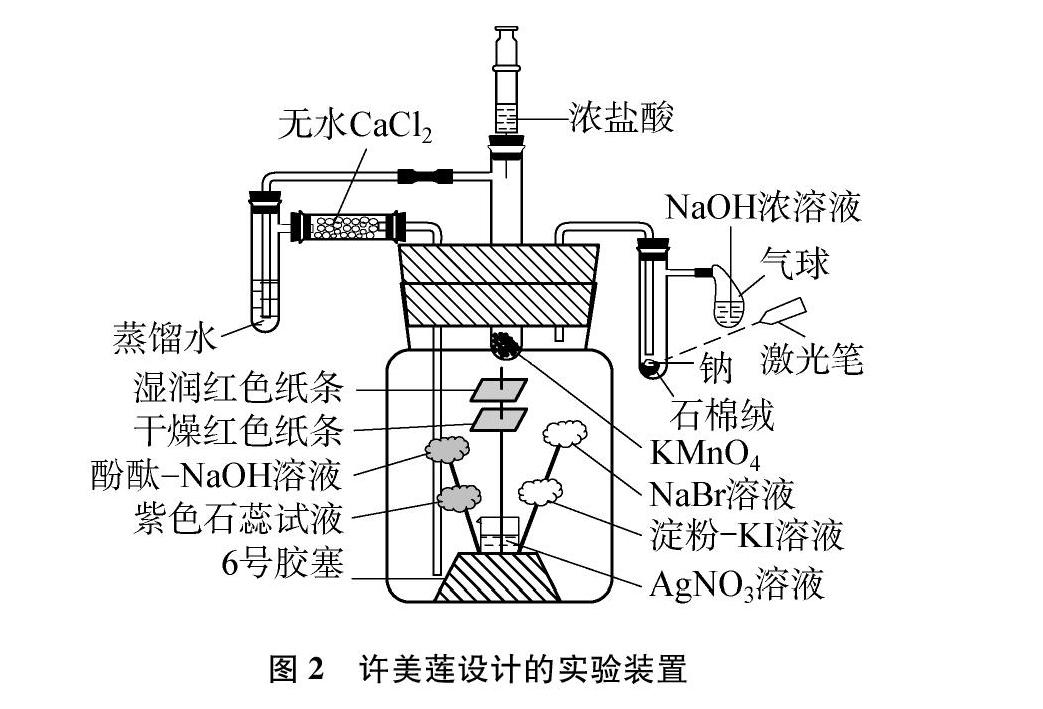
针对氯气的制备及性质实验在教学中存在的问题,不少学者从实验原理、实验装置等方面提出了多种改进方案。大多数改进方案集中于氯气制备和性质检验的一体化和微型化上。如李猛的“氯气制备及性质实验的一体化设计”[4],见图1。该装置利用硬质玻璃管检验氯气的多项性质,大大降低了实验药品的消耗,但是学生难免会产生疑惑:“先接触到氯气的试纸是否会对后面氯气性质检验造成影响”,即不同性质的检验并没有分开,科学性上不够严谨;许美莲的“氯气制备与性质实验一体化的创新设计”[5],见图2。该套装置虽然将氯气性质检验集合在一起,多種实验现象体现了化学之美,但是对于刚接触该部分内容的学生来说,同时面对氯气的诸多性质,难免会不知所措,反而导致课堂效率降低;唐梓雲的“氯气的绿色化制备及性质的整合与创新实验”[6],见图3。该套装置能连续完成湿润氯气的氧化性、酸性和漂白性等性质的检验,但是装置过于复杂,药品也难以放至装置中,并且没有解决不同性质的检验之间的干扰问题;刘江的“气体制备及性质验证综合一体化创新设计”[7],见图4。该套装置使用大量的非常规仪器,防止了有毒气体外泄,分开进行不同性质的检验,较好地完成了一体化,但却削弱了化学学科的特质和实验操作技能的训练。
3 Cl2的制备与性质检验实验的一体化设计
3.1 实验原理
2KMnO4+16HCl5Cl2↑+2MnCl2+2KCl+8H2O
3.2 性质检验
(1) 氧化性。氯气具有氧化性,可以氧化还原性物质。以卤族单质为例,氧化性Cl2>Br2>I2,故Cl2可以将Br-和I-氧化成Br2和I2。溴单质呈橙红色,碘单质遇到淀粉变蓝,现象明显。
(2) 酸性。氯气溶于水会和水发生可逆反应,生成HCl和HClO,紫色石蕊溶液遇酸变红。
(3) 遇水显漂白性。干燥有色布条遇到干燥的氯气不变色,而湿润的有色布条则褪色明显,两者形成鲜明对比。
(4) 与金属反应。在加热条件下氯气能与不活泼金属Cu反应,加入水后溶液呈现蓝色。
(5) 与碱溶液反应。氯气与氢氧化钠发生如下反应:
2NaOH+Cl2NaCl+NaClO+H2O
3.3 实验仪器及试剂
实验仪器: 单排管、10mL具支试管、恒压滴液漏斗、干燥管、烧杯、250mL抽滤瓶、三通阀、10mL注射器、透明橡胶管、玻璃导管、酒精灯、橡胶塞、止水夹
实验试剂及用品: KMnO4、浓盐酸、NaOH溶液、NaBr溶液、淀粉KI试纸、铜丝、蒸馏水、无水CaCl2、紫色石蕊溶液、红色布条、气球、滤纸
3.4 实验装置
一体化的实验装置如图5所示(夹持装置略)。单排管为单排管真空气体分配器,是有机合成科研室常用的商品化的玻璃仪器,其侧管的数量和尺寸有多种选择。恒压滴液漏斗较普通滴液漏斗多一个连通的侧管,从而使浓盐酸液面上的压力与反应瓶中的压力一致,使浓盐酸始终能够顺利滴入到反应瓶中。
3.5 装置设计原理
整个实验装置如图6所示,由气体发生、气体净化、气体收集、性质检验和尾气吸收等装置组成。(1)性质检验装置中将滤纸条用不同溶液湿润,使用透明胶带固定到玻璃导管上。(2)气体收集装置和性质检验装置使用橡胶管和玻璃导管连接,方便拆卸。(3)为了使氯气能够进入具支试管,在支管口上套一个气球以平衡气压。
3.6 实验步骤及现象
(1)如图5所示安装好实验仪器,4支具支试管从左到右分别标号为1、 2、 3、 4,检查装置气密性。打开K1、 K2,关闭K3、 K4、 K5、 K6。用洗耳球贴住开口并从恒压漏斗顶部鼓入气体,具支试管1处气球能够鼓起且不漏气。同理分别检测具支试管2、 3、 4处,若气球都能鼓起且不漏气则说明装置气密性良好。
(2)如图5所示装上药品。其中恒压漏斗中加入12mL浓盐酸,抽滤瓶中加入3g KMnO4固体,具支试管2中的紫色石蕊溶液需浸没玻璃导管末端,具支试管4中放入6cm绕成螺旋状的细铜丝,尾气处理选择1mol/L的NaOH溶液。
(3) 氧化性的检验。关闭所有活塞,打开K6,控制K1开关的大小使浓盐酸进入抽滤瓶,待单排管中明显能观察到黄绿色气体时打开K2,关闭K6,待气球鼓至有弹性时即可关闭K2,打开K6,可观察到具支试管1中蘸NaBr溶液的试纸变为橙黄色、淀粉KI试纸变蓝。
(4) 酸性的检验。关闭K6,打开K3,待气球鼓至有弹性时关闭K3,打开K6。可以观察到紫色石蕊溶液变红。
(5) 漂白性的检验。打开K4,关闭K6,待气球鼓至有弹性时即可关闭K4,打开K6。可观察到湿润的有色布条褪色,而干燥的有色布条不褪色。
(6) 与金属反应。打开K5,关闭K6。待气球微微鼓起即可关闭K5、 K1,打开K6。用止水夹夹住橡胶管,取下具支试管4,用试管夹固定并用酒精灯加热,铜丝燃烧且放出棕黄色的烟。用10mL注射器注入5mL的蒸馏水,可以观察到棕黄色的烟逐渐消失,溶液呈蓝色。
(7) 尾气吸收。打开K1、 K6,关闭K2、 K3、 K4、 K5,待少量残余的浓盐酸进入抽滤瓶后关闭K1。恒压漏斗连接三通阀(如图7所示),旋转控制阀,使三通阀的2和3连通。
在1处套上一个充满气的气球,接通1和3,再打开K1,使气球内的气体进入装置。重复上述操作2~3次使装置内气体充分被1mol/L的NaOH溶液吸收。用10mL注射器往4支具支试管中各注入2mL的1mol/L NaOH溶液吸收尾氣。
4 结语
本文以单排管和恒压滴液漏斗为主要仪器,设计了密闭体系中氯气制备、性质检验以及尾气处理一体化实验装置。新设计具有如下优点:
(1) 使用单排管。单排管各个侧管都具有控制开关,可以做到氯气的收集与性质检验分步进行。同时,各性质的检验可在单独支路中进行,使各项性质的检验可以依次进行,互不干扰,实现了氯气性质知识的讲解与相关实验演示有序进行,克服了以往实验装置存在的缺陷,提高了实验演示的教学效果。
(2) 使用恒压滴液漏斗。恒压滴液漏斗可以使反应在密闭环境下能顺利调节浓盐酸滴加速度以控制反应进行,并防止氯化氢气体外泄。使课堂实验演示与性质知识讲解有序进行。
(3) 实验装置有良好的普适性。该装置适用于固液两种反应物反应进行有毒气体的制备(如二氧化硫等)以及气体性质的有序演示和检验。
参考文献:
[1]中华人民共和国教育部制定. 普通高中化学课程标准(2017年版)[S].北京: 人民教育出版社, 2018: 13.
[2]王晶主编. 普通高中教科书·化学1(必修)[M]. 北京: 人民教育出版社, 2019: 41~44.
[3]霍本斌. 用鲁尔三通和注射器整合中学化学实验的案例[J]. 化学教学, 2020, (11): 72~79.
[4]李猛. 氯气制备及性质实验的一体化设计[J]. 化学教学, 2016, (8): 60~63.
[5]许美莲, 夏加亮. 氯气制备与性质实验一体化的创新设计[J]. 高中数理化, 2020, (16): 76~78.
[6]唐梓雲, 张水强, 黄景华等. 氯气的绿色化制备及性质的整合与创新实验[J]. 实验教学与仪器, 2017, 34(11): 17~18.
[7]刘江, 洪俊华, 赵宁东等. 气体制备及性质验证综合一体化创新设计[J]. 化学教学, 2021, (2): 62~66.
