氨磺必利联合奥氮平对精神分裂症患者糖脂代谢及睡眠质量的影响
2021-12-13张彦旭
张彦旭
(1河南省驻马店市第二人民医院制剂科 驻马店463000;2河南省驻马店市精神病医院制剂科 驻马店463000)
精神分裂症(SCH)属于严重精神障碍,多发于青壮年时期,可引起个人意识、行为、感知觉等多方面异常改变,诱发思维混乱、幻觉、抑郁等症状,导致患者社会功能逐渐丧失,甚至脱离社会[1~2]。目前,抗精神病药物是稳定SCH病情的重要手段,奥氮平为第二代抗精神病药物,口服吸收良好,可拮抗多巴胺受体、5-羟色胺受体,减轻患者阳性与阴性精神症状,促进病情好转[3~4]。但SCH病情复杂,单药治疗不利于病情稳定,且奥氮平长期单用可增加糖脂代谢紊乱风险。氨磺必利为新一代抗精神病药物,其作用机制与药物剂量存在一定相关性,小剂量给药可加快阴性症状消失,大剂量给药则能缓解阳性症状[5]。但氨磺必利与奥氮平联用是否可加重糖脂代谢紊乱备受临床关注。本研究旨在分析氨磺必利联合奥氮平治疗SCH的临床效果。现报道如下:
1 资料与方法
1.1 一般资料 选取2019年2月~2021年2月我院收治的86例SCH患者,按随机数字表法分为对照组和观察组,各43例。对照组男28例,女15例;年龄26~54岁,平均年龄(39.68±4.11)岁;体质量指数18~28 kg/m2,平均体质量指数(23.89±1.24)kg/m2;受教育年限7~15年,平均受教育年限(10.15±1.28)年;病程1~3年,平均病程(1.86±0.23)年。观察组男25例,女18例;年龄27~55岁,平均年龄(39.74±4.17)岁;体质量指数18~28kg/m2,平均体质量指数(23.93±1.27)kg/m2;受教育年限7~14年,平均受教育年限(10.12±1.24)年;病程1~3年,平均病程(1.88±0.25)年。两组一般资料对比,差异无统计学意义(P>0.05),具有可比性。本研究经医院医学伦理委员会审核批准。
1.2 入组标准 纳入标准:符合《中国精神障碍分类与诊断标准第三版(精神障碍类)》[6]中SCH诊断标准;阳性与阴性精神症状评定量表(PANSS)评分≥60分;文化程度为初中及以上;患者及家属知情同意。排除标准:肝肾功能衰竭;存在脑部器质性病变;合并代谢性疾病;对本研究用药过敏;妊娠或哺乳期。
1.3 治疗方法 对照组口服奥氮平片(国药准字H20052688)治疗,初始为5 mg/d,2周内调至15~20mg/d,2周后维持20 mg/d。观察组在对照组治疗基础上加用氨磺必利片(国药准字H20113230)口服治疗,初始为100 mg/d,2周内调至600~800 mg/d,2周后维持800 mg/d。两组均持续用药8周。
1.4 观察指标 (1)精神症状:治疗前及治疗8周后,以PANSS评分评价两组精神症状,包括阳性、阴性及一般精神病理症状,共210分,得分越低越好。(2)糖脂代谢指标:治疗前及治疗8周后,采集两组3ml空腹静脉血,离心取血清后,采用全自动分析仪测定空腹血糖(FPG)、总胆固醇(TC)、三酰甘油(TG)。(3)睡眠质量:治疗前及治疗8周后,采用匹兹堡睡眠质量指数(PSQI)评价两组睡眠质量,共21分,得分越低越好。(4)不良反应:头痛、口干、恶心等。
1.5 统计学方法 采用SPSS22.0统计学软件分析处理数据,计数资料以%表示,采用χ2检验;计量资料以(±s)表示,采用t检验。P<0.05为差异有统计学意义。
2 结果
2.1 两组治疗前后PANSS评分比较 治疗后观察组PANSS各项评分及总分均较对照组低,差异有统计学意义(P<0.05)。见表1。
表1 两组治疗前后PANSS评分比较(分,±s)
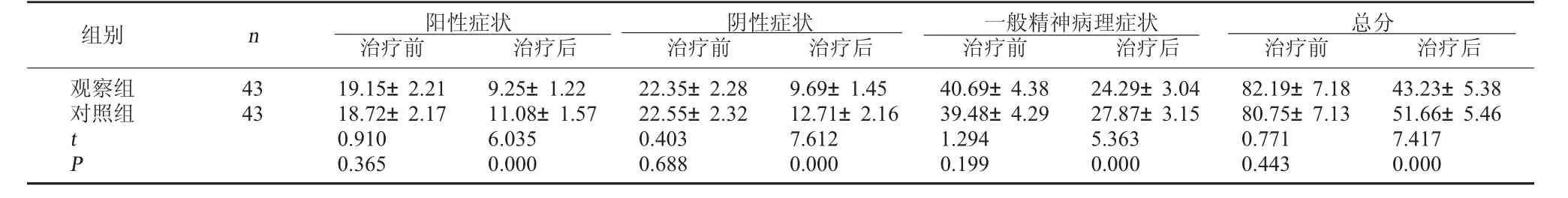
表1 两组治疗前后PANSS评分比较(分,±s)
总分治疗前 治疗后观察组对照组组别 n 阳性症状治疗前 治疗后阴性症状治疗前 治疗后一般精神病理症状治疗前 治疗后43 43 t P 19.15±2.21 18.72±2.17 0.910 0.365 9.25±1.22 11.08±1.57 6.035 0.000 22.35±2.28 22.55±2.32 0.403 0.688 9.69±1.45 12.71±2.16 7.612 0.000 40.69±4.38 39.48±4.29 1.294 0.199 24.29±3.04 27.87±3.15 5.363 0.000 82.19±7.18 80.75±7.13 0.771 0.443 43.23±5.38 51.66±5.46 7.417 0.000
2.2 两组治疗前后糖脂代谢指标比较 治疗后观察组FPG、TC、TG均低于对照组(P<0.05)。见表2。
表2 两组治疗前后糖脂代谢指标比较(mmol/L,±s)
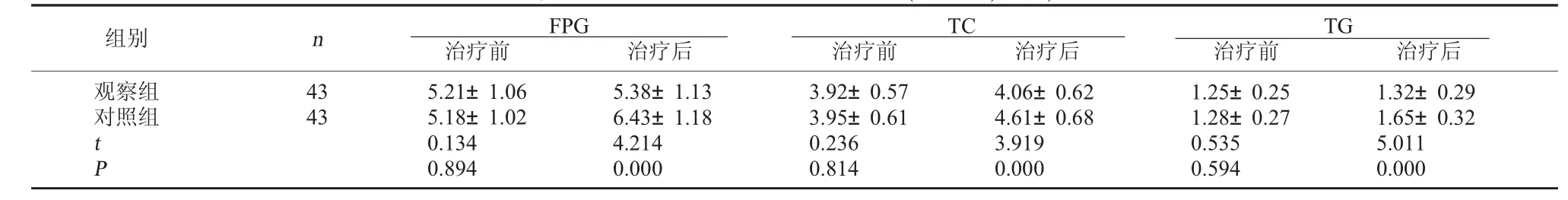
表2 两组治疗前后糖脂代谢指标比较(mmol/L,±s)
TG治疗前 治疗后观察组对照组组别 n FPG治疗前 治疗后TC治疗前 治疗后43 43 t P 5.21±1.06 5.18±1.02 0.134 0.894 5.38±1.13 6.43±1.18 4.214 0.000 3.92±0.57 3.95±0.61 0.236 0.814 4.06±0.62 4.61±0.68 3.919 0.000 1.25±0.25 1.28±0.27 0.535 0.594 1.32±0.29 1.65±0.32 5.011 0.000
2.3 两组治疗前后睡眠质量评分比较 治疗后观察组PSQI评分较对照组低,差异有统计学意义(P<0.05)。见表3。
表3 两组治疗前后睡眠质量评分比较(分,±s)
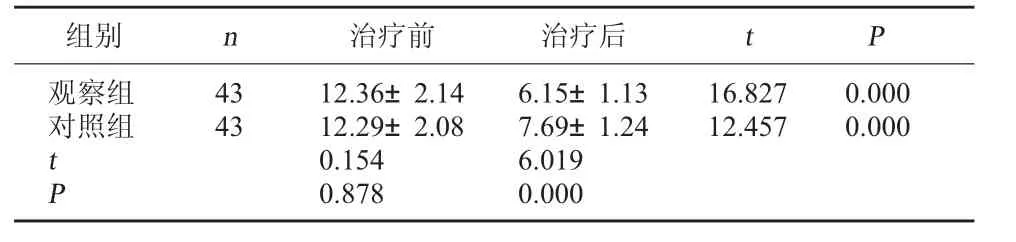
表3 两组治疗前后睡眠质量评分比较(分,±s)
组别 n 治疗前 治疗后 t P观察组对照组43 43 16.827 12.457 0.000 0.000 t P 12.36±2.14 12.29±2.08 0.154 0.878 6.15±1.13 7.69±1.24 6.019 0.000
2.4 两组不良反应发生情况比较 对照组出现口干1例,头痛2例,恶心2例,不良反应发生率为11.63%(5/43);观察组出现口干2例,恶心1例,不良反应发生率为6.98%(3/43)。组间比较,差异无统计学意义(χ2=0.138,P=0.458)。
3 讨论
SCH发病机制复杂,临床认为脑部神经递质代谢异常与疾病关系密切。多巴胺(DA)、5-羟色胺(5-HT)等神经递质作为人体情绪调节的重要物质,负责传输脑部兴奋、愉悦等信号,当其代谢异常时,则会传导错误信号,引起情绪变化失常,从而导致精神活动不协调,造成个人感知觉、行为等多方面异常变化[7]。SCH发病后不仅会降低患者的社会功能,使其逐渐脱离社会群体,反复发作的抑郁、幻觉等症状还可造成睡眠障碍,形成恶性循环,不利于疾病控制。
奥氮平为SCH常用治疗药物,为选择性拮抗5-羟色胺2A(5-HT2A)受体,可减轻SCH阴性症状,并能阻断边缘系统D2受体,缓解阳性症状,从而加快病情好转,纠正精神活动不协调情况[8]。但SCH病情存在反复发作等特点,单药作用有限,难以取得理想治疗效果。此外,奥氮平长期使用可引起胰岛素分泌异常,降低机体对胰岛素敏感性,并可造成脂蛋白脂酶活性异常,阻碍低密度脂蛋白水解,促使糖脂代谢紊乱,而糖脂代谢紊乱则会增加心血管疾病发生风险。本研究结果显示,观察组治疗后PANSS各项评分及总分均低于对照组,FPG、TC、TG均低于对照组,PSQI评分低于对照组(P<0.05),两组不良反应相比无显著差异(P>0.05)。这表明氨磺必利联合奥氮平治疗SCH效果确切,可改善患者睡眠质量,减轻精神症状,且对糖脂代谢影响小,不良反应少。氨磺必利属于多巴胺拮抗药物,具有起效快、选择性高等特点,当低剂量给药时能对突触前膜D2/D3受体进行阻滞,解除突触前抑制并阻止负反馈机制,以促进边缘系统及突触前额叶皮质释放多巴胺,缓解阴性症状;而高剂量给药时,则可选择性对边缘系统的突触后DA受体进行阻滞,发挥抗阳性症状作用[9~10]。同时,氨磺必利对5-HT2C、5-HT2A、H1受体等无明显亲和力,不易产生锥体外系不良反应,安全性高。氨磺必利与奥氮平联用可协同增效,进一步增强抗精神病效果,以稳定SCH病情,改善睡眠质量,加快患者回归正常生活,且能弥补单用奥氮平缺点,减少奥氮平用量,从而减轻对糖脂代谢的影响。
综上所述,氨磺必利联合奥氮平可减轻SCH患者阳性与阴性症状,提高睡眠质量,稳定控制病情,并能减轻对糖脂代谢的影响,安全性高。
