氨磺必利治疗精神分裂症的浓度参考范围和警戒值
2022-03-02孙丽莎崔小花戴尊孝
张 燕,孙丽莎*,李 婵,崔小花,戴尊孝,郑 璇
(1.西安市精神卫生中心,陕西 西安 710100;2.西安市药学(精神卫生)重点实验室,陕西 西安 710100;3.陕西省药品和疫苗检查中心,陕西 西安 710065
氨磺必利为2011年在我国上市的第二代抗精神病药物,其对精神分裂症症状的改善优于喹硫平、利培酮和阿立哌唑等药物[1],有助于改善精神分裂症患者的阴性症状和阳性症状,且安全性好[2-3],虽致代谢综合征风险低,但易出现高催乳素血症,继而引发血脂升高等不良反应[4]。而且催乳素会导致糖耐量降低,是致糖尿病的激素[5]。神经精神药理学与药物精神病学协会(Arbeitsgemeinschaft für Neuropsychopharmakologie und Pharmakopsychiatrie,AGNP)建议对氨磺必利进行治疗药物监测,推荐强度为强烈推荐使用(级别1)[6]。氨磺必利药物浓度存在较大的个体差异[7],在临床治疗中应结合治疗药物监测。治疗药物监测是定时采集患者的血液并测定其中的药物浓度,以药动学和药效学基本理论为基础,通过药物分析手段探讨药物在体内的代谢情况,并进行个体化治疗,以提高疗效及避免发生毒副反应的重要实验依据[8]。中国人群的氨磺必利平均药物浓度普遍高于AGNP推荐的参考范围[9-11],所以对氨磺必利的治疗药物监测制定出有效参考范围是十分必要的。本研究通过分析并探索氨磺必利浓度安全有效的参考范围及警戒值,为促进氨磺必利个体化用药提供参考。
1 对象与方法
1.1 对象
收集2019年1月-2021年3月在陕西省精神卫生中心住院治疗的精神分裂症患者为研究对象。入组标准:①无严重躯体合并症;②符合《国际疾病分类(第10版)》(International Classification of Diseases,tenth edition,ICD-10)精神分裂症诊断标准;③连续服用氨磺必利7天以上。排除标准:①合并重大、慢性疾病者;②酒精或药物依赖者;③妊娠或哺乳期妇女。符合入组标准且不符合排除标准共200例。本研究经西安市精神卫生中心伦理委员会审核批准(XAJWKY-201801)。
1.2 研究方法
1.2.1 一般资料及临床资料收集
收集患者年龄、性别、治疗时间、单日给药剂量、临床诊断、治疗前和治疗后的量表评分、出现的不良反应以及联合用药情况。
1.2.2 临床疗效评定
治疗前及治疗后的疗效评定分别于入院时和氨磺必利治疗7天以上监测其浓度时,由临床工作5年及以上的主治医师选用阳性症状量表(The Scale for the Assessment of Positive Symptoms,SAPS)和阴性症状量表(The Scale for the Assessment of Negative Symptoms,SANS)或阳性和阴性症状量表(Positive and Negative Syndrome Scale,PANSS)进行评定。上述量表在总评分及相关因子评分均显著相关(P<0.01)[12-13]。
SAPS共34个条目,包括幻觉、妄想、怪异行为、阳性思维形式障碍4个维度。SANS共24个条目,包括情感平淡或迟钝、思维贫乏、意志缺乏、兴趣/社交缺乏、注意障碍5个维度。在SAPS和SANS中,采用0~5分计分,评分越高,症状越严重[12]。计算SAPS和SANS总评分及减分率,减分率=(治疗前总评分-治疗后总评分)/治疗前总评分×100%[14]。
阳性和阴性症状量表(Positive and Negative Syndrome Scale,PANSS)共30个条目,包括阳性症状(7个条目)、阴性症状(7个条目)和一般精神病理分量表(16个条目)三个分量表。各条目按症状严重程度从无到极重,分别计1~7分[12]。在PANSS中,症状全“无”基础总评分为30分,故减分率=(治疗前总评分-治疗后总评分)/(治疗前总评分-30分)×100%[14-15]。
疗效判定标准:减分率<25%为治疗无效,≥25%为治疗有效(25%~49%为好转,50%~74%为显著进步,≥75%为基本痊愈)。
1.2.3 氨磺必利浓度测定及界值选取方法
晨起抽取患者静脉血检测氨磺必利浓度,采血时间与末次服用氨磺必利时间间隔12 h。采血管3 000 r/min离心5 min,取50µL上清液,加入乙腈500 µL,涡旋40 s,17 757 g离心10 min,吸取300µL上清液于96孔深孔板进行LC-MS/MS检测分析。采用电喷雾(ESI)离子源,多反应监测(MRM)方式进行检测,喷雾电压4.5 kV,雾化气流3 L/min,加热气流10 L/min,干燥气流10 L/min,脱溶剂管温度250℃,加热块温度350℃,氨磺必利定量离子对m/z 370.10→242.0。色谱柱为MSCB(3.0 mm×50 mm,3.3µm)C18分析柱,流动相为甲醇-0.1%甲酸水溶液(50∶50,v/v),等度洗脱,流速为0.5 mL/min,柱温为45℃,自动进样器温度设置为4℃,进样量为1µL,分析时间2 min。
根据以往监测氨磺必利浓度未超过2 000 ng/mL,故浓度为100~800 ng/mL时,以每100 ng/mL递增,浓度为800~2 000 ng/mL时,每200 ng/mL递增,分别做为探索界值,计算氨磺必利有效病例检出率,并结合不良反应发生率和减分率进行分析。
1.3 统计方法
采用SPSS 17.0进行统计分析,临床血液样本测定数据为非正态分布,以M(Q1~Q3)表示,计量资料以(±s)表示,采用单因素方差分析、皮尔逊相关和线性回归等方法进行分析,检验水准a=0.05。采用阴阳性预测值方法探索参考范围及警戒值:a为≥参考界值有效例数,b为<参考界值有效例数,c为≥参考界值无效例数,d为<参考界值无效例数。≥参考界值有效检出率为a/(a+c),<参考界值有效检出率为b/(b+d),两者相加即为参考界值的有效检出率。以参考界值的有效检出率、不良反应发生率和减分率共同确定氨磺必利浓度参考范围及警戒值。
2 结 果
2.1 患者一般资料和不同年龄段者氨磺必利浓度比较
200例精神分裂症患者中,男性72例,女性128例;年龄14~74岁[(35.79±12.04)岁],年龄<18岁5例,18~60岁191例,>60岁4例。不同年龄段的患者氨磺必利浓度差异无统计学意义(F=0.815,P=0.910)。见表1。

表1 不同年龄段的患者氨磺必利浓度比较[M(Q1~Q3),ng/mL]
2.2 患者治疗前后量表评分及疗效比较
治疗后,无效44例,好转56例,显著进步66例,基本痊愈34例。见表2。

表2 患者治疗前后量表评分及疗效
2.3 不同剂量组氨磺必利浓度比较
不同剂量组的患者氨磺必利浓度差异无统计学意义(F=0.745,P>0.05)。见表3。
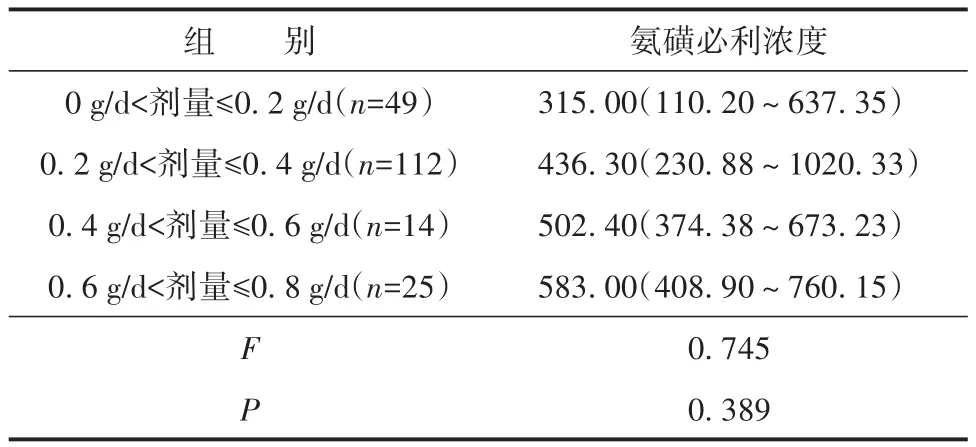
表3 不同单日给药剂量的患者氨磺必利浓度比较[M(Q1~Q3),ng/mL]
2.4 不同疗效组氨磺必利剂量和浓度比较
氨磺必利疗效与浓度的相关性无统计学意义(r=0.023,P=0.744)。不同疗效组的患者氨磺必利单日给药剂量和药物浓度差异均无统计学意义(F=0.902、1.343,P均>0.05)。见表4。
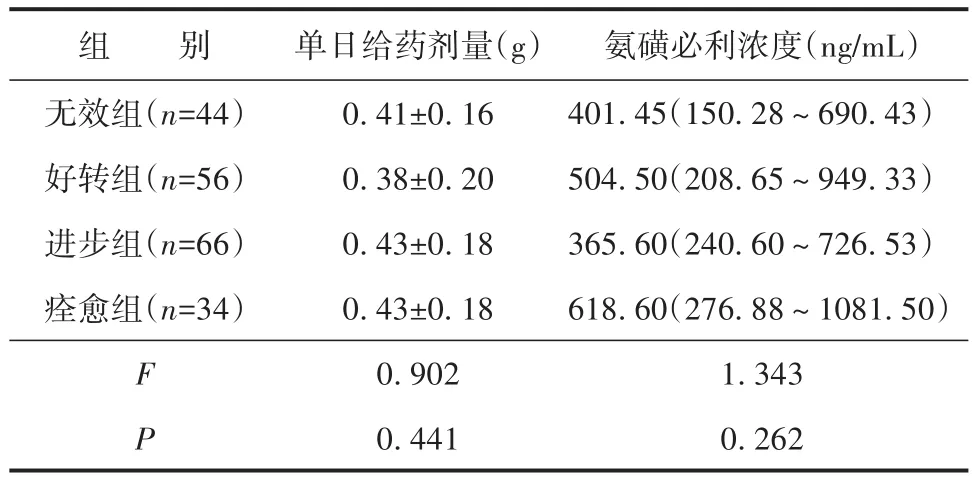
表4 不同疗效组氨磺必利剂量和浓度比较
2.5 不同浓度组不良反应发生情况
共有165例患者发生了不良反应,其中催乳素异常85例,便秘62例,锥体外系副反应48例,嗜睡、乏力21例,心动过缓16例,心慌、心动过速15例,头晕9例,白细胞升高5例,中性粒细胞偏高1例。
根据氨磺必利浓度范围,以每500 ng/mL作为分组等级,将患者划分为四组。每组氨磺必利浓度与不良反应发生率的非线性回归(曲线拟合)为:y=100x/(78.13+x),r=0.960。见表5。
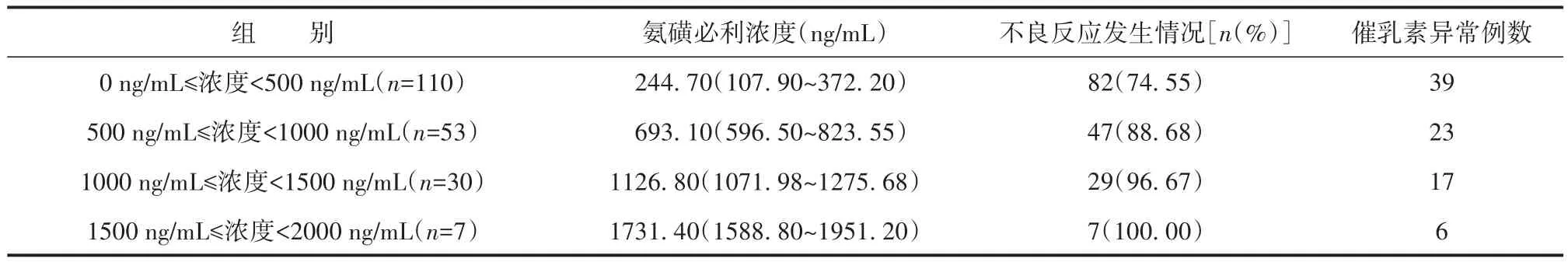
表5 不同浓度组不良反应发生情况
2.6 单一用药组与联合用药组的疗效和不良反应比较
氨磺必利单一用药组和联合用药组治疗有效率差异无统计学意义(74.29%vs.78.18%,F=2.198,P>0.05),两组不良反应发生率差异无统计学意义(74.29%vs.81.82%,F=0.095,P>0.05)。见表6。

表6 氨磺必利单一用药组与联合用药组治疗有效率与不良反应
2.7 氨磺必利浓度参考范围及警戒值的确定
依据前文1.2.3制作表7,当氨磺必利浓度超过100 ng/mL时,界值有效检出率总体呈上升趋势,直至1 400 ng/mL时,界值有效检出率降低。当氨磺必利浓度为100~600 ng/mL时,减分率均≥42%,不良反应发生率为53%~85%;当氨磺必利浓度为600 ng/mL时,不良反应发生率高达85%,之后不良反应发生率持续增加,故100~600 ng/mL可作为参考范围。当氨磺必利浓度为1 400~1 800 ng/mL时,浓度越高,减分率越低,不良反应发生率越高,故1 400 ng/mL可作为警戒值。见表7。

表7 氨磺必利浓度不同参考界值的有效检出率、不良反应发生率及减分率
3 讨 论
在当前精神科疾病发病率上升的趋势下,药物干预作为治疗精神科疾病的主要手段,在保证疗效的同时更应追求精准用药以确保用药安全性。有研究指出,氨磺必利治疗精神分裂症易发生催乳素升高的不良反应[16],在本研究收集的200例接受氨磺必利治疗的精神分裂症患者中,有165例发生了不良反应,其中催乳素异常85例。在疗效方面,氨磺必利联合心理干预或奥氮平、阿立哌唑、氯氮平等均有助于提高疗效[17-20]。本研究中,联合用药的患者中,治疗有效例数的比例高于单一用药治疗者中有效例数比例,同时不良反应发生率也高于单一用药的患者,但差异均无统计学意义。
本研究对氨磺必利药物浓度的研究表明,不同年龄段、不同单日给药剂量的患者氨磺必利浓度差异均无统计学意义(P均>0.05)。笪素娟[21]研究报道,老年人药物代谢能力差,体内游离药物蓄积可增加药物毒性。但本研究只纳入了4例老年患者,可能无法更充分地说明老年人与其他年龄段患者氨磺必利浓度的差异。最低氨磺必利浓度界值100 ng/mL对应的不良反应发生率为81%;当界值为800 ng/mL时,不良反应发生率最高,故而临床选用氨磺必利治疗时应谨慎给药。在氨磺必利剂量与浓度方面,不同单日给药剂量组氨磺必利浓度差异无统计学意义,虽然根据剂量分组的氨磺必利浓度中位数值随剂量增加而增加,但是同时在0.2~0.4 g/d组中也出现了较高的四分位数值(1 020.33 ng/mL),说明可能无法通过剂量来推测药物浓度。可能与药物代谢的个体差异有关,同时氨磺必利浓度与不良反应发生率呈非线性相关(r=0.960),提示氨磺必利浓度越高,不良反应发生率越高。
关于氨磺必利药物浓度参考范围方面,当氨磺必利药物浓度为600~800 ng/mL时,不良反应发生率均≥85%,且不同参考界值的有效检出率接近。由于氨磺必利浓度为1 800~2 000 ng/mL的患者只有3例,故不做考虑,仅将浓度为600 ng/mL时85%的不良反应发生率定为基数,超过600 ng/mL的药物浓度则不纳入参考范围,所以将600 ng/mL作为参考范围上限。当药物浓度为100 ng/mL时,减分率为43%,且不良反应发生率低于基数85%,故将100 ng/mL定为参考范围下限。当氨磺必利浓度为200 ng/mL时,不良反应发生率最低,界值有效率检出率和减分率均较高,故最佳疗效的药物浓度应为200 ng/mL。当药物浓度为1 400~1 800 ng/mL时,参考界值有效检出率与减分率大幅下降,同时不良反应发生率最高,故将1 400 ng/mL定为氨磺必利药物浓度警戒值。
综上所述,建议氨磺必利药物浓度参考值范围为100~600 ng/mL,最佳有效浓度为200 ng/mL,警戒值为1 400 ng/mL。这与广州医科大学王占璋等[10]提出的参考范围150~600 ng/mL接近,本研究与其他研究[10-11]所得出的氨磺必利有效药物浓度范围均高于AGNP指导的参考范围。由于氨磺必利2011年才在中国上市,关于中国人群氨磺必利药物浓度的报道较少,暂未查见对中国西北部人群氨磺必利药物浓度的研究报道。本研究局限性在于:①收集了200例患者,样本量有限,且只有部分分组符合正态分布;②选用SAPS和SANS或PANSS进行评定,所有患者未接受统一的量表评定;③由于采用参考界值划分的阴阳性预测值的分析方法,在对氨磺必利浓度界值划分后,部分界值对应的例数偏少。故未来应增加样本数量,采用统一的量表进行评定,进一步深入研究。
