循肝中静脉腹腔镜解剖性半肝切除术的经验体会
2021-12-08齐硕陈国栋
齐硕,陈国栋
(南华大学附属第一医院肝胆胰外科,湖南衡阳421001)
秉承“精准医疗,微创先行” 的理念,伴随影像诊断的快速发展、器械设备的持续改进及肝切除技艺的日益成熟,腹腔镜解剖性半肝切除已成为治疗肝脏肿瘤的重要术式[1-3]。解剖性半肝切除是指以肝中静脉为界,最大限度切除患侧的肝组织同时保留最多健侧肝组织的半肝切除术,此术式可有效减少术后并发症的发生[4]。而腹腔镜解剖性半肝切除术尤其是右半肝切除术,因其解剖位置的特殊性、肝脏切除体积大、腹腔镜下出血难以控制等因素,在一定程度上增加了手术的难度[5]。现就笔者所在单位开展的循肝中静脉腹腔镜解剖性半肝切除的一些经验谈些体会。
1 三维可视化技术与肝脏储备功能评估
三维可视化技术基于二维CT影像学资料通过计算机的计算、分析、重建,转换为三维立体图像,可更直观观察肝脏形态、肝脏病灶,以及肝脏脉管结构和可能变异的解剖结构,有助于术前诊治规划、评估和制定安全手术策略[6]。术前准确评估剩余半肝体积亦是至关重要的,基于CT数据进行的三维可视化技术能准确计算残肝体积,有效预防术后严重肝衰竭的发生[7]。通过三维可视化技术指导全面的术前规划、分析,选择最优手术方案,指导精准半肝切除是避免术后发生严重并发症的重要前提。
术前肝脏储备功能评估亦是防止术后发生严重肝功能衰竭的重要前提。目前临床上常见的肝功能储备评估方式主要包括影像学诊断评估、综合评估、肝功能定量实验等方式。影像学诊断评估主要包括基于超声扫描的肝脏瞬时弹性测定检查肝纤维化程度、基于CT扫描的三维可视化技术计算残肝体积及结合钆塞酸二钠(Gd-EOB-DTPA)的MRI扫描评估[8];综合评估包括Child-Pugh肝功能分级、终末期肝病模型(model for end-stage liver disease,MELD)评分等;肝功能定量实验最常用的是吲哚氰绿(indocyanine green,ICG)排泄实验,15 min ICG滞留率(indocyanine green 15 min-retention rate,ICG R15)在20%以下认为可以耐受大范围肝切除[9]。术前对肝脏储备功能进行科学的评估是解剖性半肝切除的基础及保证,临床上需要通过多种评估方式综合评估,保障半肝切除患者围术期的安全性。
2 手术操作空间的建立与入路选择
建立流程标准化的手术操作空间是术者成功实施手术的基本要求。手术操作空间的建立主要从体位的摆放、Trocar的布局、半肝的游离及腹腔内肝脏悬吊四方面进行。笔者等的体会:①患者体位取仰卧人字位;②Trocar的布局:脐下方1 cm置入10 mm的观察孔,由此孔建立气腹,分别在左、右侧锁骨中线与腋前线之间肋缘下2横指处建立副操作孔,左、右侧锁骨中线与观察孔、副操作孔连线交点下2横指建立主操作孔;③半肝的游离:使用超声刀离断肝圆韧带、镰状韧带、左/右侧冠状韧带及三角韧带,初步解剖暴露第二肝门,游离右半肝过程中尽可能充分解剖第三肝门,有时肿块巨大,原位切除时可不予充分游离;④腹腔内肝脏悬吊:主要是右半肝切除中为了更好地暴露右肝可考虑在肝脏游离后行左肝悬吊,采用自制手套外圈予3-0血管线“8”字缝合,在预留左肝前缘后从腹壁引出悬吊。通过上述方式建立的手术操作空间有利于术者成功进行半肝切除。
手术入路的个体化选择亦是手术顺利进行的重要决策。入路核心技术环节为处理第一、二肝门,目标为减少术中出血及肝脏缺血。腹腔镜半肝切除按操作方向可分为足侧入路、头侧入路、背侧入路等[10-12]。根据本中心的经验,行左半肝切除时,传统理念为采用足侧入路,在胆囊床处解剖肝中静脉终末属支后再行主干全程显露;亦可采用头-背侧入路,先解剖第二肝门,离断肝左静脉后沿肝中静脉根部,向足侧行主干全程显露;笔者等发现后者具有保护肝中静脉分支、断肝过程不“迷路” 等优势,可以作为腹腔镜解剖性左半肝切除的首选。行右半肝切除时,若肿瘤不大,一般采用足侧入路,头侧入路及背侧入路开展较少[13];若肿瘤较大,应采用原位前入路方式,使用相同的方法解剖肝中静脉终末属支后顺行找到主干,向头侧方向进行全程肝中静脉的显露,后依次处理第二、第三肝门及肝周韧带,原位前入路更符合肝脏肿瘤无瘤手术切除原则,有助于提高根治性切除率[12]。
3 循肝中静脉平面的解剖及术中操作技术
以肝中静脉为导向的解剖性肝切除可以准确把握肝切除平面,避免损失肝内重要管道,最大限度保留功能性肝组织,减少术后并发症的发生[14-16]。本中心在半肝切除时采用的肝中静脉解剖按以下方法:术中解剖离断左或右侧肝蒂明确缺血线,有条件时联合术中超声全程引导。右半肝切除时沿左右半肝的缺血线方位在胆囊床处使用超声刀切开肝实质2~3 cm左右,常可找到末梢支,“攀枝而上找主干” ,逆行从终末属支找到肝中静脉的主干[17]。左半肝切除根据情况,可采用足侧入路,先找到末梢支再显露主干;也可采用头侧入路,先解剖第二肝门离断左肝静脉及左叶间裂静脉,显露肝中静脉的起始部,向足侧顺行全程显示肝中静脉的主干,“顺藤摸瓜断枝节”[17]。整个手术基于缺血线-肝中静脉-下腔静脉三线所构平面作为解剖性半肝切除的平面,循肝中静脉所在平面的肝实质离断,有助于实现解剖性、功能性、精准性肝切除术。
术中腔镜超声、超声刀及切割闭合器灵活使用及良好团队配合是手术成功实施的安全保障。术中可使用超声进行肝中静脉的位置确定并标记预切线,指导进行精准肝切除[18];超声刀是肝实质离断比较适当的器械,合理的个体化使用可提高效率减少出血;术中切割闭合器的使用,可以减少术中的出血、加速肝切除的进程[19];良好的团队协作、娴熟的手术配合可保证手术的安全实施[20]。在肝中静脉表面的操作不能激发超声刀,必须以小口钳夹、分离为主,防止出现静脉撕裂大出血;若肝中静脉主干出现筛孔样出血,可首先予以压迫止血,若压迫止血无效,则使用6-0 Prolene线直接缝合血管或采用5-0的Prolene线缝合静脉两侧的肝组织达到压迫止血目的。精细的手术操作,可有效地防止术中大出血,保留更多的功能性肝组织,减少术后肝衰竭的发生。
4 ICG荧光手术导航及血流控制技术
传统理念左右半肝的界定为Cantlie线,但当肝脏内部肿瘤体积较大时,由于肿瘤的挤压导致肝脏的异常形态、肝内脉管的扭曲,正常的解剖学定义的Cantlie线可能无法作为左右半肝的真正分界线[21]。而ICG荧光技术术中导航,可以精准地进行肝脏切除平面界定,且可以达到不局限于肝表面的立体染色效果,辅助导航手术;同时可用于肝切除断面的残余肿瘤侦测、胆瘘侦测等,结合术中超声及术中快速病理学检查,对可疑微小癌灶进行切除及可疑胆瘘的修补,对提高手术安全性及改善预后具有重要的应用价值[22-23]。ICG荧光导航技术能同时弥补术者经验上的不足,提高手术的精准度及安全性的同时,缩短学习曲线,有助于实现解剖性、根治性肝切除术[24]。
良好的血流控制技术可有效地控制肝实质离断时的出血,是安全进行肝切除的有效保证。在进行肝脏离断时,可以通过头高脚低的手术体位、控制液体输入量及加大麻醉深度等方式来控制低中心静脉压,控制中心静脉压为1~4 cmH2O(1 cmH2O=0.098 kPa),因入肝的血管已经阻断,肝断面的出血主要来自肝静脉或者肝短静脉,控制低中心静脉压可以有效地减少术中出血[25]。另外,术中对肝静脉的分支、肝短静脉解剖位置的熟悉,做到提前预知可能发生的出血,预先对血管小分支进行解剖、血管夹夹闭等。术中的血流控制、精准解剖、减少出血是预防术后发生严重并发症的重要前提。
5 典型病例分享
5.1 3D腹腔镜解剖性左半肝切除术
3D腹腔镜与传统2D腹腔镜手术相比,还原了真实视觉中的三维立体手术视野,克服了传统腹腔镜二维视野造成的视觉误差,从而指导精准肝切除。图1为左肝肿瘤患者行3D腹腔镜解剖性左半肝切除术的临床资料。患者术前AFP为2.77 ng/ml,无乙肝病史,增强CT及MRI检查提示为肝恶性肿瘤,直径3 cm×2.5 cm,术前三维重建提示肿瘤位于S4段,肝左静脉、门静脉S4段分支均有侵犯,具有左半肝切除手术指征。术中通过3D腹腔镜视野游离肝脏后,进行第一肝门左侧肝蒂的解剖,游离肝左动脉、门静脉左支并结扎,注意保护其尾叶分支;后根据左右半肝缺血线解剖出肝中静脉主干,在控制低中心静脉压的前提下循肝中静脉全程行左半肝切除。术后复查增强CT提示肿瘤及左半肝已切除,肝断面无脓肿形成,术后病理提示胆管细胞癌(中-低分化腺癌),切缘未见癌,微血管侵犯(microvascular invasion,MVI)分级为0级。
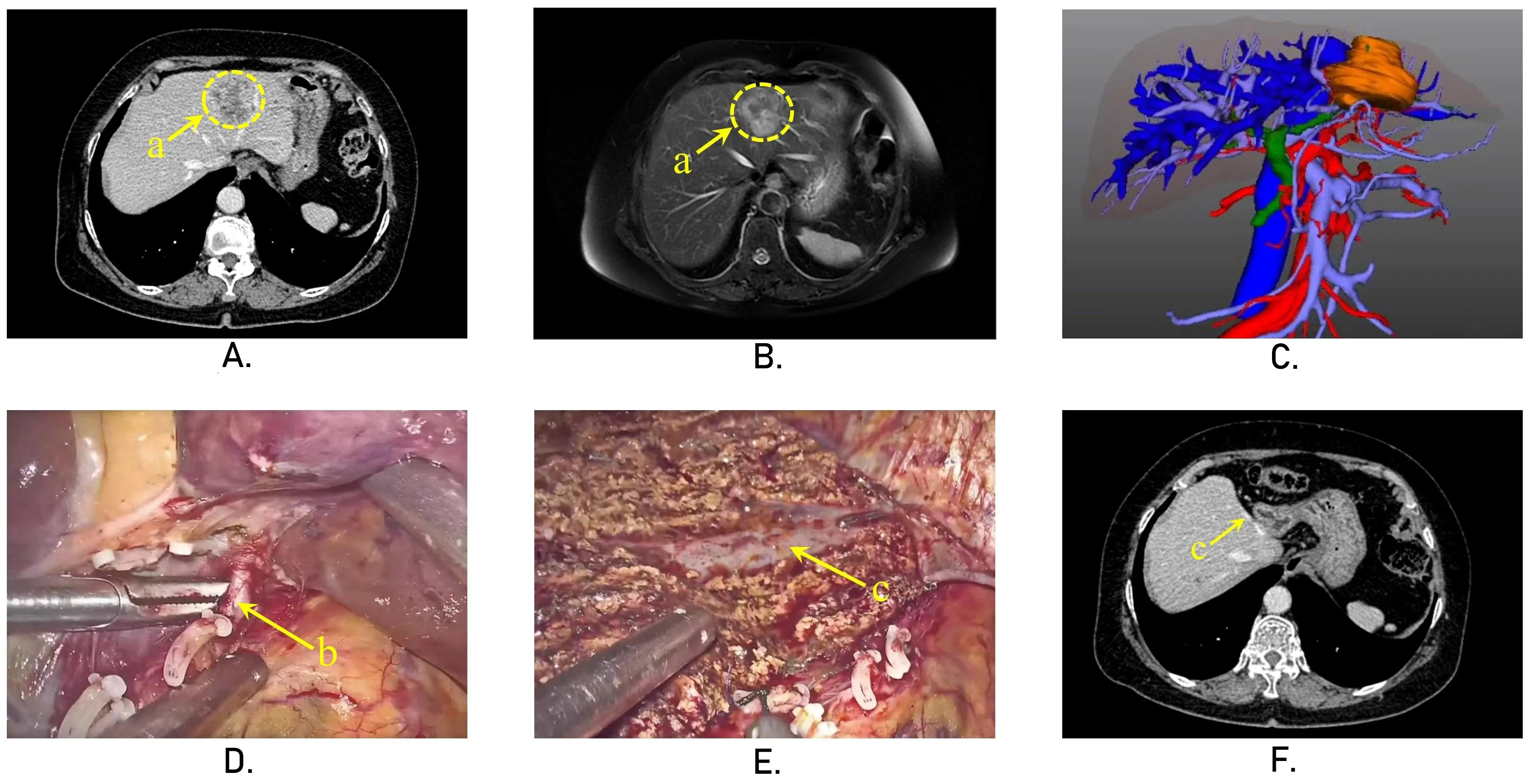
图1 3D腹腔镜解剖性左半肝切除术
5.2 原位前入路腹腔镜解剖性右半肝切除术
原位前入路肝切除作为更符合肝脏肿瘤无瘤手术切除原则的术式,对血流动力学及残肝功能的影响较小,适用于肿瘤体积过大或者与肿瘤周围组织、脏器有粘连无法游离半肝的患者。图2为右肝巨大肿瘤患者行原位前入路腹腔镜解剖性右半肝切除术的临床资料。患者术前AFP为28.6 ng/ml,有乙肝病史,术前增强CT及MRI提示右肝占位,直径约8 cm×7 cm,术前三维重建提示肿瘤主要位于S5、S6及S7段,手术方式拟行原位前入路腹腔镜解剖性右半肝切除术。术中切除胆囊后,先解剖第一肝门右侧肝蒂血管,离断右半肝入肝血流后显示出左右半肝界限,沿胆囊床缺血线切开肝实质,解剖出肝中静脉的主干,在控制低中心静脉压的条件下循肝中静脉进行肝实质的离断。术后复查右半肝及肿瘤已完整切除,肝断面无明显积液。术后病理提示肝细胞癌,切缘未见癌,MVI分级为0级。
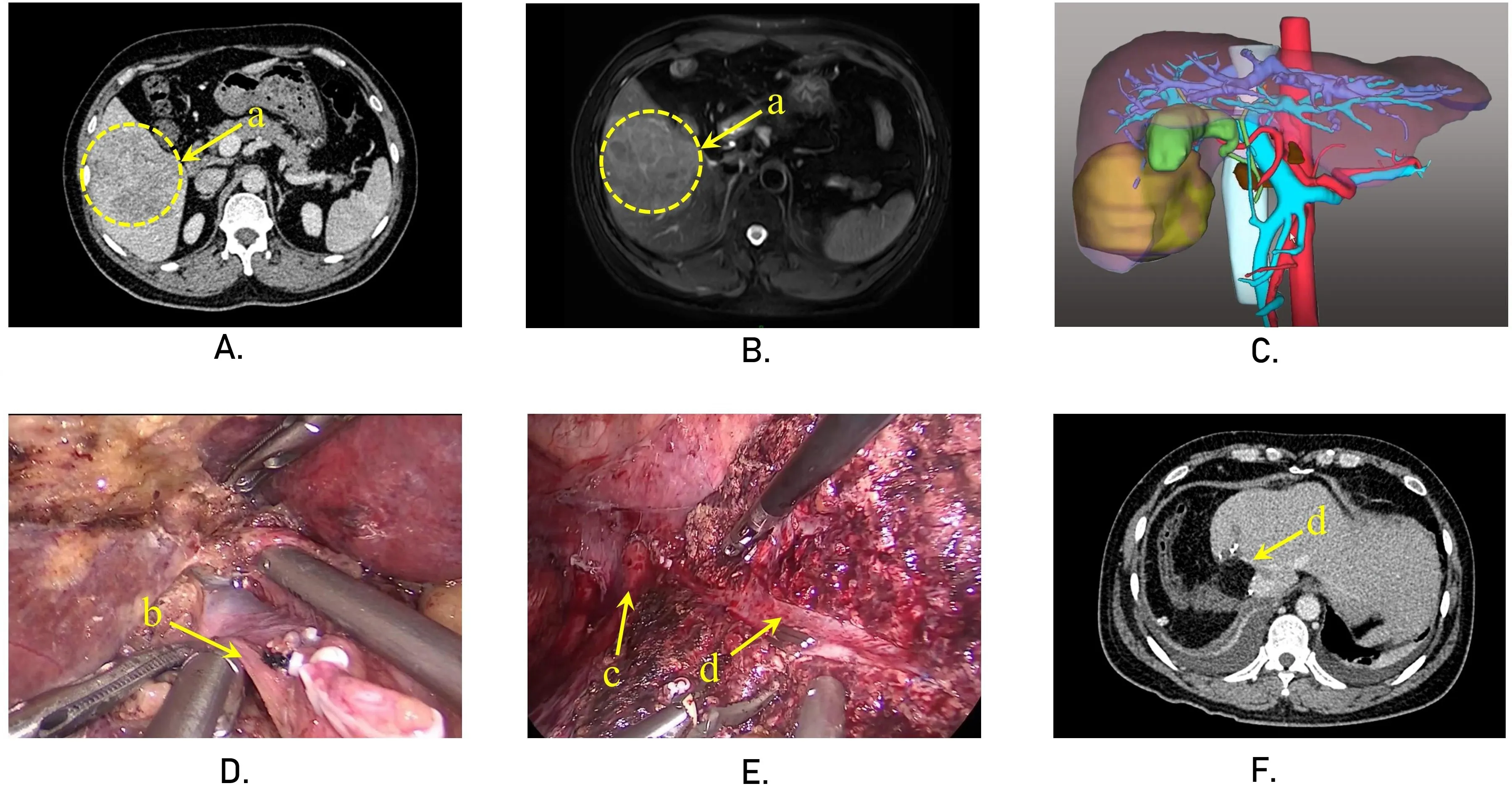
图2 前入路原位腹腔镜解剖性右半肝切除术
5.3 ICG荧光导航腹腔镜解剖性右半肝切除术
ICG荧光技术通过对肿瘤的精准定位、肿瘤边界界定、半肝界线界定等方式,对解剖性半肝切除术的导航效果更精准,可安全地进行肝切除,降低术后并发症的发生率。图3为右肝肿瘤患者ICG荧光术中导航解剖性肝切除患者的临床资料。患者术前AFP为18.41 ng/ml,有乙肝及肝硬化病史,术前增强CT提示右肝占位,直径7 cm×8 cm,肿瘤位于右半肝,有右半肝手术切除指征。通过术前48 h注射ICG后使用荧光成像设备侦测,肿瘤区域出现明显的荧光边界;术中解剖右侧肝蒂阻断右半肝血流后,静脉注射ICG反染进行左右半肝边界界定,荧光成像设备可见明显半肝界限,作为导航右半肝切除的预切线及肝中静脉的解剖位置指导;切除胆囊,沿胆囊床在预切线处切开肝实质,解剖出肝中静脉主干,向头侧解剖至第二肝门肝中静脉的根部,循肝中静脉进行右半肝肝实质的离断。术后复查右半肝及肿瘤已完整切除。术后病理提示中分化肝细胞癌,未侵犯肝脏被膜,离断面切缘无癌侵犯,MVI级为0级。
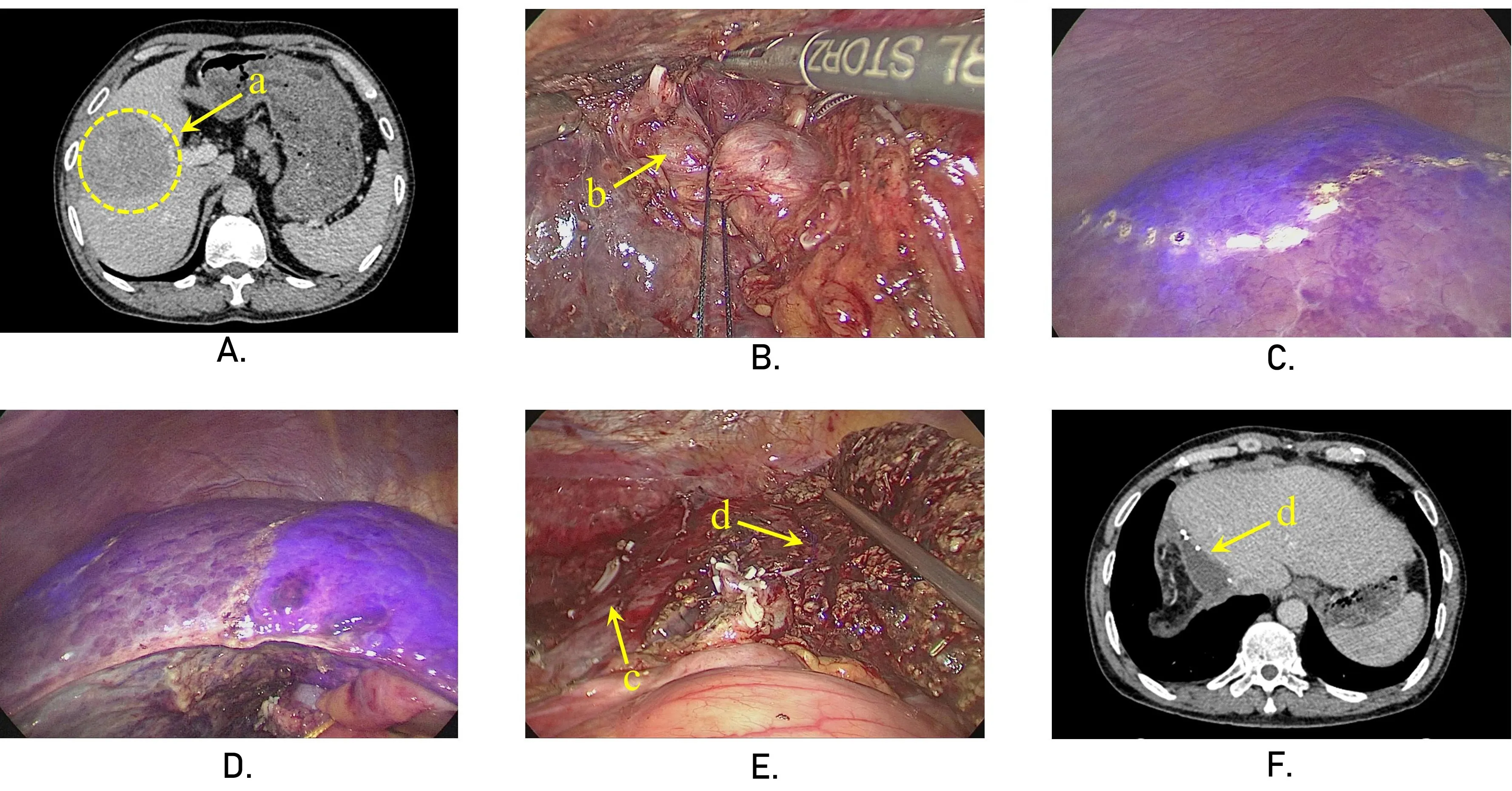
图3 ICG荧光导航腹腔镜解剖性右半肝切除术
6 结 论
随着数字智能化外科时代的来临,三维可视化、虚拟现实、混合现实、3D腹腔镜、荧光腹腔镜、达芬奇机器人等辅助的智能化影像诊疗技术的发展,为肝脏外科的发展带来了新的机遇与挑战,有助于实现真正意义上的解剖性肝切除手术的“无禁区”[26]。本中心通过三维可视化技术指导的术前精准评估,有助于保障手术的安全实施;通过建立个体化手术空间,尤其是右半肝切除的左肝悬吊技术,有助于术者更好地进行手术操作;通过综合多种手术入路,有助于安全、有效地进行肝中静脉全程解剖;基于ICG荧光导航的循肝中静脉平面肝实质离断、精细的手术操作及有效的血流控制技术,有助于实现解剖性、功能性、精准性肝切除术。数字智能化技术的临床应用,将推动肝脏外科诊疗体系的革新,实现患者疾病的精准诊治与术后加速康复[27-28]。
本研究仅针对肝脏肿瘤患者行解剖性半肝切除的研究,未涉及肝内胆管结石行解剖性半肝切除术的分析。因肝内胆管结石患者往往存在结石挤压导致的管道变异,故目前肝内胆管结石是否需行循肝中静脉的解剖肝切除尚存在争议,需要高级别的临床研究支撑。但总的来说,对于肝脏肿瘤患者,循肝中静脉解剖的腹腔镜半肝切除术是一种安全、有效的手术方式,该手术策略值得在临床肝脏外科中推广应用。希望今后可以开展多中心随机对照研究,为进一步评估循肝中静脉解剖的腹腔镜半肝切除术在肝脏外科中的应用价值提供高级别的临床证据,为肝脏外科的发展提供新的思路。
