交流电场中碳钢和镀锌钢的大气腐蚀行为
2021-12-08赵旭阳吴芳芳胡露露盛叶弘曹发和
赵旭阳,吴芳芳,胡露露,盛叶弘,洪 静,曹发和
(1. 浙江华电器材检测研究所有限公司,国家电力器材产品安全性能质量监督检验中心,杭州 310015; 2. 浙江大学 化学系,杭州 310027)
随着经济发展,为满足日益增长的电力需求,超高压输电线相继出现。近年来社会各界对超高压输电线和输电塔架的安全问题都十分关注。碳钢被广泛用于电网工程的输电塔架和输电线,电场的存在对碳钢的腐蚀失效有着重要的影响。为了延长碳钢构件在服役环境中的寿命和保证其更加安全地运行,目前采取的主要措施是在碳钢表面镀锌。由于锌不仅具有良好的耐蚀性,而且可作为牺牲阳极对碳钢提供保护,锌层可极大提高碳钢的耐蚀性,从而提高超高压输电的安全,延长输电线的服役寿命。输电塔架和输电线在自然环境中服役,主要发生大气腐蚀。研究发现,服役于海洋大气环境中的碳钢表面通常会形成一层含Cl-的液膜,该液膜会促进腐蚀发生,增大碳钢的腐蚀速率[1-2]。目前,对于镀锌钢的大气腐蚀行为研究,多关注于腐蚀产物及其演化[3]以及Cl-的影响[4]等方面。由于镀锌钢输电塔架受到大气环境因素和外加可变电场因素的协同作用,其腐蚀失效行为更为复杂,目前关于这一方面的研究相对缺乏,因此研究外加可变电场中镀锌钢的大气腐蚀行为具有现实意义。
随着电网发展,输电容量的增大,500 kV以上的超高压电塔增多,高强度电场环境对电网工程中输电塔架、输电线和相关电力金具等构件的影响也不容小觑[5-6]。张俊喜团队[7-9]利用特殊的薄液膜装置以及干湿循环装置研究了外加直流电场条件下金属锌和碳钢的腐蚀失效行为。朱紫晶等[10]研究发现,在薄液膜下外加直流电场会削弱碳酸环己胺的反应活性和吸附能力,导致其缓蚀效率降低。此外,在外加直流电场中,铜的阴极极限电流密度会随着电场强度的增大而减小,电场对薄液膜下铜的腐蚀速率有减缓作用,在直流电场的影响下,薄液膜中的Cl-从负极迁移到正极[11-13]。现有研究多关注直流电场对碳钢、锌层、铜等金属的腐蚀行为影响,关于镀锌钢在交流电场中的大气腐蚀行为研究仍鲜见报道。
本工作通过自行开发的试验装置模拟了大气环境中钢表面形成的不同厚度的液膜,并在不同交流电场强度与液膜厚度条件下对碳钢和镀锌钢进行了电化学测试,分析了液膜厚度和电场强度对钢腐蚀行为的影响。
1 试验
本试验选用输电线常用材料碳钢(20钢)和镀锌钢。采用图1所示的自制液膜装置[14]模拟大气环境中钢表面形成的液膜。试验装置主要由干燥器、水平台、电解池、带有细铂丝的螺旋测微器和铁架台等构成。工作电极表面的液膜厚度通过万用表测量电阻的突变获得。通过高压电源对装置中两个间距5 cm的不锈钢板通交流电,使工作电极和不锈钢板之间形成不同强度的电场。另外需要特别注意的是:底部极板需接地,以模拟电网中大型构件的接地环境[6,15]。待工作电极表面形成稳定薄液膜且其厚度达到预设值后,在不同电场强度下对其进行电化学测试。

图1 外加电场的液膜装置图Fig. 1 Diagram of a thin electrolyte layer device with an applied electric field
采用上海辰华CHI630C电化学工作站测试镀锌钢以及碳钢的开路电位和极化曲线,采用美国VMP2多通道恒电位仪测试镀锌钢以及碳钢在不同液膜厚度下的电化学阻抗谱。电化学试验采用传统的三电极体系:镀锌钢和碳钢为工作电极,Ag/AgCl(KCl浓度为3 mol/L)电极为参比电极,直径为0.5 mm的铂丝作为辅助电极环绕在工作电极四周。极化曲线测试时,电位扫描范围为-0.3~0 V(相对于OCP),扫描速率为1 mV/s。在液膜体系中,碳钢的阳极反应会使金属溶解影响薄液膜的厚度,导致其电流分布不均匀,因此在液膜体系中仅测试了阴极极化曲线。电化学阻抗谱测试时,外加激励信号为正弦波(扰动振幅5 mV),扫描频率范围为10 mHz~100 kHz,并应用ZSimpWin软件和符合物理模型的等效电路对试验数据进行拟合[16]。由于外加交流电场会显著影响电化学阻抗谱测量,所以仅测试没有外加交流电场条件下的电化学阻抗谱。试验温度为室温,试验介质为3.5%(质量分数)NaCl溶液。采用带有能谱功能的SU-8010扫描电子显微镜表征镀锌钢以及20钢腐蚀前后的表面形貌以及腐蚀产物的成分组成。
2 结果与讨论
2.1 极化曲线
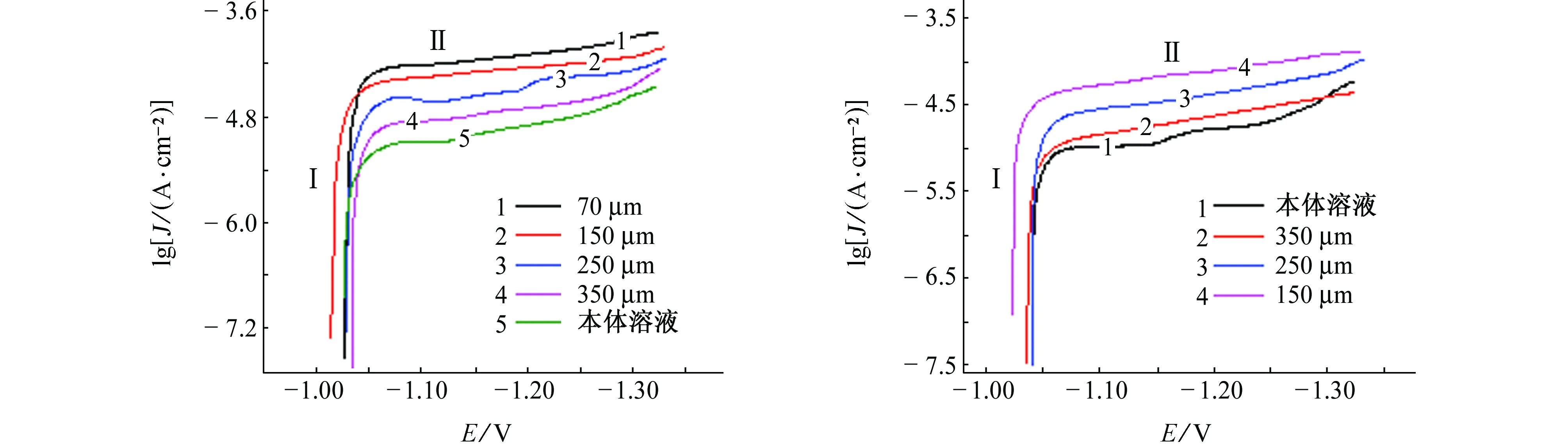
图2为不同厚度液膜下碳钢和镀锌钢的阴极极化曲线。无论是碳钢和镀锌钢,在不同液膜厚度下,其极化曲线都可以分为两个区域(Ⅰ,Ⅱ),在自腐蚀电位附近,随着电位负移,电流快速增大,到达极限值后趋于稳定,这表明反应进入氧扩散控制范围。液膜厚度对碳钢和镀锌钢的自腐蚀电位影响不大,在相同液膜厚度下,镀锌钢比碳钢的自腐蚀电位负移了约450 mV。
图2中曲线平台对应的电流密度与液膜厚度有关,液膜越厚,对应的电流密度越小。在极化曲线中取极化电位为-0.25 V(相对于开路电位)时对应的阴极电流密度作为极限电流密度,以极限电流密度为纵轴、液膜厚度为横轴作图,结果如图3所示。由图3可见:碳钢和镀锌钢在薄液膜下的极限电流密度均高于其在本体溶液中的极限电流密度,且随着薄液膜厚度减小,极限电流密度增大,这说明在液膜体系中碳钢和镀锌钢表面的氧传输比在本体溶液中更充分。在本体溶液及较厚(350 μm)液膜体系中,极限电流密度变化较小,这是因为液膜厚度的改变仅仅影响了对流层的厚度。在较薄液膜体系中,极限电流密度随着液膜减薄明显增大,因为此时液膜的厚度比扩散层的厚度小,改变液膜厚度会影响扩散层的厚度,所以极限电流密度迅速增大。随着液膜减薄,氧气的扩散路径变短,有更多的氧可参与阴极还原反应,从而使阴极极限电流密度明显增大,即碳钢和镀锌钢的腐蚀速率增大[17]。比较可见,在相同液膜厚度下,镀锌钢的极限电流密度比碳钢的小,这表明镀锌钢的腐蚀速率比碳钢小,镀锌层对碳钢起到了保护作用。

(a) 碳钢 (b) 镀锌钢图2 在不同厚度液膜下碳钢和镀锌钢的阴极极化曲线Fig. 2 Cathodic polarization curves of carbon steel (a) and galvanized steel (b) under liquid film with different thicknesses
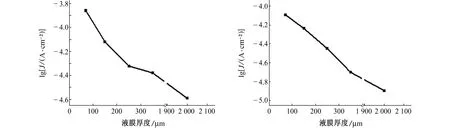
(a) 碳钢 (b) 镀锌钢图3 碳钢与镀锌钢的阴极极限电流密度与液膜厚度的关系曲线Fig. 3 Cathodic limited current density vs liquid film thickness for carbon steel (a) and galvanized steel (b)
2.2 电化学阻抗谱
图4和图5为不同厚度液膜体系中碳钢和镀锌钢在浸泡不同时间后的电化学阻抗谱。
由图4可见,在本体溶液中,碳钢电化学阻抗谱的中高频区域和低频区域分别出现一个容抗弧,阻抗随浸泡时间延长先变小后变大。在本体溶液中浸泡4 h后,碳钢的容抗弧半径比浸泡30 min后明显小,随着浸泡时间的延长,容抗弧半径变小明显,这是由于碳钢表面在空气中形成的氧化膜被破坏,碳钢的腐蚀速率加快,此时碳钢表面的腐蚀反应十分活跃。在碳钢腐蚀后期,容抗弧半径虽有增大但不明显,这是因为碳钢表面生成的腐蚀产物在一定程度上阻碍了碳钢的腐蚀。在所有液膜厚度下,电化学阻抗谱在中高频和低频区也各出现一个容抗弧(图略),与在本体溶液中的情况相似,说明液膜厚度的变化对碳钢的腐蚀机理影响较小。但是液膜厚度的减小缩短了氧气在溶液中的扩散时间[14,17]并抑制了腐蚀产物在溶液中溶解和迁移。在液膜厚度为70 μm时,除中高频区各出现一个容抗弧外,低频区出现感抗弧,这与碳钢表面吸附的腐蚀产物和蚀点分布有关。在液膜厚度较厚时(大于70 μm),未出现感抗弧,这是因为在较厚的液膜下,碳钢表面出现的蚀点相对均匀,腐蚀产物分布也较为均匀。

(a) 本体溶液 (b) 70 μm图4 不同厚度液膜体系中碳钢在浸泡不同时间后的电化学阻抗谱Fig. 4 EIS of carbon steel immersed for different time under liquid film with different thicknesses: (a) bulk solution; (b) 70 μm

(a) 本体溶液 (b) 90 μm图5 不同厚度液膜体系中镀锌钢在浸泡不同时间后的电化学阻抗谱Fig. 5 EIS of galvanized steel immersed for different time under liquid film with different thicknesses: (a) bulk solution; (b) 90 μm
由图5可见,在本体溶液中,镀锌钢电化学阻抗谱的高频和中频区分别出现一个容抗弧,腐蚀初期低频区出现扩散,24 h后出现感抗弧[18-19]。在腐蚀后期(浸泡24~48 h),随着浸泡时间的延长,镀锌钢的腐蚀速率变小,这是由于在本体溶液中镀锌层生成的腐蚀产物附着在基体表面,阻碍了基体的腐蚀,从而降低镀锌钢的腐蚀速率[20]。浸泡24 h后,低频区域出现感抗弧,这可能与镀锌钢发生活性溶解有关。浸泡初期镀锌钢在本体溶液中的容抗弧半径明显大于其在液膜中的。这是因为在本体溶液中,氧气扩散路径较长,所需时间也较长,阴极反应被抑制,导致镀锌钢的腐蚀速率减小。腐蚀初期镀锌钢在液膜体系中的腐蚀速率比其在本体溶液中的快,这与极化曲线的结果一致,且与氧易扩散有关[14-15,17]。镀锌钢电化学阻抗谱的低频区不固定出现感抗弧,这与吸附性离子的驰豫过程有关[19]。
采用图6所示的等效电路拟合碳钢和镀锌钢在不同厚度液膜下的电化学阻抗谱。其中,Rs表示溶液电阻,Rf表示镀锌钢表面生成的腐蚀产物膜电阻(膜电阻),Rct表示电荷转移电阻,Cf和Cdl分别表示产物膜电容和双电层电容。由于碳钢和镀锌钢的两个容抗弧存在不同程度的重叠,采用膜电阻和电荷转移电阻参数之和(Rf+Rct)来表征碳钢和镀锌钢的耐蚀性能及其随时间演化,结果如图7所示。

图6 不同厚度液膜体系中电化学阻抗谱的等效电路Fig. 6 Equivalent circuit for EIS under liquid film with different thicknesses
由图7(a)可见,随着浸泡时间的延长,不同厚度液膜下碳钢的Rf+Rct均先减小后增大。这主要是因为碳钢电极表面在空气中会生产一层氧化膜,随着浸泡时间的延长,氧化膜会被破坏,出现腐蚀活跃区域,腐蚀速率增大。碳钢在本体溶液中的Rf+Rct均大于其在液膜体系中的,说明碳钢在本体溶液中的腐蚀速率小于其在液膜体系中的。
由图7(b)可见,镀锌钢在液膜下的Rf+Rct小于其在本体溶液中的,且随着液膜厚度减小Rf+Rct也变小。在相同液膜厚度下(350 μm除外)或者本体溶液中,随着浸泡时间的延长,Rf+Rct呈增大趋势,这是因为在镀锌层的腐蚀过程中,锌层生成的腐蚀产物会附着在电极表面,减少了腐蚀活性点,从而降低了镀锌钢的腐蚀速率。镀锌钢在本体溶液中的腐蚀速率小于在其在液膜下的,主要是因为溶解氧在液膜下的扩散明显快于本体溶液,所以镀锌钢的腐蚀速率随着液膜减薄而增大[17]。电化学阻抗谱与极化曲线的结果具有较好的一致性。

(a) 碳钢 (b) 镀锌钢图7 在不同厚度液膜体系中碳钢和镀锌钢的Rf+Rct随时间的变化Fig. 7 Rf+Rct vs time for carbon steel (a) and galvanized steel (b) under liquid film with different thicknesses
2.3 外加交流电场的影响
实际电力系统所用碳钢通常采用锌层保护,因此此处只研究了镀锌钢在交流电场与液膜共同作用下的电化学行为。另外由于电场作用会严重影响电化学阻抗谱的测量,本工作只采用开路电位和极化曲线研究外加电场的影响。
图8为镀锌钢在交流电场和不同厚度液膜体系中的开路电位。结果表明:液膜厚度对镀锌钢开路电位的影响较小,但在外加交流电场后,镀锌钢的腐蚀电位发生一定幅度的负移,这是因为在外加电场作用下,液膜中的正电荷会向镀锌钢/液膜界面迁移,导致镀锌钢和溶液界面双电层电容的电荷密度增加,促进阴极反应,即氧的还原反应和镀锌钢的氧化反应[15]。待镀锌钢在本体溶液或不同厚度液膜下浸泡20 min,电位达到稳定后,分别施加强度为0 ,20,60,100 kV/m的交流电场10 min并测阴极极化曲线,结果如图9所示。在极化曲线中取极化电位为0.25 V(相对于开路电位)时的阴极电流密度作为极限电流密度。图10为不同厚度液膜体系中交流电场强度对镀锌钢阴极极限电流密度的影响。在外加交流电场下,镀锌钢的阴极极化曲线也可以分为两个区域。相同液膜厚度下,未施加交流电场时,镀锌钢的极限电流密度比施加交流电场后的极限电流密度小,而且随着交流电场强度的增大,镀锌钢的极限电流密度增大。交流电场会影响氧气的扩散,随着外加交流电场强度的增大,氧气的扩散能力增强,使镀锌钢的腐蚀速率加快[15,21]。

(a) 本体溶液 (b) 350 μm

(c) 250 μm (d) 150 μm图8 不同厚度液膜体系中交流电场强度对镀锌钢开路电位的影响Fig. 8 Effect of AC electric field strength on open circuit potential of galvanized steel under liquid film with different thicknesses
(a) 0 kV/m (b) 20 kV/m

(c) 60 kV/m (d) 100 kV/m图9 不同厚度液膜体系中交流电场强度对镀锌钢阴极极化曲线的影响Fig. 9 Effect of AC electric field strength on cathodic polarization curves of galvanized steel under liquid film with different thicknesses
2.4 腐蚀形貌
图11为碳钢和镀锌钢在不同厚度液膜体系中腐蚀24 h后的腐蚀形貌。结果表明,在不同厚度液膜下腐蚀24 h后,碳钢表面均生成一层红棕色的腐蚀产物,腐蚀产物呈粉末状。在本体溶液中,碳钢的腐蚀产物只有一层疏松多孔的球状腐蚀产物,易脱落;而在厚度70 μm的液膜下,除了有疏松多孔的球状腐蚀产物外,碳钢表面还生成了不易脱落的腐蚀产物,这是因为在含Cl-水溶液中,疏松多孔的腐蚀产物γ-FeOOH会转变成较为致密的腐蚀产物β-Fe2O3并附着在碳钢表面。这也可能是电化学阻抗谱低频区出现感抗行为的原因。在本体溶液中腐蚀后,镀锌钢的腐蚀产物较为疏松,没有规则的形状,主要由锌和氧组成(能谱数据略);但是在厚度为50 μm的液膜下,其腐蚀产物具有规则形状,主要含有锌、氧和氯。在液膜下镀锌钢腐蚀产物中含有的氯可能来自于碱式氯化锌。因为在极薄的液膜下,随着时间的延长,镀锌钢表面沉积大量的腐蚀产物,粒子迁移受到阻碍,锌层溶解生成Zn2+,与Cl-结合生成碱式氯化锌。在本体溶液和液膜体系中浸泡后,镀锌钢的镀层均保持完整,基体未发生腐蚀。

图10 不同厚度液膜体系中交流电场强度对镀锌钢阴极极限电流密度的影响Fig. 10 Effect of AC electric field strength on cathodic limited current density of galvanized steel under liquid film with different thicknesses
图12是不同强度交流电场中镀锌钢在厚度150 μm液膜下浸泡12 h后的SEM形貌。结果表明,在浸泡12 h后,镀锌钢表面均发生明显的腐蚀。在无电场条件下,镀锌钢表面出现较为均匀的腐蚀产物膜;施加交流电场后,镀锌钢表面均出现更为严重的局部腐蚀,电场强度为100 kV/m时,镀锌钢表面除了分布有更加致密的腐蚀产物膜,还有很多裸露出基体的点蚀坑,这表明交流电场有显著加强镀锌钢腐蚀的作用。
3 结论
采用极化曲线,开路电位和电化学阻抗谱技术,辅以表面微观形貌观察,探究了碳钢和镀锌钢的大气腐蚀行为。结果表明,碳钢和镀锌钢表面液膜厚度降低均促进阴极还原电流增大,电化学腐蚀速率增大,交流电场的存在导致开路电位负移,促进氧还原,进一步加速腐蚀。因此在电网系统实际运行环境中,应加强对处于电场条件下金属材料腐蚀失效的监测与维护。

(a) 碳钢,本体溶液 (b) 碳钢,70 μm (c) 镀锌钢,本体溶液 (d) 镀锌钢,50 μm图11 碳钢和镀锌钢在不同厚度液膜体系中腐蚀24 h后的腐蚀形貌Fig. 11 Corrosion morphology of carbon steel and galvanized steel under liquid film with different thickness: (a) carbon steel, bulk solution; (b) carbon steel, 70 μm; (c) galvanized steel, bulk solution; (d) galvanized steel, 50 μm

(a) 0 kV/m (b) 20 kV/m (c) 60 kV/m (d) 100 kV/m图12 不同强度交流电场中镀锌钢在厚度150 μm液膜下浸泡12 h后的SEM形貌Fig. 12 SEM morphology of galvanized steel immersed in liquid film with a thickness of 150 μm for 12 hours and in AC electric field with different strengths
致谢:感谢上海电力大学张俊喜教授对电场加载大气腐蚀的设计与实验支持。
