药物临床试验质量控制相关因素的调查和分析
2021-12-07黄嘉利江丽华韩欣良
黄嘉利,关 灵,江丽华,韩欣良
(东莞市人民医院药物临床试验机构办公室,广东 东莞 523000)
药物临床试验是评估某一项药物临床效果及安全性的系统性研究[1],同时也是任意一项药物研发至使用的必经过程,其作用不可替代[2]。GCP(药物临床试验质量管理规范)是国家药品安全监督部门制订的关于临床药物试验的每一个环节,包括:设计、实施、监查、记录、总结等;本次研究将结合既有文献资料及工作经验对药物临床试验中的每一个环节的质量控制及影响因素作系统性评估。
1 资料与方法
1.1 基本资料
抽取我院药物临床试验机构近年来各个专业的药物临床试验质控检查结果,对知情同意书、方案偏离、病例报告填写、方案依从性、试验药物管理、不良事件处理等环节出现的问题进行汇总和分析,根据国家食品药品监督管理总局发布的药物临床试验数据现场核查要点分级分类方法,进行全面分析并结合当前我国的实际情况简述有效处理方案。
1.2 方法
专项GCP培训:(1)对研究者进行GCP培训,根据其他同行研究提示,研究者对《药物临床试验质量管理规范》及相关法律法规掌握不充分导致方案和SOP依从性不高的主要原因,我院通过多种可行方案对各专业科室骨干研究者进行GCP培训;(2)发生方案偏离时,方案修改后,组织研究者进行方案培训以及SOP培训,增加研究者的方案依从性,减少方案偏离等问题的发生率;(3)研究者对不良事件的定义了解不全面,容易导致研究者对不良事件处理不当或出现漏报不良事件的问题发生。加强对研究者进行不良事件处理和不良事件记录的培训,培训内容包括:不良事件的定义、不良事件与药物相关性的判断、不良事件的严重程度以及发生严重不良事件的处理及上报等;(4)研究者日常临床工作比较繁重,如果科室承接项目数较多,可能会出现较多的临床试验质量问题,为了减轻研究者的工作负担,提高临床试验质量,我院很多临床试验项目已经引入了CRC,协助研究者完成各项试验相关工作,但由于部分CRC缺乏经验,对受试者管理、GCP法律法规以及临床试验方案不熟悉,容易造成误导受试者和研究者、造成受试者依从性差以及方案偏离等临床试验质量问题。加强CRC培训,减少方案偏离、受试者依从性差等临床试验问题的发生。(5)加强样本管理培训,对需要进行样本管理的临床试验,应提前对样本管理员进行培训,包括试验方案、实验室手册、药物临床试验相关法律法规的培训。
1.3 统计学方法
SPSS 19.0软件收录数据,计数资料以率(%)表示,采用χ2检验,P<0.05为差异有统计学意义。
2 结果
2.1 实施专项GCP培训前药物临床试验质量问题率
统计显示:我院实施GCP培训前抽查质控报告15份,质控例数共456例次,发现质量问题共计112例次,比例24.56%。
2.2 影响药物临床试验质量的关键环节
资料统计显示:在实施专项GCP培训前112例次药物临床试验各类问题的分布情况,详见表1。
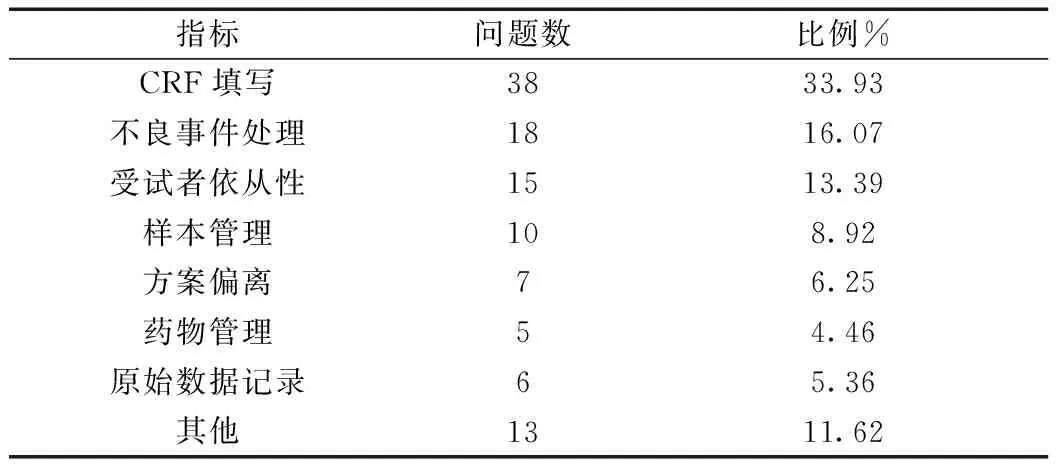
表1 实施专项GCP培训前药物临床试验各类问题分布情况
2.3 实施专项GCP培训后的效果
统计显示:我院实施专项GCP培训后抽查质控报告8份,质控例数113例次,发现质量问题共计12例次,比例10.62%,药物临床试验各类问题的分布情况,详见表2。与实施GCP专项培训前比较有明显的统计学意义(χ2=6.7027,P=0.0096)。

表2 实施专项GCP培训后药物临床试验各类问题分布情况
3.讨论
随着我国医疗卫生事业的蓬勃发展,当前我国范围内的制药企业超过6000家,临床试验专业超过2000个,在医药全球化发展的大背景下,我国药品的临床研发取得了显著的进步[3-4]。但另一方面,我国药品临床研发的发展时间相对较短,人才培养机制相对落后,我国当前在全世界药物临床药品研发的份额不足10%,其中一些关键性问题亟待解决[5-6]。临床药物研发及上市环节对药物效果及安全性的评估便是其中的重点之一,比如:针对某项尚未攻克的疾病提供一种新的治疗方案或药物,为提升受试者生活质量等。
本次研究结果显示:病例报告表填写、受试者依从性、不良事件处理、方案偏离以及样本管理五个环节占总问题的比例为78.56%,通常情况下一个具备丰富临床工作经验的诊断与一般试验研究员的诊断并无明显的高低之分;研究者职称的高低与受试者的信任之间存在正比例关系,即在面对高职称的研究者时,受试者的主观意向更为积极其依从性也明显更好,这也从侧面提示研究者在详细掌握GCP的情况下更重视对规范的使用和实践。从总体来说,一个优秀的研究者应是在熟悉理解GCP理论的情况下,熟悉试验方案并按照要求严格按照试验方案执行,在安全有效推动药物临床试验进度的同时最大程度的保证受试者的基本权益。因此,对临床试验研究团队各个角色进行GCP专项培训和考核,具有不可替代的意义和价值。另一方面,结合过往工作经验来看,包括受试者知情同意、入选筛查、药物管理、样本管理、受试者管理等环节由于形成了完善的管理方案,即便出现问题大多也不突出,但依旧可能会引起较为严重的临床试验质量问题,影响试验的理论性和科学性,这也是不容忽视的一个问题。
