高效液相色谱-高分辨质谱法鉴定拉萨大黄化学成分
2021-12-06孙玉明李文慧王玉林
孙玉明,徐 蒙,李文慧,王 静,张 华,王玉林
(1.大连理工大学分析测试中心,辽宁 大连 116024;2.大连理工大学化工学院, 辽宁 大连 116024;3.大连医科大学药学院,辽宁 大连 116044)
大黄是中药发展中最古老、使用频率最高、最重要的草药之一。该药材不仅可以食用,还具有重要的经济价值[1]。在全球范围内,大黄属植物共有60多种,我国有41种和4个变种,不同产地、品种、采收时节的不同,会造成大黄化学成分的不同,功效也有所差异[2]。我国2020版药典中收录的大黄为蓼科植物掌叶大黄(RheumpalmatumL)、唐古特大黄(RheumtanguticumMaxim.exBalf)、药用大黄(RheumofficinaleBaill)的干燥根和根茎。本研究的拉萨大黄(RheumlhasaenseA.J.LietP.K.Haiao)为蓼科大黄属多年生高大草本植物,是藏族民间常用草药,名曲札。拉萨大黄的干燥根不仅具有治疗便秘、腹胀腹痛、消肿愈创、清热解毒、破积滞、行淤血等功效[3],还可以通过改善微循环和冠状动脉流量、降低血压、抑制血小板聚集和消除自由基来治疗高血脂症及心脑血管疾病[4]。近期,Hu等[5]研究发现,拉萨大黄可以降低血液中冠状病毒,进而治疗病毒性肺炎。
拉萨大黄与一般大黄的化学成分有所不同,Liu等[6]研究发现其化学成分中含有2种白藜芦醇三聚体rheumlhasol A和rheumlhasol B,4种白藜芦醇二聚体,而不含蒽醌类化合物。龚云麟等[7]采用UV、MS、1H NMR、13C NMR以及薄层色谱法分离并鉴定拉萨大黄乙醇提取物中的去氧土大黄苷、曲札茋苷、虎杖苷、白藜芦醇、白皮杉醇和土大黄苷元-3′-O-β-D-葡萄糖苷等6种成分,其中茋类成分居多。目前,关于拉萨大黄化学成分分析的文献报道较少[6-7],一般多采用分离、纯化、鉴定的方法,且仅检测到12种化合物,无法有效完成拉萨大黄的药材质量控制及药效物质基础研究。高效液相色谱-高分辨质谱(HPLC-HRMS)具有高分离效率、高选择性及高灵敏度的检测优势,可以解决中药成分复杂性、多样性和微量性带来的分析困难,在中药材化学成分分析领域得到了广泛应用[8-11]。
本研究拟采用HPLC-HRMS法分析拉萨大黄提取物的化学成分,通过综合分析各化合物的色谱和质谱行为,为拉萨大黄的质量评价及药效物质基础研究提供科学依据。
1 实验部分
1.1 仪器与装置
LTQ-Orbitrap XL高效液相色谱-高分辨质谱联用仪:美国赛默飞世尔科技有限公司产品,配有Thermo Xcalibur 2.1数据处理系统、Accela液相色谱系统、Accela 1250四元梯度泵及Accela AS自动进样器;DF-101S集热式恒温加热磁力搅拌器、RE-52C旋转蒸发仪:巩义市予华仪器有限责任公司产品;BS124S万分之一天平:德国赛多利斯科学仪器有限公司产品;KQ-200DB数控超声波清洗器:昆山市超声仪器有限公司产品;Milli-Q超纯水机:美国Merck Millipore公司产品;CS-700中药材粉碎机:五亿海纳电器有限公司产品;GL-88B旋涡混合器:海门市其林贝尔仪器制造有限公司产品。
1.2 试剂与材料
拉萨大黄:来源于香格里拉高山植物园,由大连医科大学第一附属医院中药剂科主任中药师李永杰鉴定并确认。
无水乙醇:天津市科密欧化学试剂有限公司产品;乙酸(色谱纯):迪马科技有限公司产品;甲醇、乙腈(色谱纯):赛默飞世尔科技有限公司产品;超纯水:实验室自制。
去氧土大黄苷(HPLC≥98%,LOT:P13S9F70275)、曲扎茋苷(HPLC≥98%,LOT:P14D7F26825)、白皮杉醇(HPLC≥98%,LOT:Y15A8C33972):上海源叶生物科技有限公司产品;儿茶素(HPLC≥98%,LOT:C11263757)、表儿茶素(HPLC≥98%,LOT:C10376713)、虎杖苷(HPLC≥95%,LOT:C10083549)、丹叶大黄素(HPLC≥98%,LOT:C11251823)、没食子酸(HPLC=99%,LOT:C11062421)、4-香豆酸(HPLC=98%,LOT:C11334633):上海麦克林生化科技有限公司产品。
1.3 实验部分
1.3.1拉萨大黄的提取 取10 g粉碎的拉萨大黄干燥根粉末,加入90%乙醇,加热回流2次,每次2 h,真空抽滤,合并2次所得滤液,65 ℃减压浓缩至浸膏状。在拉萨大黄的提取和样品制备过程中均须避光操作以防止样品降解。
1.3.2样品制备 称取适量的拉萨大黄浸膏,加入无水乙醇,经超声溶解配制成400 g/L溶液;取适量的上述溶液,加入甲醇稀释,配制成20 g/L溶液,经0.22 μm微孔滤膜过滤,进样量2 μL。
取适量的对照品,加入甲醇溶解稀释,配制成约20 mg/L溶液,进样量2 μL。
1.3.3实验条件 色谱条件:Agilent Zorbax SB-C18色谱柱(150 mm×4.6 mm×5 μm),柱温为室温;流动相A为乙腈,B为水;梯度洗脱程序为0~5 min(10%~30%A),5~10 min(30%~70%A),10~12 min(70%~100%A),12~15 min(100%A),15~15.1 min(100%~10%A),15.1~20 min(10%A);流速0.5 mL/min;进样量2.0 μL。
质谱条件:电喷雾离子源(ESI),正、负离子模式;源喷雾电压分别为3.5 kV(正离子模式)和3.0 kV(负离子模式);鞘气和辅助气均为氮气,流速分别为15、5 L/min;加热毛细管温度350 ℃,毛细管电压35 V;分辨率30 000,最大允许偏差±5×10-6;一级和多级全扫描方式。
2 结果与讨论
2.1 检测条件的选择
本实验采用HPLC-HRMS法在正、负离子模式下分析鉴定拉萨大黄的化学成分。结果表明,负离子模式下检测到的化合物种类较多,且质谱响应强度相对较大,这与化合物结构中均含有酚羟基或羧基等酸性基团有关。为提高化合物的分离度,分别以纯水和0.3%乙酸水溶液作为流动相中的水相进行梯度洗脱,在水相中添加酸性改性剂后,部分化合物的峰形和分离度得到了一定程度的改善,但由于酸性改性剂在负离子模式下的离子抑制作用,导致18种化合物(化合物2,3,4,8,18,22,23,28,31,33,36,45,46,48,49,56,57,58)无法被检测,示于图1。因此,采用以纯水为流动相中的水相进行梯度洗脱。
2.2 化学成分分析
本实验采用HPLC-HRMS法分离鉴定拉萨大黄提取物的化学成分,分别对样品进行(+)-ESI-MSn和(-)-ESI-MSn检测。通过综合分析各化合物的保留时间、精确分子质量和多级质谱信息,并与文献[10-19]数据或对照品对比,共检测出鞣质类、茋类、黄酮类、苯丙酸类、苯丁酮类等63种化合物,各化合物的相关数据列于表1。
2.2.1鞣质类 鞣质又称单宁,是一类水溶性多元酚类化合物,其在大黄中分为水解鞣质和缩合鞣质两类,这两类鞣质的单体分别为没食子酸和d-儿茶素[20],也有报道将这两种类型鞣质的结合体称为复合鞣质[21]。本研究在拉萨大黄中检测到22种鞣质类化合物,其中10种水解鞣质,分别为化合物1、2、3、5、6、9、10、11、13、18;7种缩合鞣质,分别为化合物12、16、17、21、26、29、41;5种复合鞣质,分别为化合物24、30、34、40、43。下面以化合物12、16、21、29为例进行分析。
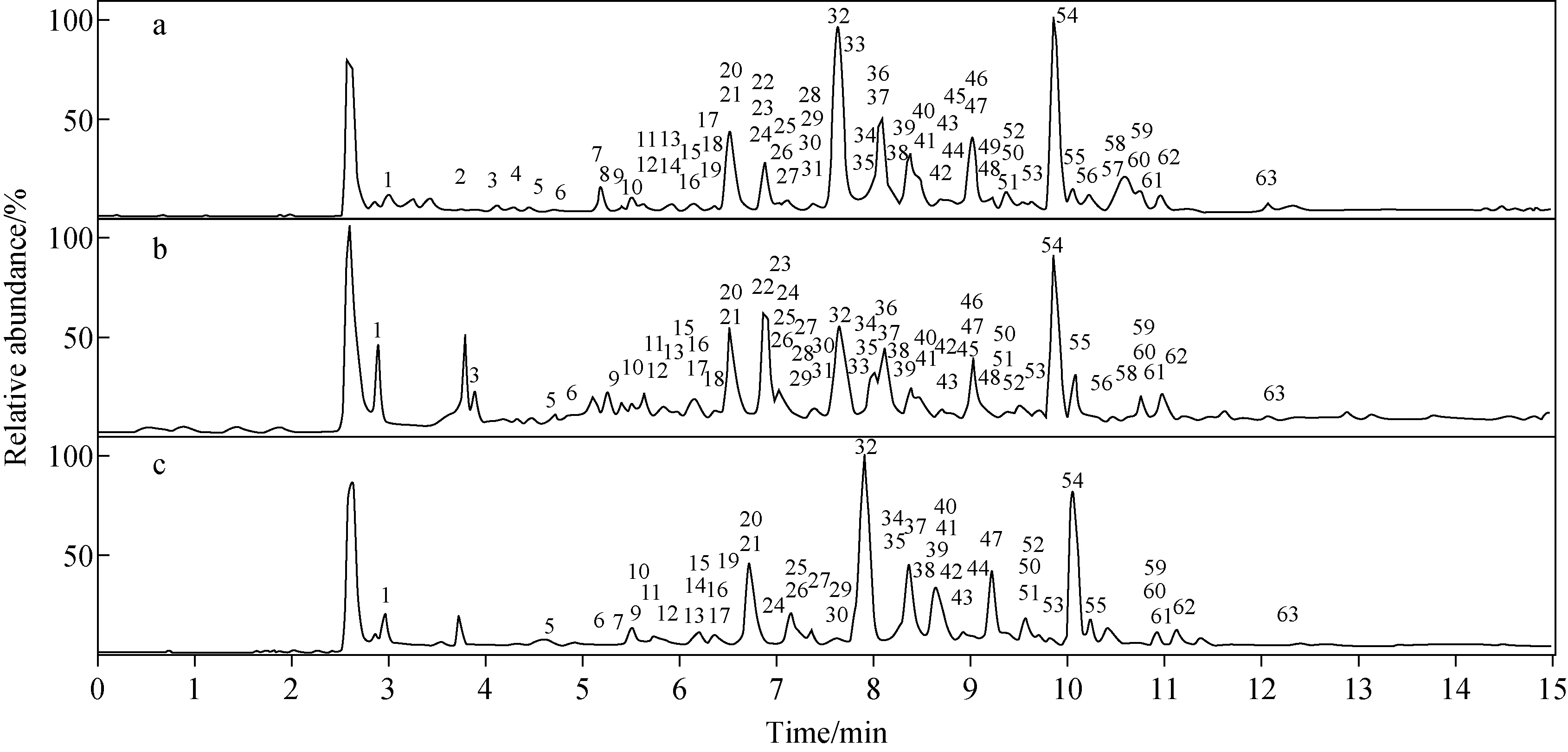
注:a.负离子模式下,以乙腈-水为流动相;b.正离子模式下,以乙腈-水为流动相;c.负离子模式下,以乙腈-0.3%乙酸水为流动相图1 拉萨大黄提取物的典型色谱图Fig.1 Typical chromatograms of Rheum lhasaense A. J. Li et P. K. Hsiao extract
化合物12(tR=5.65 min)、16(tR=6.17 min)、21(tR=6.60 min)和29(tR=7.38 min)在ESI-模式下产生的准分子离子峰[M-H]-为m/z577.135 1。根据高分辨数据拟合其元素组成均为C30H26O12,在ESI+模式下同样有质谱响应,数据列于表1,初步推断为(表)儿茶素二聚体结构。为进一步确定结构,对m/z577进行二级全扫描质谱分析,产生的主要碎片离子有m/z559、451、425、407、289,与文献[15]报道一致。其中,m/z559相比于m/z577减少了18 u,推断为该化合物脱掉1分子H2O形成的[M-H-H2O]-碎片离子;m/z451与m/z559相比减少了108 u,推测为C—C键断裂进一步脱去1分子邻苯二酚形成的[M-H-H2O-C6H4O2]-碎片离子;m/z425与母离子相比减少了125 u,推断为母离子发生逆Dials-Alder开环反应脱掉1分子C8H8O3形成的[M-H-C8H8O3]-碎片离子;m/z407与m/z425相比减少了18 u,为进一步脱去1分子H2O形成的[M-H-C8H8O3-H2O]-碎片离子;m/z289比母离子减少288 u,推断为C—C键断裂脱去1分子儿茶素形成[M-H-C15H12O6]-碎片离子,其质谱图及可能的裂解途径分别示于图2、图3。结合裂解碎片信息,并对比相关文献[15],确定化合物12、16、21和29为(表)儿茶素二聚体,因其结构中含有多个手性碳原子,所以可形成多个非对映异构体。研究发现,缩合鞣质类化合物的裂解规律为易在脱水后母核儿茶素分子上C—C键断裂脱去1分子邻苯二酚形成[M-H-H2O-C6H4O2]-碎片离子,母离子发生逆Dials-Alder开环反应脱掉1分子C8H8O3形成[M-H-C8H8O3]-碎片离子,且易脱去儿茶素单体形成[M-H-C15H12O6]-碎片离子。水解鞣质易脱去葡萄糖分子形成[M-H-C6H10O5]-碎片离子,而得到的母核离子易脱去1分子CO2,葡萄糖分子上易脱去1分子C2H4O2。其他鞣质类化合物也有相似的裂解规律。
2.2.2茋类 茋类化合物是对具有二苯乙烯母核一类化合物的总称,主要存在于植物的木质部薄壁细胞中[22],是大黄的主要成分。茋类化合物中苷类化合物易水解得到苷元,其苷元上的苯环易发生裂解脱去乙炔和乙炔醇。本研究共检测到28种茋类化合物,以化合物27和32为例进行分析。



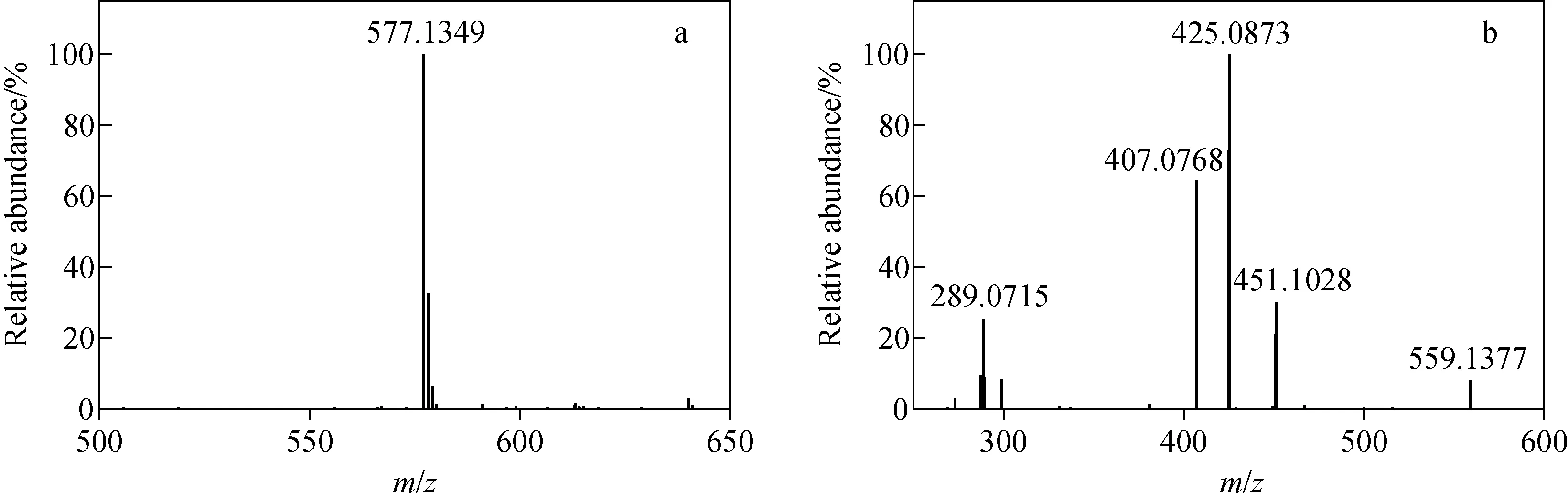
注:a.一级质谱图;b.二级质谱图图2 化合物12的质谱图Fig.2 Mass spectra of compound 12
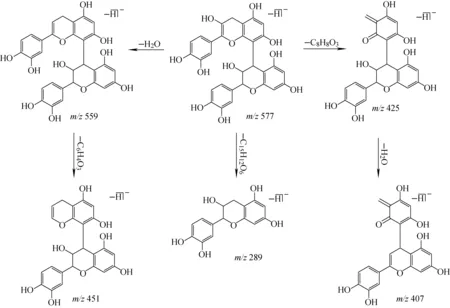
图3 化合物12可能的质谱裂解途径Fig.3 Proposed fragmentation pathways of compound 12
化合物27(tR=7.14 min)和化合物32(tR=7.65 min)在ESI-模式下产生准分子离子峰[M-H]-m/z405.119 0,根据高分辨数据拟合其元素组成均为C20H22O9,m/z441为加合离子[M-H+HCl]-,初步推断为白皮杉醇葡萄糖苷。为进一步确定结构,对m/z405进行二级全扫描质谱分析,产生的主要碎片离子为m/z243,推测为糖苷键断裂脱去1分子葡萄糖形成的[M-H-C6H10O5]-碎片离子。为进一步确定苷元结构,对m/z243进行三级质谱分析,其主要碎片离子为m/z243、225、201、175、159。其中,m/z225为m/z243脱去1分子水形成的[M-H-H2O]-碎片离子,m/z201为m/z243脱去1分子乙炔醇得到的[M-H-C2H2O]-碎片离子,m/z175是由m/z243脱去1分子乙炔醇和1分子乙炔得到的[M-H-C2H2O-C2H2]-碎片离子,m/z159是由m/z243脱去2分子乙炔醇得到的[M-H-2C2H2O]-碎片离子。通过与对照品比对,发现化合物32与对照品曲扎茋苷的色谱和质谱行为一致,确定化合物32为曲札茋苷,而化合物27为白皮杉醇葡萄糖苷。化合物32的质谱图及可能的裂解途径分别示于图4、图5。其他茋类化合物也有相似的裂解规律。

注:a.一级质谱图;b.二级质谱图;c.三级质谱图图4 化合物32的质谱图Fig.4 Mass spectra of compound 32
2.2.3苯丁酮类 苯丁酮类化合物是大黄的活性成分之一。苯丁酮衍生物的苯环4位上易被葡萄糖苷化,葡萄糖的2、6位羟基易与没食子酸或苯丙酸衍生物缩合形成酯。本研究共检测到2种苯丁酮类化合物,下面对其进行结构鉴定分析。
化合物23(tR=6.94 min)和化合物35(tR=8.01 min)在ESI-模式下产生准分子离子峰[M-H]-m/z477.140 4,根据高分辨数据推测其元素组成均为C23H26O11。这2种化合物在ESI+模式下同样有质谱响应,数据列于表1,推测其可能为莲花掌苷或异莲花掌苷。为进一步确定结构,对m/z477进行二级全扫描质谱分析,产生的主要碎片离子有m/z433、313、169,与文献[11,13-14]报道一致。m/z433相比于m/z477减少44 u,推断为苯丁酮所在部分C—C键断裂脱掉1分子CH3CHO形成的[M-H-C2H4O]-碎片离子;m/z313比m/z477减少164 u,推测为糖苷键断裂脱去1分子苯丁酮得到的[M-H-C10H12O2]-碎片离子;m/z169与没食子酸的准分子离子相同,推测为C—O键断裂脱去苯丁酮葡萄糖苷部分形成的[M-H-C16H20O6]-碎片离子,其质谱图及可能的裂解途径分别示于图6、图7。根据相关文献[11]报道,在反相色谱系统中异莲花掌苷的保留时间相对较短,结合裂解碎片信息,推测化合物23为异莲花掌苷,化合物35为莲花掌苷。

图5 化合物32可能的质谱裂解途径Fig.5 Proposed fragmentation pathways of compound 32
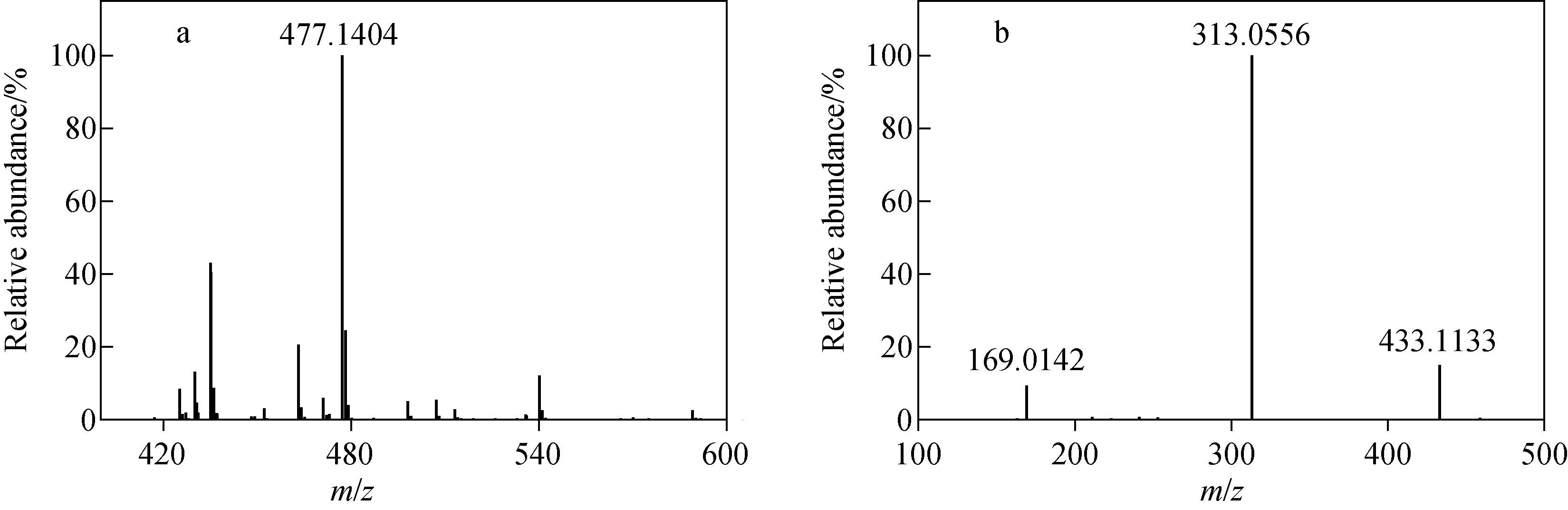
注:a.一级质谱图;b.二级质谱图图6 化合物35的质谱图Fig.6 Mass spectra of compound 35
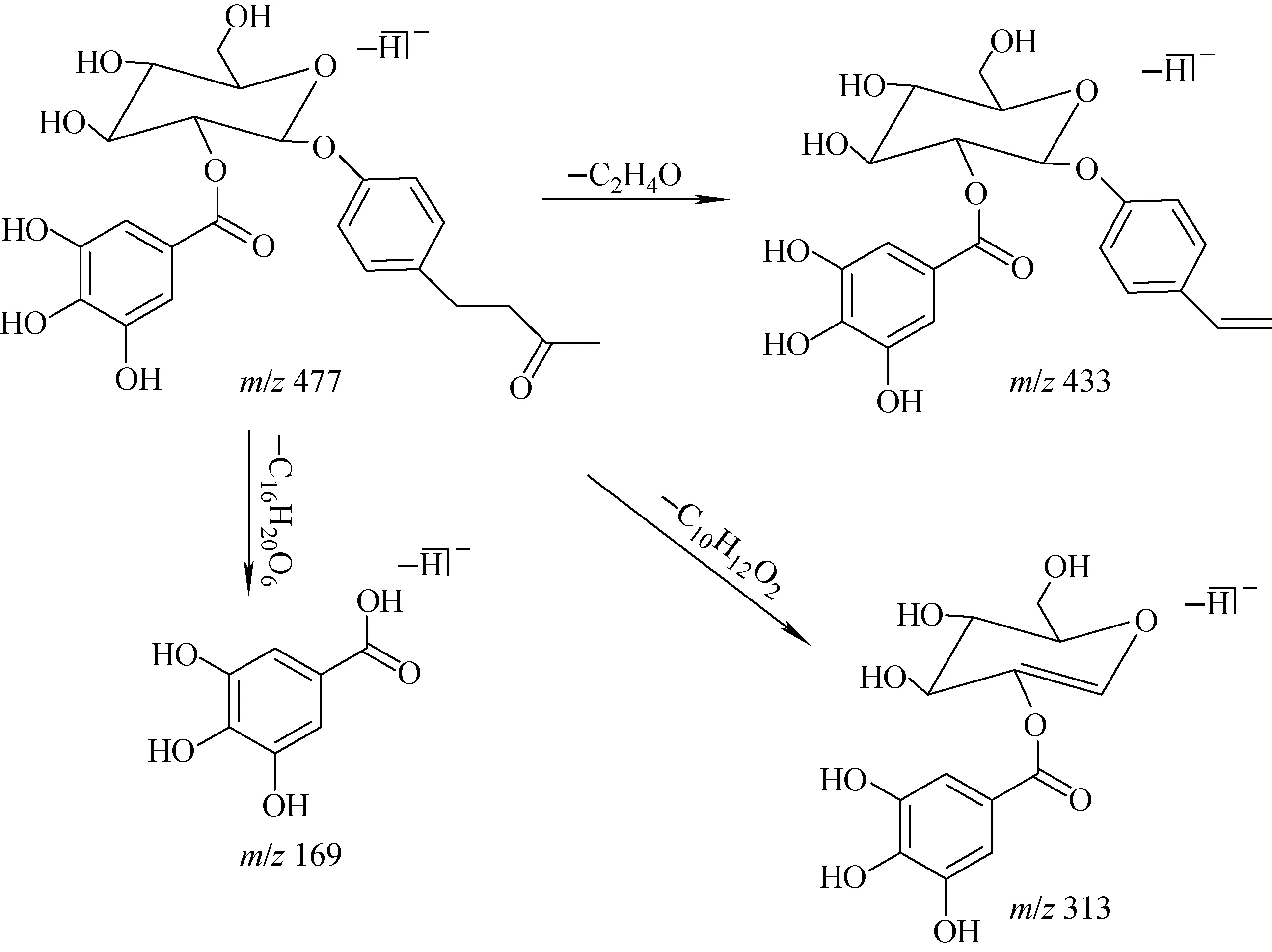
图7 化合物35可能的质谱裂解途径Fig.7 Proposed fragmentation pathways of compound 35
2.2.4黄酮类 黄酮类化合物是一类以2-苯基色原酮为母核的化合物,因其结构不同,种类繁多,具有多种药理作用。黄酮类化合物典型的裂解方式是逆Dials-Alder裂解,本研究共检测到6种黄酮类化合物,以化合物58为例进行结构鉴定分析。
化合物58(tR=10.57 min)在ESI-模式下产生准分子离子峰[M-H]-m/z287.056 1,该化合物在ESI+模式下同样有质谱响应,根据高分辨数据拟合其元素组成为C15H12O6,初步推断为圣草酚。为进一步确定结构,对m/z287.056 1进行二级全扫描质谱分析,产生的主要碎片离子有m/z269、151,与文献[16]报道一致。其中,m/z269与m/z287相比减少了18 u,推测为脱掉1分子H2O形成的[M-H-H2O]-碎片离子;m/z151比m/z287减少136 u,推测是黄酮类化合物典型的逆Dials-Alder裂解途径,脱掉1分子C8H8O2形成的[M-H-C8H8O2]-碎片离子。综合考虑元素组成及碎片信息,推断化合物58为圣草酚,其质谱图及可能的裂解途径示于图8、图9。
本研究在负离子模式下检测到63种化合物,正离子模式下检测到54种化合物,其中包括22种鞣质类化合物,28种茋类化合物,3种苯丙酸类化合物,6种黄酮类化合物,2种苯丁酮类化合物及2种有机酸类化合物。除化合物32、37、50、53、54、56、59、60、61、62外,其余均为首次在拉萨大黄提取物中发现,对拉萨大黄的成分进行了较全面的分析和补充。拉萨大黄中的主要有效成分为茋类化合物,且Hu等[5]发现,纯化的曲扎茋苷、虎杖苷等组合物和拉萨大黄的总提取物都具有抑制冠状病毒活性的作用,但拉萨大黄总提取物的效果比组合物的预防效果好。
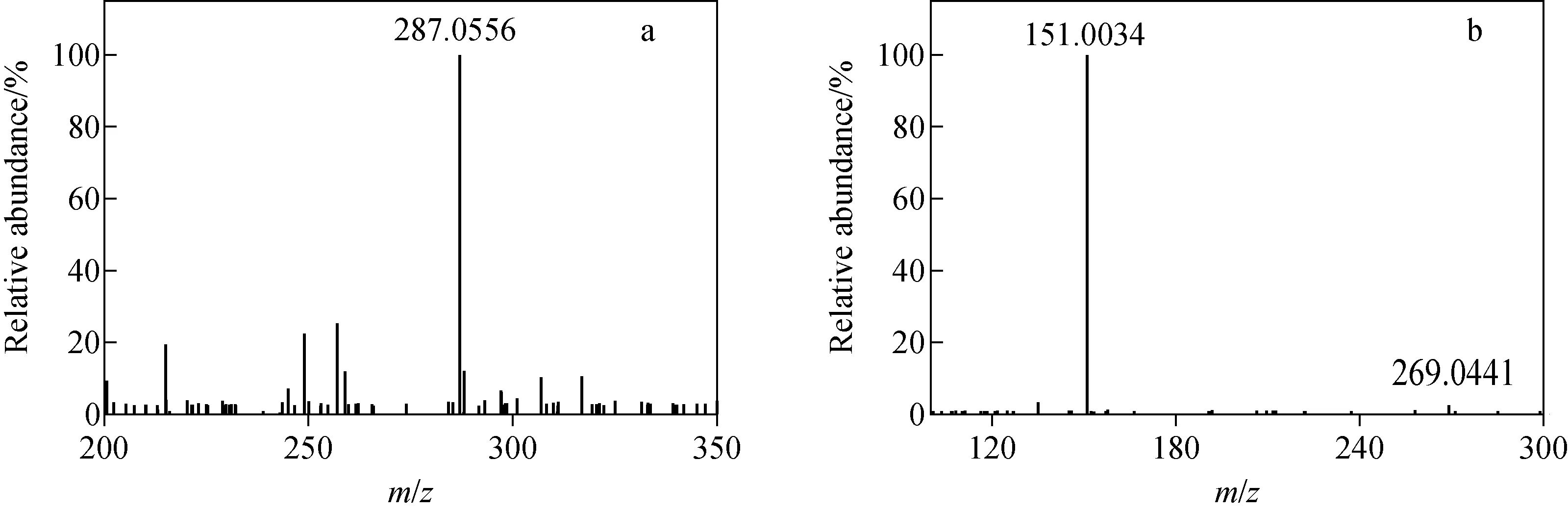
注:a.一级质谱图;b.二级质谱图图8 化合物58的质谱图Fig.8 Mass spectra of compound 58

图9 化合物58可能的质谱裂解途径Fig.9 Proposed fragmentation pathways of the compound 58
3 结论
本文建立了HPLC-HRMS法分析鉴定拉萨大黄提取物的主要化学成分,共鉴定出63种化合物,其中有53种化合物是在该药材中首次发现,但未发现蒽醌类成分。本研究为拉萨大黄药材的鉴定及质量控制提供了有效方法,也为其在临床应用及药理研究奠定了基础。
致谢:感谢大连医科大学第一附属医院中药剂科主任中药师李永杰对中药材拉萨大黄的鉴定。
