植物油脂凝胶的氧化稳定性及货架期预测
2021-12-04刘龙龙王家镔陈治同
刘龙龙 - 王家镔 - 陈治同 -
赵月莹1ZHAO Yue-ying1 张 华1,2ZHANG Hua1,2 崔明勋1,2CUI Ming-xun1,2
脂类是日常生活所必需的营养物质之一,其中固体脂肪在食品加工中具有赋予产品特殊的口感,延长保质期等特点[1]。以牛油、猪油等动物油为基底的固体脂肪具有理想的塑性范围,但由于动物油的脂肪酸组成的缺陷,容易出现返砂晶体,破坏产品的稳定性和延展性[2-3]。目前大部分应用于食品中的固体脂肪由植物油通过加氢催化制成,氢化使得油脂的饱和度降低,从而使油脂硬化,但氢化不彻底会产生大量的反式脂肪酸(TFAs)[4]。摄入过量反式脂肪酸会增加患心血管疾病、肥胖、炎症、内质网应激等疾病的风险[5]。
近年来,出于对健康和营养的需求,人们迫切寻找一种TFAs含量低且稳定性高的固体脂肪应用于食品加工中。油脂凝胶是一种由具有三维结构的凝胶剂和液态植物油组成的固体脂质体系[3],其制备条件温和且不会生成TFAs。天然植物油多含丰富的多不饱和脂肪酸,而多不饱和脂肪酸具有治疗心血管疾病、抗炎、抗癌、抗衰老和改善老年痴呆等功能[6-9],可作为制备油脂凝胶的基油。但植物油贮藏过程中易发生氧化酸败。目前,用于延缓油脂氧化酸败的方法一般为添加天然或合成抗氧化剂,天然抗氧化剂可能带入抗氧化剂本身的气味,影响油脂的口感;而合成抗氧化剂的安全性一直颇受质疑[10]。而且添加抗氧化剂无法改变液态油的塑性。罗晶等[11]研究发现,12-羟基硬脂酸有机凝胶剂制备的大豆油凝胶不但具有稳定的结构,而且能够有效减缓油脂氧化;Han等[12]研究表明卵磷脂和谷甾醇联合可成功制备植物油凝胶,且其具有良好的稳定性。不仅如此,Pan等[13]的研究表明单月桂酸甘油酯制备的山茶油凝胶过氧化值(POV)和硫代巴比妥酸值(TBA)较低,氧化稳定性较高。因此,油脂凝胶可作为固体脂肪的有效替代品,且能够提高油脂本身的稳定性。油脂凝胶最大的难题在于寻找新型的可食用凝胶剂,谷甾醇和卵磷脂不仅价格低廉、可食用,而且磷脂的加入解决了单一小分子无法形成凝胶、溶解度低的问题,能够形成稳定的油脂凝胶[14]。
目前,对于谷甾醇与卵磷脂作为凝胶剂制备油脂凝胶的结构稳定性和能否延长货架期的研究较少,因此研究拟以大豆油(SBO)、菜籽油(RSO)为基油,选用谷甾醇/卵磷脂为凝胶剂来制备大豆油凝胶(SBG)和菜籽油凝胶(RSG),与牛油(BT)、SBO和RSO作对比,通过计算POV值和TBA值对所制备的2种油脂凝胶在贮藏过程中的氧化稳定性进行研究,通过气相色谱(GC)和X射线衍射(XRD)监测贮藏过程中脂肪酸和晶型结构的变化来研究其氧化机制及结构稳定性;并采用OXITEST方法对油脂凝胶货架期进行预测,以期提高植物油的货架期,为油脂凝胶的贮藏和加工提供理论依据。
1 材料与方法
1.1 材料与试剂
菜籽油(低芥酸、三级油)、大豆油(三级油)、牛油:市售;
谷甾醇(>75%)、卵磷脂(>90%)、正丁醇、正已烷:色谱纯,阿拉丁试剂(上海)有限公司;
三氯甲烷、冰乙酸、硫代硫酸钠、淀粉、2’-硫代巴比妥酸、氘代氯仿、氢氧化钠、甲醇、三氟化硼:分析纯,国药集团化学试剂有限公司。
1.2 仪器与设备
电子分析天平:ME104型,梅特勒—托利多国际有限公司;
数显恒温水浴锅:HH-1246型,常州鸿泽实验科技有限公司;
紫外可见分光光度计:UV-1800型,上海美谱达仪器有限公司;
核磁共振仪:AV-600型,瑞士布鲁克公司;
X-射线衍射仪:D/Max 2200VPC型,日本理学电子公司;
气相—质谱仪:2010PLUS型,日本岛津公司;
油脂氧化分析仪:OXITEXT型,北京盈盛恒泰科技有限责任公司。
1.3 试验方法
1.3.1 样品的制备 根据文献[15]修改如下:称取20 mL样品油,添加油脂质量分数为12%的谷甾醇与卵磷脂形成的低分子量复合凝胶剂(m谷甾醇∶m卵磷脂为6∶4),100 ℃下磁力搅拌30 min,使凝胶剂充分溶解于油中,于4 ℃冰箱中贮藏24 h。称取100 g制备好的样品装在统一大小的敞口棕色瓶中,置于25 ℃的恒温培养箱中贮藏35 d,每隔5 d进行试验。
1.3.2 POV测定 按GB 5009.227—2016执行。
1.3.3 TBA测定 按GB/T 35252—2017执行。
1.3.4 脂肪酸测定
(1) 甲酯化:根据仇宏图等[16]的方法并修改,称取30 mg样品,加入1.5 mL 0.5 mol/L氢氧化钠甲醇溶液,摇匀,95 ℃以上反应3 min,冷却,再加入2 mL体积分数为14%的BF3甲醇溶液, 95 ℃下反应2 min,冷却,加入1 mL饱和氯化钠和2 mL正己烷,提取脂肪酸甲酯经过无水硫酸钠干燥后用于气相分析。
(2) GC条件:毛细色谱柱DM-5(30 m×250 μm,0.25 μm)。进样口温度220 ℃;分流比10∶1;隔垫吹扫3 mL/min。程序升温:初始温度60 ℃,保持3 min,以5 ℃/min的升温速率升至150 ℃,再以10 ℃/min上升至250 ℃,保持30 min。离子源温度200 ℃,连接器温度220 ℃,柱流量1 mL/min,总流量14 mL/min。
1.3.5 X-射线衍射(XRD)测定 根据Judde等[17]方法并修改,取适量的样品平铺在检测片上,仪器测试条件设定为:Cu-Kα放射源(λ=0.154 056 nm),工作电压为40 kV,工作电流为40 mA,2θ角扫描范围10.0°~30.0°,扫描步长为0.02°,扫描速率为2 ℃/min,发射和防反射狭缝1 mm,接受狭缝0.1 mm,测试温度为25 ℃。
1.3.6 氧化稳定性和货架期测定 采用OXITEST法对油脂及其凝胶(准确称取10 g)进行分析,纯氧压力0.6 MPa,90 ℃恒温,使用两个不同的反应室做重复试验。氧化稳定性通过诱导期(IP)值反映。对油脂及其凝胶在3种不同温度(70,80,90 ℃)下进行加速货架期试验。使用仪器自带的OXISoftTM程序,通过图解法自动计算氧化曲线的IP值及其货架期。
1.3.7 数据统计与分析 数据均以“平均值±标准误差”表示,平行试验至少3次,采用Excel 2016进行数据分析,采用Origin 2018进行绘图。
2 结果与分析
2.1 油脂及其凝胶的POV和TBA值变化
由图1可知,随着贮藏时间的延长,动植物油脂及其凝胶的过氧化值整体上呈上升趋势。RSO的过氧化值变化最大。至贮藏末时,RSO过氧化值达到4.315 mmol/kg,SBO为1.607 mmol/kg,RSG为3.130 mmol/kg,SBO为1.210 mmol/kg,BT为0.478 mmol/kg。这是因为菜籽油中不饱和脂肪酸含量高于大豆油的,较易发生氧化反应。而动物油与植物油相比,含有更高的饱和脂肪酸,因此有更好的氧化稳定性。油脂凝胶的POV值较原油低,可能是因为β-谷甾醇与卵磷脂发生过氧化自由基反应,并猝灭单一态的氧分子和对卵磷脂双分子层进行排序而发挥其抗氧化作用,同时,β-谷甾醇分子中的羟基和卵磷脂分子中的脂肪酸酯的羰基间可形成氢键,使得油脂过氧化被抑制[18]。贮藏过程中5种样品的TBA值变化趋势基本与POV值一致,其值大小顺序为RSO>SBO>RSG>SBG>BT(见图2)。0~20 d,TBA值无明显变化,主要是因为前20 d产生的初级氧化产物(主要为氢过氧化物)少,未能产生大量次级氧化产物。脂肪氧化链反应的传递是一种自由基反应,若这一传递过程受到阻碍则会导致次级氧化产物生成降低。油脂及其凝胶TBA值比较结果表明油脂凝胶形成的稳定网络结构能够对脂质自由基的传递起到一定的“阻碍”效果,即其能有效抑制次级氧化产物的产生[19]。

图1 贮藏过程中油脂及其凝胶的过氧化值Figure 1 POV of oils and their oleogels during storage
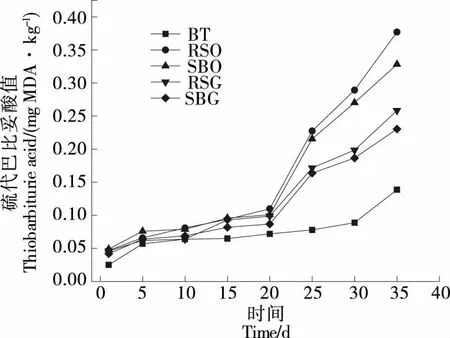
图2 贮藏过程中油脂及其凝胶的TBA值Figure 2 TBA value of oils and their oleogelsduring storage
2.2 脂肪酸组分和含量变化
由表1可知,RSO和SBO制备成RSG和SBG后脂肪酸组成无明显差异,这一结果表明油脂凝胶的制备并不会对油脂的脂肪酸造成破坏。另外,随着氧化时间的延长,SBO和RSO中主要的不饱和脂肪酸C18:1,C18:2,C18:3的含量比RSG和SBG中的下降幅度更大,这是因为油脂凝胶比油脂更加稳定。BT中C18:3含量远低于SBO和RSO中的,表明脂肪酸组成的不同与BT有更高的氧化稳定性有极大的关系,诸多学者[20-22]研究表明C18:1,C18:2,C18:3同时存在时,C18:2和C18:3首先开始氧化,且C18:2和C18:3含量越高,氧化速度越快,这与试验结果完全一致。在贮藏过程中BT的各种脂肪酸相对含量变化较小,表明它具有很强的脂肪酸保护机制,这可能与它独特的甘油三酯组成和脂肪酸排列有关。
由图3可知,两个主成分的总变异为99.1%,其中PC1为64.1%,PC2为35.0%,两个主成分基本代表了样品的主要特征信息。单从脂肪酸含量并不能够有效地区分油脂凝胶和原油,表明油脂凝胶的制作不会对脂肪酸造成破坏。
2.3 XRD分析
如图4所示,液体油RSO和SBO无晶体结构,而在油脂凝胶系统中,RSG和SBG衍射峰极为相似,说明油脂类型对凝胶的结构并无很大影响,与李丹等[23]研究结果一致。在第0~30天时,RSG与SBG中主要的晶型的短间距值均集中在0.590,0.460,0.420,0.386 nm附近;而BT的短间距值主要集中在0.420,0.386 nm附近,表明凝胶和动物油之间存在的晶型并不完全一致,这也是BT的氧化稳定性不同于SBG和RSG的原因之一。经典油脂学认为0.460 nm附近的短间距值为β晶型的特征衍射峰,而0.380~0.420 nm的为β′晶型,在凝胶体系中出现的衍射信号可认为是β和β′晶型的衍射峰,具有这种两种晶型的凝胶口感好,熔点较高,稳定性也好[24]。放置30 d RSG和SBG晶型结构并未发生改变,说明凝胶在氧化过程中仍然能够保持结构的稳定。
2.4 氧化稳定性及其货架期
90 ℃下,油脂及其凝胶的IP值大小依次为RSG>SBG>RSO>BT>SBO(图5)。这一结果表明凝胶比油脂具有更好的氧化稳定性。此外,利用OXITEST法在高温高压(70,80,90 ℃;0.6 MPa)条件下对油脂货架期进行预测,其结果如表2所示,RSG与SBG相比,SBG具有更长的货架期,这不仅与它们的脂肪酸组成有关,也可能与大豆油中的某些成分(各类磷脂等)溶出与凝胶剂结合,形成更加稳定的三维网络结构有关。

图3 油脂及其凝胶的PCA图Figure 3 PCA of oils and their gels
3 结论
通过加速氧化试验,研究了油脂凝胶在贮藏过程中过氧化值和硫代巴比妥酸值的变化。结果表明:油脂凝胶能够抑制初、次级产物的生成,且在短期的贮藏过程中菜籽油凝胶和大豆油凝胶的晶型结构稳定。另外,凝胶结构能够抑制菜籽油凝胶和大豆油凝胶中的C18:2和C18:3等不饱和脂肪酸的氧化,达到延长货架期的目的。油脂凝胶能够直接改变油脂的物理性状,有效提高油脂的货架期,相比于菜籽油,大豆油有更好的氧化稳定性、外观及货架期,因此,更适合制备油脂凝胶。油脂凝胶的制备对植物油的进一步开发利用有着重要的意义,是一种控制油脂氧化的有效策略。

图4 油脂及其凝胶在贮藏过程中的XRD图Figure 4 XRD patterns of oils and their oleogels during storage

图5 90 ℃下油脂及凝胶的IP值Figure 5 IP value of oils and theiroleogels at 90 ℃

表2 OXITEST测定货架期结果†Table 2 Results of accelerated shelf-life test conducted with OXITEST
