基于氨基功能化离子液体萃取番茄中超氧化物歧化酶
2021-12-02李梦瑶王书雅谢云峰
王 涛,翟 晨,王 亮,*,李梦瑶,,王书雅,谢云峰
(1.新疆大学生命科学与技术学院,新疆 乌鲁木齐 830017;2.中粮营养健康研究院,营养健康与食品安全北京市重点实验室,北京 102209)
我国是农业大国,每年的果蔬产量都远超其他国家,而番茄正是我国众多果蔬品种中产量较高的一种,其富含大量的番茄红素、VC以及超氧化物歧化酶(superoxide dismutase,SOD),营养价值极高[1-2],但同时也容易发生劣变。SOD是一种广泛存在于动植物以及微生物体内的金属抗氧化酶,它与过氧化氢酶、多酚氧化酶等的活性是评判果蔬副产品品质劣变程度的重要指标,SOD可以清除细胞代谢有害物质,抑制果蔬腐败变质[3-5]。
功能化离子液体是根据离子液体的可设计性,在离子液体的阴、阳离子中引入氨基、羧基和羟基等单个或多个官能团,从而使离子液体具有某些特异性功能或性质,是离子液体应用的一个重要分支[6-8]。功能化离子液体是近几年发展的一种新型绿色化学功能溶剂,因具有蒸汽压低、不易挥发、化学稳定性好、热稳定性好、溶解性优异,易与无机盐类形成双水相以及可循环使用,且不会造成环境污染和不会危及操作者健康等多种优势,引起了学术界的广泛关注[9-15]。功能化离子液体在具有普通离子液体特性的同时,又由于其结构的变化,在黏度、熔点、配位能力、亲水性等方面有极大的优越性。功能化离子液体可以直接从水相中萃取重金属离子、有机物,且其相对于易挥发有机溶剂而言,萃取率大幅提高[16]。目前,功能化离子液体已经在电化学、有机合成、分离萃取等领域有广泛的应用[17-20],而氨基功能化离子液体正是当前研究比较多的一种功能化离子液体。双水相体系因萃取条件高效温和而被广泛应用于生物大分子物质的萃取分离。功能化离子液体-双水相体系是由亲水性功能化离子液体和无机盐组成的两相[11]。基于功能化离子液体-双水相体系,Chen Jing等[21]合成了羟基功能化离子液体,该体系对牛血清白蛋白的萃取得率高达99.6%。施娅楠等[11]采用[C4Mim]Br/K2HPO4双水相抽提技术从辣木叶蛋白中分离凝乳酶,其酶活性回收率达到85.5%。
目前,番茄等植物性农产品抗氧化酶的萃取多依赖于传统的缓冲溶液法[1-3],利用缓冲溶液法提取的酶活性一般较低,而且提取一般需要40 min,耗时较长;近些年也有利用普通离子液体法对抗氧化酶进行萃取的研究,但大多数关于离子液体的研究都集中于二氧化碳、二氧化硫等气体的分离以及催化反应,针对萃取蛋白质类物质的研究很少。离子液体萃取SOD是由于其具有较强的溶剂作用,且与蛋白质之间有多种分子作用力,尤其是氢键作用力、极性作用力、离子电荷作用力,均会极大提高SOD在离子液体中的溶解度。功能化氨基官能团比普通离子液体更容易与SOD形成氢键,而氢键作用力是离子液体与蛋白质的多种作用力之一[16]。而氨基功能化离子液体在生物大分子方面的萃取研究还相对较少。
因此本研究拟选用1-丁基-3-甲基咪唑氯盐([C4Mim]Cl)、1-丙基-3-甲基咪唑氯盐([C3Mim]Cl)、1-胺丙基-3-甲基咪唑氯盐([(H2NC3)Mim]Cl)和1-胺乙基-3-甲基咪唑溴盐([(H2NC2)Mim]Br)4 种离子液体与无机盐形成的双水相体系,对番茄中的SOD进行萃取研究。以SOD活力为指标,考察离子液体的种类及质量浓度、无机盐质量浓度、萃取时间和萃取温度等参数对SOD活力的影响,根据单因素试验结果进行响应面试验设计,对实验条件进行再次优化,以期为果蔬中蛋白酶类物质的高活性萃取提供新的思路。
1 材料与方法
1.1 材料与试剂
SOD(1 500 U/mg) 上海士锋生物科技有限公司;磷酸氢二钾(K2HPO4)、磷酸二氢钠(NaH2PO4)、30% H2O2、磷酸氢二钠(Na2HPO4)(均为分析纯) 北京化工厂;[C4Mim]Cl、[C3Mim]Cl、[(H2NC3)Mim]Cl、[(H2NC2)Mim]Br 上海默尼化工科技有限公司。
1.2 仪器与设备
Milli-Q Reference超纯水系统 美国Millipore公司;11-102-49SH涡旋混匀器 德国IKA公司;U-3900紫外-可见分光光度计 日本Hitachi公司;THZ-103B恒温培养摇床 上海一恒科学仪器有限公司;PB-10型pH计德国Sartorius公司;Thermo ST16R离心机 德国Eppendorf公司;Multi-mode Synergy Mx酶标仪 美国Bio-Tek公司。
1.3 方法
1.3.1 相图的绘制
采用浊度滴定法[22-23]进行相图的绘制。首先分别称取1 g的离子液体([C4Mim]Cl、[C3Mim]Cl、[(H2NC2)Mim]Br和[(H2NC3)Mim]Cl)置于10 mL的离心管中,加入一定量的蒸馏水使离子液体完全溶解之后,向含有离子液体溶液的离心管中加入一定量的K2HPO4直至溶液变浑浊,再加蒸馏水至双水相消失,同时记录下所添加的无机盐和蒸馏水的用量,并进行多次如此反复操作以绘制相图,其中横坐标为K2HPO4的质量摩尔浓度,纵坐标为离子液体的质量摩尔浓度。
1.3.2 氨基功能化离子液体双水相萃取SOD
称取一定质量的氨基功能化修饰的离子液体(终质量浓度为0.4 g/mL)和K2HPO4(终质量浓度为0.6 g/mL)加入到带有刻度的离心管中,并加入1.5 mL蒸馏水溶解,待其溶解完全后可观察到体系分为上相(富集离子液体)、下相(富集K2HPO4)的双水相体系,再向双水相体系中加入0.5 g研磨成浆的番茄泥振荡混合均匀。将离心管放置于35 ℃、300 r/min恒温培养摇床中,振荡萃取25 min后取出离心管,静置使两相完全分开,取上清液(粗酶液)进行SOD活力测定。
1.3.3 缓冲液法萃取SOD
根据文献[18]方法,配制0.05 mol/L磷酸盐缓冲液(phosphate buffered saline,PBS)(pH 7.8)用于萃取番茄中的SOD。具体操作步骤:取新鲜的番茄,放入匀浆机中进行匀浆,再将其倒入研钵中在冰浴状态下研磨至泥状,称取0.5 g研磨成浆的番茄泥加入到含有4.5 mL PBS的离心管中混合均匀,将其放入高速离心机中,在4 ℃条件下以5 000 r/min的转速离心40 min,离心结束后取上清液于4 ℃环境中待用。
1.3.4 氨基功能化离子液体双水相萃取SOD工艺优化
准确称取0.5 g研磨成浆的番茄泥,采用氨基功能化离子液体双水相萃取法提取粗酶液,考察不同离子液体、氨基功能化离子液体质量浓度(0.3、0.4、0.5、0.6、0.7 g/mL)、K2HPO4质量浓度(0.5、0.6、0.7、0.8、0.9 g/mL)、萃取温度(20、25、30、35、40 ℃)以及萃取时间(5、10、15、20、25、30 min)对SOD活力的影响,并在单因素试验的基础上设计四因素三水平响应面试验。
1.3.5 响应面试验设计
根据单因素试验结果,选取氨基功能化离子液体质量浓度(A)、K2HPO4质量浓度(B)、萃取温度(C)以及萃取时间(D),利用Design-Expert 8.0.6软件设计四因素三水平响应面试验,以SOD活力为响应值,建立响应回归模型,优化试验设计,选择获得SOD活力最大的萃取工艺,因素水平如表1所示[24-26]。
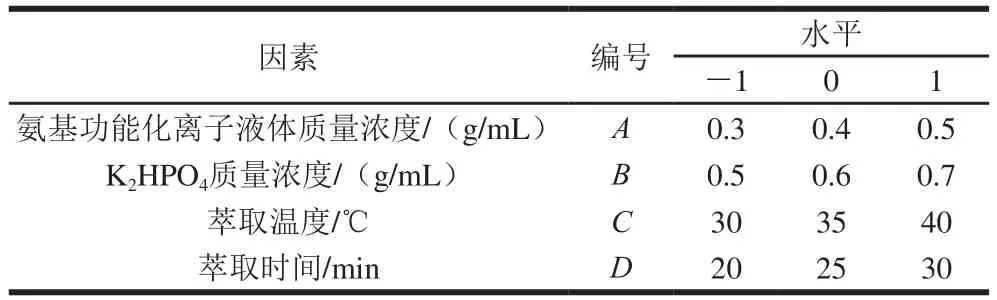
表1 响应面试验设计Table 1 Level and code of independent variables used for response surface design
1.3.6 SOD活力测定
SOD活力测定采用邻苯三酚法[27]。在25 ℃恒温条件下,以每克番茄样品每分钟抑制邻苯酚自氧化率达50%所需的酶量定义为1 个酶活力单位(U)。SOD活力单位为U/g,结果以番茄湿质量计。
1.4 数据统计与分析
实验过程中均进行3 次独立重复实验,结果取平均值,响应面试验采用Design-Expert 8.0.6软件进行实验设计及数据分析。
2 结果与分析
2.1 双水相体系的相图
大多数无机盐(K3PO4、K2HPO4和Na2CO3)都能与离子液体形成双水相,且具有较好的成相能力,其中K2HPO4与离子液体形成的双水相体系条件相对温和,因此本实验拟选用K2HPO4作为成相盐[22]。从[C4Mim]Cl、[C3Mim]Cl、[(H2NC2)Mim]Br和[(H2NC3)Mim]Cl与K2HPO4体系的相图(图1)可知,各离子液体的成相能力大小依次为[(H2NC2)Mim]Br>[C4Mim]Cl>[C3Mim]Cl>[(H2NC3)Mim]Cl;而离子液体的成相能力与其亲水能力相反,故其亲水性由高到低依次为[(H2NC3)Mim]Cl>[C3Mim]Cl>[C4Mim]Cl>[(H2NC2)Mim]Br。
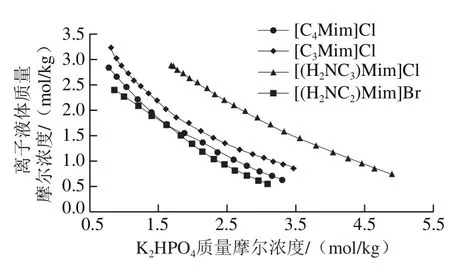
图1 双水相体系的相图Fig. 1 Phase diagrams of aqueous two-phase systems
2.2 SOD萃取参数优化结果
由于不同类型的离子液体对SOD萃取效果有很大的影响。因此,实验考察了[C4Mim]Cl、[C3Mim]Cl、[(H2NC3)Mim]Cl和[(H2NC2)Mim]Br 4 种不同类型的离子液体对SOD活力的影响。如图2A所示,氨基功能化离子液体比普通离子液体更容易与SOD形成氢键,而氢键作用力是离子液体与蛋白质的多种作用力之一[16],和其他离子液体相比,[(H2NC2)Mim]Br形成的双水相体系对SOD具有最好的萃取效果,因此选择[(H2NC2)Mim]Br制备双水相体系对酶进行提取。
[(H2NC2)Mim]Br质量浓度对SOD萃取效果的影响如图2B所示,离子液体质量浓度为0.3 g/mL时,对SOD的萃取效果较差,当质量浓度达到0.4 g/mL时,萃取效果最好,之后随着离子液体质量浓度升高,SOD部分二级结构被改变,并且离子液体胶束的形成也会使部分酶失活,导致活力降低[28],因此最佳离子液体质量浓度应控制在0.4 g/mL。
无机盐质量浓度对SOD萃取效果的影响如图2C所示,当K2HPO4的质量浓度为0.6 g/mL时,SOD能够保持最高的活力。随着K2HPO4质量浓度继续增大,可能会使已经萃取到离子液体相中的酶再转移到水相中,同时过多的盐也可能导致酶活力的下降,因此,K2HPO4的最优质量浓度为0.6 g/mL。
萃取温度、萃取时间对SOD萃取效果的影响分别如图2D、E所示,随温度升高,SOD活力先快速升高再略下降,其中35 ℃下萃取得到的SOD活力最高,因此最优萃取温度为35℃;随萃取时间延长,SOD活力逐渐增加,当萃取时间达到25 min后,SOD活力逐渐稳定,因此,萃取时间选择为25 min。
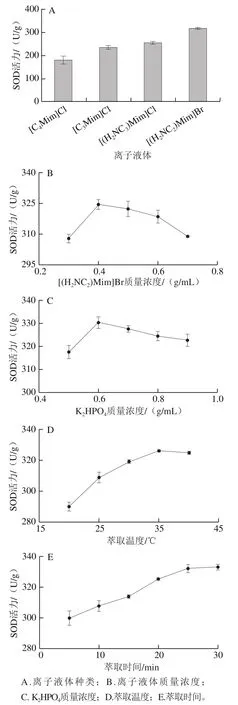
图2 不同因素对所萃取的SOD活力的影响Fig. 2 Effects of different extraction parameters on SOD activity
2.3 响应面试验结果
2.3.1 试验设计方案及结果
利用Design-Expert 8.0.6软件对表2数据进行分析,得到二次回归拟合方程Y=344.94+2.51A+3.21B+1.89C+0.58D+0.47AB-1.57AC+2.68AD+1.83BC-0.25BD-0.39CD-26.18A2-26.08B2-22.08C2-22.16D2。

表2 不同因素对SOD活力影响的响应面试验设计方案及结果Table 2 Experimental design with experimental values of SOD activity for response surface analysis
对回归方程进行显著性检验,结果如表3所示,模型P<0.000 1,说明数据模型方程达到极显著水平;失拟项是模型中数据的变异,失拟项P=0.476 7>0.05,说明数据变异不显著;即回归方程与实际结果拟合良好,能充分反映实际情况,误差小,模型合适。回归方程各项方差分析表明,回归模型一次项A、B、C为模型显著因素,二次项A2、B2、C2、D2为模型极显著因素,其余各项对SOD活力影响均不显著。因此,可用此模型SOD的提取工艺和条件进行分析及预测。回归方程各项方差分析中F检验可以判断自变量对因变量的影响,由此得到各因素对SOD活力影响由大到小依次为B>A>C>D,即K2HPO4质量浓度对SOD影响最显著,[(H2NC2)Mim]Br质量浓度与萃取温度影响次之,萃取时间影响最小。

表3 不同因素对SOD活力影响的方差分析结果Table 3 Analysis of variance for the effects of different extraction parameters on SOD activity
2.3.2 响应面试验结果分析
响应曲面图可以反映各因素之间相互作用的强弱,采用Box-Behnken软件对响应曲面图进行分析,可以得到各因素交互作用对响应值的影响,结果见图3。
三维响应面曲线图可以更直观地观察到两个变量对因变量的影响,等高线图即为响应面图的投影,可从等高线图中得到最佳范围。由图3可知,[(H2NC2)Mim]Br质量浓度和K2HPO4质量浓度交互作用的响应曲面最陡峭,说明对SOD活力影响最显著;[(H2NC2)Mim]Br质量浓度与萃取时间、萃取温度之间以及K2HPO4质量浓度与萃取时间、萃取温度的交互作用的响应曲面相对陡峭,说明对SOD活力影响显著程度次之;萃取时间与萃取温度的交互作用对提取率的影响显著程度较小,表现为曲面较平滑,说明对SOD活力无显著性影响。通过模型优化,得到SOD的最佳提取条件为[(H2NC2)Mim]Br质量浓度0.40 g/mL、K2HPO4质量浓度0.61 g/mL、萃取温度35.22 ℃、萃取时间25.08 min;并得到该条件下的SOD活力预测值为345.15 U/g。


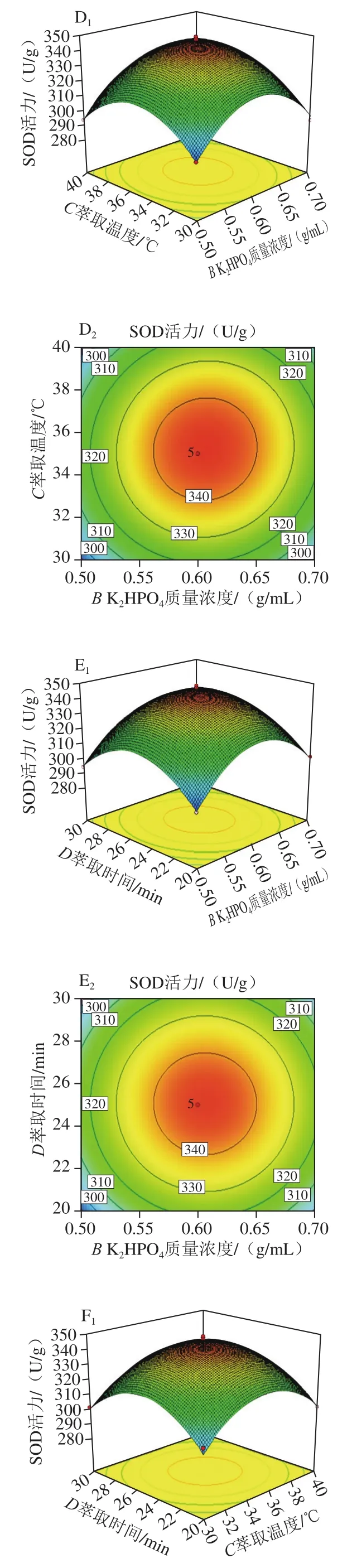

图3 各因素交互作用对SOD活力影响的响应面图及等高线图Fig. 3 Response surface and contour plots for the interactive effects of various factors on SOD activity
2.3.3 验证实验结果
考虑到实际操作因素,将各因素最佳条件设定为氨基功能化离子液体质量浓度0.40 g/mL、K2HPO4质量浓度0.60 g/mL、萃取温度35℃、萃取时间25 min,进行3 次平行实验,得到萃取的SOD活力平均值为345.68 U/g,与2.3.2节的预测值345.15 U/g接近,验证了此模型的有效性,说明预测模型与实际情况拟合较好。
2.4 不同方法萃取SOD效果比较结果
在该优化的条件下,实验以0.4 g/mL [(H2NC2)Mim]Br和0.6 g/mL K2HPO4制备双水相体系,于35 ℃条件下对番茄中的SOD萃取25 min,对萃取后的SOD活力进行测定,结果如表4所示。[(H2NC2)Mim]Br/K2HPO4双水相萃取得到的SOD活力高于传统的缓冲液萃取法及[C4Mim]Br/K2HPO4双水相法,且标准偏差较小,导致这一现象发生的原因主要是氨基功能化离子液体-双水相是基于目标物与萃取剂之间的相互作用力(如范德华力、氢键作用、盐析效应和疏水作用)导致分配系数的改变,从而达到萃取分离的目的[29-30]。总体来说,氨基功能化离子液体双水相萃取法优于传统的萃取方法,该方法受到的外界干扰更小。

表4 [(H2NC2)Mim]Br/K2HPO4双水相法与缓冲液法、[C4Mim]Br/K2HPO4双水相法萃取SOD效果比较结果Table 4 Comparison of SOD activity values determined by [(H2NC2)Mim]Br/K2HPO4-based two aqueous phase extraction, buffer solution extraction and[C4Mim]Br/K2HPO4-based two aqueous phase extraction
3 结 论
本研究基于[(H2NC2)Mim]Br/K2HPO4双水相体系,建立了萃取分离番茄中SOD的新方法。以SOD活力为指标,对离子液体的种类及质量浓度、萃取时间、无机盐质量浓度、萃取温度等条件进行了优化,并根据单因素试验结果设计响应面试验,最后对传统缓冲液法及[C4Mim]Br/K2HPO4双水相法进行萃取效果的比较。结果表明[(H2NC2)Mim]Br/K2HPO4双水相法萃取番茄中SOD的最佳条件为[(H2NC2)Mim]Br离子液体质量浓度0.40 g/mL、K2HPO4质量浓度0.60 g/mL、萃取温度35 ℃、萃取时间25 min。通过本研究建立的萃取方法成功萃取了番茄中的SOD,得到的SOD活力比传统缓冲液萃取方法高,且萃取时间缩短了15 min。
