茶多酚对小麦淀粉理化特性和面包品质的影响及机理
2021-12-02曾维才
陈 南,陈 龙,何 强,孙 群,曾维才,,*
(1.四川大学轻工科学与工程学院,四川 成都 610065;2.四川大学 食品科学与技术四川省高校重点实验室,四川 成都 610065;3.四川大学生命科学学院,四川 成都 610064)
淀粉是食品工业中的常见加工原料,也是人体所需碳水化合物的主要来源。淀粉按结构可分为直链淀粉和支链淀粉,其中直链淀粉由大量葡萄糖分子以α-1,4-糖苷键连接而成,而支链淀粉的侧链以α-1,6-糖苷键与主链相连[1]。小麦淀粉提取于小麦面粉,相比于其他来源的淀粉,具有更高的透明度,是面包、馒头等淀粉制品的主要成分,其在加工和储运过程中,理化特性(糊化特性、回生特性等)的变化会影响其加工特性(感官特性、质构等)和营养品质[2]。研究表明,来源于植物的无毒无害多酚类提取物能够影响小麦淀粉的品质,赋予其制品独特的风味、色泽及口感,并强化其营养功效[2-3]。因此,关于植物多酚和淀粉间相互作用的探索已成为相关领域的研究热点。
茶(Camellia sinensis(L.) O. Ktze.)以其独特的滋味及诸多的保健功效而广受欢迎。茶多酚作为茶叶中重要的生物活性物质,主要由表没食子儿茶素没食子酸酯(epigallocatechin gallate,EGCG)、表儿茶素没食子酸酯(epicatechin gallate,ECG)、表没食子儿茶素(epigallocatechin,EGC)和表儿茶素(epicatechin,EC)构成,具有抗氧化、抗炎症和预防癌症等保健功效[4-5],因此,茶多酚已被广泛应用于食品、日用化学品和医药等领域。
目前,虽有大量关于多酚-淀粉相互作用体系的研究,但在分子水平上对其作用机理进行阐释的研究较少。因此,本实验测定了茶多酚对小麦淀粉理化特性以及面包品质的影响,然后通过分子动力学模拟技术探究其相互作用机理,为茶多酚在淀粉及制品中的广泛应用提供参考。
1 材料与方法
1.1 材料与试剂
金龙鱼高筋小麦面粉 浙江益海嘉里食品工业有限公司;干酵母 安琪酵母股份有限公司;茶多酚(绿茶提取物,纯度≥99%) 西安通泽生物科技有限公司;实验用水均为蒸馏水。
1.2 仪器与设备
5K5SS小型和面机 美国Kitchen Aid公司;SM-40SP醒发箱 新麦机械(中国)有限公司;21U3-P1电热式烘烤炉 台湾浩胜食品机械有限公司;UV-1800紫外-可见分光光度计 上海美谱达仪器有限公司;差示扫描量热(differential scanning calorimetry,DSC)仪梅特勒-托利多仪器(上海)有限公司;TA.XT Plus质构仪 英国Stable Micro Systems有限公司;JSM-7500F场发射扫描电子显微镜 日本电子株式会社;CM-5色差色度仪 日本Konica Minolta公司。
1.3 方法
1.3.1 小麦淀粉的制备及添加茶多酚的小麦淀粉理化特性测定
1.3.1.1 小麦淀粉的制备
向80 g小麦面粉中加入40 mL蒸馏水,充分揉捏使其形成面团,然后将面团浸泡于装有100 mL蒸馏水的烧杯中,室温静置20 min,取出面团用手轻揉并同时用蒸馏水冲洗,直至将淡黄色的面筋组分分离,收集上述静置和冲洗操作中的蒸馏水,并用30 目筛过滤,所得滤液在25 ℃下4 000 r/min离心10 min,收集下层沉淀于45 ℃下热风干燥12 h,所得干物质即为小麦淀粉[6]。
1.3.1.2 透光率的测定
向质量分数1%的淀粉乳浊液(小麦溶于蒸馏水配制,下同)中分别添加质量分数(以淀粉的质量计,后同)0、5%、10%和20%的茶多酚,沸水浴中连续搅拌30 min。结束后用冰水浴迅速冷却至室温(25 ℃),于620 nm波长处测定其透光率[7]。
1.3.1.3 糊化特性的测定
精确称量2 mg淀粉于液体铝坩埚中,使用微量进样器分别向其中加入4 μL不同质量分数(0、5%、10%和20%)的茶多酚溶液,密封后于20 ℃静置24 h。随后,使用DSC仪对样品坩埚进行升温处理,升温速率为10 ℃/min,从20 ℃加热至100 ℃,并以空坩埚作为参照[8]。淀粉糊化的初始温度、峰值温度、终值温度及糊化焓通过DSC热流曲线计算并记录。
1.3.1.4 老化特性的测定
向质量分数12%的淀粉乳浊液中分别添加质量分数0、5%、10%和20%的茶多酚,沸水浴中连续搅拌30 min,随后迅速转入冰水中冷却至室温(25 ℃),然后将样品置于4 ℃条件下冷藏48 h,测定样品(圆柱形,直径40 mm、高25 mm)的质构,记录样品的硬度[9]。探头型号P/36R、测试前速率、测试速率和测试后速率均为1 mm/s、下压距离10 mm、感应力5 g、两次压缩时间间隔5 s。
1.3.1.5 凝胶微观结构的观察
将1.3.1.4节制得的淀粉凝胶置于冷冻干燥机内,-55~-65 ℃干燥48 h,将所得冻干样品切割成1 cm×1 cm×0.5 cm长方体。对样品进行喷金处理后,用场发射扫描电子显微镜(电压15.0 kV、放大倍数200)观察样品的微观结构[10]。
1.3.2 添加茶多酚面包的品质分析
1.3.2.1 面包模型的制备
向500 g高筋小麦面粉中加入7 g干酵母、50 g白砂糖和质量分数分别为0、0.025%、0.05%、0.1%、0.2%和0.4%(以面粉质量计)的茶多酚,干粉混匀后,加入300 g蒸馏水和4 g盐,使用和面机进行搅揉,直至面团能被拉成均匀的半透明状。将搅拌成熟的面团置于28 ℃、85%相对湿度条件下发酵30 min,对其进行分块和整型后于38℃、85%相对湿度条件下再发酵70 min。然后置于面火180 ℃、底火220 ℃的烘箱内烘焙12 min[3]。面包于室温(25 ℃)下冷却30 min后备用。
1.3.2.2 面包比容的测定
采用油菜籽等体积置换法测定面包的比容[11]。分别测定面包的体积V和质量m,再根据下式计算面包的比容。
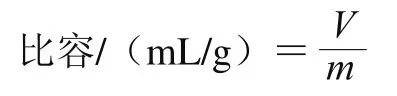
式中:V为面包的体积/mL;m为面包的质量/g。
1.3.2.3 面包质构的测定
用切片机将面包切成2 cm的均匀薄片,取最中间的一片面包芯用于质构(硬度、内聚性、胶黏性和咀嚼性)测定[12]。实验设定参数:探头型号P/36R,测试前速率、测试速率和测试后速率均为1 mm/s,形变量50%,感应力5 g,两次压缩时间间隔5 s。
1.3.2.4 面包颜色的测定
采用色差色度仪以D65作为照明光源,对面包表皮和面包芯的颜色进行测定。测定前使用标准白板对仪器进行校准,测定区域直径为3 mm,对不同样品的同一部位进行测定,每组样品重复测定3 次。使用国际照明委员会制定的颜色度量Lab模式表征样品的颜色,测定参数分别为亮度(L*值)、红度(a*值)和黄度(b*值)。
1.3.3 分子动力学模拟分析
设计意图 通过练习帮助学生进一步理解三角函数的概念,并能运用概念灵活求直角三角形中锐角的函数值,使学生对知识的理解螺旋上升,形成能力,达到了较高要求.
分别构建淀粉模型-短链葡萄糖(short-chain glucose,SGS)、茶多酚主要成分(EC、EGC、ECG和EGCG)以及反应环境水盒子(TIP3PBOX,65 Å×46 Å×49 Å)的分子模型,采用分子动力学模拟的方法,探究茶多酚与小麦淀粉的相互作用。淀粉模型-SGS通过GLYCAM官网(https://www.glycam.org)在线构建,SGS由18 个D-吡喃葡萄糖通过α-1,4-糖苷键连接组成,其中每6 个D-吡喃葡萄糖回转形成1 个左手螺旋;茶多酚主要成分的分子模型通过ChemBio3D Ultra 12.0软件构建,并采用Discovery Studio 4.5软件进行结构优化[13];反应环境水盒子模型(TIP3PBOX)通过AMBER 18.0软件构建并优化。分子动力学模拟实验通过AMBER 18.0软件完成,首先调用多糖力场GLYCAM-06j-1和小分子力场GAFF,分别对SGS和茶多酚主成分的分子进行识别和优化;接着以TIP3PBOX水盒子为模拟环境,对SGS及茶多酚主成分进行溶剂化处理,构建淀粉-茶多酚-水的反应模拟体系[14]。模拟反应启动前,调动能量最小化程序分别对TIP3PBOX水盒子和整个模拟体系的能量进行优化,避免模拟体系在反应过程中崩塌,然后使用加热程序,将体系温度由0 K升温至370 K,共计加热50 ps,以模拟淀粉糊化的高温环境。随后对体系状态(分子数、温度及压力)进行平衡,共计平衡50 ps,使体系密度无限趋近于1。最后,对平衡体系进行共计4 ns的模拟(包含2 000 帧模拟轨迹),记录并计算模拟体系中SGS空间结构的变化、结合位点的数量和变化、结合力的类型和强度、结合作用的稳定性、结合自由能的强度等淀粉和茶多酚主要成分间分子相互作用的类型及相互作用力的变化情况[15]。分子动力学模拟过程中,调用SHAKE法则限制氢原子的运动,将步长设置为2 fs。模拟轨迹的可视化截图通过Visual Molecular Dynamics 1.9.3软件获取;轨迹中数据的处理由AMBER 18.0软件的CPPTRAJ程序完成[16];结合自由能的计算采用AMBER 18.0软件的分子力学泊松-玻尔兹曼比表面积法(molecular mechanics Poisson-Boltzmann surface area,MM-PBSA)完成[17]。
1.4 数据处理与分析
每组实验重复进行3 次,结果以平均值±标准差表示。采用Origin 2018软件进行作图。采用SPSS 20.0软件进行统计学分析,单因素法进行显著性差异分析,P<0.05表示差异显著。
2 结果与分析
2.1 茶多酚对小麦淀粉理化特性的影响
2.1.1 透光率
淀粉糊的透光率常用于表征淀粉分子间缔合的程度,可间接地反映淀粉与茶多酚之间是否发生相互作用。由图1可知,茶多酚的添加明显降低了淀粉糊的透光率,当茶多酚质量分数为20%时,透光率下降至7.80%。结合相关研究分析可知,淀粉糊化时颗粒破裂并吸水膨胀,淀粉链迅速扩散,此时淀粉分子相对分散,光线更易透过,而茶多酚的加入诱使淀粉分子之间通过氢键和范德华力等作用发生一定程度的聚集,从而降低了淀粉糊的透光率[18]。结果表明,糊化过程中,茶多酚与淀粉之间发生了相互作用,使得糊化后的淀粉分子间发生了较强的相互缔合作用。
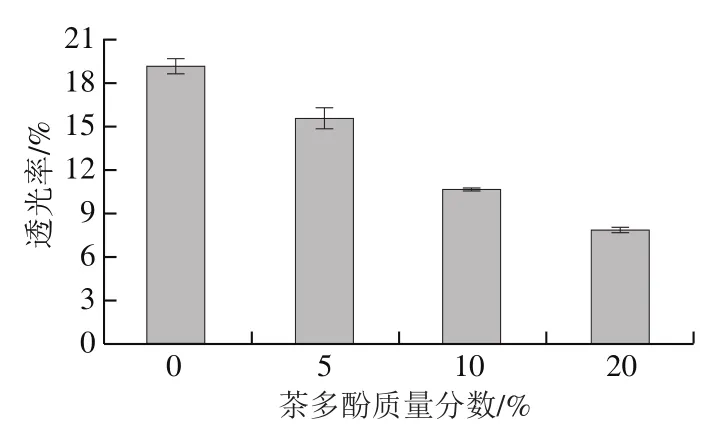
图1 茶多酚对小麦淀粉糊透光率的影响Fig. 1 Effects of tea polyphenols on the transmittance of starch paste
2.1.2 糊化特性
淀粉糊化是指淀粉颗粒在高温下溶胀、分裂,形成均匀糊状溶液的过程,淀粉糊化特性对淀粉的加工特性有较大的影响[19]。由表1可知,茶多酚的加入显著降低了淀粉糊化的初始温度、峰值温度、终值温度及糊化焓(P<0.05),当茶多酚质量分数为20%时,糊化焓由17.12 J/g降低至3.30 J/g。相关研究指出,淀粉的糊化涉及到淀粉分子结晶胶束结构的破坏与结晶片的熔化,需要加热以提供热量,而较低的糊化温度与糊化焓表明淀粉糊化所需能量降低,糊化更易发生[19-20];此外,近期的研究发现,茶多酚能够与淀粉链通过氢键结合,削弱淀粉颗粒内部结晶结构的强度,同时提高颗粒的吸水膨胀能力,促进淀粉的糊化[2]。本实验结果表明,茶多酚能够与淀粉结合,降低糊化所需热能,促进淀粉分子在糊化过程中与水分子的结合,影响淀粉的糊化特性。

表1 茶多酚对淀粉糊化特性和老化特性的影响Table 1 Effects of tea polyphenols on the gelatinization and retrogradation of starch
2.1.3 老化特性
淀粉的老化是指糊化后的淀粉分子重新排列形成有序结晶结构的过程,老化过程的持续发生将降低淀粉制品的品质与口感[21]。由表1可知,茶多酚的添加显著降低了淀粉凝胶的硬度(P<0.05),当茶多酚质量分数为20%时,淀粉凝胶硬度由483.67 g降低至228.87 g。结合相关研究分析可知,淀粉发生老化时,淀粉分子重排并相互缠绕,形成双螺旋等致密结构[21-22]。同时,淀粉的侧链还能与其周围游离的淀粉分子结合,形成三维网状结构,赋予淀粉凝胶一定的硬度。淀粉老化过程中,淀粉制品硬度的降低表明淀粉老化过程的发生受到抑制,其三维网状结构的形成受到影响;此外,相关研究表明,茶多酚分子中的多酚羟基结构能够与淀粉分子的侧链相结合,占据淀粉链的氢键结合位点,阻碍淀粉分子间的缠绕与结合[21-23]。本实验结果表明,茶多酚能够抑制老化过程中淀粉分子的重结晶,影响淀粉的老化特性。
淀粉凝胶的微观结构可用于反映淀粉老化缔合的程度,其与淀粉制品的质构特性密切相关[24]。茶多酚对淀粉凝胶微观结构的影响如图2所示,茶多酚质量分数为0时,淀粉凝胶网络结构呈清晰的层状,层间彼此交联形成许多分布较为均匀、连续的孔洞,呈现较为完整的三维网状结构(图2A);茶多酚质量分数为5%和10%时,其网络结构表面的粗糙度增加,破坏了淀粉凝胶的网络结构(图2B、C);茶多酚质量分数为20%时,网络结构的交叉处被大而粗糙的块体填充,阻碍了周围柱状连接与孔洞的形成(图2D)。实验结果表明,茶多酚的加入影响了淀粉凝胶的交联程度和网络结构的形成方向,对淀粉凝胶的三维网状结构有明显影响。
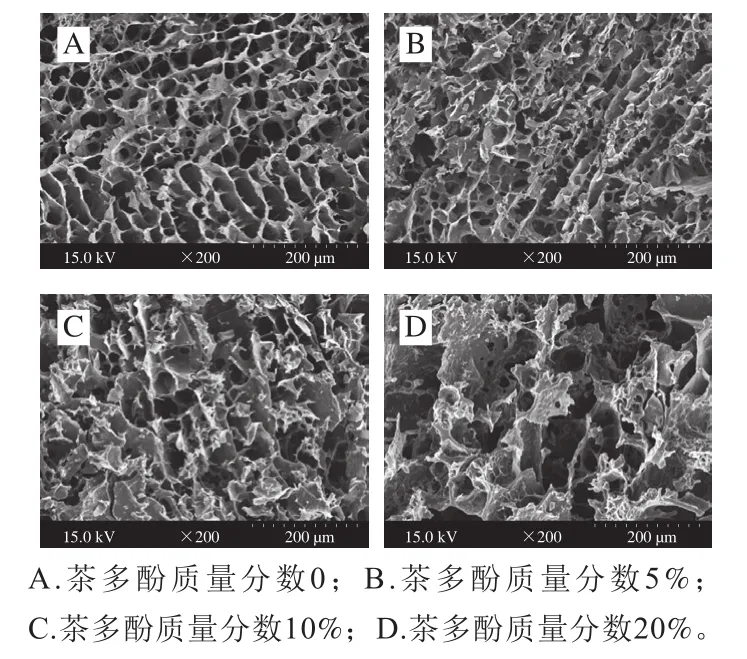
图2 茶多酚对淀粉凝胶微观结构的影响Fig. 2 Effects of tea polyphenols on the microstructure of starch gel
2.2 茶多酚对面包品质的影响
2.2.1 比容
比容反映样品在质量相同的情况下其体积发生的变化。由图3可知,随着茶多酚质量分数的增加,面包的比容呈现先增大后减小的趋势。当茶多酚质量分数低于0.1%时,茶多酚对面包比容并未产生负面影响,当茶多酚质量分数继续增加时,面包比容逐渐低于茶多酚质量分数为0组。结合相关研究分析可知,茶多酚的添加会促进小麦粉中淀粉的糊化,提高淀粉对水分的争夺能力,促进淀粉颗粒的吸水膨胀[25-26]。本实验结果表明,较低质量分数(≤0.1%)的茶多酚会增大面包的比容,改善产品的品质。

图3 茶多酚对面包比容的影响Fig. 3 Effects of tea polyphenols on the specific volume of bread
2.2.2 质构
质构特性作为淀粉制品一项重要的品质指标,不仅可以用来反映产品的口感、细腻度和组织状态等,还能进一步反映产品的质量稳定性。硬度指样品发生一定形变所需的力;内聚性反映样品内部的黏合力,指样品经第一次压缩变形后所表现出来的对第二次压缩的相对抵抗能力;胶黏性指样品内部的收缩力;咀嚼性指将样品咀嚼成吞咽状态时所需的能量[12]。茶多酚对面包质构特性的影响如图4所示,面包的硬度、胶黏性和咀嚼性均随着茶多酚质量分数的增加而呈现增大的趋势(图4A、C、D);而内聚性随着茶多酚质量分数的增加而减小(图4B)。相关研究指出,淀粉制品硬度和咀嚼性的降低可使其更柔软,更易咀嚼和吞咽[3]。同时,适中的内聚性和胶黏性会赋予淀粉制品更好的口感。本实验中,面包质构特性的变化可能与淀粉分子缠绕形成的三维网状含水胶体结构受茶多酚的影响有关,较低质量分数(≤0.1%)的茶多酚会赋予面包更优的质构特性,使其质地更加松软,口感更加丰富。

图4 茶多酚对面包质构特性的影响Fig. 4 Effects of tea polyphenols on the texture of bread
2.2.3 颜色
颜色是一项重要的食品感官指标,与消费者对食品的可接受度密切相关[27]。茶多酚对面包颜色的影响如图5所示,不同质量分数茶多酚的添加显著降低了面包皮和面包芯的L*值(图5A),显著增加了面包皮和面包芯的a*、b*值(图5B、C)(P<0.05),使面包颜色整体偏暗、偏红和偏黄。本实验结果表明,较低质量分数(≤0.1%)的茶多酚可以赋予面包独特且诱人的颜色,提高产品的市场竞争力。
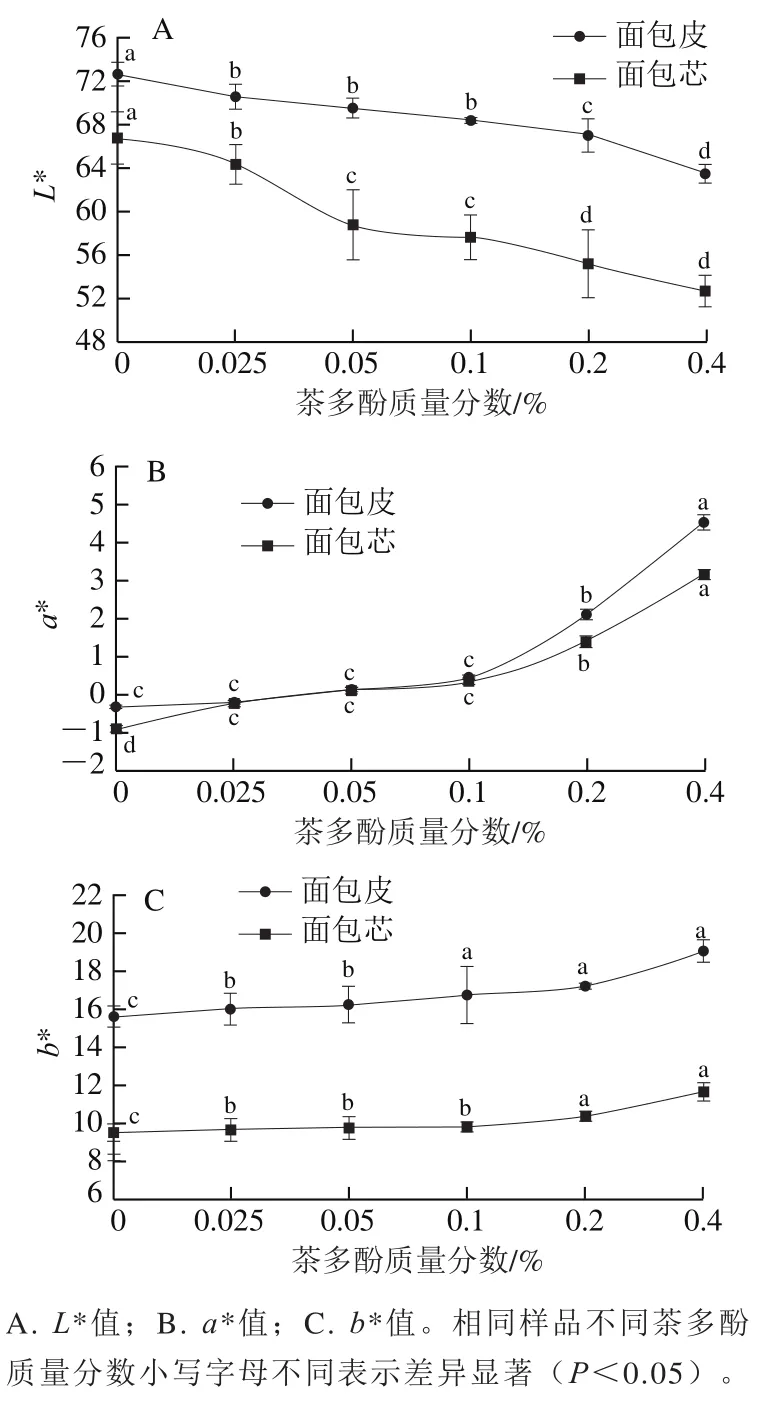
图5 茶多酚对面包颜色的影响Fig. 5 Effects of tea polyphenols on the color of bread
2.3 分子动力学模拟分析结果
2.3.1 分子模型及相互作用轨迹
分子动力学模拟是目前用于对分子相互作用进行解释或预测的研究方法。淀粉模型-SGS、茶多酚主要成分(EC、EGC、ECG和EGCG)以及TIP3PBOX水盒子的分子模型如图6所示。根据AMBER官网的说明及文献[28]的分析,分子结构内不适当的结构张力会使得模拟体系崩塌,因此正式模拟前需对分子模型进行结构优化,结构优化后的分子模型为分子动力学模拟的基础。
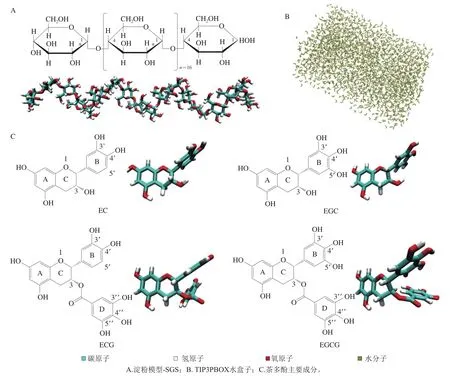
图6 分子模型Fig. 6 Molecular models
SGS和茶多酚主要成分(EC、EGC、ECG及EGCG)之间相互作用的分子模拟轨迹如图7所示。SGS的起始结构呈左手螺旋状,模拟期间其分子内氢键的断裂和新氢键的不断形成,使得SGS构象不断发生变化,呈现无规律、随意的卷曲,模拟结束后,SGS的螺旋结构发生伸展,形成更疏松的螺旋链状结构(SGS空白组);在EC/SGS模拟组中,EC与SGS几乎没有发生结合,但由于体系中EC的加入,影响了SGS的构象,使其发生了盘绕;在EGC/SGS模拟组中,相比于EC,EGC分子在B环5′位上存在一个酚羟基(图6C),略微增强了EGC与SGS的结合能力,故EGC在模拟前期(0~1.0 ns)与SGS发生了短暂的结合;而在ECG/SGS模拟组中,相比于EC,ECG结构中D环上没食子酰基的存在(图6C)不仅增加了能与SGS作用的活性酚羟基数目,还影响了B环电子云的分布,增强了B环上酚羟基的反应活性,故ECG在模拟后期(1.0~4.0 ns)与SGS一直紧密结合;在EGCG/SGS模拟组中,EGCG与SGS一直处于紧密结合的状态,相比于ECG,EGCG分子的B环5′位上存在一个酚羟基,而B环上3 个相邻酚羟基之间的弱氢键作用所产生的共轭稳定性赋予了EGCG更强的反应活性[29];此外,在EGCG分子B环上的3 个酚羟基中,由于B环5′位置上的酚羟基更靠近D环的没食子酰基,因此该位点的酚羟基对B环的反应活性更加重要。模拟轨迹分析结果表明,D环没食子酰基以及B环5′位上酚羟基的存在使得EGCG拥有更高的反应活性,使其与SGS的结合更为稳定。
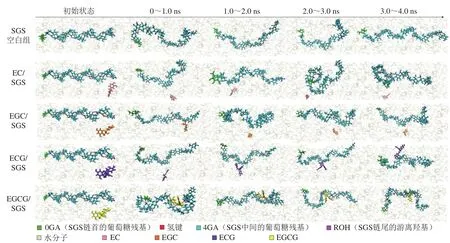
图7 SGS和茶多酚主要成分之间相互作用的分子模拟轨迹Fig. 7 Molecular trajectories of interactions between SGS and major components of tea polyphenols
2.3.2 模拟体系的评价
为了评估现有分子动力学模拟的合理性与稳定性,进一步记录了质心距离和均方根偏差(root mean square deviation,RMSD)。
质心距离表示分子间质量中心的距离,质心距离可用于评价分子间结合状态的稳定性。由图8可知,EC/SGS和EGC/SGS的质心距离起伏波动较大,这与EC、EGC两分子与SGS的结合不稳定有关,ECG/SGS的质心距离整体呈减小趋势,表明两个分子彼此靠近并逐渐结合在一起,而EGCG/SGS的质心距离整体处于相对平稳的状态,这与两个分子的紧密结合相关。

图8 SGS与茶多酚主要成分质心距离Fig. 8 Centroid distance between SGS and major components of tea polyphenols
RMSD值是以体系初始构象作为参照,计算模拟中产生的每一帧构象与其偏差值。由图9可知,EC/SGS和EGC/SGS的RMSD值波动较大,ECG/SGS和EGCG/SGS的RMSD值整体上趋于相对平稳的状态,表明ECG和EGCG这两种茶多酚主要成分与SGS的结合更为稳定,可能对淀粉理化和加工特性的影响更大。

图9 不同模拟组的RMSDFig. 9 Root mean square deviation values of various simulation groups
2.3.3 分子间相互作用机制
氢键是分子相互作用中的一种非共价结合力,葡萄糖链的空间构型主要依赖于3 种类型的分子内氢键(O6—O2、O6—O3以及O2—O3),而具有多酚羟基结构的酚类物质能够与淀粉形成氢键,竞争性抑制淀粉分子内氢键的形成[30-31]。因此,本实验分析了SGS的分子内氢键以及SGS与EC、EGC、ECG、EGCG分子间氢键的变化。由表2可知,SGS空白组(未添加茶多酚主成分)中分子内氢键出现比例最高的是4GA_4@O2与4GA_3@H3O形成的氢键,比例为11.1%;EC、EGC、ECG和EGCG的加入都不同程度地影响了SGS分子内氢键的形成;EGCG对SGS分子内氢键形成的影响最为显著,该类氢键(受体氧原子为4GA_10@O2、供体氢原子为4GA_9@H3O)的比例高达39.6%,在2 000 帧的模拟轨迹中出现了792 帧,而EC/SGS、EGC/SGS、ECG/SGS中氢键的最高比例均未超过20%。表3记录了茶多酚4 种主要成分与SGS分子间氢键的形成情况。EC、EGC及ECG与SGS所形成的分子间氢键的最高比例分别为0.05%(受体氧原子为4GA_6@O2、供体氢 原子为EC_1@H12)、1.05%(受体氧原子为4GA_6@O5、供体氢原子为EGC_1@H9)及1.20%(受体氧原子ECG_1@O3、供体氢原子4GA_12@H6O),且在EC/SGS中仅发现一类比例极低的分子间氢键;而在EGCG/SGS组中,氧原子4GA_13@O2与氢原子EGCG_1@H7形成的分子间氢键比例达到9.20%,表明EGCG在与SGS的紧密结合中形成了连续的分子间氢键网络。本实验结果表明,EGCG是茶多酚中与SGS结合最为稳定的成分,它通过与SGS形成稳定、连续的分子间氢键,占据SGS的氢键结合位点,影响SGS分子内氢键的形成,改变SGS的空间构象。

表2 茶多酚主要成分对SGS分子内氢键的影响Table 2 Effects of major components of tea polyphenols on the intramolecular hydrogen bonds of SGS
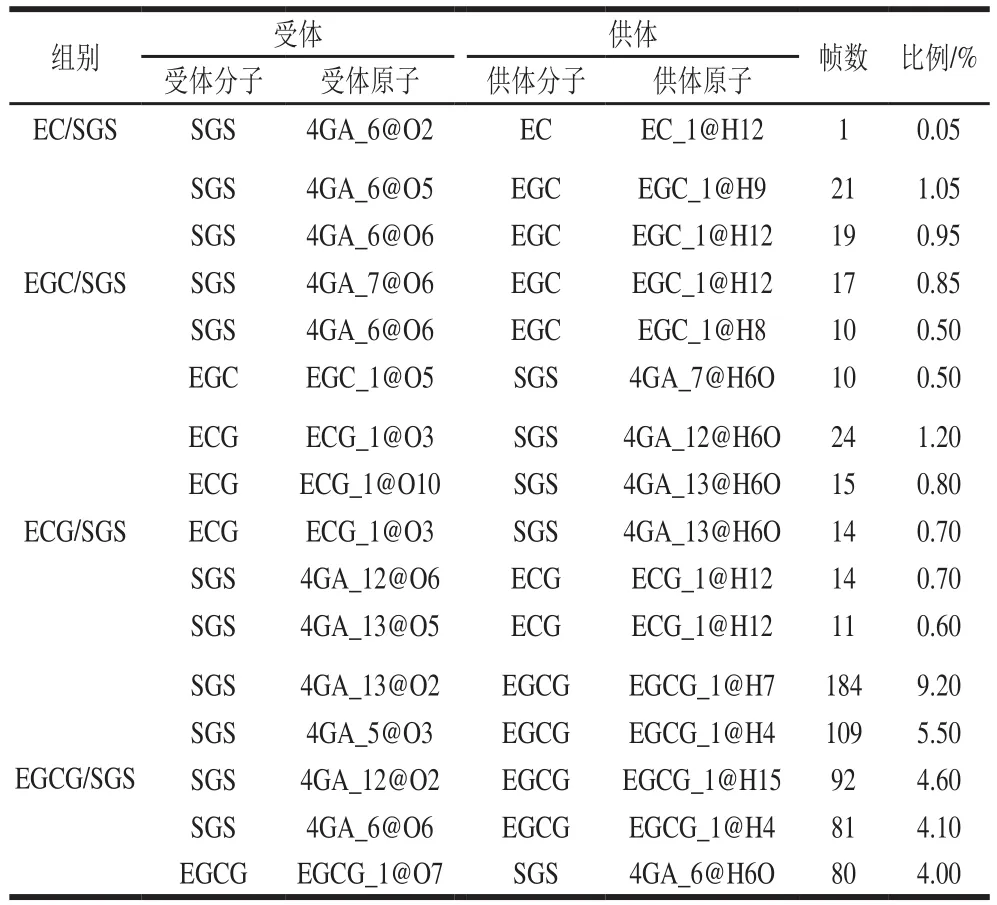
表3 SGS和茶多酚主要成分之间形成的分子间氢键Table 3 Intermolecular hydrogen bonds between SGS and major components of tea polyphenols
2.3.4 结合自由能
通过MM-PBSA法分别对茶多酚中的4 种主成分与SGS的结合自由能进行计算,默认参数包括范德华力作用能、静电作用能、极性溶剂化自由能、非极性溶剂化自由能,其中,结合自由能=范德华力作用能+静电作用能+极性溶剂化自由能+非极性溶剂化自由能,茶多酚主成分与SGS发生相互作用时,范德华力作用能和静电作用能等能量共同决定了结合自由能,而结合自由能的高低决定了茶多酚主成分与SGS相互作用的强弱、彼此结合发生的可能性及稳定性大小,结合自由能越低,结合越稳定[18]。如表4所示,EGCG/SGS的结合自由能最低,为-8.206 5 kJ/mol;此外,EC/SGS、EGC/SGS的范德华力作用能(分别为-4.237 8 kJ/mol和-4.997 9 kJ/mol)及静电作用能(分别为-1.716 9 kJ/mol和-2.383 4 kJ/mol)不利于它们与SGS的结合;而ECG/SGS与EGCG/SGS相比,较高的范德华力作用能(-11.573 7 kJ/mol)和静电作用能(-3.064 2 kJ/mol)使得ECG与SGS结合能力低于EGCG。结果表明,EGCG/SGS的结合最为稳定,相互作用最强。
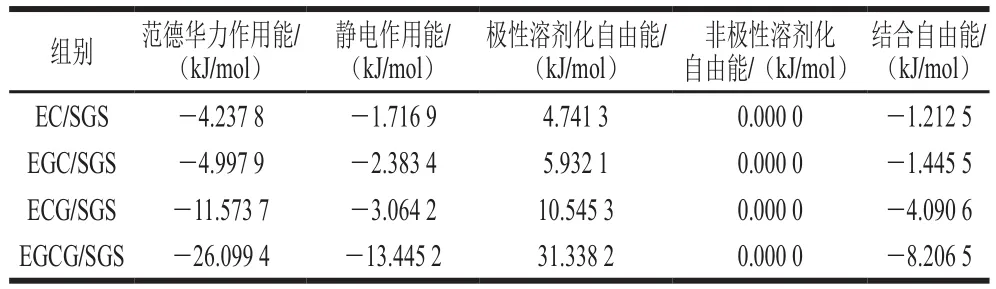
表4 SGS和茶多酚主要成分的结合自由能Table 4 Binding free energies of SGS with major components of tea polyphenols
3 结 论
茶多酚与小麦淀粉通过分子间氢键形成多酚-淀粉复合物,改变了淀粉的分子内氢键,影响了淀粉的理化特性和制成面包的品质;此外,在茶多酚的4 种主要成分中,EGCG分子结构中D环没食子酰基和B环5′位上羟基的存在,使其与淀粉模型-SGS的结合更稳定,相互作用更强。本实验为茶多酚在淀粉类食品的加工及生产中的应用提供了参考。
