后路病灶清除术治疗胸腰段非特异性感染并椎管脓肿形成
2021-11-30王文涛白露露郝定均葛朝元薛旭凯
王文涛,白露露,郝定均,葛朝元,薛旭凯
(西安交通大学附属红会医院脊柱病院,陕西 西安 710054)
非特异性脊柱感染多为由细菌感染引起的椎间盘及相邻软骨终板的感染性病变,其发病率相对较低,约占骨髓炎患者的2%~7%,发生部位最常见于腰椎,其次为胸椎,背痛是最常见的首发症状[1-2]。在疾病早期,由于其起病隐匿,症状和体征无特异性,实验室检查和影像学变化易与脊柱结核等混淆,非特异性脊柱感染极易被误诊[3]。在临床工作中,关于非特异性脊柱感染患者的治疗,目前存在很大争议,主要包括保守治疗和手术治疗[4-5]。
在成人中,非特异性胸腰段脊柱感染并椎管脓肿形成是非常罕见的临床情况。然而,近年来,其发病率似乎正在上升[6]。由于非特异性胸腰段脊柱感染并椎管脓肿形成可能会导致急性神经恶化,因此需要充分的手术和保守治疗相结合。到目前为止,非特异性脊柱感染的手术方法主要包括前路、后路及前后路联合手术。有学者认为早期前路病灶清除植骨融合内固定术可直接彻底清除病灶,且对脊柱的稳定性影响较小,但前路手术无法解除椎管内脓肿的压迫,存在手术并发症较多、内固定容易松动等缺点[7]。前后路联合手术可完全清除病灶并获得稳定脊柱内固定,但存在手术创伤大,手术时间长且术中需要改变体位等缺点[8]。有研究得出后路手术可获得满意的椎管减压、后凸畸形矫正且手术创伤小,但对于成人非特异性胸腰段脊柱感染并椎管脓肿形成的患者行后路减压病灶清除植骨融合内固定治疗的研究较少[9]。本研究回顾性分析2019年1月至2020年1月我院采用后路减压病灶清除经椎间孔植骨融合内固定治疗的成人非特异性胸腰段脊柱感染并椎管脓肿形成患者31例的临床结果,为其治疗提供依据,现报告如下。
1 资料与方法
1.1 一般资料 纳入标准:(1)患者符合非特异性脊柱感染的诊断标准且持续性腰背疼痛并活动明显加重;(2)影像学资料表现为胸腰段(T11~L2)单一椎间隙感染并椎管脓肿形成;(3)完善术前检查并接受后路减压病灶清除经椎间孔植骨融合内固定手术治疗;(4)术后病理支持慢性炎症或标本细菌培养阳性(金黄色葡萄球菌、大肠埃希菌、表皮葡萄球菌等)。排除标准:(1)诊断为结核、布鲁杆菌病、真菌感染、梅毒的脊柱特异性感染患者;(2)术后病理检查结果显示脊柱肿瘤;(3)不能耐受手术而行保守治疗的非特异性脊柱感染;(4)未能完成随访及临床病历资料不全者。
回顾性分析2019年1月至2020年1月于西安市红会医院脊柱病院行后路减压病灶清除经椎间孔植骨融合内固定的成人非特异性胸腰段脊柱感染并椎管脓肿形成的患者共31例,其中男19例,女12例;年龄57~81岁,平均(66.90±6.19)岁。患者中有9例合并糖尿病,4例合并乙型肝炎,7例有胸腰部侵袭性操作史。
1.2 手术方法 入院后完善术前检查并进行术前评估。所有手术均由我院经验丰富的副高级医师完成。取俯卧位,全身麻醉,以病变椎间隙为中心行后正中切口,向两侧显露至小关节及横突基底部,于“人”字嵴顶点区域植入椎弓根螺钉,去除病变节段棘突及双侧椎板。病灶清除从脓肿较大、骨质破坏严重的一侧进入,术中保护好神经根和硬脊膜后彻底清除病灶内脓液、死骨及坏死间盘等组织,刮除上下椎体终板,反复用大量双氧水及生理盐水冲洗椎间隙及切口,将切除下来的自体骨制成合适大小的骨粒经椎间孔植入椎间隙并夯实,安装预弯连接棒并锁紧螺帽,放置引流管,切口逐层缝合。
1.3 术后处理 手术取标本常规做细菌培养、药敏试验及手术病理标本检查。术后常规应用高效广谱抗生素,根据细菌培养药敏回报结果及时调整使用敏感抗生素,待红细胞沉降率和C反应蛋白降至正常后,停用抗生素。持续引流,待引流液<50 mL/24 h后拔除引流管。在支具保护下适当下床活动,支具佩戴3个月。
1.4 功能评价及随访 所有评估均由同一研究助理独立完成,记录患者术前、术后1个月及末次随访时疼痛视觉模拟评分(visual analogue scale,VAS),日本骨科协会(Japanese orthopaedic association scores,JOA)评分,感染控制指标(红细胞沉降率和C反应蛋白);术前及末次随访时神经功能障碍评估采用ASIA评级,末次随访时采用Eck[10]融合分级标准评估植骨融合情况。
1.5 影像学资料 所有患者术前均行X线、CT及MRI检查。X线片可表现为无明显变化或椎间隙变窄、模糊,出现骨破坏。CT检查示椎间隙明显变窄,上下椎体终板不规则破坏,MRI扫描示椎间盘及椎体信号异常改变,软骨终板界限不清,并脓肿形成。

2 结 果
2.1 一般资料比较 本研究31例患者均顺利完成手术,术中无血管、神经及内脏器官损伤等严重并发症。平均手术时间(161.1±11.74)min,术中平均出血量(323.8±44.92)mL,平均随访(16.7±3.01)个月。
2.2 实验室检查结果 31例患者术后病理标本细菌培养结果提示:金黄色葡萄球菌10例,表皮样葡萄球菌3例,大肠埃希菌1例,17例细菌培养结果为阴性。所有病例术后病理结果均提示炎性改变伴出血坏死及死骨。患者术后1个月时红细胞沉降率和C反应蛋白较术前比较,差异有统计学意义(P<0.05,见表1),末次随访时各指标全部恢复正常。

表1 患者实验室检查结果比较
2.3 功能评价指标 患者术后VAS、JOA评分与术前比较均有明显改善,差异有统计学意义(P<0.05)。末次随访时,患者均获得骨性融合,ASIA评级由术前C级3例,术后恢复至D级2例,E级1例;D级17例,术后恢复至E级15例,D级2例,E级11例,未发生神经功能加重病例(见表2)。
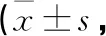
表2 患者术前、术后VAS、JOA评分比较分)
2.4 典型病例 65岁男性患者,因腰背部疼痛2个月伴双下肢麻木无力半个月入院。既往体健,入院诊断脊柱感染并椎管内脓肿形成(T10~11)。术前VAS评分7分,JOA评分10分,行后路减压病灶清除经椎间孔植骨融合内固定术,术后患者症状明显缓解,术后1个月时VAS评分2分,JOA评分21分。手术前后影像学资料见图1~6。
3 讨 论
非特异性脊柱感染并椎管脓肿形成是一种极其少见的,主要影响老年人群或有某些危险因素患者的疾病,常常导致顽固性腰背部疼痛、肌肉痉挛等症状,严重影响患者的生活质量,给患者带来极大的负担[11]。成人非特异性胸腰段感染并椎管脓肿形成的患者早期手术治疗至关重要。
近年来,非特异性脊柱感染的发病率有逐年上升的趋势,多发于成年人,男性发病率约为女性的4倍,尤其好发于并发免疫功能缺陷、糖尿病及腰背部针灸及小针刀等侵袭性操作等病史[6,12]。目前,关于非特异性脊柱感染的发生机制仍有争议,主要集中在以下方面:细菌感染、无菌性炎症、人体自身免疫反应,但仍以细菌感染为主,特别是慢性低毒力性细菌感染[13]。细菌感染可能有以下原因:(1)直接接种:包括从受感染的传染源直接传播和医源性传播,随着腰背部针灸及小针刀等侵袭性操作的逐渐发展,细菌通过直接侵入或接种到达椎间盘,最终导致非特异性脊柱感染。(2)血源性感染,当机体存在败血症或免疫功能低下或缺陷的情况下,细菌可能通过椎体静脉丛到达椎体,之后以局部蔓延的途径穿过椎体终板感染椎间隙,从而导致相邻终板和椎体的破坏。Kuker等[14]认为椎间盘间隙不太可能发生血源性感染,因为在成年期椎间盘间隙的血管供应被消除。然而,血源性感染途径仍然是金黄色葡萄球菌脊柱感染最常见的发病机制。在本研究中,我们通过术后病理标本细菌培养发现金黄色葡萄球菌10例,表皮样葡萄球菌3例,大肠埃希菌1例,17例细菌培养结果为阴性。因此,我们认为成人非特异性脊柱感染通过细菌感染的途径可能性更大,细菌累及椎间盘及椎体,造成相邻终板和椎体的破坏。

图1 术前正侧位X线片未见明显异常 图2 术前CT示上下终板及椎体不规则破坏 图3 术前MRI示椎间盘及椎体信号异常改变,软骨终板界限不清,并椎管脓肿形成

图4 术后病理检查为骨组织化脓性炎症伴出血坏死及死骨

图5 术后1个月X线片示病灶清除后植骨满意,内固定牢靠 图6 末次随访CT示椎间植骨已融合
非特异性脊柱感染早期缺乏明显特征,虽然目前医疗技术水平有明显提高,但诊断仍较为困难,从而延误最佳治疗。非特异性脊柱感染诊断主要依靠临床表现、实验室及影像学检查结果。大部分患者临床表现为痉挛性、顽固性剧烈腰背部疼痛、活动障碍、病变椎体节段局部深压痛、椎旁无明显压痛点、伴或不伴不规则低热的主要症状。实验室检查方面的表现:有研究报道称白细胞计数升高者不超过一半[13],红细胞沉降率升高的敏感性大于78%,C反应蛋白升高的敏感性大于64%,但红细胞沉降率和C反应蛋白不具有特异性,仅可作为病情好转期观察病情治疗效果的监测指标[15]。影像学方面的表现:脊柱非特异性感染X线及CT检查早期可无特异性改变,随着病情的进展3~4周后可出现椎间隙变窄,病变节段椎体终板可有虫噬样破坏,后期可有椎间隙狭窄、硬化的表现。MRI可在非特异性感染早期即表现出异常信号,有研究报道得出MRI改变的敏感性大于92%,是非特异性脊柱感染早期诊断的重要手段[16]。MRI能够清晰、全面反映病变椎间盘和邻近椎体的病理改变特征,表现为T1WI呈低信号改变,而T2WI呈高信号或者混杂信号影,甚至脓肿形成压迫硬膜囊。细菌培养阳性是诊断非特异性脊柱感染的金标准[17],有研究得出血培养阳性率约为50%[16],若血培养结果为阴性时,穿刺培养和手术病理标本活检细菌培养为诊断非特异性脊柱感染最可靠的方法。术前影像学变化是重要参考指标,如出现相邻上下椎体终板不规则破坏、椎旁脓肿等特征时应高度怀疑非特异性脊柱感染。
非特异性脊柱感染治疗的基石是及时准确的诊断,防止严重并发症的发生,包括保守治疗和手术治疗。保守治疗可通过严格的卧床休息、局部制动和大剂量的敏感抗生素迅速缓解患者的疼痛,加速炎症的吸收[5,18]。但一些学者[19]认为成人椎间盘血运的特殊性,抗生素难以彻底清除炎症,且由于细菌培养阳性率不高导致难以选择敏感抗生素治疗。因此,有学者主张非特异性脊柱感染应及时手术治疗,可缩短病程,加速康复[20]。手术治疗的目的是缓解疼痛症状,彻底清除坏死组织,重建脊柱稳定性和解压神经结构,恢复神经功能。关于采用前路、后路和前后路联合手术,目前仍有争议。有学者认为早期前路手术可直接清除病灶且对脊柱稳定性破坏较小,但存在无法清除椎管内压迫、内固定不牢靠且手术并发症较多等缺陷[7]。前后路联合手术虽可彻底清除病灶并获得坚强固定,但存在手术创伤大,手术时间长且术中需要改变体位等缺点[8]。也有研究认为后路手术可清除感染病灶,解除椎管压迫,矫正后凸畸形,重建脊柱的稳定性且手术创伤较小,但后路手术可能存在神经损伤,脑脊液漏等风险[21]。在本研究中,针对成人非特异性胸腰段脊柱感染并椎管脓肿形成,我们采用后路减压病灶清除经椎间孔植骨融合内固定术治疗,患者术后腰背部疼痛较术前明显缓解,无严重手术并发症,末次随访时内固定无松动、断裂,无感染复发。因此,后路减压病灶清除经椎间孔植骨融合内固定术可以有效缓解炎症反应导致的疼痛,彻底清除病灶,缩短病程,促进感染愈合,固定可靠,获得满意的植骨融合,是治疗成人非特异性胸腰段脊柱感染并椎管脓肿形成的有效方法之一。
本研究存在以下几个局限性。首先,本研究为回顾性研究,但我们术前的VAS评分、JOA评分及影像学资料均在患者住院期间由同一科研助理评估并记录,且进行了平均12个月的随访。其次,我们的病例是从单一中心获取且数量相对较小,虽然我国目前医疗技术水平有明显提高,但非特异性脊柱感染的诊断仍较为困难,因此,需要进行大数据的多中心研究以进一步支持我们的发现。最后,虽然我们通过研究发现后路减压病灶清除经椎间孔植骨融合内固定术是治疗成人非特异性胸腰段脊柱感染并椎管脓肿形成的有效方法之一,但如何提升早期诊断和更及时的治疗仍然是我们面临的挑战。
