活性炭深度脱除硫化氢的研究进展
2021-11-29左宋林刘斌
左宋林,刘斌
(南京林业大学化学工程学院,林产化学与材料国际创新高地,江苏省农林生物质资源国家重点实验室培育建设点,南京 210037)
硫化氢(H2S)是一种有毒且具有腐蚀性的酸性气体,具有强烈的臭鸡蛋味,嗅觉阈值极低。H2S 的污染源十分广泛,包括炼焦炉、污水处理、炼油工业、煤炭与天然气化工、垃圾填埋、水道、生物腐烂等工业生产和生活过程。在这些生产和处理过程中释放出不同浓度的H2S气体,容易引起化工生产过程中催化剂的失活,严重影响产品质量;或释放到大气或尾气中,成为气体的主要污染物,刺激呼吸道,危害生命健康。在工业上,H2S的酸性和腐蚀性严重腐蚀设备和管路,因此,净化气体中H2S成为脱硫的主要内容,是环境治理和工业生产过程的重要技术。
目前,对于较高浓度H2S (100 mg/L以上)的处理已有较多且较成熟的技术,主要包括吸收法、生物法、电化学法、氧化法等技术,通过回收或转化为单质硫、硫氧化物达到净化气体的目的。随着工业的快速发展和人们生活水平的不断提高,很多领域对硫含量提出了更高的要求,例如半导体生产、高品质油气、绿色催化等很多情况下需要对存在的低浓度或极低浓度(1 mg/L以下)H2S进行深度脱除,技术要求高,大多数针对较高浓度H2S气体的净化技术已不适用。目前,常用的深度脱除H2S气体的有效技术主要是吸附法[1-2],可操作性强。吸附材料是该技术应用效果的关键,在研究和实际应用中使用的吸附材料包括多孔质炭材料、多孔金属氧化物、沸石分子筛、金属有机框架(MOFs)等[3]。在这些吸附材料中,活性炭具有商业化生产技术较成熟、成本较低、结构易于调控和物理化学性质稳定等显著优点;因此,在工业上活性炭是目前深度脱除H2S的主要吸附剂,活性炭吸附成为深度脱除H2S的主要技术。我国是世界制造大国,大量生产过程涉及H2S的释放,给环境质量和生命健康造成许多隐患,因此,活性炭深度脱除H2S 应用越来越广泛;不仅已成为活性炭应用和环境治理领域的主要技术,也成为化工生产等工业过程确保产品质量、延长催化剂使用寿命、降低生产成本的常用工艺步骤。尽管有关活性炭脱除H2S的研究和应用已有近几十年的历史,然而,还未见有关活性炭深度脱除H2S方面的综述文献。活性炭脱除H2S技术涉及各种理论知识,包括活性炭的孔隙结构、表面化学结构、吸附机理、吸附热力学和动力学等,以及各种工艺影响因素。笔者综合国内外近几十年的相关研究进展,并结合笔者在活性炭脱除H2S气体方面的研究结果和工业应用技术经验,从活性炭、催化剂以及吸附条件等方面全面总结分析了活性炭的结构、催化种类以及吸附脱除条件的影响规律,论述了活性炭深度脱除H2S气体的吸附机理,希望能为活性炭深度脱除H2S理论和技术的进一步研究开发提供科学的指导。
1 活性炭孔隙结构及表面化学特性对吸附H2S的影响
1.1 孔隙结构的影响
活性炭具有发达的孔隙结构,其比表面积通常大于1 000 m2/g。然而工业生产的活性炭通常不仅具有发达的微孔结构,而且具有不同比例的中孔,因此掌握活性炭的孔隙结构对吸附脱除H2S的影响规律是研究的首要任务。Feng等[4]研究发现以微孔结构为主要特征的高比表面积活性炭纤维对H2S具有优良的吸附能力。Tanada等[5]分别采用甲基三聚氰胺、尿素溶液浸渍基炭,通过高温处理后活性炭的H2S吸附量明显增加,其原因是浸渍处理使活性炭的微孔容积提高了12.2%。Boki等[6]研究发现吸附H2S的主要孔隙是活性炭的较小孔径微孔。这些结果表明,H2S的吸附主要发生在较小的微孔中。
活性炭微孔容积与H2S吸附热的相关性研究进一步说明了活性炭微孔对于吸附H2S气体的重要性[7-8]。比表面积很低的炭黑对H2S的吸附热在20.6 kJ/mol左右,而活性炭对H2S的吸附热都大于38 kJ/mol,是无孔的炭黑表面对H2S分子吸附热的1.9~2.3倍[9]。这是由于H2S分子与活性炭中吸附H2S分子有效的微孔之间具有较强的作用力。在干燥状态下,活性炭对H2S气体的吸附热随着微孔比例的提高而增大,且具有较好的相关性[6],这表明它们主要是以物理吸附的方式进行。
1.2 活性炭表面化学基团的影响
1.2.1 含氧基团的影响
H2S是一种酸性气体,因此,根据吸附的基本原理推测,活性炭的碱性表面有利于H2S的吸附。含氧碱性基团是常见的活性炭表面基团。Shen等[10]研究了活性炭表面含氧基团对H2S吸附的影响,结果显示,吡喃酮、羰基、羧基是吸附H2S的活性位点,羟基基本不起作用,H2S可以直接和羰基氧反应,生成C—S、C—OH和C—SH等。吡喃酮是活性炭的典型表面碱性基团,有利于增强活性炭对H2S的吸附能力。活性炭表面上与羰基不在同一芳环的环氧基团,可以促进羰基氧的碱性,从而提高活性炭对H2S的吸附能力。Feng等[4]的相关研究也得出了类似的结果。吴博等[11]研究了在低温条件下活性炭吸附催化去除H2S的性能,认为活性炭表面的π-π*键、羰基、醚基等基团是活性炭表面吸附催化H2S的活性位点,能显著增强活性炭脱除H2S的能力。
另外,活性炭表面含氧基团是极性基团,能够增强活性炭吸附水蒸气的能力[12],尤其是在低的水蒸气相对压力下更为显著[13-14]。因此,在活性炭的孔隙表面引入含氧基团,提高活性炭表面吸附水蒸气的能力,有利于在活性炭表面形成水膜,最终促进活性炭对H2S的吸附,也能促进H2S在活性炭孔隙表面的吸附/氧化作用[15-16]。
1.2.2 含氮基团的影响
活性炭含氮基团是活性炭表面碱性的主要来源之一。在活性炭表面引入碱性含氮基团通常会提高活性炭的pH,促进活性炭对H2S的吸附。Adib等[17]通过尿素高温改性木质活性炭,在活性炭表面引入含氮基团,显著增强了活性炭对H2S的吸附能力,并发现在活性炭的微孔中,H2S被氧化成S和SO2,最后溶解在水中转变成H2SO4。Bagreev等[18]采用三聚氰胺、尿素和高温改性煤质活性炭,在活性炭中引入合适的含氮基团可以将活性炭的H2S吸附量提高10倍,而且发现在微孔形成的水膜能促进H2S氧化成单质S和SO2并形成硫酸,在较大尺寸的孔隙范围中H2S则被氧化形成含硫的聚合物。Tanada等[19]研究了含氮活性炭对H2S的吸附,结果显示在50 Torr(1 Torr=0.231 MPa)的平衡压力下,活性炭的氮含量与H2S的吸附容量呈正相关。具体结果如表1所示。
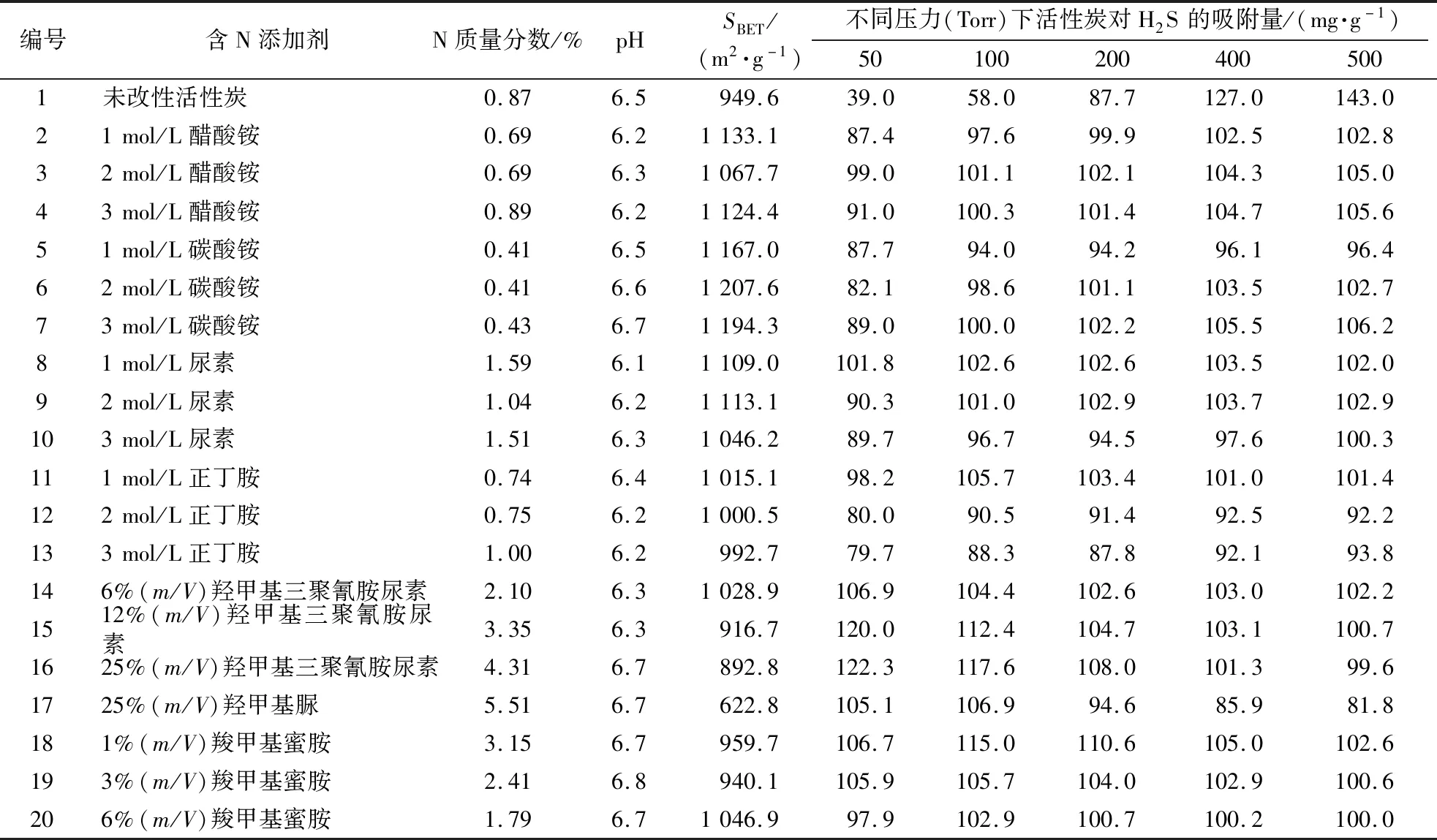
表1 活性炭氮含量与H2S吸附容量[19]Table 1 N-content and H2S adsorption capacity of activated carbons
通常情况下,较高含氮基团数量的活性炭对H2S吸附能力优于浸渍碱性化学物质的活性炭的吸附性能。这可能是因为含氮基团能够高度分散在活性炭孔隙表面,显著提高了活性炭表面中碱性活性位点与H2S气体分子的接触面积,促进H2S的快速氧化转化,而负载的碱性催化剂难以达到高度分散状态[20]。与含氧碱性基团相比,含氮基团的碱性更强一些,能与H2S分子之间产生更强的作用力。
不同活化方法制备的活性炭的表面化学结构也会有差异。有关研究结果表明, CO2和水蒸气活化的活性炭均呈现碱性[21-23]。经强氧化剂氧化处理活性炭的pH降低,表面酸性含氧基团数量增加,降低了活性炭的H2S吸附能力。通常情况下,活性炭表面碱性基团越多,无论是含氧基团还是含氮基团,活性炭的H2S吸附容量就会越高。
2 活性炭制备方法对吸附H2S的影响
生产活性炭的方法主要有使用水蒸气和/或CO2为活化剂的气体活化法与使用 H3PO4、ZnCl2、KOH等化学药品为活化剂的化学活化法两大类。不同活化方法的活化原理不同,形成活性炭的孔隙结构特点也不同,因此,不同活化方法制备的活性炭的吸附H2S能力有差异。众所周知,气体活化法是以形成微孔为主,不同的气体活化剂所制备的活性炭的孔隙结构也存在差异。通常情况下,水蒸气活化制得的活性炭比二氧化碳活化制得的活性炭孔径大[24-26]。在化学活化法制备中,H3PO4活化法生产的活性炭孔径尺寸比物理法生产的活性炭尺寸大,有利于形成中孔[21,27]。ZnCl2活化法生产的活性炭孔径尺寸比H3PO4的大,形成的孔隙结构是以中孔为主[28]。KOH法生产的活性炭也能形成较发达的中孔结构[29-30]。 有研究比较了KOH、NaOH、ZnCl2、水蒸气活化污泥所制备的活性炭H2S吸附能力,结果显示, KOH活化制备的活性炭具有最大的H2S吸附量,但仅有5 mg/g[31]。Li等[32]比较了KOH、ZnCl2、NaOH等活化剂活化稻草制备的活性炭对H2S的吸附能力,结果显示,30%的ZnCl2溶液与原料按照3∶1的质量比混合浸渍,在550 ℃下炭化制得的活性炭对H2S的吸附性能最好,穿透时间达到198 min。Zhang等[33]发现水蒸气活化造纸黑浆制备的活性炭也具有较好的吸附去除H2S的能力。李秀玲等[34]研究表明,ZnCl2活化核桃壳制备的活性炭硫容量也可以达到300 mg/g。鲍国臣[35]的研究结果表明,以污泥为原料, ZnCl2活化和KOH活化制得的活性炭对H2S的吸附性能要远好于H3PO4活化制备的活性炭;在60%的ZnCl2溶液、活化温度为600 ℃、活化时间为2 h、污泥与活化剂质量比为1∶2等条件下制备的活性炭的H2S吸附能力最好。上述研究结果显示,采用不同的活化方法都可以制备出吸附脱除H2S的活性炭产品。从本质上而言,不同的原料、活化方法和工艺影响活性炭的H2S吸附能力是由于制备的活性炭具有不同的孔隙结构和表面化学结构。
3 负载催化剂活性炭对H2S的脱除效果
从以往的研究结果看,在H2S浓度较低情况下,普通活性炭的H2S吸附量都较低,通常只有10~20 mg/g,难以达到深度脱除H2S气体的目的。尽管提高活性炭表面的碱性基团浓度,可以成倍增加其吸附量,但每克活性炭的H2S吸附量也只能达到几十毫克。因此,需要进一步负载合适的催化剂,显著提高活性炭的H2S吸附量,是高效深度脱除H2S活性炭的主要研发和工业应用方向。
3.1 碱金属化合物催化剂
碱金属化合物是最为常用的提高活性炭H2S吸附能力的催化剂,主要包括NaOH、KOH、Na2CO3等[36-38]。浸渍这些碱金属化合物能大幅提高活性炭对H2S的吸附能力,这主要是由于碱金属化合物通常具有较强的碱性所致。Choo等[39]研究了椰壳活性炭及其浸渍3种碱金属化合物(NaOH、KOH 和 K2CO3)制备的负载活性炭对H2S的吸附情况,结果显示,按照椰壳活性炭与金属化合物K2CO3的质量比为2.0∶1进行浸渍制备的活性炭对H2S的吸附量最大,是未浸渍碱金属化合物的椰壳活性炭吸附量的25倍,达到37 mg/g。Sitthikhankaew等[40]研究发现,浸渍了KOH、NaOH、K2CO3和Na2CO3的商业活性炭,在高温条件下对H2S的吸附量提高了3~29倍, 负载KOH和Na2CO3的活性炭能使H2S出口浓度控制在30 mg/L以下。Phooratsamee等[41]研究了3种碱金属化合物催化剂(NaOH、KI和K2CO3)对活性炭吸附H2S气体的影响,结果发现浸渍了K2CO3和KI的活性炭对H2S气体的吸附能力提高最为明显,其中K2CO3浸渍的活性炭吸附能力最优,而浸渍NaOH对活性炭吸附H2S气体能力的改善效果不佳。
对于催化剂而言,催化剂的种类和负载量是影响活性炭H2S吸附能力的主要因素。是Bansal等[42]浸渍了不同含量Na2CO3和KIO3的稻壳活性炭的吸附效果见表2。从表2可以看出,浸渍了Na2CO3和KIO3的活性炭具有很高的吸附H2S的能力;随着它们的负载量增加,活性炭的H2S吸附量不断提高,而且浸渍KIO3比浸渍Na2CO3的促进效果更加明显。Wang等[43]研究结果显示,随着NaOH负载量的增加,活性炭对醋酸和H2S的吸附量均增大。Wu等[44]的研究也显示,增加负载量增大了活性炭对H2S和SO2的吸附量。

表2 活性炭负载催化剂种类及数量对H2S吸附的影响[42]Table 2 Influence of the amount and type of activated carbon catalyst on H2S adsorption
3.2 碱土金属化合物催化剂
在碱土金属类化合物中MgO是最常见的催化剂,能显著催化H2S的转化[45-47]。Siriwardane等[48]研究发现,负载纳米MgO能使活性炭的H2S吸附量提高5倍以上,达到275 mg/g。张紫晓[49]采用中孔炭球负载MgO,其穿透硫容高达2.46 g H2S/(g催化剂),是目前商用活性炭催化剂的4倍左右;采用层级孔炭负载MgO用于H2S吸附,其穿透硫容最高可达3.02 g H2S/(g催化剂)。负载MgO之类碱土金属化合物的活性炭,具有碱性特点,不仅可以促进水膜的形成,而且有利于H2S分子化学吸附在活性炭表面,提高活性炭吸附脱除H2S的能力。与碱金属化合物不同的是,碱土金属化合物在水中的溶解度低,有利于多次重复利用,并提高其性能稳定性。
此外,碱土金属化合物催化剂可以与其他催化剂复合,形成催化能力更强的催化剂体系,主要包括Fe/MgO体系[50]、V/MgO体系[51]、Zn/MgO体系[52]和Mo/MgO体系[53]等复合催化剂体系。
3.3 重金属化合物催化剂
重金属化合物也是提高活性炭H2S吸附能力的催化剂。Yang等[54]研究显示,负载纳米ZnO颗粒能使煤质活性炭的硫容量提升了1倍以上,达到了62.5 mg/(g活性炭)。负载纳米ZnO颗粒能显著提升形成水膜的碱度,增强水膜溶解H2S的能力,因而增强了ZnO的催化能力。Cal等[55]研究发现,浸渍Cu和Zn能提高ZnCl2化学活化制备的活性炭的吸附性能,其中负载Zn的效果最好;硝酸氧化能提高负载Zn化合物活性炭对H2S的吸附能力。Zhang等[56]研究了负载二氧化锰活性炭的H2S吸附能力。在MnO2和活性炭质量比为1∶1条件下制得的活性炭,对H2S的吸附效果最好,达到110.7 mg/g;与未改性的活性炭相比,吸附量增大了96.9 mg/g。Huang等[57]还研究发现,负载铜能明显提高活性炭对H2S的吸附能力。

4 活性炭吸附脱除H2S的影响因素
4.1 温度的影响
温度是影响活性炭吸附H2S的主要因素。大量研究表明,提高吸附温度有利于活性炭对H2S的吸附。由于物理吸附是一个放热过程,因此升高温度不利于物理吸附。然而,Choo等[39]研究了温度对浸渍K2CO3的椰壳活性炭吸附H2S的影响,结果显示,在30 ℃时吸附量最小,随着温度升高吸附量增加,在50 ℃时达到最大吸附量,约100 mg/g,而在70 ℃时稍有下降。有研究发现,在200 ℃以下,随着反应温度升高,活性炭对H2S吸附能力提高,氧化选择性降低[62]。如果温度高于单质硫的熔点,活性炭的吸附效率会先增大至最大值,然后逐渐降低。Sitthikhankaew等[63]研究了负载催化剂的活性炭在30~550 ℃的范围内对H2S的吸附情况,结果显示,随着温度的升高,活性炭对H2S的吸附显著提升,在550 ℃达到最大。以上研究结果表明,活性炭吸附H2S气体涉及显著的化学吸附过程。Masuda等[64]认为,活性炭对H2S的吸附同时涉及物理吸附和化学吸附,尽管升高温度不利于活性炭物理吸附H2S,但能显著提高对H2S的化学吸附,增加H2S吸附量。
4.2 气体组分的影响
4.2.1 氧气含量
氧气是影响活性炭吸附H2S的重要因素之一,它能明显影响硫化物的产物组成。氧气的存在会增加H2S在活性炭层的穿透时间[65]。于英民等[66]在研究褐煤半焦吸附H2S的过程中发现,氧气能参与H2S的催化转化过程,促进H2S的脱除。Choi等[37]研究发现,活性炭负载催化剂能够显著提高吸附量与气流中氧气浓度,这是由于催化剂催化了H2S与O2之间的氧化反应。Ghosh等[67]研究了在125~200 ℃范围内活性炭催化H2S氧化的动力学和反应机理,发现不同氧气浓度催化氧化H2S的动力不同,效率也不一样。
氧气促进活性炭吸附H2S是通过在活性炭表面形成一层水膜实现的。当活性炭表面形成一层水膜时,氧气处于一定的相对湿度环境中,能溶解在水膜中参与H2S的氧化反应。在干燥状况下,即使有氧气存在,低温环境的活性炭吸附H2S主要还是以物理吸附为主[7]。Bandosz等[68]研究发现,活性炭表面预先吸收水分也能提高氧气氧化H2S的能力。Bagreev等[69]的研究同样显示,在活性炭吸附脱除H2S的过程中,预先用水湿润活性炭能提高氧气氧化H2S的能力。他们还发现,当氧气体积分数从1%升高到2%时,活性炭对H2S的穿透吸附容量变化不大[70]。王学谦等[71]研究发现浸渍Na2CO3的活性炭在吸附净化 H2S 过程中,反应温度及气体中的氧气含量是影响脱除H2S气体的关键因素,增加气体中的含氧量或提高反应温度均可显著提高净化效率。但增加到一定值后(温度>80 ℃,氧含量>1.0%)净化效果不再明显提高。
4.2.2 气流的湿度
研究表明,活性炭表面的水对H2S的吸附历程有非常重要的影响[72-74]。不管是浸渍催化剂,还是增加气流的相对湿度都能促进活性炭对H2S的吸附[75]。Kaliva 等[72]研究发现,随着空气中相对湿度的增加,活性炭对H2S的吸附量显著增加,且大大加速了H2S被氧化的速率。Xiao等[36,76]研究显示, 随着相对湿度的增加,浸渍Na2CO3和未浸渍的煤质活性炭对H2S的吸附性能都不断增强。在工业操作过程中,采用压缩空气将水汽引入活性炭床来预先湿润活性炭,可显著促进活性炭对H2S的吸附[75,77],相对于干燥的活性炭,其H2S吸附量提升了2~6倍[70]。活性炭的表面一般具有疏水性质[72,78],相对湿度的增加会促进H2S的吸附,最高的吸附量能增加100倍。
4.2.3 氨气的影响
氨气也有助于提高活性炭对H2S的吸附性能。Turk等[79]研究发现,在气流中通入氨气,能够提高活性炭对H2S和甲硫醇的吸附性能;且采用在气流中通入氨气的方式比在活性炭中浸渍碱催化剂更为有效,前者的H2S吸附量是后者的3倍,前者对甲硫醇的吸附量是后者的3~4倍。氨气能够显著提升活性炭去除H2S的能力,主要是因为氨气极易溶于水且溶解度非常大,氨气溶于水呈碱性。因此,气流中氨气能使活性炭内表面和外表面都快速形成水膜,且溶解大量氨气形成较强碱性的表面,促进H2S快速溶解和快速氧化去除;即使氧化过程产生了H2SO4,也会被气流中不断补充的氨气中和,不会抑制H2S溶解。
4.3 接触时间的影响
在固定床的吸附装置中,不同的体积流量会改变与活性炭层的接触时间,从而影响H2S的去除效率[80]。延长接触时间就会增加吸附质到达吸附位点的几率,提升去除能力[39]。一般通过体积流量与接触时间的乘积来确定活性炭的用量。接触时间不是通过理论推算得到的,一般需要通过具体实验确定[81]。
5 活性炭吸附脱除H2S的机理
没有表面改性或负载催化剂的普通活性炭对H2S分子的吸附主要发生物理吸附,因此普通活性炭的H2S吸附容量比较低,通常是在20~50 mg/g范围内。对于表面改性和负载催化剂的活性炭来说,它们对H2S气体的吸附机理则转变为以化学吸附为主,从而可以成倍提高活性炭的H2S吸附量。因此,理解活性炭对H2S的物理吸附和化学吸附机理,是研究开发高性能深度脱除H2S气体活性炭的基础。
5.1 活性炭的H2S吸附脱除机制
由于活性炭的孔隙表面总体上表现为疏水性,而H2S分子是一种弱电解质,具有较强分子极性。根据许多研究结果和吸附基础理论,一些学者提出吸附-溶解-氧化是活性炭吸附脱除H2S的主要机制[59,69,76,82]。这一吸附脱除机制包括物理吸附过程与化学转化过程,具体过程如图1所示。根据这一机制,活性炭吸附脱除H2S气体过程包括:首先是H2S分子物理吸附在活性炭孔隙表面,气流中存在的水蒸气富集到活性炭孔隙表面形成一层水膜;然后是H2S分子在极性水膜中的溶解及其部分电离成H+和HS-的过程。因此,活性炭的表面碱性官能团主要是通过与水膜作用形成碱性的水膜表面,促进活性炭吸附H2S分子[15]。当然,表面酸性官能团将大大抑制H2S分子的电离,降低了H2S分子在水膜中的溶解度,因而不利于活性炭吸附脱除H2S分子。根据这一机理可知,气流中合适的湿度将能显著促进活性炭吸附脱除H2S分子[75,77]。

图1 未浸渍活性炭吸附H2S的机理示意图Fig. 1 H2S adsorption mechanism on unmodified activated carbons
物理吸附在活性炭孔隙内部的H2S分子,在不同的条件下将进一步经历较为复杂的化学转变过程,以达到脱除H2S的目的。溶解在活性炭孔隙中的H2S分子部分解离成HS-后,提高了硫原子的还原性,因此,很容易被O2或其他具有氧化能力的组分[20,72,83-85]将它们氧化成为单质硫、四价S+4甚至六价S+6,显著促进了活性炭对H2S分子的吸附脱除能力,图1显示了其化学转变过程[86]。显然,理解影响吸附在活性炭孔隙中的H2S的化学转变过程与影响因素是掌握活性炭脱除H2S分子机理的主要内容。
研究结果表明,对于没有负载催化剂的活性炭来说,吸附在活性炭表面的H2S分子发生的化学转变及其产物种类主要取决于活性炭表面官能团性质及其含量。当活性炭表面是以酸性官能团为主时,吸附在水膜中的H2S分子离解为HS-离子的数量很少;因此,在温度不太高的情况下,它们通常不能被O2等氧化剂氧化成单质硫或高价硫合物。当活性炭表面是以碱性官能团为主时,如果其表面碱性官能团含量不高、或碱性很弱时,水膜中的HS-离子浓度较低,被氧化成单质硫后将形成高度分散的单质硫,它们容易被进一步氧化成SO2或者SO3,形成亚硫酸或硫酸。如果活性炭表面碱性基团浓度较高,相应地将在活性炭孔隙的水膜内形成较高浓度的HS-离子,氧化形成的较高浓度的S0原子之间相互作用产生聚硫化物[86],通常以稳定的链状或者环状结构出现,如S8分子。由于聚硫化物的氧化比单原子的硫单质困难得多,因此在这种情况下活性炭吸附的H2S分子最终将主要以单质硫的形式存在于孔隙中。值得指出的是,在活性炭吸附脱除H2S的过程中,如果单质硫被氧化成SO2或者SO3后,在水膜中水化将形成H2SO3或H2SO4,提高水膜的酸性,从而阻碍H2S的溶解,抑制吸附过程,降低活性炭脱除能力,使H2S氧化成单质硫的分子数量越来越少。
根据这些机理可以理解,不管是活性炭的孔隙结构、表面化学结构,还是吸附过程中气流的各种化学组分、吸附温度等因素都将影响H2S分子在活性炭孔隙内的吸附能力与化学转变过程,最终影响活性炭脱除H2S的效果。显然,活性炭深度脱除H2S分子,主要来源于H2S分子在活性炭孔隙内的化学吸附,仅仅依靠物理吸附作用,其吸附量很低,这也是普通活性炭的H2S吸附量很低的本质原因。以论述的具有各种性质官能团活性炭吸附脱除H2S的氧化转变机理见图2。

图2 H2S 具有不同性质官能团的未浸渍活性炭上的氧化反应脱除H2S路线Fig. 2 Proposed removal pathways of H2S oxidation on unmodified activated carbon with surface functional groups of different natures
5.2 催化剂的促进作用
根据上述活性炭吸附脱除H2S气体机制可以理解,负载各种金属化合物催化剂可以显著促进活性炭脱除H2S的效果。对于负载碱金属化合物KOH、NaOH、K2CO3和Na2CO3的活性炭,由于这些碱金属化合物,尤其是强碱KOH和NaOH的碱性比较强,能够直接与吸附在活性炭孔隙中的H2S分子反应生成水分,在催化剂位点周围形成局部水膜及强碱性表面,增加了高浓度的HS-和S2-,加快后续的氧化过程,从而促进H2S分子的吸附脱除。其反应过程如图3所示。显然,如果气流具有一定的湿度,将显著加快水膜的形成,促进后续的化学转化步骤。

图3 在干燥状态或非干燥状态下H2S在浸渍活性炭上的吸附Fig. 3 H2S adsorption on modified activated carbon at dry or moisture conditions
上述吸附过程的具体反应式为:
H2S(g)+NaOH(s)-C→HSNa(q)-C+H2O
H2S(g)+2NaOH(s)-C→SNa2(q)-C+2H2O
H2S(g)+CuO(s)-C→SCu(q)-C+H2O
(1)
式中:H2S(g)为干燥状态下H2S气体分子;NaOH(s)-C和CuO(s)-C为活性炭表面催化剂;HSNa(q)-C、SNa2(q)-C和 SCu(q)-C为被水覆盖的反应产物。
H2S(g)+NaOH(q)-C→HSNa(q)-C+H2O
H2S(g)+2NaOH(q)-C→SNa2(q)-C+2H2O
H2S(g)+CuO(q)-C→SCu(q)-C+H2O
(2)
式中,NaOH(q)-C和CuO(q)-C为活性炭表面被水包裹的催化剂。
H2S(q)+NaOH(q)-C→HSNa(q)-C+H2O
H2S(q)+2NaOH(q)-C→SNa2(q)-C+2H2O
H2S(q)+CuO(q)-C→SCu(q)-C+H2O
(3)
式中,H2S(q)为溶解状态下的H2S分子。

对于负载Fe、Co、Ni、Cu等重金属化合物的活性炭,由于它们的氧化物是不同强度的路易斯酸,作为缺电子的金属离子,有利于结合富电子的硫原子,形成难以溶于水的金属硫化物,如图3中铜离子的作用机理。同时,这些缺电子的路易斯酸可能催化HS-和S2-的氧化反应,促进活性炭的吸附脱除能力[87]。另外,重金属化合物也具有较强极性,有利于气流中水分在活性炭表面形成水膜。显然,重金属化合物催化剂具有与碱金属和碱土金属化合物不同的促进机理。对于碱土金属和重金属氧化物在活性炭孔隙内负载的状态,例如这些催化剂的粒度大小与分布,都可能对它们的促进效果产生影响,因此,研究和掌握活性炭结构对负载这些催化剂的影响规律,也是制备高性能深度脱除H2S活性炭的主要方向。另外,在吸附脱除过程中,生成的硫单质可能对催化剂的催化活性产生很大影响,因此,其催化寿命也会明显不同,在选择催化剂种类时需要注意这些问题。
6 展 望
笔者从活性炭、催化剂、吸附脱除工艺条件等几个方面综述了活性炭吸附脱除H2S的影响规律,在此基础上系统评述了活性炭吸附脱除H2S机制,可以看出,活性炭深度脱除H2S气体是一项工艺复杂、影响因素很多的环保技术。从机理方面来看,活性炭吸附脱除H2S是一个以化学吸附和转化为主的过程,包括H2S在活性炭表面的物理吸附、活性炭表面水膜的形成、H2S分子在水膜中的解离与转化。在这一脱除H2S过程中,负载在活性炭中的催化剂起着至关重要的作用。进一步分析得出,活性炭孔隙表面形成水膜是深度脱除H2S的前提,形成碱性水膜或具有较强催化转化能力的表面是关键。通过本综述可有助于理解并掌握活性炭的孔隙结构和化学性质、催化剂、气体的化学组成等是影响活性炭深度脱除H2S效率的主要因素,将为进一步研发高质量的深度脱除H2S用活性炭提供重要参考。
除化工生产和微生物发酵过程外,H2S污染气体主要来源于石油、煤和天然气化石资源中存在的硫元素。毫无疑问,这些化石资源利用过程产生的各种气体中都可能含有不同浓度的H2S气体。因此,活性炭脱除H2S气体是现代煤化工、石油化工和天然气化工的重要技术组成。我国是世界化石资源利用大国,化工产业齐全,H2S气体脱除技术要求高、应用范围广。与其他国家相比,在我国发展先进的活性炭深度脱除H2S气体技术显得尤为重要。我国是世界上最大的活性炭生产和应用国,拥有各种活性炭生产技术,活性炭品种齐全,应用广泛。在H2S深度脱除技术的发展过程中,一方面需要研发较为低廉、脱除H2S能力强的催化剂负载活性炭,进一步优化催化剂的负载方法、提高负载催化剂的活性和寿命,从而降低活性炭的使用成本;另一方面,需要针对实际需求,研发高于200 ℃环境下高温脱除H2S气体的活性炭产品和脱除技术,进一步优化吸附脱除工艺和设备设计,提高脱除效率、降低成本。同时,脱除H2S气体产生的废弃活性炭的利用也需要受到高度重视,防止产生二次污染。总之,活性炭深度脱除H2S不仅是活性炭产业服务于环保、医药、化工和电子等领域的重要技术和活性炭应用的主要发展方向,也是现代化石清洁能源、石油化工、煤化工和天然气化工产业发展的迫切需求,将具有广阔的应用前景。
