基于网络药理学和分子对接探讨健脾益肾方治疗慢性肾脏病的作用机制
2021-11-29卢锦华陈剑平
索 娟,赵 元,卢锦华,陈剑平*
(1.深圳市中医院,广州中医药大学第四临床医学院,广东 518033;2.深圳南粤药业有限公司,广东 518110)
慢性肾脏病(cronic kidney disease,CKD)是各种因素引起的慢性疾病,且其肾脏结构和功能障碍持续3个月以上[1]。目前西医对慢性肾脏病的治疗主要是控制原发病、采取对症处理及减慢其进展速度等。尽管现代医学对该病发病机制研究日益深入,但其临床治疗尚未取得突破性进展。慢性肾脏病属中医“虚劳”、“关格”、“溺毒”等的范畴,其病机以脾肾虚损为本,水湿、湿热、浊毒、瘀血为标,虚实夹杂。脾阳亏损、肾阳衰微,阳不化阴、肾阴耗竭,进而累及心、肝、胃等多个脏器,其病位主要在脾肾[1]。《素问·至真要大论篇》:“诸湿肿满,皆属于脾”,盖脾主运化水液。如其健运失常,津液不得正常流通,则留聚为湿,湿积而成痰。肾主水,肾气不足,膀胱气化不利,水液排泄障碍,亦可聚水成饮,饮凝成痰,终致肾病的发生发展,由此可见,脾肾二脏在痰饮的形成占有举足轻重的地位,故曰:“脾肾相关”,因此,健脾益肾法可用于临床治疗CKD。
健脾益肾方由“玉屏风散”、“四精丸”、“大黄甘草汤”加减而成,包括黄芪、山药(怀)、丹参、白术(生)、肉苁蓉、豆蔻、大黄(生)、甘草(炙)8味中药,具有健脾益肾、通腑泻浊之功。方中黄芪、山药、生白术益气健脾祛湿,白豆蔻温中化湿行气,丹参活血化瘀,大黄通腑泻浊,肉苁蓉补肾壮阳、润肠通便,甘草调和诸药。健脾益肾方是本院的临床协定处方,该方加减用于治疗慢性肾脏病疗效确切,且已在临床运用多年[2-5]。临床研究表明,健脾益肾方可显著提高血液白蛋白含量,显著降低血液中的尿酸、肌酐、尿素以及尿液中的蛋白质含量[2,4];另有研究表明其作用可能与通过NF-κB通路抑制炎症反应[6]、促进线粒体生成、融合,减少线粒体自噬及裂变,改善线粒体的质量控制网络[7]等有关。但具体的活性物质及其作用机制仍不明确。因此,探讨其关键活性成分及其作用机制对临床应用及其进一步的开发都具有积极意义。
1 材料与方法
1.1 健脾益肾方有效活性成分的筛选和靶点的收集 在中药系统药理学数据库和分析平台(https://tcmspw.com/tcmsp.php,TCMSP)和中医药整合药理学研究平台(Integrative Pharmacology-based Research Platform of Traditional Chinese Medicine,TCMIP)v2.0检索健脾益肾方中黄芪、山药、丹参、白术、肉苁蓉、豆蔻、大黄、甘草的化学成分,筛选条件为口服生物利用度(OB)≥30%且类药性(DL)≥0.18;在TCMSP及其Swiss Target Prediction(http://www.swisstargetprediction.ch)网站查询这些活性成分所对应的候选靶标。
1.2 慢性肾脏病疾病靶点的筛选 在人类基因数据库(GeneCards,https://www.genecards.org/)、《人类孟德尔 遗 传》数 据 库(OMIM,https://www.omim.org/)、Drugbank(https://go.drugbank.com/)、疗效药靶数据库(TTD,http://db.idrblab.net/ttd/)中检索慢性肾脏病所对应的靶标,关键词为Chronic kidney disease,将各个数据库所得靶标汇总去重,得到慢性肾脏病的疾病靶标。
1.3 健脾益肾方治疗慢性肾脏病的蛋白互作网络构建 在疾病靶点标准化数据库Uniprot中,将蛋白种属设置为“Homo sapiens(Human)”,获取健脾益肾方及其慢性肾脏病所有靶点的标准基因名。取健脾益肾方与慢性肾脏病候选靶标的交集,即为健脾益肾方治疗慢性肾脏病的靶标。将上述获得的靶标录入String数据库(https://string-db.org/),获得基因间互作关系,随后,将基因关系导入Cytoscape 3.7.1,构建蛋白互作网络。通过Network Analyzer插件选择节点的拓扑特征值中符合度中心性(Degree Centrality)值、接近中心性(Closeness Centrality)值及其中间中心性(Between Centrality)值均大于各自均值的节点为关键靶标。
1.4 GO富集分析和KEGG通路富集分析 将“1.3”中得到的关键靶标通过David数据库进行GO富集分析,并采用R语言进行KEGG通路富集分析,筛选具有统计学意义的条目(P<0.05)。
1.5 “中药-关键活性成分-核心靶标-信号通路”可视化网络构建 将健脾益肾方各味药的候选化合物、关键靶标、相关通路信息导入Cytoscape 3.7.1软件,构建“中药-关键活性成分-核心靶标-信号通路”网络[8],采用Cytoscape插件cytoHubba筛选大于平均自由度到最大自由度的节点作为核心网络节点,以探讨健脾益肾方的整体药理作用。
1.6 关键活性成分与核心靶标的分子对接 选择核心网络节点中主要活性成分与关键靶标进行分子对接。在PDB数据库寻找关键靶标的PDB文件,在TCMSP数据库下载活性成分的mol2文件,利用Auto Dock Vina软件进行分子对接。
2 结果
2.1 健脾益肾方有效活性成分筛选及其靶标收集 健脾益肾方有效活性成分共筛选得到221个活性成分,其中黄芪12个,山药16个,丹参64个,白术6个,肉苁蓉4个,豆蔻9个,大黄15个,甘草85个,黄芪、甘草共有活性成分5个,黄芪、白术共有活性成分1个,黄芪、豆蔻、甘草共有活性成分1个,黄芪、肉苁蓉、甘草、豆蔻共有活性成分1个,丹参、豆蔻共有活性成分1个,肉苁蓉、大黄共有活性成分1个。TCMSP网站中查询得到药物靶标254个,Swiss Target Prediction共查询得到药物靶标154个,剔除重复靶标,共查询得到药物候选靶标254个。
2.2 慢性肾脏病疾病靶点的筛选 在GeneCards数据库中共检索得到14 131个候选靶标、OMIM数据库145个候选靶标、Drugbank数据库178个靶标、TTD数据库26个候选靶标,将各个数据库所得靶标汇总并去除重复靶标,共检索慢性肾脏病所对应的候选靶标14167个。
2.3 健脾益肾方与慢性肾脏病“药物-疾病”交集靶点的筛选及蛋白互作网络的构建 健脾益肾方与慢性肾脏病共249个候选靶标,将其导入String数据库中,设置minimum required interaction score为0.900,去除与其他靶标无关联的孤立靶标共40个,将209个蛋白互作信息导入cytoscape 3.7.1中,其相互作用可视化图如图1所示,其中靶标的节点面积越大代表度值越大;靶标之间的边线越粗代表介数中心性(betweenness)越大。前30位基因之间的作用频次统计见图2。其中蛋白频次前5位的有酶结合基因:淀粉样β前体蛋白(APP)、非受体酪氨酸激酶(SRC)、AKT丝氨酸/苏氨酸激酶1(AKT1)、信号转导和转录激活子3(STAT3),凋亡过程的负调控基因:磷酸肌醇-3-激酶调节亚基1(PIK3R1)。说明这些基因在健脾益肾方治疗慢性肾脏病中发挥着重要作用。

图2 健脾益肾方与慢性肾脏病共有靶标相互作用频次前30位靶标
2.4 GO富集分析与KEGG信号通路富集分析 将图1中的共有靶标网络通过拓扑特征值计算,筛选大于度中心性值、接近中心性值及中间中心性值均值的节点为关键靶标,共32个,包括ESR1、APP、SRC、STAT3、EGFR、PIK3R1、PPARG、AKT1、NCOA1、RELA、PPARA、FOS、CASP3、CDK1、RB1、MAPK8、CCND1、APOB、PSMD3、CDK5、PRKCA、IL6、PCNA、NCOA2、MDM2、F2、VEGFA、HIF1A、NR3C1、AR、CASP8、PTK2。32个关键蛋白靶标的相互作用关系见图3。将“2.3”中得到的32个关键蛋白靶标通过David 6.8数据库进行GO功能注释分析,结果显示共获得具有统计学意义(P<0.01)的413个生物学过程(BP)、61个细胞组分(CC)、128个分子功能(MF)。说明健脾益肾方主要通过调控对药物的反应、凋亡过程的负调控、老化、对乙醇的反应、氧化还原过程、细胞增殖、蛋白质磷酸化、蛋白质自磷酸化、一碳代谢过程及碳酸氢盐运输等生物学过程,作用于胞质溶胶、质膜、核质、细胞外泌体、细胞外空间、蛋白质复合物、突触后膜、不对称突触、膜筏、基底外侧质膜等细胞组分,影响酶结合、碳酸盐脱水酶活性、药物结合、RNA聚合酶Ⅱ转录因子活性,配体激活的序列特异性DNA结合、蛋白激酶活性、类固醇激素受体活性、蛋白激酶结合、相同的蛋白质结合、氧化还原酶活性、蛋白质结合等分子功能。详见图4~6。将“2.3”中得到的32个关键蛋白靶标经信号通路富集最终得到151条调控通路,其中与慢性肾脏病相关的前10位信号通路分别为VEGF信号通路、胰岛素抵抗、PI3K-Akt信号通路、TNF信号通路、FoxO信号通路、HIF-1信号通路、细胞凋亡、ErbB信号通路、甲状腺激素信号通路、IL-17信号通路。见图7。

图1 健脾益肾方与慢性肾脏病共有靶标的蛋白互作网络图

图3 健脾益肾方治疗慢性肾脏病的核心靶标

图4 健脾益肾方治疗慢性肾脏病潜在靶标生物过程的GO分析

图7 健脾益肾方治疗慢性肾脏病排名前10位的KEGG信号通路
2.5“中药-关键活性成分-核心靶点-信号通路”可视化网络的构建 为了更直观地观察健脾益肾方治疗慢性肾脏病的相互作用关系,本研究在Cytoscape软件中构建“中药-关键活性成分-核心靶点-信号通路”网络图,见图8,图中箭头状节点代表药物成分,圆形节点代表靶点,菱形节点代表信号通路,三角形节点代表中药药味。图中共502个节点,平均自由度为12.570,度值最大的靶标为ESR1,度值最大的化合物为槲皮素(MOL000098,quercetin)。取前10位自由度的节点作为核心网络,依次为槲皮素、山柰酚(MOL000422,kaempferol)、木犀草素(MOL000006,luteolin)、雌激素受体1(ESR1)、雄激素受体(AR)、前列腺素-内过氧化物合酶1(PTGS1)、过氧化物酶体增殖物激活受体γ(PPARG)、核受体共激活剂2(NCOA2)、甘 草。结 果 说 明 基 因ESR1、AR、PTGS1、PPARG、NCOA2与健脾益肾方的活性成分关联性最强。文献研究表明,选择性雌激素调节剂雷洛昔芬可调控ESR1表达[9],减轻肾脏纤维化[10],减慢血清肌酐的增加速度,并显著减慢了肾小球滤过率的减少[11]。血管钙化是CKD的常见并发症,是一种炎症性疾病;Pang H等[12]的研究表明,巨噬细胞中沉默AR可抑制无机磷酸盐诱导的人主动脉平滑肌细胞钙化。Verzola D等[13]研究报道,在睾酮存在时,AR调控JNK/c-Jun信号通路的激活,诱导近端小管细胞凋亡,这可能是增加近曲小管细胞凋亡易感性的关键细胞事件。代谢综合征患者中PTGS1水平与CKD患病率有关[14];高血压是CKD的危险因素,而PTGS1和PPARG均为高血压患者中CKD的易感基因[15]。核受体共激活剂可显著增强核受体的转录活性,Zhou T等[16]的研究表明CKD患者血清中NCOA2与NCOA1、NCOA3、缺氧诱导因子-1α及血管内皮生长因子正相关,而VEGF是CKD疾病的危险因素。以上说明经过网络药理学筛选出的关键靶点与CKD的发生发展关系密切;另外,八味药中甘草与其他药味的联系最为紧密,也从侧面印证了甘草调和诸药的功效。见图9。

图8 健脾益肾方治疗慢性肾脏病“中药-关键活性成分-核心靶点-信号通路”可视化网络图
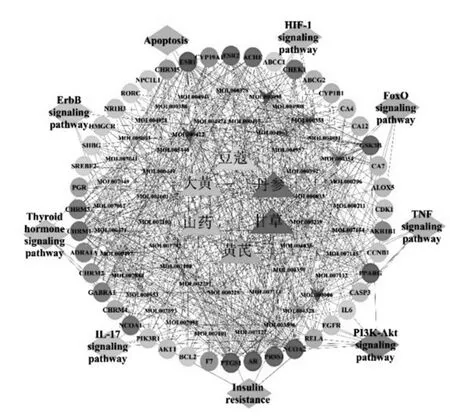
图9 健脾益肾方治疗慢性肾脏病核心网络图
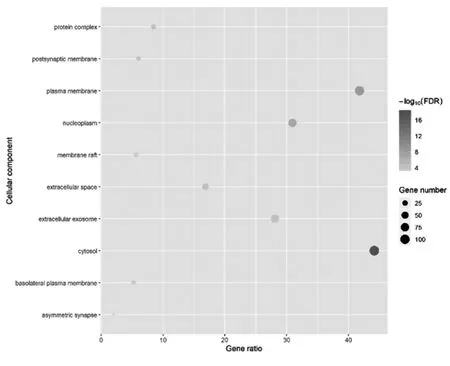
图5 健脾益肾方治疗慢性肾脏病潜在靶标细胞组分的GO分析

图6 健脾益肾方治疗慢性肾脏病潜在靶标分子功能的GO分析
2.6 关键活性成分与核心靶标的分子对接验证 将“2.5”项下所得的活性成分与关键靶标进行分子对接验证,对文中所得的网络药理学数据进行验证。配体与受体结合能越低,结合可能性越大越稳定。见图10和表1。由表1可知,木犀草素和AR得分最高,为-8.5;得分最低的是山柰酚与ESR1,得分-6.9;对接结合能均小于-5.0 kcal/mol[17,18],说明本文筛选出的活性成分与关键靶标的结合活性较好,筛选出的活性成分可能是健脾益肾方发挥抗慢性肾脏病的关键活性成分,健脾益肾方可能通过筛选出的关键靶标发挥治疗慢性肾脏病的作用。
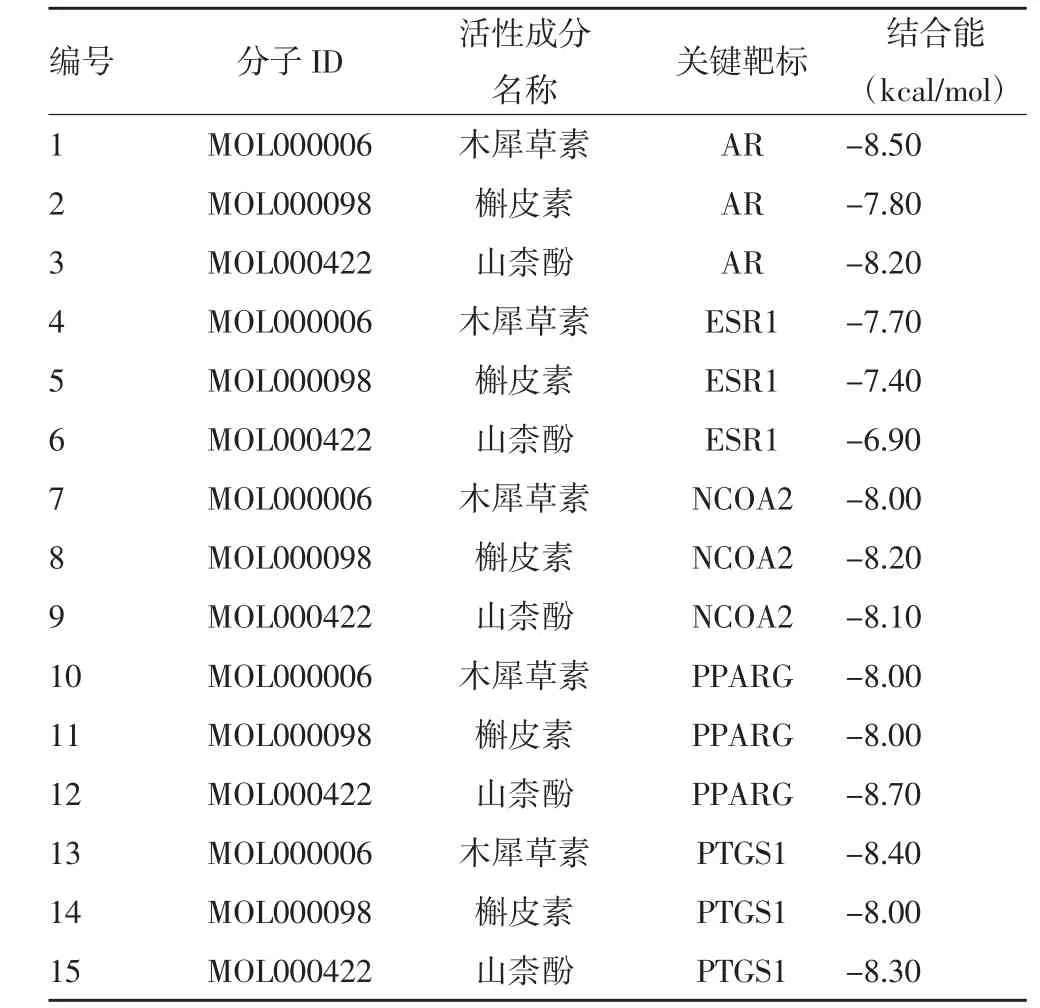
表1 关键活性成分与关键靶标的结合能

图10 关键活性成分与关键靶标的分子对接三维图
3 讨论
中药复方是中医临床治疗疾病的首选方式,但由于其活性成分复杂、作用靶点数目较多及其中药系统调控的特点,传统单一的研究思路并不适用,因此需要寻求合适的研究方法阐释其作用机制。网络药理学就是在这样的背景下应运而生,其通过数据挖掘技术将中药活性成分及其作用靶点、疾病发生发展的靶标、生物信息学等构建“中药-关键活性成分-核心靶标-信号通路”网络。本研究即是探索健脾益肾方与慢性肾脏病的关联性网络,以期全面细致地预测和发现健脾益肾方治疗慢性肾脏病的作用机制。
本研究通过网络数据库的筛选,共得到221个活性成分,其中122个活性成分可能与慢性肾脏病有关,其中槲皮素、山柰酚、木犀草素可能发挥关键性作用。研究表明槲皮素可通过降低血糖、抗氧化应激、抗炎及抑制肾脏纤维化等机制对肾脏起保护作用[19,20]。山柰酚通过阻断转化生长因子和炎性细胞因子的激活,进而降解肾脏组织中细胞外基质积聚而改善肾脏纤维化疾病[21]。木犀草素可通过激活抗氧化蛋白及抗氧化酶的表达,清除ROS,反馈性抑制NF-KB通路,保护肾脏系膜细胞[22]。
健脾益肾方与慢性肾脏病的249个共有靶标中,共筛选出大于度中心性值、接近中心性值及中间中心性值均值的节点为关键靶标32个,包括ESR1、APP、SRC等。对关键靶标进行GO功能分析及KEGG信号通路富集分析,得出了健脾益肾方治疗慢性肾脏病可能的生物过程、调控的分子功能、作用的细胞组分及调控的信号通路信息;根据网络药理学的分析结果及现有文献研究成果,健脾益肾方治疗慢性肾脏病可能与改善组织局部血供(HIF-1 signaling pathway)、促进血管生成(VEGF signaling pathway)、改善氧化应激状态(FoxO signaling pathway)、调节慢性炎症(IL-17 signaling pathway、TNF signaling pathway)、改善甲状腺激素水平(thyroid hormone signaling pathway)、改善慢性肾脏病的胰岛素抵抗(insulin resistance、PI3KAkt signaling pathway)、抑制慢性肾脏病细胞凋亡(apoptosis、ErbB signaling pathway)有关。例如,减少血管内皮生长因子(VEGF)的表达在慢性肾脏疾病中起着至关重要的作用,HIF-1α可能参与慢性肾脏病的进展,可作为评价CKD的指标之一[23]。He Y等[24]的研究表明,姜黄素通过阻断mTOR/HIF-1α/VEGF信号通路的激活而具有肾脏保护作用。CKD主要致病因素白蛋白通过改变缺氧诱导因子(HIF)/缺氧反应元件途径抑制血管内皮生长因子[25]。研究表明,肾纤维化是具有各种病因的进行性慢性肾脏疾病的常见病理标志,抗缺氧作用的新有效疗法可减轻肾脏纤维化并抑制CKD的进展[26]。氧化应激的增加和抗氧化能力的下降亦与肾功能减退相关[27]。激活FoxO信号通路可抑制肾间质纤维化和氧化应激[28]。Mehrotra P等[29]的研究表明,IL-17可能通过募集中性粒细胞参与AKI诱导的纤维化的发病。王妮妮[30]研究表明,慢性肾脏病是甲状腺功能减退的高危因素,甲状腺功能减退又可加速肾脏病变进展、增加CKD患者全因死亡率和心血管疾病发生风险。研究亦表明,慢性肾脏病患者常出现胰岛素抵抗,胰岛素抵抗既是CKD致病因素,又是其进展的机制之一[31],可导致肾脏疾病的进展及代谢紊乱,因此改善胰岛素抵抗可能是降低慢性肾脏病患者心血管病死率的重要治疗靶点[32]。
本文建立了“中药-关键活性成分-核心靶标-信号通路”相互作用网络图,并筛选了健脾益肾方治疗慢性肾脏病核心网络图,结果显示活性成分槲皮素、山柰酚、木犀草素及关键靶标ESR1、AR、PTGS1、PPARG、NCOA2在核心网络中发挥重要作用;而且分子对接结果同样显示这些活性成分与关键靶标的对接得分均小于-5.0 kcal/mol,对接活性良好。说明本研究通过网络药理学筛选出的活性成分可以作为健脾益肾方治疗慢性肾脏病的关键活性成分,亦说明了中药复方治疗疾病时,多成分作用于多靶点的系统调控特点。
综上所述,本研究通过网络药理学的方法分析了健脾益肾方治疗慢性肾脏病可能的作用靶标及途径,建立了“中药-关键活性成分-核心靶标-信号通路”相互作用网络图,揭示了健脾益肾方治疗慢性肾脏病的多维调控网络,说明健脾益肾方中多种活性成分具有调节慢性肾脏病的功能,且可通过多种信号通路发挥作用,最终达到调节慢性肾脏病的作用,为健脾益肾方的进一步开发利用提供参考。本研究是基于网络大数据所做的预测,研究结果还需要通过进一步的实验研究加以验证。
