重组人肠道病毒71 型病毒样颗粒等电点全柱成像毛细管等电聚焦电泳测定方法的建立及验证
2021-11-26王文伟何成王蓓楼觉人
王文伟,何成,王蓓,楼觉人,
1. 上海至成生物科技有限公司,上海 200051;2. 上海生物制品研究所有限责任公司,上海 200051
等电点(isoelectric point,pI)是蛋白质的一种物理化学属性,在一定的pH 条件下,蛋白质的氨基酸分子所带的正、负电荷相等,即净电荷为零,此时的pH 称为该蛋白质的pI[1]。pI 的测定能够反映蛋白药物的电荷异质性,广泛应用于重组蛋白药物的质量评价,是重组蛋白药物质量控制的一个重要手段[2-4]。
等电聚焦(isoelectric focusing,IEF)电泳是测定蛋白质pI 的常用方法,包括凝胶等电聚焦(gelbased isoelectric focusing,gIEF)电泳、毛细管等电聚焦(capillary isoelectric focusing,CIEF)电泳和全柱成像毛细管等电聚焦(whole column imaging detectioncapillary isoelectric focusing,WCID-CIEF)电泳。IEF 的基本原理是:两性电解质在电场下形成一个pH 梯度,当待测样品迁移至某一pH 位置时,其所带的净电荷为零,不再移动,则该处的pH 值即为样品的pI[5-6]。gIEF 所能分离的分子量范围较小,分辨率低,准确度差,无法满足重组病毒样颗粒(virus-like particles,VLPs)等生物大分子pI 的测定。传统的CIEF 在聚焦完成后,需将样品区带迁移至检测窗口,在迁移过程中易导致蛋白质聚集或沉淀,谱带展宽,从而影响分离度和分辨率。WCID-CIEF 克服了传统CIEF 的不足,聚焦完成后无需进行样品迁移,聚焦和检测能够同步完成,广泛应用于重组蛋白药物pI 的测定和电荷异质性的分析[7-10]。
重组人肠道病毒71 型(enterovirus 71,EV71)VLPs由病毒的衣壳蛋白VP0、VP1 和VP3 组装而成,直径约30 nm[11-12],结构复杂,分子量大(约5 660 000),目前鲜有对重组EV71 VLPs pI 研究的报道。本研究旨在建立重组人EV71 VLPs pI WCID-CIEF 测定方法,并对方法进行验证。
1 材料与方法
1. 1 样品 重组人EV71 VLPs 采用巴斯德毕赤酵母表达,由上海至成生物科技有限公司制备。
1. 2 主要试剂及仪器 两性电解质Pharmalyte pH 3-10 购自美国GE 公司;尿素购自国药集团化学试剂有限公司;0. 5%甲基纤维素、1%甲基纤维素、阴阳极电解液、pI marker(4.05、5.85、7.05 和8. 40)、Maurice CIEF 毛细管卡盒和Maurice 毛细管电泳仪均购自美国Protein simple 公司。
1. 3 样品处理 重组人EV71 VLPs 经0.22 μm 滤膜过滤后,用双蒸水稀释5 倍。取两性电解质Pharmalyte pH3-10 4 μL,1%甲基纤维素35 μL,4. 05 和8. 40 的pI marker 各1 μL,双蒸水39 μL,稀释后的EV71 VLPs 20 μL,置涡旋混匀器中充分混合均匀,1 000 × g 离心5 min,吸取90 μL 转移至96 孔样品板中,盖上盖板,4 ℃,1 000 × g 离心5 min。
1. 4 WCID-CIEF 采用预制Maurice CIEF 毛细管卡盒,卡盒内的毛细管内壁为氟碳涂层,内径100 μm,有效长度5 cm。阳极液为含0. 1%甲基纤维素的80 mmol / L 磷酸,阴极液为含0. 1%甲基纤维素的100 mmol / L 氢氧化钠,待测样品采用真空进样,进样时间为55 s。毛细管等电聚焦过程参数设置为:1 500 V 预聚焦1 min,3 000 V 聚焦5 min,检测波长280 nm。
1. 5 聚焦时间的优化 按照1.4 项进行WCID-CIEF,聚焦过程中Maurice 电泳仪会进行实时监测,每隔10 s 采集1 次数据,比较不同聚焦时间下重组人EV71 VLPs 的聚焦效果,选择合适的聚焦时间。
1. 6 尿素浓度对重组人EV71 VLPs 分离效果影响的检测 样品混合液中添加8 mol / L 尿素,设置终浓度为0、1、2 mol / L 3 个尿素浓度梯度,按照1. 4 项分别进行WCID-CIEF,比较不同尿素浓度对重组人EV71 VLPs 分离效果的影响。
1. 7 方法的验证
1. 7. 1 专属性 将空白制剂组分(空白缓冲液)和重组人EV71 VLPs 分别作为待测样品,按照1. 4 项分别进行WCID-CIEF。
1. 7. 2 准确度 将pI marker 5.85 和pI marker 7.05分别作为待测样品,按照1.4 项分别进行WCID-CIEF,测定pI marker 的pI,每个pI marker 重复测定6 次,计算6 次结果的相对标准偏差(relative standard deviation,RSD)及6 次结果的平均值与理论值的相对偏差。
RSD(%)= 测定结果的标准偏差/ 测定结果的算术平均值× 100%;
平均值与理论值的相对偏差=|测定结果的算术平均值-理论值| / 理论值× 100%
1. 7. 3 重复性 将重组人EV71 VLPs 作为待测样品,按照1. 4 项进行WCID-CIEF,测定EV71 VLPs的pI,重复测定6 次,计算6 次结果的RSD。
1. 7. 4 中间精密度 将重组人EV71 VLPs 作为待测样品,在不同日期,由不同实验人员按照1. 4 项进行WCID-CIEF,测定EV71 VLPs 的pI,分别重复测定6 次,计算12 次结果的RSD。
2 结 果
2. 1 聚焦时间的优化 3 000 V 聚焦1 min,重组人EV71 VLPs、pI marker 4. 05 和pI marker 8. 40 均未完成聚焦;3 000 V 聚焦2 min,pI marker 4. 05 聚焦完成;3 000 V 聚焦3 min,pI marker 8. 40 聚焦完成;3 000 V 聚焦4 ~5 min,图谱不再变化,表明重组人EV71 VLPs 聚焦完成。见图1。选择3 000 V聚焦5 min 作为后续试验的聚焦条件。
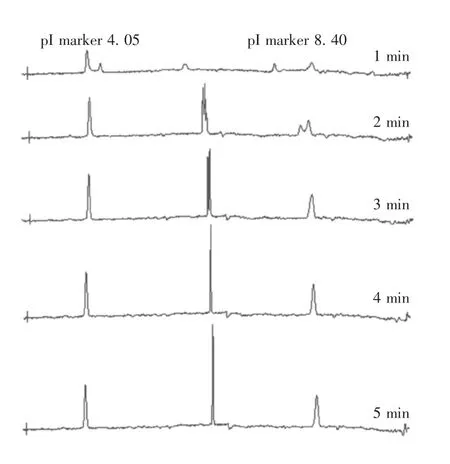
图1 聚焦时间对重组人EV71 VLPs 分离效果的影响Fig. 1 Effect of focusing time on separation of recombinant human EV71 VLPs
2. 2 尿素浓度对重组人EV71 VLPs 聚焦效果的影响 在0、1、2 mol / L 3 个尿素浓度条件下,重组人EV71 VLPs 的等电聚焦图谱基本一致,表明尿素浓度对重组人EV71 VLPs 的分离效果影响不大,见图2。因此选择重组人EV71 VLPs 样品处理时不添加尿素。

图2 尿素浓度对重组人EV71 VLPs 分离效果的影响Fig. 2 Effect of urea concentration on separation of recombinant human EV71 VLPs
2. 3 方法的验证
2. 3. 1 专属性 空白制剂组分在pI marker 4. 05和pI marker 8. 40 之间无紫外吸收峰,而重组人EV71 VLPs 有特异紫外吸收峰,表明空白缓冲液对重组人EV71 VLPs pI 的测定无干扰,方法的专属性良好。见图3。
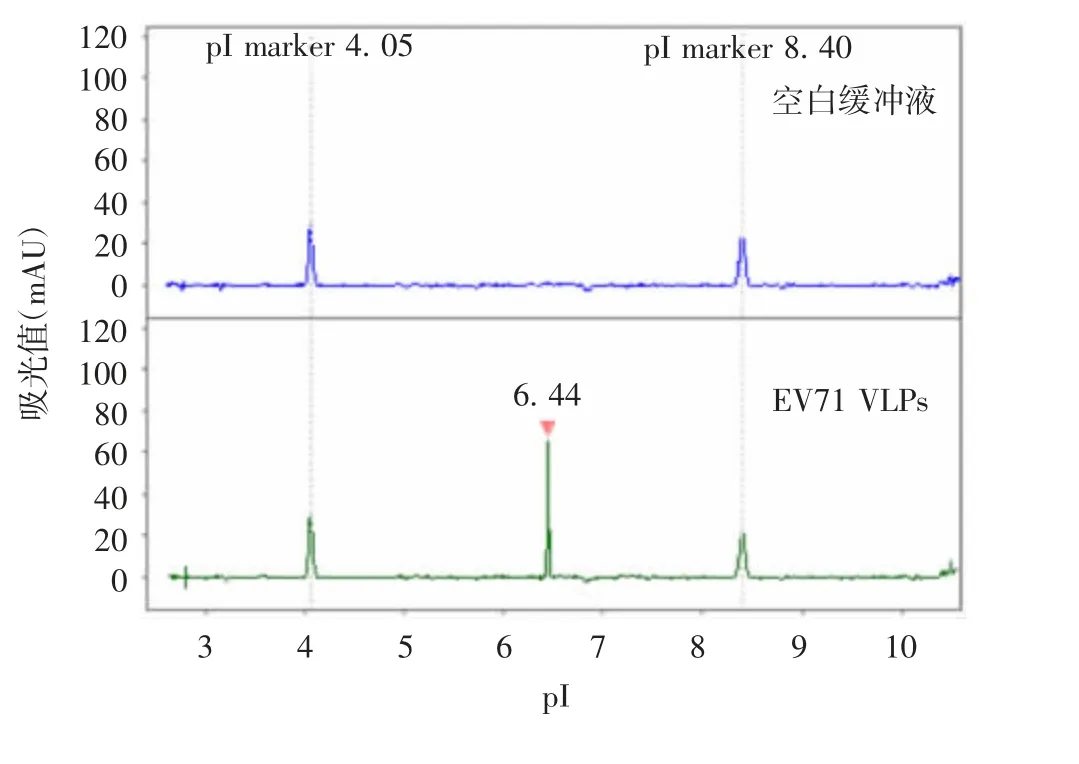
图3 方法的专属性验证Fig. 3 Verification for specificity of WCID-CIEF electrophoresis
2. 3. 2 准确度 pI marker 5. 85 作为待测样品,6次重复测定结果的平均值为5. 81,RSD 为0. 18%,6 次重复测定结果的平均值与理论值的相对偏差为0. 63%;pI marker 7. 05 作为待测样品,6 次重复测定结果的平均值为7. 16,RSD 为0. 06%,6 次重复测定结果的平均值与理论值的相对偏差为1. 54%。表明方法的准确度良好。见表1。
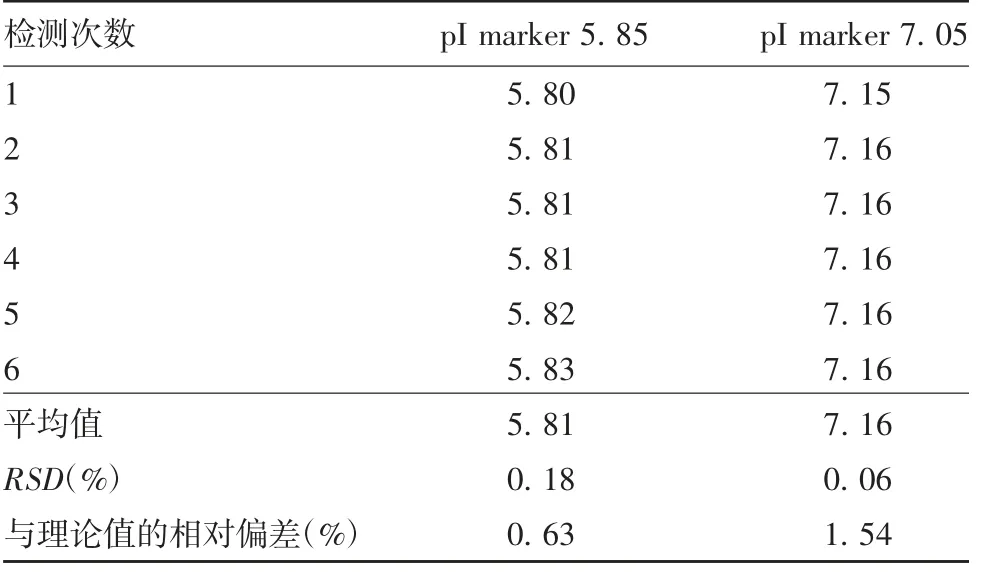
表1 方法的准确度验证结果(pI)Tab.1 Verification for accuracy of WCID-CIEF electrophoresis(pI)
2. 3. 3 重复性 重组人EV71 VLPs pI 6 次重复测定结果的平均值为6. 47,RSD 为0. 08%,表明方法的重复性良好,见表2。

表2 方法的重复性验证结果Tab. 2 Verification for reproducibility of WCID-CIEF electrophoresis
2. 3. 4 中间精密度 不同实验人员在不同日期对重组人EV71 VLPs pI 12 次重复测定的平均值为6. 46,RSD 为0. 14%,表明方法的中间精密度良好,见表3。
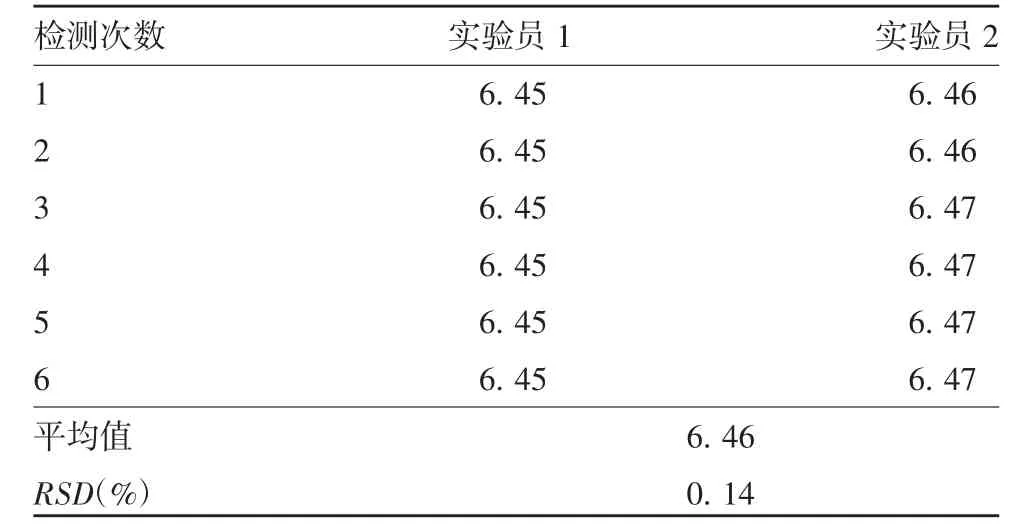
表3 方法的中间精密度验证结果(pI)Tab. 3 Verification for intermediate precision of WCID-CIEF electrophoresis(pI)
3 讨 论
WCID-CIEF 是20 世纪90 年代发展起来的一项检测技术,其将成像技术和CIEF 结合在一起,通过基于电荷耦合元件(charge-coupled device,CCD)或互补金属氧化物半导体(complementary metal-oxidesemiconductor,CMOS)的成像装置对整个毛细管柱内的分离过程进行动态跟踪成像[13],可实时观察样品的等电聚焦过程,整个过程中无需进行样品迁移,一次检测即可完成对样品聚焦时间的优化,大大节约了方法开发所需时间。由于省略了复杂的样品迁移过程,WCID-CIEF 与传统的CIEF 相比,具有分析时间短(通常<10 min)、准确度高、重复性好等优点,可实现高通量检测,尤其适合重组蛋白等复杂的生物大分子药物pI 的精确测定。目前,WCID-CIEF已成功应用于重组人乳头瘤病毒(human papillomavirus,HPV)、诺如病毒(Norovirus,NV)和乙型肝炎病毒(hepatitis B virus,HBV)VLPs pI 的测定[14-16]。
本研究采用WCID-CIEF 技术测定重组人EV71 VLPs 的pI,考察了聚焦时间和尿素浓度对重组人EV71 VLPs pI 检测的影响,结果表明,在3 000 V 电压下,重组人EV71 VLPs 在4 ~5 min 即可完成聚焦,添加1 ~2 mol / L 尿素对重组人EV71 VLPs 的分离效果基本无影响。因此,EV71 VLPs pI 检测方法确定为:4% Pharmalyte pH3-10,0. 35%甲基纤维素,1% pI marker(4. 05 和8. 40),1 500 V 预聚焦1 min,3 000 V 聚焦5 min。方法的验证结果显示,该方法专属性、准确度、重复性和中间精密度良好。重组人EV71 VLPs 的实测pI 为6. 46(n = 12,RSD =0. 14%),与其理论pI(6. 08)相差0. 38 个pH 单位,实测值和理论值基本一致。
综上所述,本研究建立了重组人EV71 VLPs pI的WCID-CIEF 测定方法,为EV71 VLPs 的质量评价提够了有效手段。
