快速冻融睾丸精子在无精子症患者中应用的潜在影响
2021-11-26赵激浪欧阳杰王田田罗沛琦陆诗佳
董 竞 赵激浪 欧阳杰 张 伟 马 猛 王田田 罗沛琦 陆诗佳 彭 惠 李 斌
无精子症的患病率在男性人群中约为1%,在不育男性人群中约为10%~15%[1]。胞质内单精子注射(intracytoplasmic sperm injection,ICSI)技术的引入开启了无精子症患者治疗的新纪元[2]。睾丸精子提取(testicular sperm extraction,TESE)和ICSI的结合成为无精症男性的有效治疗手段[3,4]。虽然无精子症患者可以在配偶取卵日进行睾丸穿刺手术后直接行新鲜睾丸精子ICSI,但是即使诊断性睾穿时有活动精子存在,再次重复进行的TESE也不能确保取卵日可以得到可用活动精子[5]。因此,睾丸精子的提前冷冻保存是非常有必要的。睾丸精子的提前冻存可以避免因取精失败导致的ICSI周期取消和再次ICSI周期的重复睾丸活检[6,7]。
无精子症患者通过手术获取的少量精子极其珍贵,常规精液冷冻保存程序中离心和清洗不仅会导致精子的丢失而且容易造成精子损伤。研究显示,常规精液冷冻睾丸精子的复苏回收率只有1%[8]。TESE获得的精子头部DNA不够稳定,细胞膜也未完全成熟,常规方式冷冻精子复苏率低[9]。本研究采用快速微量精子冷冻方法,避免了常规冷冻程序中离心洗涤造成的精子丢失。已有研究表明对于稀少精子使用快速精子冷冻法冷冻保存非常有效[10,11]。
当前,关于冻融睾丸精子在临床上的应用效果尚未达成一致。一些研究发现,冻融睾丸精子行ICSI后的受精率显著低于新鲜睾丸精子,并且种植率和活产率也显著降低[12,13]。Madureira等[14]研究也发现,新鲜睾丸精子注射后的受精率和临床妊娠率比冻融睾丸精子更高。但是,也有研究者报道睾丸精子冷冻保存不会损害活动精子的可用性,冻融睾丸精子与新鲜睾丸精子ICSI的结局比较,差异无统计学意义[15~17]。甚至还有研究报道了冻融睾丸精子行ICSI的妊娠率和着床率显著优于新鲜睾丸精子[18]。除此之外,女方因素也是影响无精子症治疗成功与否的重要因素,而现有的研究却常常忽略了其潜在影响[17]。
基于上述可能存在的问题,本研究将通过倾向性评分匹配法消除两组女方因素差异的条件下,对比分析快速冻融睾丸精子组和新鲜睾丸精子组的无精子症患者的临床治疗结局,进一步确认快速冷冻保存的睾丸精子在辅助生殖治疗中的应用是否会给患者的临床妊娠带来不利影响。
对象与方法
1.研究对象:回顾性分析了用倾向性评分匹配法收集的272例睾丸精子抽吸术(testicular sperm aspiration,TESA)取精后行ICSI的无精子症患者:新鲜睾丸精子组(对照组)为136例取卵日用新鲜睾丸精子行ICSI的患者;快速冻融睾丸精子组(研究组)为136例取卵日使用冻融睾丸精子行ICSI的患者,其在进行诊断性睾穿时,使用快速微量精子冷冻法提前对睾丸精子进行了冷冻保存。患者纳入标准:①首次体外受精(in vitro fertilization,IVF)周期患者;②女方年龄<43岁;③基础卵泡刺激素(follicle stimulating hormone,FSH)<10;④窦卵泡数≥5;⑤男方在TESA前均进行多次的精液常规检查,并经精液离心沉淀证实为无精子症,且经诊断性睾穿证实睾丸内存在成熟精子。遗传分析显示,所有患者的核型均正常。排除标准:①夫妇双方先天性或遗传性疾病;②女方有明显宫腔畸形;③严重的内外科系统性疾病不适宜接受促排卵治疗及不能耐受妊娠患者。对照组与研究组根据年龄、不孕年限和体重指数等基本资料进行1∶1倾向性评分匹配[19]。倾向性评分匹配是一种工具,由Rosenbaum和Rubin于1983年首次提出,用于调整非随机研究中被测混杂因素的治疗效果,可以有效降低混杂偏倚,并且在整个研究设计阶段,得到类似随机对照研究的效果[20,21]。本研究严格遵守《赫尔辛基宣言》并得到医院医学伦理学委员会的审核和批准,参与对象均签署知情同意书。
2.超促排卵及取卵:本研究未对不孕症患者的促排卵方案做限定,所用方案包括:孕激素方案、拮抗剂方案、长方案、短方案、微刺激和黄体期促排[22,23]。简言之,卵泡期促排的患者从月经周期的第3~5天开始促排;黄体期促排的患者则在排卵后的第1~3天,对卵泡<8mm的患者开始促排。当有1个以上卵泡的直径达到20mm或者3个以上的卵泡直径达到18mm以上时扳机,扳机34~36h后在阴道超声引导下行取卵术。
3.TESA:取男性患者截石位,会阴部常规消毒、铺巾。用2%利多卡因注射液约2ml对术侧阴囊行精索封闭。麻醉起效后,以阴囊皮肤无血管分布区作为穿刺点,在睾丸实质内钳取适量睾丸组织,置于添加了10%血清的配子准备液(modified HTF medium,MHTF,美国Irvine Scientific公司)中,在解剖显微镜下用无菌BD注射器针头将睾丸组织撕碎,倒置显微镜下观察有无活动精子。如有活动精子则行微量精子快速冷冻,在取卵日解冻行ICSI;若采用新鲜睾丸精子行ICSI,如上方法操作,倒置显微镜下观察到有活动精子后,用配子准备液MHTF洗涤离心,留取沉淀,置于室温下备用。
4.睾丸精子快速冷冻与复苏:本研究中采用Strawtop快速微量精子冻融法进行睾丸精子的冷冻保存。简言之,即将等量的精子冷冻保护剂(丹麦Origio公司)逐滴加入含有精子的睾丸组织悬液中,每加1滴后都小心将溶液混匀,室温放置10min。精子冷冻管(法国CBS公司)的一端剪出开放性的凹槽,将混合样品移入该凹槽中(约50微升/支)。将精子冷冻管在1min内由液氮表面约50cm处缓慢降低至刚刚离开液氮表面,然后保持直至观察到冷冻溶液凝固后装入冷冻支架,投入液氮罐进行保存。取卵日,从液氮罐中取出相应的精子冷冻管,将盛有精子的一端浸入37℃预温的油中待液滴溶解后,将其移入精子操作滴内,备后续ICSI操作。
5.授精、胚胎培养与观察:所有患者行常规ICSI授精后约16~18h观察受精情况,72h观察胚胎卵裂情况。采用Cummins′标准对第3天胚胎进行评级[24]。其中Ⅰ级和Ⅱ级胚胎作为优质胚胎进行冷冻保存;Ⅲ级和Ⅳ级胚胎继续培养至囊胚期。囊胚采用Gardner和Schoolcraft评分系统进行评级。胚胎冷冻根据既有方法采用Cryotop进行[25]。
6.胚胎移植与妊娠结果判断:笔者医院常规采用冻融胚胎移植(frozen-thawed embryo transfer,FET),胚胎移植的内膜准备主要有自然周期、微刺激和激素替代3种方式,均按常规进行[22]。胚胎移植操作均在超声监测下进行,移植后14天行尿hCG检测,阳性为生化妊娠,再经14天行阴道超声检查,见孕囊者为临床妊娠。
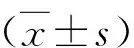
结 果
1.患者基本资料:经过倾向性评分匹配后共入选272例患者,其中研究组和对照组各136例。匹配后两组患者的年龄、不孕年限、体重指数、基础FSH、基础黄体生成素(luteinizing hormone,LH)和成熟卵数等基本资料比较,差异均无统计学意义(P>0.05,表1)。
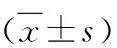
表1 患者的基本资料
2.睾丸精子快速冻融对胚胎早期发育的影响:两组中患者的异常受精率、优胚率、有效囊胚形成率和卵子利用率比较,差异无统计学意义(P>0.05),但研究组中患者的受精率和正常受精率显著低于对照组(P<0.05),详见表2。
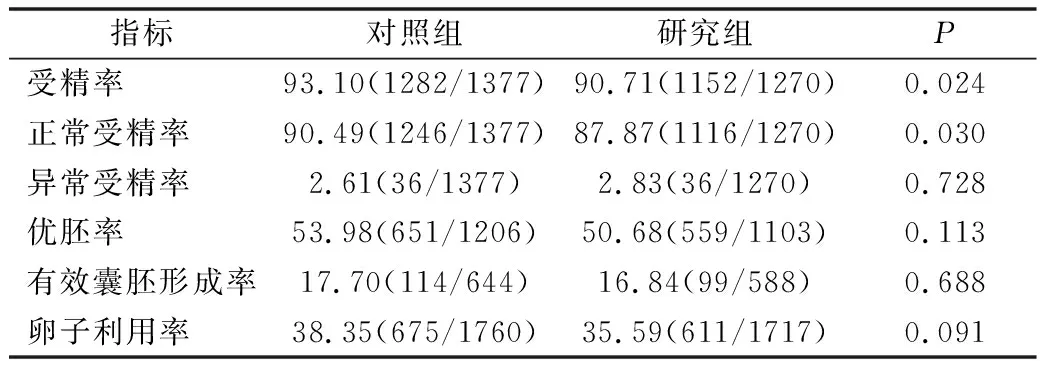
表2 睾丸精子快速冻融对胚胎早期发育的影响 [%(n/N)]
3.睾丸精子快速冻融对患者妊娠结局的影响:研究组和对照组的患者在临床妊娠率、宫外孕率、流产率、种植率、活产率、早产率、累积活产率、孕周等方面比较,差异均无统计学意义(P>0.05)。研究组中新生儿的出生体重和出生缺陷率与对照组比较,差异无统计学意义(P>0.05),详见表3。
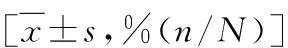
表3 睾丸精子快速冻融对患者妊娠结局的影响
讨 论
随着辅助生殖技术的发展,传统意义的无精子症患者可以通过经睾丸或附睾穿刺取精,再联合ICSI技术实现正常生育。然而30%~50%的非梗阻性无精子症患者的睾丸组织中没有精子[26]。目前也没有可靠的术前指标可以有效预测睾丸穿刺手术能否获得可用精子[27]。由于生精小管中的精子分布不均,即使是先前的睾丸活检也没有统计学意义的预测价值[28]。冷冻保存睾丸精子可以将取卵手术和睾丸活检手术分割开来,可有效避免因无可用精子导致周期取消。但是,无精子症患者通过手术获取的精子通常很少,常规精液冷冻保存程序中离心和清洗会导致精子的回收率和复苏率低[8,9]。精子快速冷冻法由于快速越过冰晶形成的温度,且省去了离心的步骤,可最大限度保存精子。但是,目前关于使用冻融睾丸精子行ICSI后的治疗结果尚存在一些问题,有研究发现,使用冻融或新鲜睾丸精子可以获得相似的受精率、种植率和临床妊娠率[15]。另有研究发现,使用冻融精子会损害睾丸精子的受精能力,并引起种植率和活产率降低[12]。
基于上述的这些争议,我们有必要进一步确认快速冷冻保存的睾丸精子在辅助生殖治疗中的应用是否会给患者的临床妊娠带来不利影响。在本研究中,通过对快速冻融睾丸精子组与新鲜睾丸精子组的治疗结果进行比较,笔者发现快速冻融睾丸精子组中患者的受精率和正常受精率显著性低于新鲜睾丸精子组(分别为90.71% vs 93.10%,87.87% vs 90.49%,P<0.05)。
De Croo等[12]和Madureira等[14]采用麦管液氮蒸汽熏蒸法冷冻睾丸精子的研究也发现,冻融睾丸精子获得的受精率低于新鲜睾丸精子获得的受精率。笔者推测潜在的原因可能是:(1)由于睾丸精子不成熟,冻融会导致部分精子活动力和受精能力下降[13]。(2)冷冻、解冻和冷冻保护剂暴露期间精子的结构和功能会发生显著变化,精子的冻结可引起精子顶内膜和质膜的膨胀和破裂。(3)在冷却和解冻过程中,氧自由基的产生均增加,导致继发于质膜脂质过氧化的自由基损伤。除此之外,笔者的研究结果显示,快速冻融睾丸精子组的患者可以获得与新鲜睾丸精子组患者相似的优胚率(50.68% vs 53.98%)、卵子利用率(35.59% vs 38.35%)、临床妊娠率(60.57% vs 58.51%)及活产率(54.29% vs 49.47%)比较,差异无统计学意义(P>0.05),这与既往研究结果相一致[15]。本研究结果提示,虽然快速冻融睾丸精子可能导致了精子受精能力的下降,但并没有进一步影响受精后合子的早期发育。
为了进一步确认快速冻融睾丸精子的应用是否会给患者的子代带来潜在的影响,笔者详细分析比较了两组患者的多种临床妊娠指标。研究结果显示,患者行FET后的宫外孕率、流产率和早产率等指标比较,差异均无统计学意义(1.89% vs 0.91%,8.49% vs 14.55%,18.95% vs 15.05%,P>0.05),提示睾丸精子的快速冻融不会增加不良的产科结局。此外,进一步比较两组的新生儿情况,结果显示,两组中新生儿的出生孕周和出生体重均没有显著区别(38.08±2.10周 vs 37.91±2.34周,2999.88±611.00g vs 2980.00±605.19g,P>0.05)。两组中新生儿的先天缺陷发生率比较,差异也无统计学意义(P>0.05),其中快速冻融睾丸精子组中出现了5例先天缺陷的新生儿,新鲜睾丸精子组中未发现有先天缺陷的新生儿。已有报道显示,正常受孕情况下发现的先天畸形率,加拿大约为4.2%、南澳大利亚州约为5.8%。与此相比,研究组中新生儿的出生缺陷率(4.10%)处在正常水平,并没有增加。因此,本研究结果提示,快速冻融睾丸精子行ICSI是一种简便且安全的无精子症男性不育患者的临床治疗方案,通过手术取精获得的精子都应考虑提前冷冻保存,即使对于只取出很少精子的患者也是建议的。
临床治疗无精子症患者时,TESA-ICSI的治疗结局可能会受到男女双方多种因素的影响,如男方因素(年龄、精子质量等)和女方因素(如年龄、卵巢储备等)。现有的研究常常忽略了女方因素的影响[17]。针对此问题,本研究采用了倾向性评分匹配法控制了女性人群特征数据的影响,包括女方年龄、不孕年限、体重指数、基础激素水平、获卵数等。当然,本研究也存在不足:本研究是一个单中心的回顾性研究,虽然笔者用倾向性评分匹配来尽量消除组间可能存在的差异,但回顾性偏倚仍不能完全避免。活产和子代安全是评估不同治疗方法的金标准,但它涵盖两个周期(取卵和移植),包含了很多混淆因素。今后笔者将继续积累相关数据并在研究设计上优化,进一步在更单纯的背景和更多的样本量下进行分析研究,给临床诊疗提供更精准的信息。条件成熟时,也将考虑开展RCT的研究,以期得到更高质量的研究结果。
综上所述,虽然快速冻融睾丸精子与新鲜睾丸精子行ICSI的受精率有显著性差异,但是受精后合子的早期发育,移植后的临床妊娠率、活产率以及子代出生孕周、体重和先天缺陷率比较,差异均无统计学意义。快速冻融睾丸精子行ICSI可以获得和新鲜睾丸精子相似的临床结局,睾丸精子的微量快速冷冻是一种简便且安全的无精子症男性不育患者的临床治疗方案,可避免患者的反复睾丸活检,有利于患者临床治疗的安排。
