高效液相色谱-串联质谱法测定电子烟烟液及气溶胶中4种烟草特有N-亚硝胺类化合物
2021-11-25王天南汪阳忠
王天南,汪阳忠,刘 鸿,陈 敏,费 婷,吴 达
(上海烟草集团有限责任公司 技术中心,上海 201315)
烟草特有N-亚硝胺类化合物(TSNAs)是由烟草内源性生物碱与硝酸盐或亚硝酸盐通过亚硝化作用产生的,其中研究较多的为N-亚硝基去甲基烟碱(NNN)、N-亚硝基假木贼碱(NAB)、N-亚硝基新烟草碱(NAT)和4-(N-甲基-N-亚硝胺)-1-(3-吡啶基)-丁酮(NNK)[1]。TSNAs是烟草及烟草制品中的重要致癌物质,会引起肺部、口腔、食道、胰脏、肝脏等部位形成肿瘤[2],其中NNK 和NNN 已被国际癌症研究机构(IARC)列为强致癌物[3]。电子烟又叫做电子烟碱传送系统,是一种新型烟草制品[4],由于其避免了传统烟丝的燃烧过程,且烟液成分相对简单,有害成分的释放量与传统卷烟相比大大减少[5]。但是,多数电子烟为了保持卷烟口感,会在烟液中添加烟草提取物,从而引入了TSNAs,因此有必要对电子烟烟液及其抽吸产生的气溶胶中TSNAs含量进行测定[6-7]。
目前传统卷烟主流烟气中TSNAs的检测方法已相对成熟,常用方法有气相色谱-热能分析法(GC-TEA)[8-9]、气相色谱-质谱法(GC-MS)[10-11]以及液相色谱-串联质谱法(LC-MS/MS)[12-16]等。GC-TEA 灵敏度高、选择性强,但是不能有效区分TSNAs[13],且存在样品纯化步骤多,分析时间长等不足[14]。GC-MS一般用于分析TSNAs含量较高的烟叶、烟丝或烟气样品,无法满足痕量TSNAs的检测需求[13]。LC-MS/MS 具有高选择性、高灵敏度的优点,逐渐成为测定传统卷烟主流烟气TSNAs的重要方法。但是由于电子烟烟液及气溶胶中TSNAs含量极低,对方法的灵敏度要求较高,采用以上方法进行准确定量的难度较大。目前,相关检测方法不仅报道的较少,而且分析对象主要为电子烟烟液,除此之外,还存在方法灵敏度较低,检出限较高,前处理过程需要使用固相萃取小柱,操作繁琐、耗时等问题[6-7,12,17]。鉴于此,本工作通过优化抽吸口数、电子烟功率、萃取条件和色谱条件,建立了高效液相色谱-串联质谱法(HPLC-MS/MS)测定电子烟烟液及气溶胶中TSNAs含量的方法,方法稳定性好、灵敏度高,可以满足痕量TSNAs准确定量需求,可为电子烟产品中TSNAs含量的监控提供技术参考,对电子烟安全性评价具有重要意义。
1 试验部分
1.1 仪器与试剂
Agilent 1290 infinity 型高效液相色谱仪,配AB SCIEX QTRAP 5500 型三重四极杆质谱检测器;Milli-Q50型超纯水制备仪;KQ-700DE 型数控超声波清洗器(功率1 000 W);CP2245型电子天平(感量0.000 1 g);X500E型吸烟机。
一级混合标准溶液:取NNN、NAT、NAB 和NNK 标准品,用甲醇溶解并稀释配制成1 mg·L-1的一级NNN、NAT、NAB 和NNK 混合标准溶液。
二级混合标准溶液:取适量1 mg·L-1的一级NNN、NAT、NAB 和NNK 混合标准溶液,用甲醇稀释配制成10μg·L-1二级NNN、NAT、NAB 和NNK 混合标准溶液。
混合内标储备溶液:取适量NNN-d4、NAT-d4、NAB-d4和NNK-d4的标准品,用甲醇溶解并稀释配制成4 mg·L-1的NNN-d4、NAT-d4、NAB-d4和NNK-d4混合内标储备溶液。
混合标准溶液系列:取二级混合标准溶液及混合内标储备溶液,用0.1 mol·L-1乙酸铵溶液逐级稀释配制成0.010,0.025,0.050,0.10,0.25,0.50,2.5,5.0μg·L-1混合标准溶液系列,内含10μg·L-1混合内标溶液。
NNN、NAT、NAB、NNK 标准品的纯度不小于98%;NNN-d4、NAT-d4、NAB-d4、NNK-d4标准 品的纯度不小于99%。
甲醇、乙腈、乙酸铵均为色谱纯;甲酸铵、甲酸为质谱纯;试验用水为超纯水;电子烟液及烟具均为市售产品。
1.2 仪器工作条件
1)色谱条件 Agilent Eclipse Plus C18RRHD色谱柱(100 mm×2.1 mm,1.8μm),柱温60 ℃;流量0.3 mL·min-1;进样量5 μL;流动相A为0.01 mol·L-1甲酸铵溶液;B为含0.025%(体积分数,下同)甲酸的乙腈溶液;梯度洗脱程序:0~2.0 min时,A 为90%;2.0~4.0 min时,A 由90%降至60%;4.0~6.0 min时,A 由60%降为40%;6.0~8.0 min时,A 由40%降至10%;8.0~8.1 min时,A 由10%跳转至90%;检测时间10 min。
2)质谱条件 电喷雾离子源(ESI),离子源温度550 ℃;气帘气压力241 kPa;电喷雾电压3 000 V;辅助气1 压力414 kPa,辅助气2 压力448 kPa;多反应监测(MRM)模式;正离子扫描模式;离子对驻留监测时间50 ms。其他质谱参数见表1,其中“*”为定量离子对。

表1 质谱参数Tab.1 MS parameters
1.3 试验方法
1.3.1 电子烟烟液样品
取1 g 电子烟烟液于50 mL 样品瓶中,加入0.1 mol·L-1乙酸铵溶液20 mL 及4 mg·L-1混合内标溶液50μL,超声萃取30 min,经0.2μm 聚四氟乙烯滤膜过滤,滤液按仪器工作条件测定。
1.3.2 电子烟气溶胶样品
采用国际烟草科学研究合作中心(CORESTA)推荐的电子烟抽吸参数,抽吸容量55 mL、抽吸频率为每30 s抽吸一口、抽吸持续时间3 s[18]。可调功率电子烟在最大功率下进行抽吸试验,每种品牌电子烟抽吸3支,将抽吸20口释放的气溶胶捕集在一张直径为44 mm 剑桥滤片上,每支烟具收集2张滤片,置于50 mL 样品瓶中,加入0.1 mol·L-1乙酸铵溶液20 mL 及4 mg·L-1混合内标溶液50μL,超声萃取30 min,经0.2μm 聚四氟乙烯滤膜过滤,滤液按仪器工作条件测定。
2 结果与讨论
2.1 色谱条件的选择
试验比较了Proshell 120 SB-C18色谱柱(100 mm×3.0 mm,2.7μm)和Eclipse Plus C18RRHD 色谱柱(100 mm×2.1 mm,1.8μm)对电子烟烟液及气溶胶中4种TSNAs的分离效果。结果显示:用Proshell 120 SB-C18色谱柱分离时,目标物的峰形欠佳,其中NNK 色谱峰容易出现分叉,NAT 色谱峰拖尾严重;在Eclipse Plus C18RRHD色谱柱上,4种TSNAs可达到有效分离,色谱峰峰宽较窄且峰形较好。因此,试验选择Eclipse Plus C18RRHD 色谱柱作为分析柱。
试验对流动相的组成进行了优化,结果发现,以0.01 mol·L-1甲酸铵溶液作为水相时,色谱峰峰形可得到有效改善,峰宽变窄且峰形较好。以乙腈为有机相时,气溶胶样品中NNN 与杂质未完全分离,而NAB 彻底被杂质掩盖。以含0.025%甲酸的乙腈溶液为有机相时,4种TSNAs可得到有效分离,峰形较不加酸时更加尖锐和对称,其中NNN 及NAB 与相应杂质峰彻底分离。因此,试验以含0.025%甲酸的乙腈溶液作为有机相。
试验还考察了不同流动相流量(0.2,0.3,0.4,0.5 mL·min-1)和不同柱温(30,40,50,60 ℃)对电子烟液及气溶胶样品中TSNAs分离效果的影响。结果显示:当流量为0.3 mL·min-1时,NNN和NAB分离度最好,目标物峰形较好且峰宽较窄;随着柱温的升高,NNN 和NAB 的分离度逐渐提高。由于乙腈的沸点为81.6 ℃,考虑到溶剂的稳定性,试验选择60 ℃作为分析柱温,0.3 mL·min-1作为流动相流量。
2.2 萃取方式和萃取时间的选择
以CORESTA 推荐的0.1 mol·L-1乙酸铵溶液作为萃取溶剂[19],对比了振荡萃取和超声萃取两种萃取方式萃取电子烟烟液及气溶胶样品时的萃取效果。试验发现两种方式的萃取效果基本一致,考虑到振荡萃取会导致剑桥滤片破碎溶解,不利于后续样品处理,因此选择超声萃取方式。进一步考察了不同超声萃取时间对电子烟烟液及气溶胶样品萃取效果的影响,结果见图1。

图1 不同超声萃取时间得到的电子烟烟液和气溶胶中TSNAs的含量Fig.1 Contents of TSNAs in e-cigarette liquid and aerosol obtained with the different ultrasonic extraction time
由图1可知:烟液中的4 种TSNAs含量在超声萃取时间10 min时已达到平衡,气溶胶中的在超声萃取时间30 min时达到平衡,萃取时间均小于传统振荡萃取法(60 min)[19]。因此,试验选择以超声萃取30 min来提取样品中的TSNAs。
2.3 电子烟气溶胶释放稳定性试验
电子烟气溶胶释放稳定性是评判电子烟质量的一项重要指标,而气溶胶的释放量与电子烟种类及抽吸口数有关。试验根据每20口抽吸产生气溶胶捕集量(ACM20口)的不同选取了3款具有代表性的电子烟为待测对象,分别是:1#自带烟弹的一次性电子烟(ACM20口不大于100 mg);2#不可调功率大烟(ACM20口为100~200 mg);3#可调功率大烟(ACM20口为200~300 mg)。每支烟总共抽吸100口,每间隔20口为一个单位,将所得气溶胶粒相物捕集在一张滤片上,测定5 张滤片的ACM及TSNAs含量,并计算每张滤片不同抽吸口数(20,40,60,80及100)收集的电子烟气溶胶ACM、4种TSNAs的测定值及总量,以及ACM 质量和TSNAs总量的相对标准偏差(RSD),结果见表2和图2。
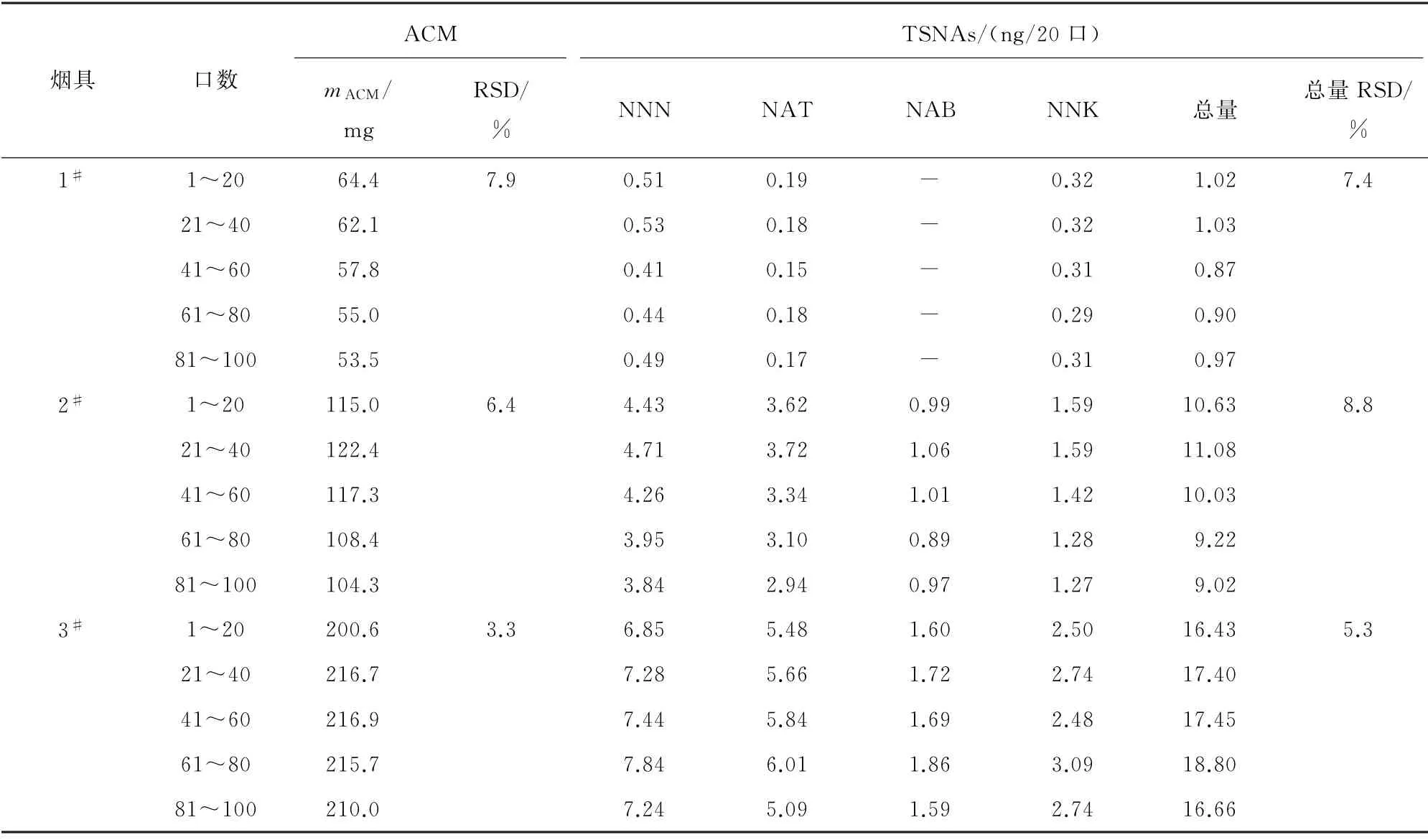
表2 以抽吸20口为一个单位时气溶胶释放稳定性试验结果(n=5)Tab.2 Results of test for aerosol release stability with 20 puff numbers as a unit(n=5)

图2 不同抽吸口数所得气溶胶ACM 及其中TSNAs含量Fig.2 Contents of ACM and TSNAs in aerosol with different puff numbers
由表2和图2可知,对于不同类型的电子烟器具来说,抽吸同样的电子烟烟液,每抽吸20口气溶胶中4种TSNAs可实现准确定量,且随着抽吸口数的增加,烟具1#和烟具2#电子烟气溶胶ACM及TSNAs含量均随之增加,且两者呈正相关关系,烟具3#气溶胶ACM 及TSNAs先随之增加后逐渐稳定,这是由于烟具3#每抽吸20 口气溶胶ACM较大,随着抽吸口数的增加,单张滤片对气溶胶中粒相物的捕集能力趋于饱和。以抽吸20口为一个单位,抽吸5个单位所得测定值的RSD 均小于10%,说明每20口的气溶胶的释放稳定性较好。电子烟中TSNAs含量非常低,为了保证痕量的TSNAs能够被检出,必须捕集足够多的气溶胶,因此在实际样品测定中可以20口气溶胶为一个单位进行滤片捕集,收集2张滤片,以其检测结果的平均值作为测定值。
2.4 电子烟功率的选择
功率是市售电子烟的一个重要规格参数,与电子烟雾化效果关系密切,试验选用可调功率电子烟考察了不同功率(10,20,40,80,120,170,225 W)下电子烟抽吸产生的气溶胶ACM 及4种TSNAs含量的变化趋势,结果表明:电子烟气溶胶ACM 及4种TSNAs释放量随着电子烟功率的增加而增加并逐渐趋于稳定,因此在本试验中,对于可变功率电子烟均在其最大功率下进行抽吸,对于不可变功率电子烟就在产品设定功率下进行抽吸。
2.5 色谱行为
按照优化的试验条件分析电子烟烟液及气溶胶,所得色谱图见图3。

图3 电子烟烟液及气溶胶中TSNAs的MRM 色谱图Fig.3 MRM chromatograms of TSNAs in e-cigarette liquid and aerosol
2.6 标准曲线、检出限和测定下限
按照仪器工作条件测定混合标准溶液系列,以4种TSNAs的质量浓度为横坐标,其对应的峰面积与内标物的峰面积的比值为纵坐标绘制标准曲线,其线性参数见表3。
以3倍、10倍信噪比(S/N)分别计算目标物的检出限(3S/N)和测定下限(10S/N),结果见表3。

表3 线性参数、检出限和测定下限Tab.3 Linearity parameters,detection limits and lower limits of determination
由表3可知,4种TSNAs的检出限为0.002~0.015 ng·g-1(烟液)和0.001~0.008 ng/20口(气溶胶);测定下限为0.007~0.052 ng·g-1(烟液)和0.004~0.026 ng/20口(气溶胶),低于相关文献报道[6-7,12,17],满足电子烟烟液及气溶胶样品中痕量TSNAs的测定需求。
2.7 精密度和回收试验
按照试验方法分析电子烟烟液和气溶胶,以一天之内连续5次测定值的相对标准偏差(RSD)考查日内精密度,以连续5天的测定值RSD 考查日间精密度,结果见表4。
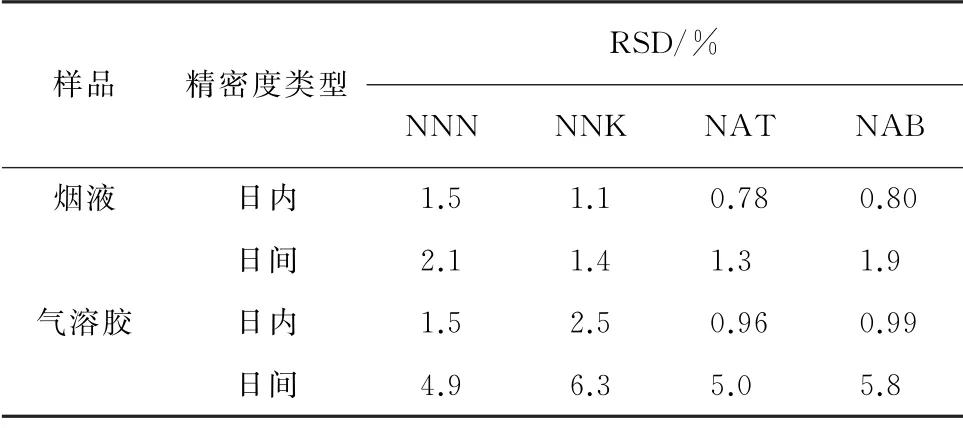
表4 精密度试验结果(n=5)Tab.4 Results of test for precision(n=5)
由表4 可知,电子烟烟液样品日内RSD 为0.78%~1.5%,日间RSD 为1.3%~2.1%;电子烟气溶胶样品日内RSD 为0.96%~2.5%,日间RSD为4.9%~6.3%,说明方法具有很好的重复性。
按照试验方法对电子烟烟液及气溶胶进行低、中、高等3个浓度水平的加标回收试验,并计算回收率,结果见表5。

表5 回收试验结果Tab.5 Results of test for recovery
由表5 可知,电子烟烟液样品中4 种TSNAs的回收率为90.7%~103%,气溶胶样品中的回收率为92.0%~108%,满足电子烟TSNAs含量的检测要求。
2.8 样品分析
按照试验方法分析市售不同品牌电子烟样品1#~14#,其中1#~10#为可添加烟液的电子烟,11#~14#为自带烟液的一次性电子烟(所用烟液无法取出测试),并计算烟液和气溶胶中4种TSNAs的含量和总量,结果见表6。

表6 样品分析结果Tab.6 Analytical results of samples
由表6可知,传统卷烟较电子烟中TSNAs含量高了近百倍[14],电子烟中NNN 及NAT 的检出量相对较高,质量分数分别在40.57 ng·g-1以内、31.94 ng·g-1以内(烟液)及6.40 ng/20 口以内、5.03 ng/20口以内(气溶胶);NAB的检出数量及含量均较低,质量分数分别为8.33 ng·g-1以内(烟液)和1.28 ng/20口以内(气溶胶);另一种强致癌物NNK 的质量分数分别为11.22 ng·g-1以内(烟液)、1.89 ng/20 口(气溶胶)。其中样品6#与9#TSNAs含量远高于其他样品,推测可能与其烟液配方有关,比如可能添加了TSNAs含量较高的烟草提取物。此外,电子烟气溶胶中TSNAs与对应烟液成分密切相关,电子烟抽吸之后产生的气溶胶中TSNAs含量与所用烟液中的TSNAs含量呈正相关,TSNAs含量较高的烟液抽吸之后产生的气溶胶中TSNAs含量也较高,如样品6#和样品9#;未检出TSNAs的烟液抽吸之后产生的气溶胶中TSNAs同样未检出,如样品1#和样品2#。
本工作建立了HPLC-MS/MS测定电子烟烟液及气溶胶中4种TSNAs含量的方法,该方法的检出限低、灵敏度高、重复性好、准确度高,可以满足电子烟烟液及气溶胶中痕量TSNAs的快速准确测定,可为今后电子烟的研发、质量安全监管、参数设置以及滤片捕集方式选择等提供重要的技术参考。
