林可霉素注射液非法添加盐酸左旋咪唑的HPLC检测方法研究
2021-11-25刘雪红
郑 洁,刘雪红,陈 玲
(大连市检验检测认证技术服务中心,辽宁大连 116037)
盐酸左旋咪唑(levamisole hydrochloride),是一种广谱抗线虫药,对马、牛、绵羊、猪、犬和鸡的大多数线虫具有活性,还能明显提高免疫反应。在兽医临床上用作牛、羊、猪、犬、猫和禽的胃肠道线虫、肺线虫以及犬心丝虫和猪肾虫感染的治疗,也用于免疫功能低下动物的辅助治疗和提高疫苗免疫效果[1]。但该药具有潜在的基因毒性,摄入过量对皮肤、神经、消化、心血管、免疫等多个系统造成损害,导致癌变、畸变,甚至死亡[2]。兽医临床使用剂量为每日7.5 mg/kg,禽类为每日7.5 mg/kg。国内对肉源性组织和生鲜乳中左旋咪唑残留已经发布了相关标准[3-4],但饲料和兽药中非法添加左旋咪唑还缺少相关的检验标准,导致检出左旋咪唑而无法判定的情况。在2020年兽药检测过程中,按照《农业农村部公告169号》[5]筛查后,就发现一例林可霉素注射液中非法添加盐酸左旋咪唑的案例,针对出现的左旋咪唑添加物,开展方法学研究,建立林可霉素注射液非法添加盐酸左旋咪唑的HPLC检测方法,以期对林可霉素注射液质量控制和左旋咪唑的相关检测标准的制定提供参考。
1 材料与方法
1.1 材料
1.1.1 药品与试剂 Levamisole Hydrochloride(99.9%, TMstandard);甲醇(色谱纯,天津市科密欧化学试剂);磷酸二氢钠(分析纯,天津市科密欧化学试剂);三乙胺(分析纯,天津市科密欧化学试剂);氢氧化钠(分析纯,天津市科密欧化学试剂);盐酸林可霉素注射液(10 mL:0.3 g):四川显华动物药业有限公司,经检测不含盐酸左旋咪唑。
1.1.2 仪器设备 BS21S电子天平(Sartorius);2695高效液相色谱仪(Waters);2998二极管阵列检测器(Waters);超声波清洗机(上海科导超声仪器有限公司)。
1.2 方法
1.2.1 色谱条件 Waters Atlantis®T3 C18色谱柱(4.6×250 mm,5 μm);流动相:磷酸二氢钠溶液(取磷酸二氢钠3.0 g,加水1000 mL,加三乙胺0.5 mL,用饱和氢氧化钠溶液调节pH值至7.0)-甲醇(70∶30);流速1.00 mL/min;柱温30.0 ℃;检测波长230 nm;进样体积10.0 μL。
1.2.2 供试品溶液的制备 溶剂空白溶液的制备:取甲醇试剂,过滤后作为溶剂空白溶液。对照品溶液的制备:精密称取盐酸左旋咪唑对照品适量,用甲醇溶解并稀释成0.1 mg/mL的溶液。样品空白溶液的制备:精密量取不含盐酸左旋咪唑的盐酸林可霉素注射液1 mL,置50 mL容量瓶中,加甲醇稀释至刻度,摇匀;精密量取1 mL,置25 mL容量瓶中, 加甲醇稀释至0.024 mg/mL的盐酸林可霉素溶液,作为空白样品溶液。阳性添加溶液的制备:在林可霉素注射液中添加盐酸左旋咪唑对照品,用甲醇配制成含盐酸左旋咪唑0.1 mg/mL的溶液,作为阳性添加溶液。
1.2.3 专属性 按1.2.1项色谱条件,对1.2.2项中的试剂空白溶液、对照品溶液、样品空白溶液、阳性添加溶液分别进样,对色谱图进行比对。
1.2.4 最低检测限和定量限 按1.2.1项色谱条件,将对照品溶液逐级稀释,分别配制成浓度为0.0032、0.0016、0.0008、0.0004、0.0002、0.0001 mg/mL的溶液注入高效液相色谱仪,同时记录色谱图及光谱图。将信噪比大于等于2时对应的浓度定义为最低检测限,将信噪比大于等于10时对应的浓度定义为定量限。
1.2.5 精密度 采用重复性试验考察,精密称取盐酸左旋咪唑对照品10 mg,定容于100 mL容瓶中,配制成浓度为0.1 mg/mL 盐酸左旋咪唑对照品溶液,将其重复进样6次,进样体积为10.0 μL,记录色谱图,计算其峰面积相对标准偏差(RSD)。
1.2.6 线性关系 精密称取盐酸左旋咪唑对照品100 mg,置100 mL容量瓶中,用甲醇定容至刻度,摇匀,精密量取1、2、3、5、10、20 mL分别置50 mL容量瓶中,加甲醇稀释至刻度,摇匀,过滤后取精密量取10.0 μL注入液相色谱仪,记录色谱图。按盐酸左旋咪唑对照品溶液浓度与对应的盐酸左旋咪唑峰面积作标准曲线,计算回归方程和相关系数。
1.2.7 回收率 取1 mL盐酸林可霉素注射液,添加盐酸左旋咪唑对照品100 mg,置50 mL容量瓶中,加甲醇溶解并稀释至刻度,摇匀;再精密量取1 mL置25 mL容量瓶中,加甲醇至刻度,摇匀,作为供试品溶液,平行配制6份。对照品溶液的配制同1.2.2项。分别精密量取供试品和对照品溶液10.0 μL注入液相色谱仪,记录色谱图,按外标法计算峰面积。
1.2.8 耐用性 考察3个不同的色谱柱(Waters Sunfire®C18 4.6×250 mm, 5 μm、Waters Atlantis®C18 4.6×250 mm, 5 μm、Waters Atlantis®T3 C18 4.6×250 mm, 5 μm),3个不同的柱温(20.0、25.0、30.0 ℃),3个不同的pH值(6.8、7.0、7.2),流动相甲醇的比例分别为28%、30%、32%时,对峰保留时间、理论板数等方面的影响。
2 结果与分析
2.1 专属性 结果如图1所示,对照品溶液和阳性添加溶液在39 min左右出峰,且光谱图无差异,空白溶剂和盐酸林可霉素样品在39 min左右均无色谱峰出现。说明在此色谱条下盐酸林可霉素不影响酸左旋咪唑的检测,甲醇溶剂对左旋咪唑的检测亦没有干扰。
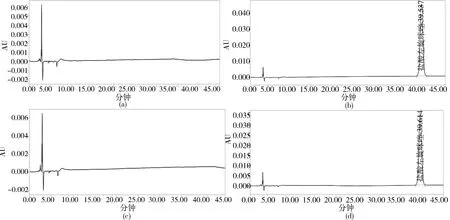
a.溶剂空白溶液 b. 对照品溶液c. 样品空白溶液d. 阳性添加溶液
2.2 最低检测限和定量限 对逐级稀释后的盐酸左旋咪唑溶液测定后,结果显示,盐酸左旋咪唑浓度为0.0002 mg/mL时信噪比为2.8,浓度为0.0016 mg/mL时信噪比为11.6,所以盐酸左旋咪唑的最低检测限为0.0002 mg/mL,定量限为0.0016 mg/mL。
2.3 精密度 对重复性试验记录的色谱图进行处理,计算6次进样的峰面积RSD为0.6%,表明本方法具有良好的重复性,符合精密度试验的要求。
2.4 线性关系 将浓度分别为0.02、0.04、0.06、0.1、0.2、0.4 mg/mL的左旋咪唑溶液色谱图进行处理,分别计算其峰面积。以盐酸左旋咪唑浓度为横坐标x,峰面积(AU)为纵坐标y,绘制标准曲线,其线性回归方程为y=1.528×107x-14689,R2=0.9999(图2)。表明盐酸左旋咪唑在浓度0.02~0.4 mg/mL时,线性关系良好。
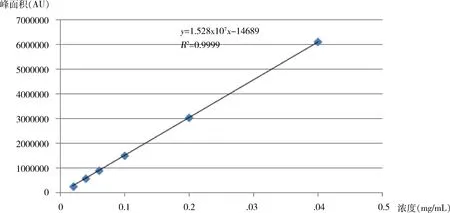
图2 盐酸左旋咪唑标准曲线
2.5 回收率 将6份添加浓度为0.08 mg/mL的供试品溶液的色谱图进行处理,分别计算峰面积值,按外标法计算盐酸左旋咪唑的含量,平均回收率为99.7%,RSD为0.8%。结果见表1。
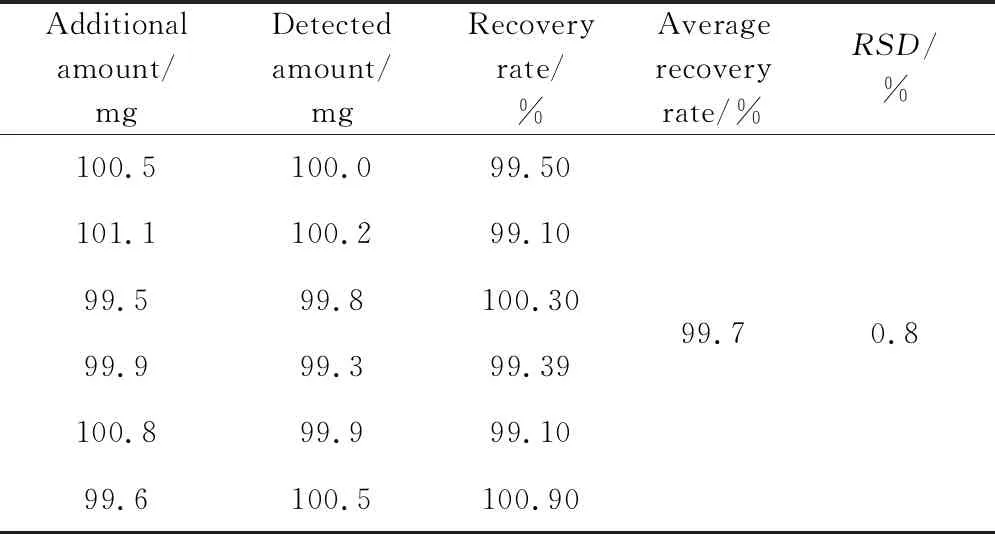
表1 盐酸林可霉素注射液中盐酸左旋咪唑回收率试验结果(n=6)
2.6 耐用性 试验结果显示,使用3种色谱柱分离后结果显示,T3色谱柱的理论板数和峰形明显优于其它色谱柱,分析T3色谱柱具有亲水性强的特点,当流动相水相占比例较大时,采用此种色谱柱可以有效提高盐酸左旋咪唑的理论板数;柱温的升高可以使盐酸左旋咪唑的保留时间略有提前,但3个柱温条件下无明显差异(保留时间差值小于1 min),柱温的提高有利于增加盐溶液的溶解性,提高其流动性、降低流路压力,但柱温的设定还需要参考实验室内的室温,避免与室温相差太大;3个pH值条件下,盐酸左旋咪唑的保留时间差小于1 min、峰面积相对偏差小于1.5%、理论板数相对偏差小于1.5%,均无明显差异,提示pH的变化对实验影响不大;流动相中有机相甲醇的比例升高可以缩短目标峰的出峰时间,但由于无机相为盐溶液,有机相比例的升高会加大色谱柱的柱压,甚至导致管路堵塞,在有机相甲醇比例为30%以下时,能达到稳定的柱压,甲醇比例在28%时保留时间较30%时延后,且理论板数降低,说明甲醇比例在30%时系统稳定性和理论板数最好。
供试品溶液色谱图中如出现与盐酸左旋咪唑对照品色谱峰保留时间一致的峰(差异小于等于5%),且为单一物质峰;在200~400 nm范围波长内,二者紫外光谱图一致,最大吸收波长无明显差异(差异小于等于±2 nm),判为检出盐酸左旋咪唑。供试品溶液色谱图中的峰保留时间与盐酸左旋咪唑对照品峰相同,但峰面积小于检测限峰面积,判定为未检出盐酸左旋咪唑。
3 讨论与结论
3.1 添加目的分析 盐酸林可霉素临床用于治疗猪痢疾的常用药物[6],抗菌谱广,对敏感葡萄球菌属、链球菌属、肺炎链球菌及一些敏感性厌氧菌所致的呼吸道感染、肠道感染、皮肤软组织感染都有效果。同时在联合交叉用药时,不会产生耐药性[7]。盐酸左旋咪唑针对动物肠道球虫病所致的感染有增效作用[8-9],还可以提高免疫[10-11]。林可霉素制剂中添加盐酸左旋咪唑的问题鲜有报道,我院也是首次在林可霉素注射液中检出盐酸左旋咪唑,林可霉素与此抑菌药配伍后,可以显著增强其药用效果。但添加的剂量无法控制,超量易导致动物死亡[12-14]。
3.2 检测波长的选择 将二极管阵列检测器记录的盐酸左旋咪唑的3D色谱图放大,可以看到在230 nm处左旋咪唑的峰强度最强,响应值最大,且无干扰,所以在230 nm通道监测和记录。
3.3 方法评价 盐酸林可霉素注射液在与盐酸左旋咪唑对照品相同的保留时间处无色谱峰出现,说明林可霉素对盐酸左旋咪唑的检查无干扰,即本检查法适用于盐酸林可霉素注射液。与传统的容量分析法和气相、液质等方法相比,高效液相法具有方便迅速、灵敏度高、线性关系良好、精密度高的优点,是国内外普遍使用的方法[15-17]。由于林可霉素注射液的基质效应弱,缓冲盐的洗脱能力好,可以达到较高的回收率(99.7%),有利于对非法添加物质进行定量分析。在实际监测过程中,结合现有的筛查标准还可以实现多组份同时筛查添加物质,省时省力。
建立了高效液相色谱法测定盐酸林可霉素注射液中非法添加盐酸左旋咪唑的检查方法。试验结果表明,本方法专属性、精密度、线性、回收率试验均符合《中国兽药典2015年版一部》[18]的要求,能有效检测盐酸林可霉素注射液中是否添加盐酸左旋咪唑及添加量。
