湿法混炼对NBR/Kaolin复合材料溶胀行为的影响*
2021-11-24蒋兴旺史兴辉刘广永蔡颖辉郝福兰刘振学
蒋兴旺,史兴辉,刘广永**,王 辉,,蔡颖辉,郝福兰,刘振学
(1.青岛科技大学 橡塑材料与工程教育部重点实验室,山东 青岛 266042;2.黄河三角洲京博化工研究院有限公司,山东 滨州 256500)
橡胶的湿法混炼最早是由美国的CABOT公司提出并发展至今,湿法混炼的提出主要是为了改善填料在橡胶中的分散,增强填料与橡胶之间的结合[1-3]。相对于干法混炼,湿法混炼不仅能够使干法混炼中难以分散的填料更好地分散,使橡胶得到更好的应用性能,而且还更加符合我国新时代对绿色环保的要求[4-7]。陈巧等[8]将天然橡胶(NR)与稀土掺杂改性高岭土(Kaolin)利用乳液凝聚共沉法制备了NR/Kaolin复合材料,研究发现湿法混炼填料有着更好的分散性,且与橡胶基体形成的界面结合力更强。
自湿法混炼提出之后,科研工作者们主要的研究方向是湿法混炼与干法混炼对橡胶物理性能上影响的差别[9-10],很少有人研究湿法混炼相对于干法混炼对橡胶耐溶剂性能的影响,本文通过研究湿法混炼和干法混炼制备的丁腈橡胶(NBR)/Kaolin复合材料在溶剂中溶胀行为的差异,填补了这方面研究的空白。
1 实验部分
1.1 原料
NBR胶乳:固体质量分数为25%,丙烯腈质量分数为34%,南帝化学工业股份有限公司;Kaolin:市售工业品;硫磺s-80、促进剂MBTS-75、氧化锌、硬脂酸:莱茵化学公司。
1.2 仪器及设备
热失重分析仪:TG209F1,德国耐驰公司;双辊开炼机:BL-6175-BL,宝轮精密检测仪器有限公司;无转子硫化仪:MDR2000,美国Alpha公司;扫描电子显微镜(SEM):JSM-7500F型,日本Jeol公司。
1.3 实验配方
基本配方(质量份)为:NBR胶乳400,Kaolin为变量(0、25),硫磺s-80 1.2,促进剂MBTS-75 2.5,氧化锌 3,硬脂酸 1。
1.4 制备过程
1.4.1 湿法混炼
取400 g的NBR胶乳,室温下用搅拌机进行搅拌,慢速加入25份Kaolin继续搅拌30 min,再用酒精进行破乳、絮凝、清洗、剪碎、真空干燥。过辊后做热失重分析,然后在开炼机上进行混炼,混炼时间约为10 min,室温停放24 h后在平板硫化机上进行硫化。
1.4.2 干法混炼
根据热失重结果,向由400 g NBR胶乳破乳得到的NBR固体胶中加入相同含量的Kaolin,后续的加工工艺与湿法混炼保持一致。
1.5 分析与测试
1.5.1 热失重分析
根据GB/T 27761—2011 对均匀下片后的LNBRK进行热失重实验,氧气氛围下30~900 ℃恒速升温[11]。
1.5.2 溶胀实验
分别将硫化后的NBR、湿法和干法混炼得到的NBR/Kaolin复合材料胶片制成多个1 g左右的长条状试样,于25 ℃下,分别放置在乙酸甲酯、乙酸乙酯、乙酸丙酯和乙酸丁酯4种溶剂中进行溶胀实验,每隔固定时间对其进行质量测量并记录,当3次测量的质量之间差值小于0.005 g时,认为其达到溶胀平衡[12]。
1.6 理论基础
1.6.1 最大溶胀比
最大溶胀比的计算公式如式(1)所示。
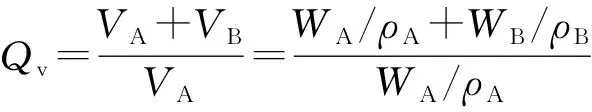
(1)
式中:Qv为橡胶试样的最大溶胀比;VA为橡胶试样的初始体积;VB为吸收溶剂的体积;WA为橡胶的初始质量;ρA为橡胶的密度;WB为橡胶试样溶胀平衡时的吸收溶剂的质量;ρB为溶剂的密度[13]。
1.6.2 摩尔吸收率
摩尔吸收率的计算如式(2)所示。
(2)
式中:Qt为橡胶对溶剂的摩尔吸收率,即t时刻100 g橡胶吸收溶剂的摩尔百分比[14],Mmol为溶剂的摩尔质量。
1.6.3 扩散系数
计算如式(3)所示。
(3)
式中:D为扩散系数,表示溶剂在橡胶试样中扩散速度的快慢,取决于橡胶链段的运动能力;h为橡胶试样的厚度;θ为Qt对t1/2作图得到的曲线线性部分的斜率;Q∞为橡胶试样溶胀平衡时的摩尔吸收率[15]。
2 结果与讨论
2.1 热失重分析结果
图1为LNBRK在氧气氛围下于30~900 ℃下进行热失重分析的曲线,当温度接近400 ℃时,试样的质量快速下降,当温度达到500 ℃左右时,NBR橡胶基体基本完全分解,Kaolin含量逐渐稳定,最终剩余填料由初始添加量25份减少为22.29份,质量百分比为17.83%,根据此数据制得与LNBRK相同填料含量的SNBRK。
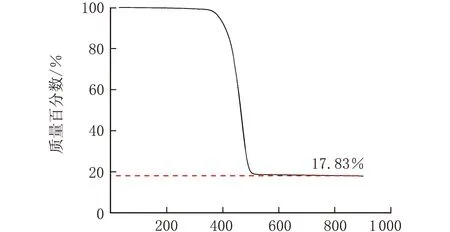
温度/℃图1 LNBRK的热失重曲线
2.2 SEM分析
图2为NBR/Kaolin复合材料的SEM图。

(a) LNBRK

(b) SNBRK图2 NBR/Kaolin复合材料的SEM图像
从图2可知,由湿法混炼获得的LNBRK中Kaolin分散更为均匀,Kaolin聚集体的颗粒更小,而SNBRK中的Kaolin则分散较差,且存在较大的集聚体,说明湿法混炼改善了Kaolin在NBR中的分散。
2.3 湿法混炼对NBR复合材料溶胀行为的影响
2.3.1 摩尔吸收率
图3为NBR0、LNBRK和SNBRK3种硫化胶在4种溶剂中的Qt曲线。
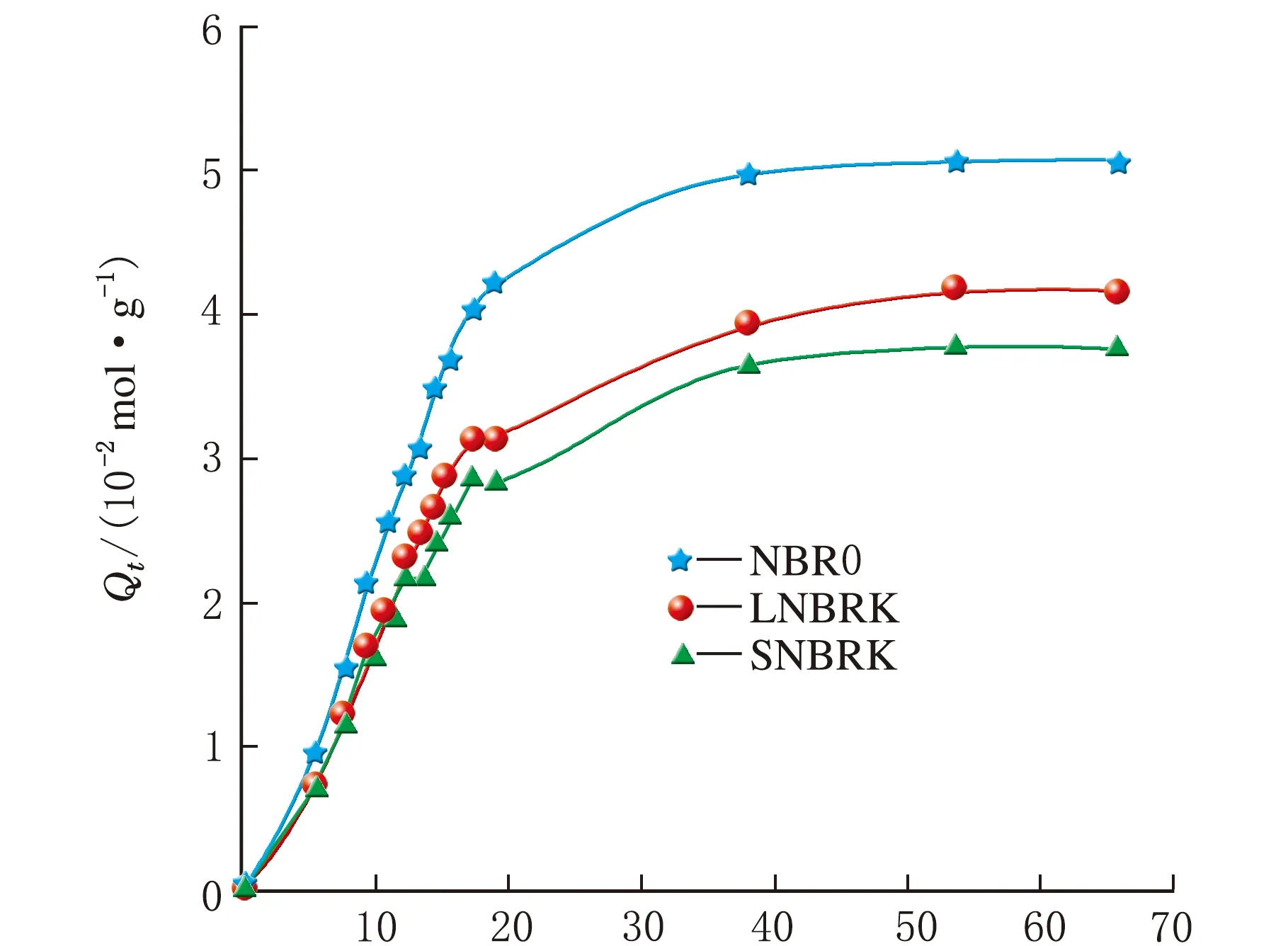
t1/2/min1/2(a) 乙酸甲酯

t1/2/min1/2(b) 乙酸乙酯
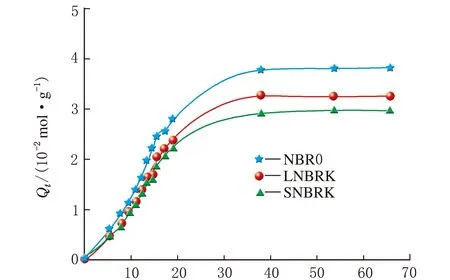
t1/2/min1/2(c) 乙酸丙酯
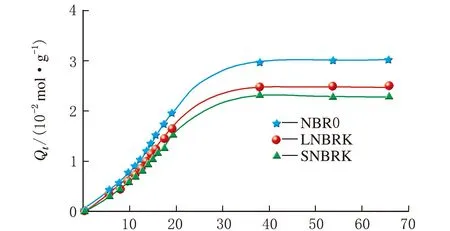
t1/2/min1/2(d) 乙酸丁酯图3 NBR0、LNBRK和SNBRK在4种酯类溶剂中的Qt曲线
对比图3(a)、(b)、(c)和(d)中NBR0、LNBRK和SNBRK以及其在不同溶剂中的Qt曲线可以发现,无论是Qt曲线的斜率,还是Q∞,都是NBR0>LNBRK>SNBRK,且随着酯类溶剂碳原子数的增加,3种溶剂的Qt曲线之间的距离逐渐较小,这是由于溶剂分子的碳原子数越多,其分子链越长,扩散进入聚合物也就越困难。
2.3.2 扩散系数
对图3中的Qt曲线中的线性部分线性拟合,可以得到其摩尔吸收率线性增长阶段的斜率,再根据公式(3)进一步计算得到其扩散系数。扩散系数随溶剂碳原子数变化的曲线如图4所示。
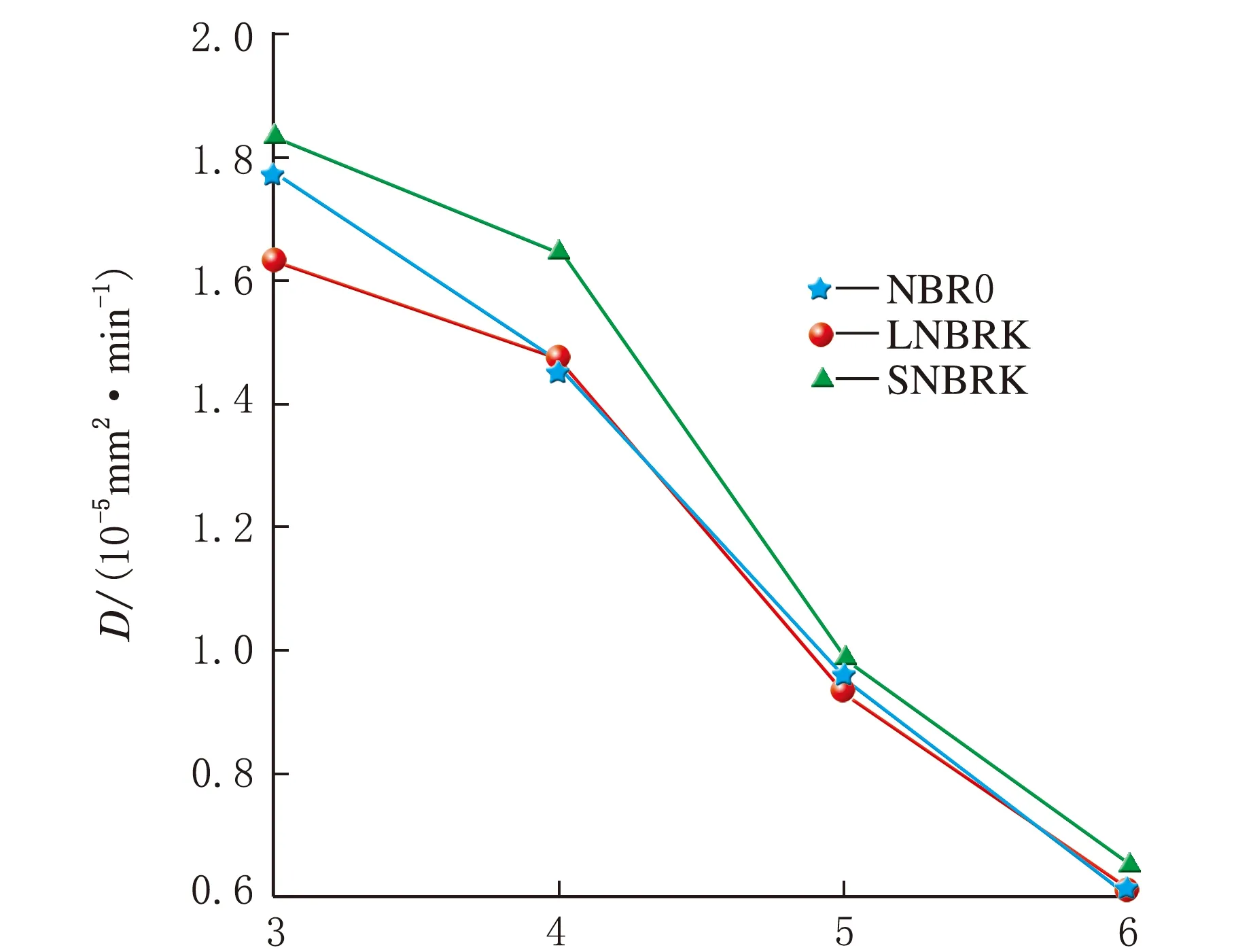
溶剂碳原子数图4 扩散系数随溶剂碳原子数变化的曲线
由图4可知,在添加Kaolin后,除了乙酸甲酯外,其他3种溶剂在LNBRK和NBR0的扩散系数几乎是相同的,但对于SNBRK来说,溶剂在其中的扩散系数则要略高于在NBR0和LNBRK中的扩散系数。这是因为LNBRK中Kaolin颗粒聚集体更小,分布的更加密集,因而使溶剂在其中的扩散路径比在SNBRK中更加复杂而使扩散速度减慢,扩散系数减小。此外,随着酯类溶剂碳原子数的增加,溶剂在橡胶中的扩散系数都呈现近似线性减小的趋势。
2.3.3 最大溶胀比与平衡摩尔吸收率
根据公式(1)计算出NBR0、LNBRK和SNBRK在4种溶剂中的最大溶胀比,取图2中Qt曲线平衡时的值为平衡摩尔吸收率。
从图5(a)可以看出,添加Kaolin后,NBR橡胶的最大溶胀比下降,SNBRK最大溶胀比的下降程度要大于LNBRK的下降程度,原因为干法混炼添加高岭土的分散性差,不均匀,对聚合物网络膨胀的限制要比分散性好时大一些,从而导致SNBRK对酯类溶剂的最大吸收能力小于LNBRK。图5(b)为NBR0、LNBRK和SNBRK溶胀平衡时摩尔吸收率随溶剂碳原子数变化的曲线,和Qv曲线相同的是,LNBRK和SNBRK的Q∞都小于NBR0的Q∞,SNBRK的Q∞也小于LNBRK的Q∞,与Qv曲线不同的是NBR0、LNBRK和SNBRK的Q∞曲线随着溶剂中碳原子数的增加而下降,且近乎呈线性关系,对其进行拟合可以得到式(4)~式(6)。
Q∞NBR=-0.68x+7.14 (R2=0.998)
(4)
Q∞LNBRK=-0.54x+5.80 (R2=0.998)
(5)
Q∞SNBRK=-0.48x+5.24 (R2=0.998)
(6)
式中:x为酯类溶剂的碳原子数。

溶剂碳原子数(a) Qv曲线
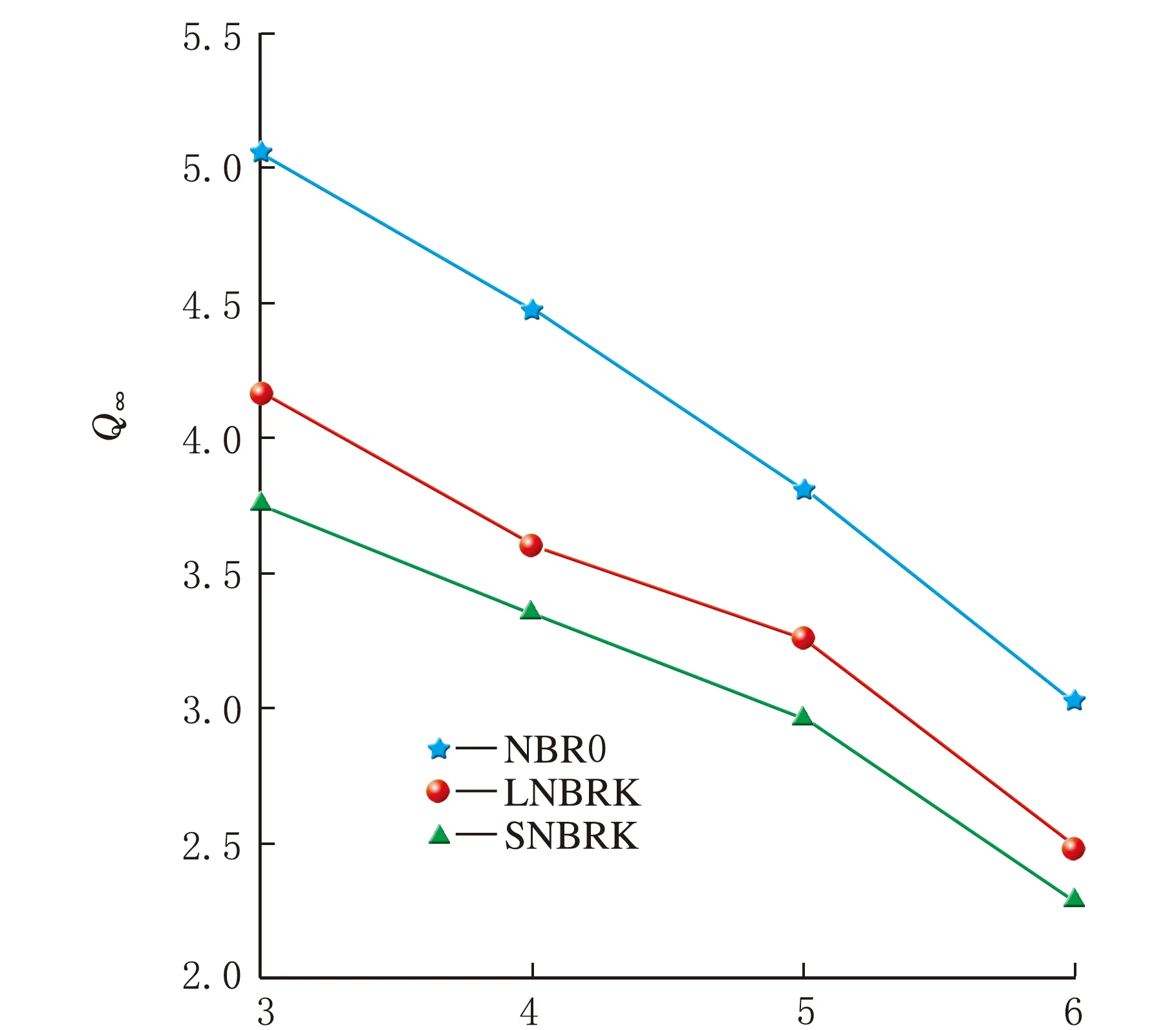
溶剂碳原子数(b) Q∞曲线图5 NBR0、LNBRK和SNBRK的Qv和Q∞曲线
通过图5(a)与图5(b)的比较可以看出,Q∞更能体现溶剂的分子结构对橡胶最大溶胀度的影响。这是因为与橡胶的最大溶胀比不同,平衡时的摩尔吸收率不考虑溶剂的摩尔质量的影响,而是从数量上对橡胶吸收的溶剂进行评价,最大溶胀比实际上是将溶剂的摩尔质量和分子结构同时考虑进去,但摩尔质量和分子结构有很大的相关性,因此对于同种胶在不同溶剂中溶胀行为之间的比较,Q∞更能体现出溶剂的影响。
3 结 论
(1)湿法混炼Kaolin比干法混炼Kaolin分散的更为均匀,Kaolin聚集体颗粒更小,与NBR基体的结合更好。
(2)相比于干法混炼,湿法混炼虽然会使材料基体的最大溶胀程度升高,但可以降低溶剂在材料基体中的扩散速率。
(3)Q∞比Qv更能明显地表示溶剂的分子结构对橡胶溶胀的影响,随着酯类溶剂中碳原子数的增加,试样溶胀平衡时的摩尔吸收率逐渐降低,且近乎呈线性关系。
