白术药材-饮片-配方颗粒主要成分量值传递规律及对脾虚模型大鼠肠道调节作用的研究*
2021-11-19俞忠明郑纯威施佳君富丹婷
俞忠明 郑纯威 施佳君 富丹婷 寿 旦
浙江省中医药研究院 浙江 杭州 310007
白术始载于《神农本草经》,为菊科植物白术(Atractylodes Macrocephala Koidz.)的干燥根茎[1]。白术具有健脾益气、燥湿利水、止汗等功效,主治脾虚食少、腹胀泄泻、痰饮眩悸、水肿、自汗等症,为“健脾补气第一要药”。本实验在白术药材-饮片-颗粒剂中主要成分白术内酯Ⅰ、Ⅱ、Ⅲ成分研究的基础上,对脾虚大鼠模型胃泌素(GAS)、血管活性肠肽(VIP)指标检测,初步探讨白术药材-饮片-配方颗粒中主要成分的量值传递规律及对脾虚大鼠模型肠道调节作用,以期为白术的进一步开发研究提供实验基础。
1 材料
1.1 仪器:Power Wave XS型全波长酶标仪(美国BioTek公司);J-15R冷冻型高效台式离心机[贝克曼库尔特商贸(中国)有限公司];U3000高效液相色谱仪(赛默飞世尔公司);YJ-40L/h型超纯水机(杭州余杭亚洁水处理设备有限公司);FW177型中草药粉碎机;AE-50电子天平(瑞士梅特勒);HH-8水浴锅(常州市江南实验仪器厂);KQ400超声提取器(江苏昆山);GS-6R离心机(Beckman公司)。
1.2 药材与试剂:大黄(批号:200508),白术药材10批( 批 号 分 别 为 20180269、20180270、20180272、20180274、20180275、20180277、20180278、20180279、20180280、20180281),白术饮片 10批(批号分别为20180289、20180294、20180296、20180299、201802101、201802103、 201802104、 201802105、 201802106、201802107),麸炒白术配方颗粒选择同一批号不同时间段生产的10个品种(批号为K2004022,每3g颗粒剂相当于白术饮片10g),均购自浙江景岳堂药业有限公司;白术内酯Ⅰ、Ⅱ、Ⅲ对照品(批号分别为111975-201501、111976-201501、111978-201501),均购自中国食品药品检定研究院;GAS试剂盒[酶联免疫吸附测定(ELISA)法,批号:JL21322]、VIP试剂盒(ELISA法,批号:JL12942),均购自上海江莱生物科技有限公司;其余试剂均为分析纯,水为蒸馏水。
1.3 动物:SPF级雄性SD大鼠30只,体重200±20g,购自杭州医学院,生产许可证号:SCXK(浙)2019-0002。
2 方法与结果
2.1 白术药材-饮片-颗粒剂中白术内酯Ⅰ、Ⅱ、Ⅲ的量值传递规律研究:分述如下。
2.1.1 白术内酯Ⅰ、Ⅱ、Ⅲ含量测定:①色谱条件[2]:ThermosyncronisC18色 谱 柱(4.6mm×250.0mm,5μm),以乙腈(A)和水(B)为流动相,梯度洗脱条件:0~16min、40%~24%B,16~18min、24%~0B;18~30min、0%B,流速:1.0ml/min,柱温:25℃,进样体积10μl。白术内酯Ⅰ检测波长276nm、白术内酯Ⅱ和白术内酯Ⅲ检测波长220nm。理论塔板数按白术内酯Ⅰ、Ⅱ、Ⅲ计算高于5000。②对照品溶液的制备:取三种白术内酯对照品适量,精密称定,加入甲醇制成每1ml含白术内酯Ⅰ、Ⅱ、Ⅲ分别为0.114mg、0.078mg、0.321mg的溶液,即得。③供试品溶液制备:取白术药材、饮片、配方颗粒样品粉末(过三号筛)约1g,精密称定,置于具塞锥形瓶中,加入甲醇50ml,密塞,称重,超声提取30min,放至室温,称重,加甲醇补足重量,摇匀,取上清液滤过,取续滤液25ml蒸发皿75℃水浴浓缩至约2ml,转移至5ml容量瓶中并定容,即得。④样品含量测定:按照上述色谱条件测定不同批次白术药材、饮片和配方颗粒中白术内酯Ⅰ、Ⅱ、Ⅲ的含量。
2.1.2 白术内酯Ⅰ、Ⅱ、Ⅲ量值传递规律分析:将白术配方颗粒的含量转换成相当于每1g饮片含量白术内酯Ⅰ、Ⅱ、Ⅲ的含量(mg/g),采用SPSS 20.0作白术药材-饮片-配方颗粒中白术内酯Ⅰ、Ⅱ、Ⅲ的比较分析,以探讨其量值传递规律。结果显示,白术药材中白术内酯Ⅱ含量最高,白术内酯Ⅲ次之,白术内酯Ⅰ最少;白术饮片中白术内酯Ⅱ含量反而最低,白术内酯Ⅲ最高,白术内酯Ⅰ次之;同样在白术配方颗粒中白术内酯Ⅱ的含量也是最低的,白术内酯Ⅲ最高,白术内酯Ⅰ其次,详细结果见图1。
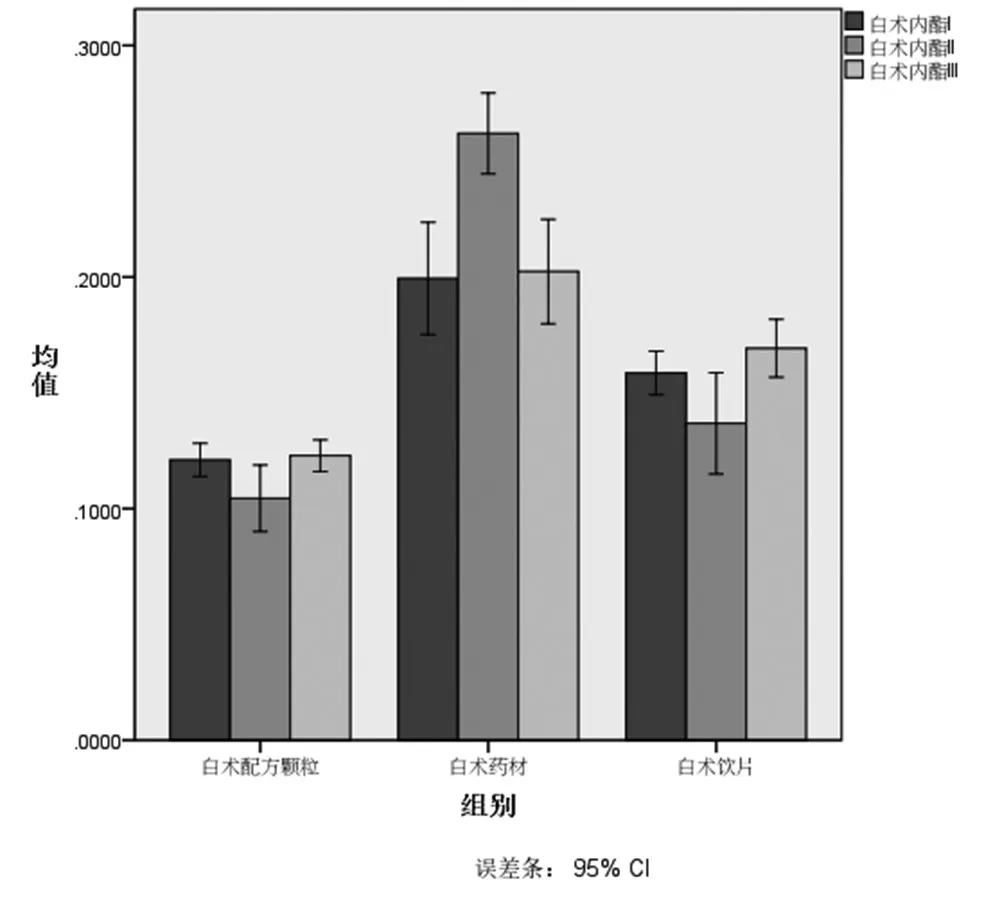
图1 白术药材-饮片-配方颗粒中白术内酯Ⅰ、Ⅱ、Ⅲ含量比较图
2.2 白术药材、饮片及配方颗粒对脾虚模型大鼠相关指标的影响:分述如下。
2.2.1 给药样品的制备:①白术药材提取液制备:取白术药材适量,加入8倍量水,浸泡30min,煎煮1.5h,过滤,药渣加6倍量水,煎煮1h,过滤,合并2次滤液,浓缩成每1ml相当于含1g白术生药的溶液,即得。②白术饮片提取液制备:取白术饮片适量,加入8倍量水,浸泡30min,煎煮1.5h,过滤,药渣加6倍量水,煎煮1h,过滤,合并2次滤液,浓缩成每1ml相当于含1g白术饮片的溶液,即得。③白术配方颗粒药液制备:取白术配方颗粒适量,加水适量,加热溶解,制成每1ml相当于含1g生药的溶液,即得。④大黄水煎液制备:取大黄饮片适量,第1次加8倍量水,浸泡30min,提取1h,过滤;药渣加6倍量水,提取0.5h,过滤,合并2次提取液,浓缩,制成每1ml相当于含1g大黄的浓缩液,即得。
2.2.2 分组、造模和给药:将30只雄性SD大鼠随机分成5组,分别为空白组、模型组、白术药材组、白术饮片组、白术配方颗粒组,每组6只。适应性饲养1周后,空白组大鼠按10ml/kg灌胃给予生理盐水,其余各组均按10ml/kg灌胃给予大黄水煎液,以制备大鼠脾虚模型,每天1次,连续15天。自第16天起,空白组和模型组均按10ml/kg给予生理盐水,其余各组均按10ml/kg分别给予白术药材提取液、白术饮片提取液、白术配方颗粒溶液,每天1次,连续10天。
2.2.3 大体观察:观察各组大鼠的皮毛、大鼠排泄物情况以及活动状况,并分别于造模前、造模后(给药前)以及末次给药后称定体重,采用SPSS 20.0软件对数据进行统计分析,以±s表示,组间比较采用单因素方差分析,P<0.05为差异有统计学意义。
结果显示,造模前,各组大鼠体重比较差异不明显,结果无统计学意义(P>0.05)。造模后,除空白组外,其余各组大鼠均出现食量减小、体型消瘦、大便溏稀、皮毛枯槁、精神萎靡、蜷缩等不同程度的由于脾虚泄泻导致的胃肠道症状;造模后,空白组大鼠体重比同组造模前显著增加,与空白组比较,其余各组大鼠的体重均显著降低,差异具有统计学意义(P<0.01),与模型组比较,白术药材组、白术饮片组大鼠体重显著增加,差异具有统计学意义(P<0.05或P<0.01),白术配方颗粒组大鼠体重变化不明显,差异无统计学意义(P>0.05)。末次给药后,各组大鼠上述脾虚症状均有不同程度改善,空白组、白术药材组、白术饮片组、白术配方颗粒组大鼠的体重均比同组造模前显著增加,与空白组比较,模型组大鼠的体重显著降低,差异具有统计学意义(P<0.05或P<0.01);与模型组比较,白术药材组、白术饮片组、白术配方颗粒组大鼠体重均显著增加,差异均有统计学意义(P<0.01)。结果见表1。
表1 白术药材-饮片-配方颗粒对脾虚模型大鼠体重的影响(±s,g,n=6)

表1 白术药材-饮片-配方颗粒对脾虚模型大鼠体重的影响(±s,g,n=6)
注:与空白组比较,*P<0.01;与模型组比较,#P<0.01。
组别空白组模型组白术药材组白术饮片组白术配方颗粒组末次给药后296.50±10.64 241.00±4.78**285.83±8.04*##281.00±7.32**##266.17±4.40**##造模前243.33±10.67 240.17±4.79 244.83±9.06 241.33±9.87 232.83±4.75造模后276.17±10.59 232.33±4.76**254.17±8.13**##248.33±9.44**#238.00±5.22**
2.2.4 血清GAS、VIP含量测定:末次给药后,将所有大鼠禁食、不禁水12h,腹腔注射3%戊巴比妥钠麻醉,腹主动脉取血,静置1h后,以4000r/min离心10min,分离血清,采用ELISA法,以全波长多功能酶标仪于450nm波长处检测血清GAS和VIP含量。
结果显示,与空白组比较,模型组大鼠血清GAS含量显著降低,VIP含量显著升高,差异均有统计学意义(P<0.01),白术药材组、白术饮片组、白术配方颗粒组大鼠血清GAS含量显著降低,差异具有统计学意义(P<0.01),白术药材组、白术饮片组、白术配方颗粒组大鼠血清VIP含量升高不明显,差异无统计学意义(P>0.05);与模型组比较,白术药材组、白术饮片组、白术配方颗粒组大鼠血清GAS含量均显著提高,白术药材组、白术饮片组、白术配方颗粒组大鼠血清VIP含量均显著降低,差异均具有统计学意义(P<0.01),详细结果见表2。
表2 白术药材-饮片-配方颗粒对脾虚模型大鼠GAS、VIP含量的影响(±s,pg/L,n=6)

表2 白术药材-饮片-配方颗粒对脾虚模型大鼠GAS、VIP含量的影响(±s,pg/L,n=6)
注:与空白组比较,*P<0.01;与模型组比较,#P<0.01。
组别空白组模型组白术药材组白术饮片组白术配方颗粒组VIP 184.50±6.50 221.67±31.65*187.33±8.71#189.33±9.65#190.00±10.51#GAS 245.50±20.32 129.00±7.46*153.17±10.36*#162.67±13.60*#161.50±9.75*#
3 讨论
白术的主要功效为健脾益气,现代药理研究表明其具有调节胃肠道作用,且作用强度与剂量有关,并且炮制、提取方法等对白术的胃肠道作用影响显著。白术中的白术内酯Ⅰ、Ⅱ、Ⅲ是其主要活性成分和特征性成分,通常作为衡量白术药材质量的参考指标[3]。有研究表明,炮制过程中主要的内酯类成分白术内酯Ⅰ、Ⅱ、Ⅲ[4]和苍术酮之间发生复杂的相互转化。本研究结果显示,白术内酯Ⅰ、Ⅱ、Ⅲ在药材中的含量最高,在饮片、配方颗粒中3种成分的含量都有一定程度的降低,表明白术内酯类成分不稳定,易转化,炮制、加热、提取等方法的运用可以促进其转化成其他成分。
中医学认为,脾主运化,称其为“气血生化之源”,其功能与小肠吸收、胃肠激素分泌等密切相关。在中医理论中,脾虚泛指脾气虚损造成的一系列身体脏器失调的多种生理现象。脾虚包含运化功能失常导致营养吸收功能出现障碍,水液失于布散导致体湿痰多等。脾失健运可导致腹胀、泄泻等肠道功能紊乱症状。大黄泻下致大鼠脾虚模型是公认的脾虚模型经典方法之一,故本研究选择该方法建立大鼠脾虚模型[5-7]。脾虚泄泻可导致大鼠肠道功能紊乱,体重下降,故大鼠体重的高低也间接反映了其肠道功能的正常与否。本实验中,造模后大鼠体重明显下降,而给药后白术药材、饮片和配方颗粒组大鼠体重均有明显提升,间接表明了白术药材、饮片、配方颗粒具有调节大鼠胃肠道功能、改善脾虚症状的作用,印证了白术的健脾益气之功效。
GAS是一种很重要的胃肠道激素,主要是由胃窦G细胞分泌,具有调节吸收、转运及代谢等生理活性,是衡量胃肠道生理功能的主要指标,其含量的降低提示消化道功能处于低下或紊乱状态[8]。VIP是肠道主要的抑制性神经递质之一,其可抑制胃酸的分泌,是胃肠道疾病研究的重要指标[9]。本研究中,造模后模型组大鼠血清GAS含量较空白组有显著降低,而VIP含量显著升高。用药后,白术药材、饮片、配方颗粒组大鼠血清GAS含量有一定程度的提升,而其VIP含量有明显降低,这表明白术药材、饮片、配方颗粒对脾虚模型大鼠肠道的改善作用与调节肠道GAS、VIP含量有一定的关系。本实验研究结果并没有揭示白术药材组、白术饮片组、白术配方颗粒组对脾虚模型大鼠的作用与白术内酯Ⅰ、Ⅱ、Ⅲ有明确的量效关系,有待进一步实验研究。
