Al(OH)3胶体、腐殖酸和碳酸铀酰在饱和多孔介质中的共迁移①
2021-11-13王红强胡鄂明雷治武王清良
李 惠,王红强,侯 伟,胡鄂明,雷治武,王清良
(南华大学 资源与环境安全工程学院,稀有金属矿产开发与废物地质处置技术湖南省重点实验室,湖南 衡阳 421001)
CO2+O2地浸采铀具有成本低、污染小、资源利用率高等优点[1]。但我国已知的砂岩型铀矿大都具有矿层堵塞问题,一旦铀在迁移过程中出现沉积、阻塞,就会降低铀的提取效率。地浸采铀工艺中形成的Al(OH)3胶体对重金属有很强的吸附作用,从而对铀的迁移造成影响,导致矿层严重堵塞[2-3]。此外,地下水中含有的腐殖酸(HA)在铀迁移过程中扮演了重要角色[4-6]。胶体在多孔介质中的释放、运移和沉积机制受到流速、离子强度、pH值、介质粒径和含水量等一系列因素的影响[7-8],其中流速是影响胶体与铀在多孔介质中迁移行为的重要因素[9]。
本文在pH=7.6条件下,通过柱实验考察不同流速下,Al(OH)3胶体、UC(Ⅵ)、Al(OH)3-UC(Ⅵ)和Al(OH)3-UC(Ⅵ)-HA在饱和石英砂介质中的迁移规律,以期了解CO2+O2地浸采铀工艺中Al(OH)3胶体和HA对UC(Ⅵ)迁移的影响。
1 实 验
1.1 实验试剂及仪器
实验试剂:石英砂、腐殖酸(HA)、Al(NO3)3·9H2O、NH3·H2O、HCl、NaOH、碳酸铀酰溶液等,均为分析纯试剂;实验用水为去离子水。
实验仪器:85-2C型磁力搅拌器、TSX-100型超声仪、麦克ASAP460型自动比表面积仪、883 Basic IC plus Metrohm型阴离子色谱仪、Nano ZS90 Malvern型激光粒度仪、pHBJ-260型pH测量仪、BQ80S型蠕动泵、202-2A型电热恒温干燥箱、UV-2400型紫外-可见分光光度计、BSZ-100型自动收集器等。
1.2 材料制备方法
腐殖酸(HA)溶液:用去离子水配制成20 mg/L的HA悬浮液。
Al(OH)3胶体由Al(NO3)3·9H2O和NH3·H2O制备而成[2],并通过低温冷冻干燥技术获得Al(OH)3胶体粉末。
Al(OH)3(100 mg/L)胶体溶液:称取100 mg Al(OH)3胶体粉末,加入1 L去离子水,用磁力搅拌器搅拌15 min后超声处理30 min,得到均匀分散的100 mg/L Al(OH)3胶体溶液。采用浓度均为0.1 mol/L的HCl或NaOH调节溶液pH=7.6。
饱和石英砂(SQS)的制备:将石英砂过0.212~0.500 mm分析筛后,用0.1 mol/L HNO3(70%)和0.1 mol/L NaOH反复清洗去除杂质后,105℃干燥,备用。
1.3 实验方法
柱实验流程如图1所示。采用湿法填充的SQS作为多孔介质,在亚克力柱(柱长153 mm、内径26 mm)中进行柱实验,孔隙率0.47,容重1.403 g/cm3。用蠕动泵控制溶液按不同流速(0.401、0.802、2.005 cm/min)以下进上出方式穿透SQS柱。实验前注入10个孔隙体积(PV)所需pH值的背景溶液,对柱进行预平衡。然后将7PV的Al(OH)3/UC(Ⅵ)抽入SQS中进行穿透实验。最后,再次通过5PV的背景溶液洗脱。流出液用自动收集器定期收集。测定流出液中Al(OH)3/UC(Ⅵ)浓度、pH值、Zeta电位和粒径。每组实验参数下的SQS柱均在重新填充后使用。以10 mg/L的Br-作为示踪剂进行穿透试验,过程与胶体实验相同。

图1 柱实验流程图
分析方法:用紫外-可见分光光度计测定UC(Ⅵ)和Al(OH)3胶体浓度,用阴离子色谱仪测定Br-浓度。分别用激光粒度仪和Zeta电位分析仪测定胶体粒径和Zeta电位。
根据Br-的穿破数据拟合CXTFIT结果计算纵向分散系数(D)[10]。假定胶体的分散系数与示踪剂相同。在柱实验中,穿透曲线用BTCs表示,BTCs为孔隙体积的函数,以相对浓度C/C0表示,其中C和C0分别表示UC(Ⅵ)或Al(OH)3流出液浓度和溶液初始浓度。
2 实验结果及讨论
2.1 流速对单一迁移体系的影响
2.1.1 流速对UC(Ⅵ)单一迁移体系的影响
运移模型纵向分散系数(D)拟合结果如表1所示。UC(Ⅵ)浓度20 mg/L,不同流速下UC(Ⅵ)在饱和石英砂中的穿透曲线如图2所示。随着流速增加,UC(Ⅵ)的BTCs峰值从右向左明显移动,峰值逐渐增加(0.401、0.802和2.005 cm/min时BTCs分别为0.92、0.95和0.97),迁移率也相应增加。说明UC(Ⅵ)的运移受流速的影响较小。此外,随着流速增加,UC(Ⅵ)穿透时间提前,出水相对浓度提高。淋洗曲线存在一定拖尾现象,说明UC(Ⅵ)的解吸具有一定的滞后性[11]。
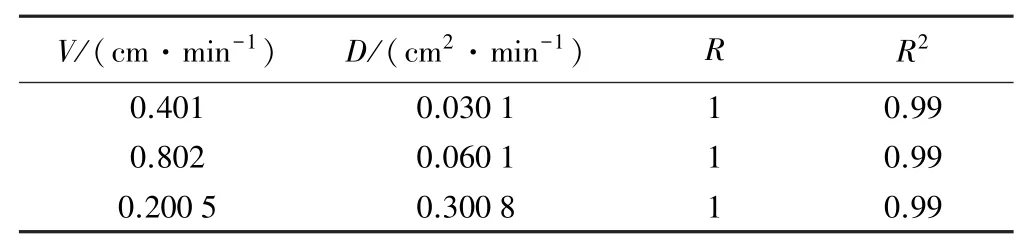
表1 不同流速下保留示踪剂在饱和石英砂柱中的运移拟合参数

图2 流速对UC(Ⅵ)单一迁移体系的影响
2.1.2 流速对Al(OH)3单一迁移体系的影响
Al(OH)3浓度100 mg/L,流速对Al(OH)3单一迁移体系的BTCs如图3所示。与UC(Ⅵ)的单一迁移相比,Al(OH)3的运移受流速影响较大。低流速下,有利于Al(OH)3胶体的沉积,增大堵塞的几率;流速增加,Al(OH)3胶体流出量逐渐增多,Al(OH)3的BTCs峰值呈现增加趋势。这是因为表面带正电荷的Al(OH)3胶体与表面带负电荷的石英砂产生了较强的静电引力,使Al(OH)3胶体有可能沉积、堵塞在砂柱的孔隙中。此现象与文献[12-13]研究结论一致。

图3 流速对Al(OH)3单一迁移体系的影响
2.2 流速对Al(OH)3-UC(Ⅵ)二元迁移体系的影响
2.2.1 流速对Al(OH)3-UC(Ⅵ)二元体系中UC(Ⅵ)运移的影响
Al(OH)3浓度100 mg/L、UC(Ⅵ)浓度20 mg/L,不同流速下Al(OH)3-UC(Ⅵ)二元体系中UC(Ⅵ)在饱和石英砂中的BTCs运移规律见图4。与UC(Ⅵ)单独迁移相比,UC(Ⅵ)-Al(OH)3体系中UC(Ⅵ)运移的BTCs峰值随着流速增大先增大后减小。随着流速增大,UC(Ⅵ)在介质中的沉积量增加,多孔介质堵塞几率增加,迁移率降低。当流速为2.005 cm/min时,UC(Ⅵ)流出量明显少于其他流速,沉积量最多,迁移率最小。这说明,二元迁移体系中,UC(Ⅵ)的运移受流速的影响,Al(OH)3的存在会在一定程度上抑制UC(Ⅵ)的运移。
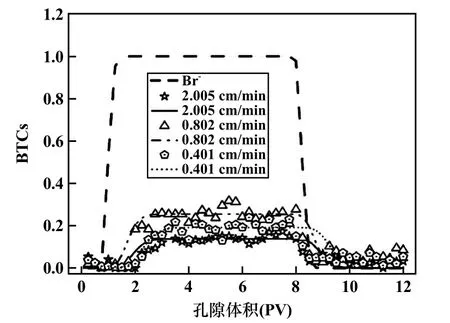
图4 流速对Al(OH)3-UC(Ⅵ)二元体系中UC(Ⅵ)运移的影响
2.2.2 流速对Al(OH)3-UC(Ⅵ)二元体系中Al(OH)3运移的影响
图5为不同流速下Al(OH)3-UC(Ⅵ)二元迁移体系中UC(Ⅵ)在饱和石英砂中的运移规律,其中Al(OH)3浓度100 mg/L,UC(Ⅵ)浓 度20 mg/L。与Al(OH)3单独迁移相比,UC(Ⅵ)的存在也会在一定程度上抑制Al(OH)3的运移。Al(OH)3的运移受流速的影响,在流速为2.005 cm/min时,Al(OH)3流出量最少,沉积量最多,更有利于矿层堵塞,从而导致迁移率最小。
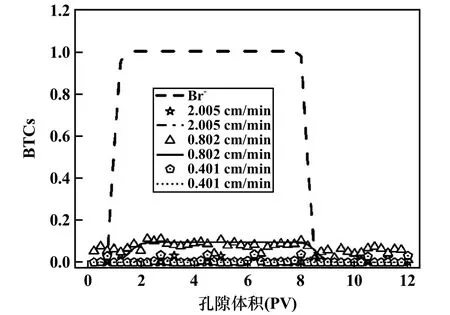
图5 流速对Al(OH)3-UC(Ⅵ)二元体系中Al(OH)3运移的影响
不同体系柱实验的参数以及胶体和UC(Ⅵ)的电动性能和质量回收率见表2。由表2可知,当流速从0.401 cm/min增至2.005 cm/min时,Al(OH)3的Zeta电位均为负值,但粒径从862.0 nm减至322.6 nm再增至1 426.3 nm。在运移初期,粒径增加使得Al(OH)3和UC(Ⅵ)更难通过石英砂介质之间的孔隙。Arnarson等人将这种增加归因于配体交换反应引起的Al(OH)3与HA之间的化学结合[14]。
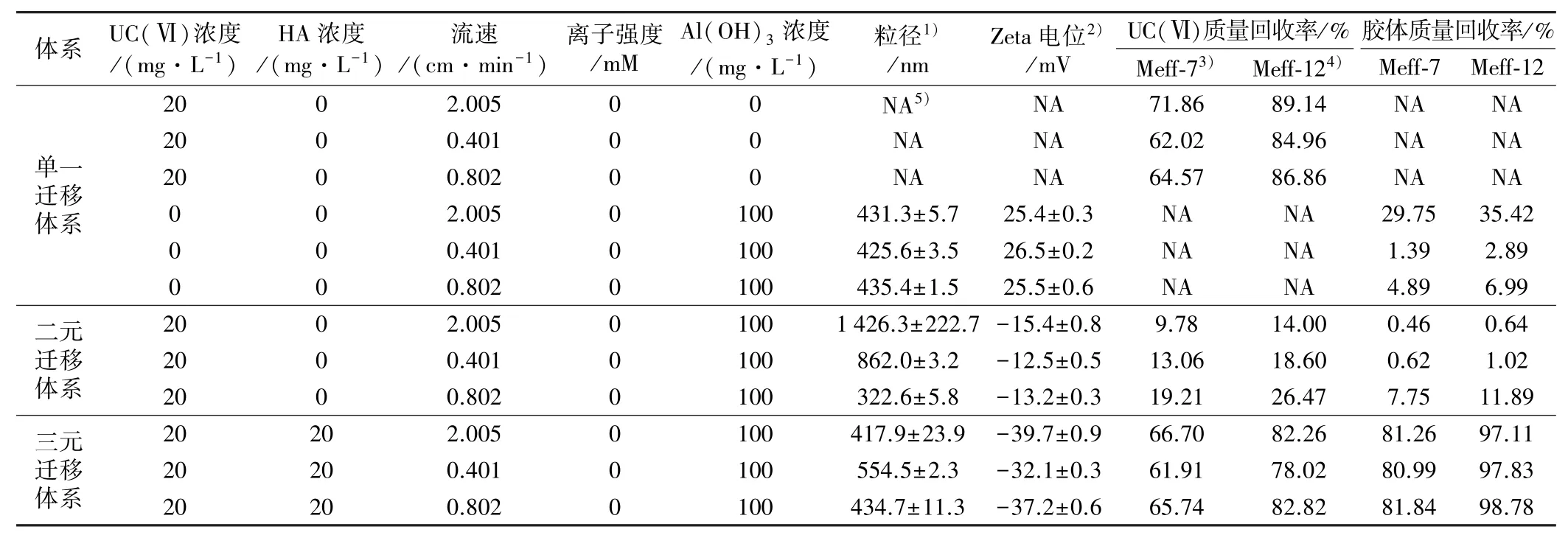
表2 不同体系柱实验参数以及胶体、UC(Ⅵ)电动性能和质量回收率(Meff)
2.3 流速对Al(OH)3-UC(Ⅵ)-HA三元迁移体系的影响
2.3.1 流速对Al(OH)3-UC(Ⅵ)-HA三元体系中UC(Ⅵ)运移的影响
流速对Al(OH)3-UC(Ⅵ)-HA三元迁移体系中UC(Ⅵ)运移的影响见图6,其中Al(OH)3浓度100 mg/L、UC(Ⅵ)浓度20 mg/L、HA浓度20 mg/L。由图6可知,三元迁移体系中UC(Ⅵ)的BTCs峰值相差不大,且流速为0.802 cm/min和2.005 cm/min时的BTCs峰值几乎重叠。这说明,当流速增至0.802 cm/min时,UC(Ⅵ)的运移基本不再随着流速增加而变化。但对比UC(Ⅵ)单独迁移,三元迁移体系中低流速的突破时间都相对提前,这表明HA在一定程度上能促进UC(Ⅵ)的运移。这一结论与文献[15]研究结论一致。在富含HA胶体的石英砂柱中,UC(Ⅵ)作为HA胶体携带物质而迁移,可以促进U(Ⅵ)的迁移。对比同一流速下UC(Ⅵ)单独迁移,三元体系中的质量回收率(Meff)相对下降,说明部分UC(Ⅵ)运移受阻,这可能是多孔介质对胶体的过滤作用所致。

图6 流速对Al(OH)3-UC(Ⅵ)-HA体系中UC(Ⅵ)运移的影响
2.3.2 流速对Al(OH)3-UC(Ⅵ)-HA三元体系中Al(OH)3运移的影响
流速对Al(OH)3-UC(Ⅵ)-HA三元体系中Al(OH)3运移的影响见图7,其中Al(OH)3浓度100 mg/L、UC(Ⅵ)浓度20 mg/L、HA浓度20 mg/L。由图7发现,对比Al(OH)3单独迁移,UC(Ⅵ)-Al(OH)3-HA三元体系中Al(OH)3的BTCs几乎与示踪剂的穿透曲线重叠,Al(OH)3的迁移速度与示踪剂相当。这说明,在这种条件下,Al(OH)3的运移基本不受流速影响。但对比Al(OH)3单独迁移,HA存在条件下,能够显著促进Al(OH)3运移,大幅度增加质量回收率,相应加快穿透速度。结合表2数据可知,这是由胶体表面的Zeta电位变化引起的,胶体表面电荷从正变为负,胶体与介质表面之间的相互作用从静电引力变为静电斥力,从而促进了HA和Al(OH)3的迁移,所以HA的存在有利于Al(OH)3的运移,这与先前的研究结果一致[16-17]。
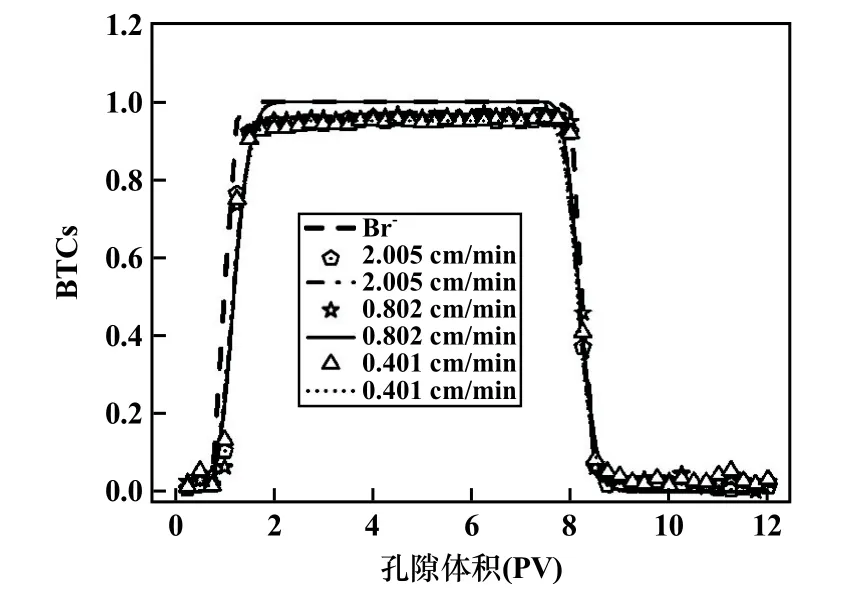
图7 流速对Al(OH)3-UC(Ⅵ)-HA体系中Al(OH)3运移的影响
2.4 DLVO相互作用能
胶体作为污染物的携带者,其稳定性对污染物的迁移具有重要影响[15]。而介质间的范德华力和静电斥力所决定的粒径大小、团聚快慢和团聚可逆性会影响胶体稳定性[4]。本文采用Derjaguin-Landau-Verwey-Overbeek(DLVO)理论对Al(OH)3稳定性和UC(Ⅵ)迁移进行定性分析。
通过DLVO理论计算得到Al(OH)3胶体与石英砂表面的总相互作用能(ФDLVO),总相互作用能为正值表示胶体与介质表面主要为静电斥力,负值则表示主要为静电引力。Al(OH)3-UC(Ⅵ)二元迁移体系在不同流速下的总相互作用能见图8,其中Al(OH)3浓度100 mg/L、UC(Ⅵ)浓度20 mg/L。

图8 Al(OH)3-UC(Ⅵ)二元迁移体系在不同流速下的总相互作用能
在本研究中,这两种胶体表现出负的Zeta电位电荷均匀性,溶质UC(Ⅵ)主要以UO2(CO3)34-形式存在。然而,随着体系的变化,胶体粒子的粒径变化明显(见表2)。从图8可以看出,Al(OH)3胶体与石英砂表面之间的相互作用主要为静电斥力。在Al(OH)3-UC(Ⅵ)二元迁移体系中,当流速从0.401 cm/min增至2.005 cm/min时,最大排斥势垒(Фmax)从166.47减至66.59后增至361.7 KBT。Фmax越大,Al(OH)3颗粒之间的排斥力越强,团聚和沉积在柱中的可能性越小[18]。因此,理论上在高流速(2.005 cm/min)下,Al(OH)3和UC(Ⅵ)的迁移性大。但实际上,流速0.802 cm/min时的迁移性最高,Al(OH)3和UC(Ⅵ)的质量回收率(Meff)分别为11.89%和26.41%。这说明,在运移过程中,Al(OH)3胶体发生了强烈的吸附反应而沉积到了石英砂的表面,并且流速增大所产生的静电斥力小于Al(OH)3胶体与石英砂之间的吸附力,导致Al(OH)3胶体吸附性增强[2]。
2.5 保留剖面与出水特性
将保留剖面绘制为UC(Ⅵ)、Al(OH)3的归一化固相浓度随柱入口距离的变化,不同迁移系统中UC(Ⅵ)和Al(OH)3的保留剖面见图9。图9所示的出水悬浮液的保留剖面(RPs)有助于解释Al(OH)3和UC(Ⅵ)的沉积/吸附机理。在二元迁移体系中,UC(Ⅵ)的质量比初始浓度值(S/C0)随流速增加先减小后增加,随运移距离增加而减小。Al(OH)3的S/C0随流速增加先增加后减小,随运移距离增加而减小。随着距离增加,所有迁移体系都出现了超指数下降,流速0.802 cm/min时,下降指数比其他条件小得多,这表明流速0.802 cm/min时,可以促进UC(Ⅵ)和Al(OH)3的运移。

图9 不同迁移系统中UC(Ⅵ)和Al(OH)3的保留剖面
Al(OH)3颗粒粒径和Zeta电位在二元运输体系中的变化规律如图10所示。在二元体系中,随着PV增加,Al(OH)3颗粒粒径变化不大。流速0.401 cm/min和2.005 cm/min时Al(OH)3颗粒粒径大于流速0.802 cm/min时的粒径。粒径增大会增强沉积作用。Zeta电位随PV增加而增加。较小的粒径和较大的负Zeta电位意味着Al(OH)3颗粒之间静电斥力增加,Al(OH)3颗粒和UC(Ⅵ)更易于在柱中迁移[3]。
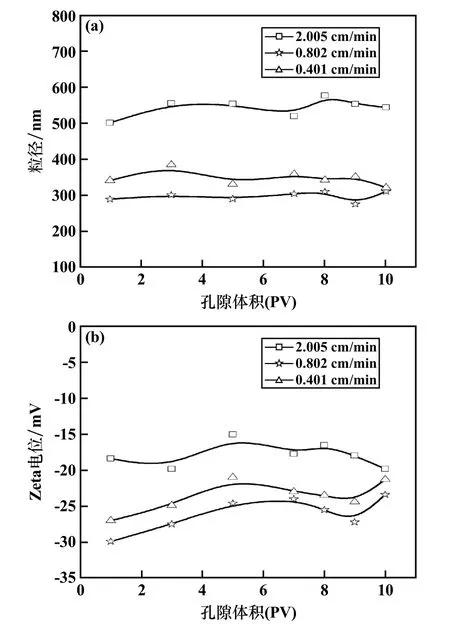
图10 不同迁移系统中出水Al(OH)3粒径和Zeta电位变化
3 结 论
1)单一迁移体系中,流速对Al(OH)3运移的影响大于对UC(Ⅵ)运移的影响。
2)二元迁移体系中,流速对UC(Ⅵ)和Al(OH)3的运移产生影响,流速为2.005 cm/min时,UC(Ⅵ)和Al(OH)3的迁移率最小;UC(Ⅵ)和Al(OH)3在一定程度上相互抑制迁移。
3)三元迁移体系中,UC(Ⅵ)和Al(OH)3的运移基本不会随着流速变化而发生改变。相比其他运移体系,UC(Ⅵ)和Al(OH)3的迁移率都会因腐殖酸(HA)的存在而显著提高。
