复方庆大霉素颗粒剂制备与含量测定方法的建立
2021-11-12彭君茹左儒楠陈胡羚李引乾
彭君茹,左儒楠,陈胡羚,李引乾*
(1.拉萨市第一中等职业技术学校,西藏拉萨 850000;2.南京农业大学动物医学院,江苏南京 210095;3.西北农林科技大学动物医学院,陕西杨凌 712100)
庆大霉素是一种从小单孢子菌属中生产的具有相似构造的多组方氨基糖苷类抗生素[1],常用其硫酸盐形式。与其他氨基糖苷类抗生素抗菌机制类似,均是通过阻碍细菌蛋白质的正常合成,并破坏细胞膜而发挥抗菌作用[2]。庆大霉素抗菌谱广,对多种革兰氏阳性菌与阴性菌都具有抑菌和杀菌作用[3]。但随着庆大霉素在临床中的不合理应用,其抗菌活性降低,且长期大量使用可能对肾脏和耳神经产生伤害。黄芩苷具有抗菌、消炎、抗肿瘤、抗病毒及消除体内毒素、降压镇静、清热燥湿等多种药理作用[4]。黄芩苷的加入不仅能降低庆大霉素对耳的毒性,而且能够减少其耐药菌株[5]、增强其抗菌活性[6]。硫酸庆大霉素与双黄连口服液联合使用,体外抑菌试验表明,两者联合后抑菌效果加强,呈相加作用[6]。本试验根据致病机制和临床用药,将两种药物按一定的配比制成复方颗粒剂,并对其含量进行测定,以保证药物含量,提高联合用药的效率,降低庆大霉素在临床应用中的不合理性[7]。
1 材料与方法
1.1 材料
1.1.1 菌种 多杀性巴氏杆菌、无乳链球菌、沙门氏菌、大肠埃希氏菌、金黄色葡萄球菌,由西北农林科技大学动物医学院病原微生物实验室惠赠。
1.1.2 药品与试剂 硫酸庆大霉素原料药(含量99.2%),批号20160916,烟台只楚药业有限公司产品;黄芩苷原料药(含量85%),批号20160922,四川恒瑞通达生物科技有限公司产品;硫酸庆大霉素对照品(含量90.0%),批号20160912,中国兽药监察所产品;黄芩苷对照品(含量95.5%),批号20160918,中国药品生物制品检定所产品;β-环糊精,分析纯,天津市天力化学试剂有限公司产品;蛋白胨(批号20160715)、牛肉膏(批号20160716)、琼脂(批号20160721),北京奥博星生物技术有限责任公司产品;氯化钠(批号20160913)、氢氧化钠(批号20160928),天津科密欧化学试剂有限公司产品。
1.1.3 主要仪器 电热恒温水浴锅(HH-S1),大连医疗器械厂产品;电子分析天平(BS-210S),德国赛多利斯sarto-rius股份有限公司产品;高压蒸汽灭菌锅(YXQ-LS-SⅡ),济南思卓医疗器械有限公司产品;洁净工作台100级(SW-CJ-1F),苏州安泰空气技术有限公司产品;电热恒温培养箱(DH-420AS),由北京科伟永兴仪器有限公司产品;L5紫外分光光度计,上海仪电分析仪器有限公司产品;旋光仪、制粒筛、标准检验筛,江阴市祝塘机械厂产品;BKH气流烘干器,河南予华仪器有限公司产品。
1.2 方法
1.2.1 复方庆大霉素颗粒剂的制备
1.2.1.1 普通琼脂平板的制备 琼脂15 g、蛋白胨10 g、牛肉膏5 g、氯化钠5 g,将其溶于1 000 mL蒸馏水内,加热至溶解,待其冷却到适宜温度后,无菌条件下倒入培养皿中,冷却后备用。
1.2.1.2 细菌悬液制备 将9支灭菌的试管分别标记为1号~9号管,然后向每支试管内加入9 mL生理盐水。无菌环境下,用移液枪吸菌液1 mL加入1号试管中,混匀后吸1 mL加入2号试管,按上述方法,稀释至9号试管。
制备好的普通琼脂培养皿20套,5号~9号管各标记4套。依次从5号~9号管内吸取100 μL菌液放入培养皿,用棉签涂布均匀,37℃培养24 h,统计菌落数为30~300的培养皿,计算平均值,配成浓度为5×106CFU/mL的菌悬液,于4℃冰箱保存[8]。
1.2.1.3 庆大霉素和黄芩苷最佳比例的确定 保持庆大霉素和黄芩苷的总质量不变,设计5个浓度梯度,庆大霉素和黄芩苷比例依次为1∶1、2∶1、3∶1、4∶1和5∶1。精确称取相应的药品,分别取对应质量的黄芩苷溶于蒸馏水用1 mol/mL的氢氧化钠调pH至7.0,至溶液溶解,再加入庆大霉素溶解、过滤除菌。无菌环境下将制备好的上述5种细菌悬液,用灭菌棉签均匀涂布于固体培养皿中;植入牛津杯、加入不同比例的药物200 μL;每个病原菌做3个样,37℃培养24 h后,测抑菌圈大小,取平均值,直径越大效果越佳;当直径相同时以庆大霉素用量最少的为最佳方案。
1.2.2 复方庆大霉素颗粒剂配方的确定 以庆大霉素为主药,以黄芩苷为辅药,待两者比例确定后加入赋形剂β-环糊精,根据兽药典相关规定,确定3种物质在该剂型中的配比。
1.2.3 复方庆大霉素颗粒剂的制备工艺 按上述试验中确定的药物比例,准确称取庆大霉素原料药、黄芩苷原料药和β-环糊精,均匀混合、加入蒸馏水适量,搅拌均匀,使其呈现“握之成团、轻拍即散”状态。经16目制粒筛制备,烘干箱内60℃放置30 min,冷却至室温过20目筛,即可。
1.2.4 复方庆大霉素颗粒剂中庆大霉素的含量测定
1.2.4.1 确定合适的波长 依据相关文献,确定用旋光法测定庆大霉素含量时所用的波长,其波长为589.3 nm[9]。
1.2.4.2 制备标准曲线 精密称取庆大霉素对照品10.028 8 mg,烧杯中加蒸馏水,待溶解后移入100 mL容量瓶,定容后为100 mg/mL庆大霉素溶液。分别吸取1、2、3、4、5、6、7 mL庆大霉素溶液,定容于200 mL容量瓶中分别得0.5、1、1.5、2、2.5、3、3.5 mg/mL的庆大霉素溶液。空白对照组是蒸馏水,在确定波长下测上述7个样品比旋度,绘制标准曲线,横坐标为比旋度,纵坐标为浓度。
1.2.4.3 回收率试验 按制作标准曲线中的方法,分别制备质量为0.5、1.8、3.5 mg/mL的庆大霉素标准溶液,空白对照组以蒸馏水代替,测定其回收率。
1.2.4.4 重复性试验 用测定回收率试验中质量浓度为1.8 mg/mL的样品,重复测定6次比旋度之后计算RSD。
1.2.4.5 精密度试验 用回收率试验中3个样品,测定日内、日间精密度。日内精密度测定方法:每隔4 h测定1次,连测3次;日间精密度测定方法:每天测1次,连测3 d;计算对应浓度和平均值RSD。
1.2.4.6 复方庆大霉素颗粒剂中庆大霉素含量测定 准确称取10.046 0 g复方庆大霉素颗粒剂,于研钵磨碎溶于烧杯内,取1 mol/mL的氢氧化钠溶液调节pH至中性,完全溶解后转到100 mL容量瓶中,制成质量浓度为100 mg/mL的复方庆大霉素颗粒剂药液(以庆大霉素含量计算),2 500 r/min离心30 min,取上清后过滤,直至澄清。取2.5 mL稀释到100 mL容量瓶,得质量浓度是2.5 mg/mL的溶液(以庆大霉素含量计算)。空白对照以蒸馏水代替,按建立的测定方法,在已确定的波长下扫描,测定其比旋度,每组平行3个样,代入标准曲线计算出实际浓度,并计算复方庆大霉素颗粒剂中庆大霉素的含量。
1.2.5 复方庆大霉素颗粒剂中黄芩苷的含量测定
1.2.5.1 选择紫外吸收波长 取黄芩苷标准品41.20 mg,烧杯中加蒸馏水使其溶解,用1 mol/mL的氢氧化钠调节pH到中性,待完全溶解,转移至200 mL容量瓶,制得质量为200μg/mL黄芩苷样品。吸取10 mL上述液体稀释到100 mL,得20 μg /mL黄芩苷样品。空白对照组是蒸馏水,190 nm~400 nm处扫描,记录波长。
1.2.5.2 制备标准曲线 依次从制备好的200 μg/mL的黄芩苷样品中吸取0.5、1.5、2.5、3.5、4.5、5.5、6.5 mL,分别用蒸馏水定容至100 mL容量瓶,得浓度为1、3、5、7、9、11、13 μg/mL的黄芩苷标准溶液,空白对照为蒸馏水。190 nm~400 nm处测上述7个样品的吸光度,绘制标准曲线,横坐标代表吸光度,纵坐标代表浓度。
1.2.5.3 回收率试验 用制作标准曲线中方法,制备浓度为2、8、14 μg/mL的黄芩苷标准溶液,空白对照组以蒸馏水代替,测定其回收率。
1.2.5.4 重复性试验 用测定回收率试验中8 μg/mL的黄芩苷标准溶液,于确定的波长处重复测定6次吸光度,之后计算RSD。
1.2.5.5 精密度试验 取回收率试验中3个样品,测定日内、日间精密度。日内精密度测定方法:每隔4 h测定1次,连测3次;日间精密度测定方法:每天测1次,连测3 d;计算对应浓度和平均值RSD。
1.2.5.6 复方庆大霉素颗粒剂中黄芩苷含量测定 准确取1 g复方庆大霉素颗粒剂,研钵磨碎并溶解在烧杯内,取1 mol/mL的氢氧化钠调节其pH到中性,完全溶解后移到250 mL容量瓶,制200 μg/mL的溶液(以黄芩苷含量计算),2 500 r/min离心30 min,取上清后过滤,至澄清。取1 mL上述溶液稀释至80 mL,得浓度为2.5 μg/mL的黄芩苷样品,空白对照以蒸馏水代替,依建立的方法,测定吸光度,每组测3次,代入标准曲线计算黄芩苷的含量。
2 结果
2.1 复方庆大霉素颗粒剂制备结果
庆大霉素∶黄芩苷=1∶1,抑菌圈直径为26.13 mm±1.42 mm;庆大霉素∶黄芩苷=2∶1,抑菌圈直径为27.71 mm±1.44 mm;庆大霉素∶黄芩苷=3∶1,抑菌圈直径为28.16 mm±0.89 mm;庆大霉素∶黄芩苷=4∶1,抑菌圈直径为29.25 mm±2.1 mm。庆大霉素∶黄芩苷=5∶1,抑菌圈直径为28.45 mm±0.73 mm。庆大霉素与黄芩苷比例为4∶1时抑菌圈直径最大,具有良好的抑菌效果,因此4∶1为最佳配比。按中国兽药典对于黄芩苷和庆大霉素相关规定及两者最佳配比,确定复方庆大霉素颗粒剂中各组分所占比例分别为庆大霉素10%,黄芩苷2.5%,β-环糊精87.5%。制备复方庆大霉素颗粒剂500 g,5袋分装,每袋100 g。外观呈淡黄色,其大小为200 μm~1 700 μm。
2.2 复方庆大霉素颗粒剂中其含量测定结果
中国兽药典附录中记载,旋光法测量庆大霉素含量时所用波长为589.3 nm。庆大霉素标准曲线见表1。庆大霉素标准曲线方程为:α=0.205 14C+0.004 6,相关系数为0.997 6,表明庆大霉素于0.5 mg/mL~3.5 mg/mL范围内线性关系良好。庆大霉素平均回收率98%~99%(表2),RSD小于1%,提示回收率良好,可用来测庆大霉素含量。平均比旋度为0.378±0.003,RSD为0.31%,远小于2%,表明重复性良好(表3)。日间和日内精密度RSD都小于5%(表4),该法精密度良好。复方庆大霉素颗粒剂中庆大霉素含量测定结果为2.37、2.39、2.44 mg/mL,平均含量为2.40 mg/mL,为标示量的96%,符合兽药典的规定。

表1 不同浓度庆大霉素溶液的旋光度测定结果
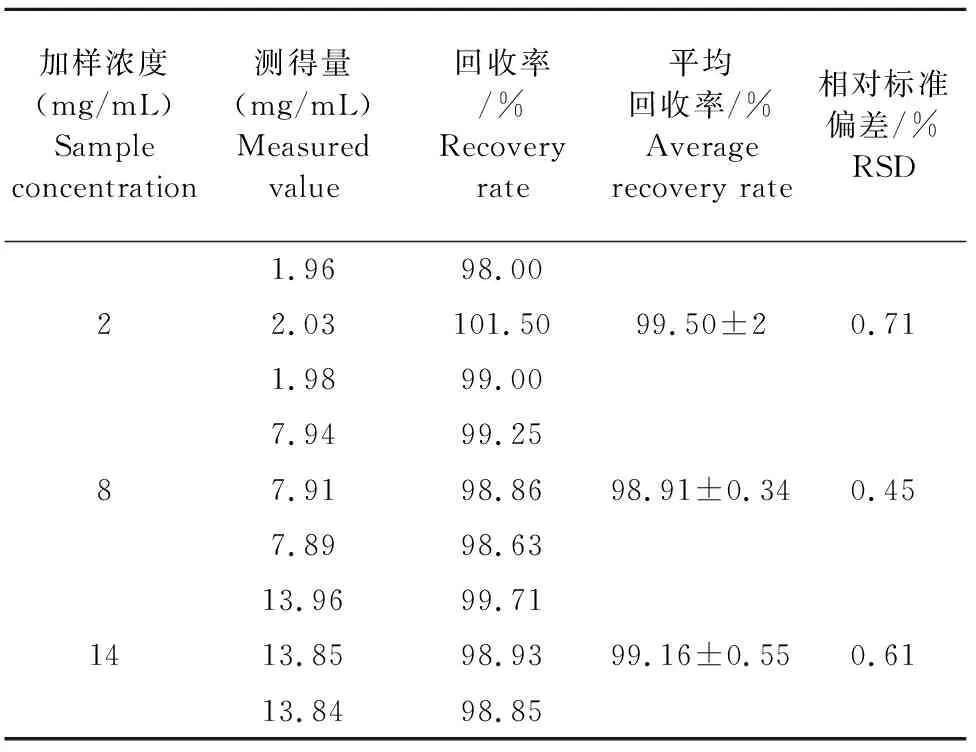
表2 庆大霉素回收率试验结果

表3 庆大霉素的重复性试验结果

表4 庆大霉素精密度试验结果

表5 不同浓度黄芩苷溶液的紫外吸光度测定结果
2.3 复方庆大霉素颗粒中黄芩苷含量测定结果
图1曲线有2个峰,1个在200 nm处,1个约在276 nm处,200 nm为氢氧化钠的波峰,则黄芩苷在276 nm有最大吸收峰。黄芩苷的标准曲线方程为:A=0.064C+0.002 2,其相关系数为0.999 8(表5);说明黄芩苷溶液在1 μg/mL~13 μg/mL范围内线性良好。黄芩苷平均回收率为98%~102%,RSD均小于1%,回收率良好(表6),可用于测黄芩苷的含量。黄芩苷重复性试验中,黄芩苷平均吸光度是0.159 9,RSD是1.50%,小于2%,该法重复性良好。日间和日内精密度RSD均小于5%,该法精密度良好(表7)。复方庆大霉素颗粒剂中黄芩苷的平均含量为2.43 μg/mL,为标示量的97.2%,符合相关规定。
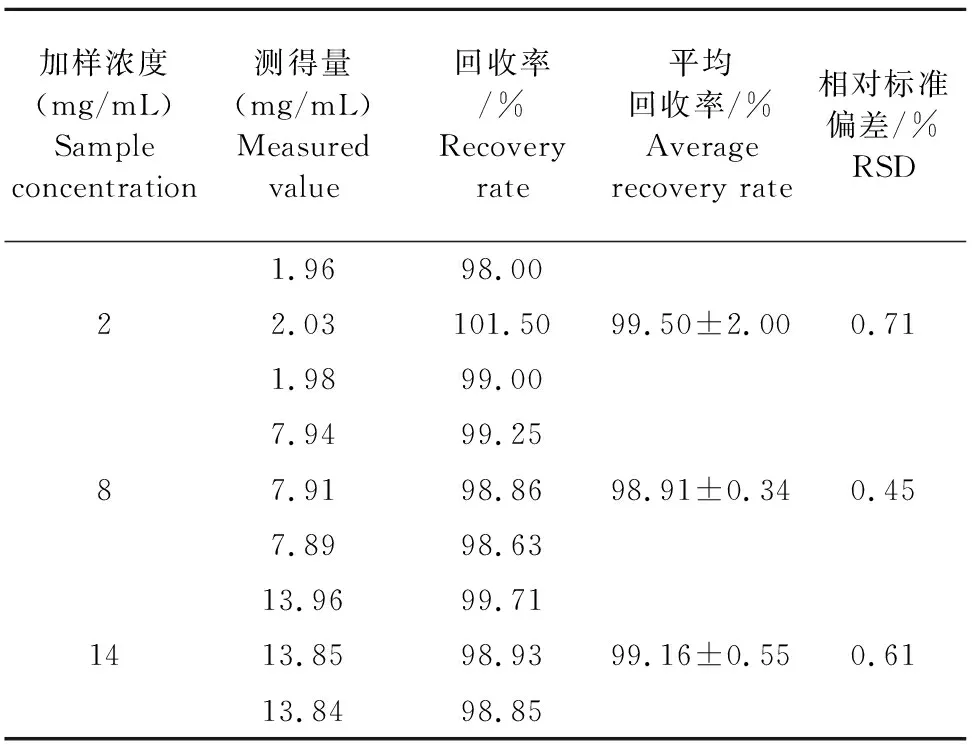
表6 黄芩苷回收率试验结果

表7 黄芩苷精密度试验结果

图1 黄芩苷紫外吸收波谱图
3 讨论
庆大霉素和黄芩苷含量测定方法较多,有紫外分光光度法、旋光仪法、高效液相色谱法(HPLC)等。HPLC方法的建立程序复杂且操作繁琐,而使用紫外分光光度法则要求药物浓度不宜太高,否则会同吸收峰的物质所干扰,而无法得到准确的数据;旋光法是利用物质的旋光性来测定溶液浓度。对于有旋光性的物质来说,使用旋光法测定则更有意义。同时旋光法操作简单快捷,适用于颗粒剂中具有旋光性物质的含量测定。用旋光仪法测定庆大霉素含量,结果发现其与微生物法、比色皿法无显著差异,且样本不需特殊处理,方便快捷,适用于生产要求。对于黄芩苷含量的测定则以紫外分光光度法最为便捷,操作方法简单,灵敏度高且黄芩苷本身不具有旋光性。同时测定结果准确度与精确度高,且和HPLC无明显差异[10]。本研究通过选择特定波长,建立一系列含量测定方法,最终确定用紫外分光光度法于276 nm处测定黄芩苷的含量,用旋光法在589.3 nm处测定庆大霉素的含量。
复方庆大霉素颗粒剂含有黄芩苷和β-环糊精,二者均不易溶于水,制备过程中会产生一些杂质,故配制的复方庆大霉素颗粒剂溶液中略显浑浊,因此在制备之前需先采用离心取上清的方法,再进行测定含量。另一方面,黄芩苷在水中溶解度较低,水溶液呈酸性,因此在配制相应溶液时,需用1 mol/mL的氢氧化钠调节其pH至中性,使其溶解完全。
本试验分别采用旋光法和紫外分光光度法测定复方庆大霉素颗粒剂中庆大霉素和黄芩苷的含量,其检测结果精确度较高,可用于两种成分的含量测定。此外,该方法可为复方庆大霉素颗粒剂的质量控制提供依据,并为复方庆大霉素颗粒剂的深入研究奠定了基础。
