一种用于过氧化氢检测的新型银纳米簇荧光探针的制备
2021-11-09徐鹤丹马艺璇罗湖深张园园廖晓玲
徐鹤丹 马艺璇 罗湖深 张园园 廖晓玲
(重庆科技学院冶金与材料工程学院, 重庆 401331)
骨关节炎(OA)是关节组织的最常见疾病,被称作世界头号高致残性疾病,易发于负重关节,如颈椎、腰椎、膝盖等部位,通常伴随着关节疼痛和僵硬,致病因素一般认为是关节负荷过重、受力不均衡[1]。有关数据显示,早在2015年,我国OA患者累计超过1亿人,且随着老龄化趋势的加重,OA患病人数与日俱增。每年的10月12日被世界卫生组织确立为世界骨关节日,旨在呼吁人们重视对OA的预防和治疗。早期诊断是对OA治疗的关键,但通常的影像学检查对早期患者的症状体征并不敏感[2]。关节软骨细胞通常处于低氧环境中,但在出现关节病变时,氧分压处于一种波动的状态,为了应对高氧分压和炎症,关节软骨细胞中的活性氧物质(H2O2)会大量增加,故对H2O2含量的检测常被用作判定OA的早期标准[3]。此外,对H2O2的测定也是食品、生物医学和环境保护领域的一项重要任务。鉴于检测H2O2的重要性,研发了一种对H2O2敏感的纳米荧光探针,检测H2O2浓度对OA的辅助诊断和治疗起着重要的作用。
基于H2O2传感的荧光探针有多种类型,目前使用较多的荧光探针当属碳量子点[4]和金属纳米簇[5]。尽管其他荧光材料也可以作为荧光探针,但金属纳米簇具有较大的斯托克斯位移、优越的生物相容性以及独特的光学性质[6],近年来在生物传感、新型催化剂、生物标记、荧光成像等领域得到了广泛的应用[7]。在金属纳米簇中,金纳米簇(AuNCs)、铜纳米簇(CuNCs)、银纳米簇(AgNCs)的研究最多,主要是因为其拥有优异的荧光性能,制备方法简便且多种多样。但是金属纳米簇的制备存在较多问题,如所制备的金属纳米簇体系不稳定,以及基于金属纳米簇的高灵敏度和高选择性分析方法还有待提升等问题[8]。利用封装分子与无机核的表面原子之间形成强有力的化学键是增强金属纳米簇稳定性最直接有效的方法,因此制备一种含封装分子的金属纳米簇作为荧光探针,可进一步使其在H2O2检测中具有更高的稳定性和准确性。
1 银纳米簇
金属纳米簇是一种新型荧光纳米材料,其独特的纳米尺寸使其具有优异的物化性质,如稳定的荧光性能、低生物毒性、良好的生物相容性等。不仅如此,金属纳米簇合成方法简便且环保,前驱体可选用常见氨基酸、蛋白质等生物分子。相较于AuNCs和CuNCs,AgNCs更具经济易得的优势。
AgNCs通常由几十到几百个尺寸小于2 nm的银纳米粒子团聚而成[9],不仅具有普通金属纳米簇的一般性质,还具有独特的光吸收、容致变色效应、电化学发光等特性,根据其独特的光吸收特性极易将其与其他金属纳米簇区分开来。模板合成法是一种高效、简便的制备高纯度AgNCs的方法,常用的模板有核酸、聚合物、肽、蛋白质等[10],银离子(Ag+)与硫原子间存在较强的共价结合,因此AgNCs也可以与含巯基的生物分子配体结合。合成水溶性荧光AgNCs的常用方法是通过化学、光化学或声化学还原法还原含有合适模板的银盐前体[11]。基于AgNCs的卓越性质,其在生物分析、细胞成像、环境监测以及电子器件等领域的研究及应用具有非常广阔的前景[12]。例如,Adhikari等人[13]利用硼氢化钠(NaBH4)来还原Ag+,合成了具有近红外荧光发射的AgNCs,该AgNCs的斯托克斯位移大于200 nm,有应用于细胞成像的潜力。Zhang等人[14]开发了一种以DNA稳定的银纳米簇(DNA-AgNCs)为荧光探针来选择性检测水体中汞离子的新方法,其检测原理基于一种简单的静态猝灭机制,此DNA-AgNCs具有环境友好、灵敏度高、选择性好等优点。AgNCs在H2O2高效灵敏的传感应用中也受到研究者的青睐。Liu等人[15]以谷胱甘肽为配体,制备了一种谷胱甘肽包裹的呈蓝色荧光的AgNCs,水溶性、稳定性好且平均尺寸在3 nm左右,用于H2O2检测。Deng等人[16]建立了一种以DNA为模板,用NaBH4还原Ag+合成的AgNCs传感器,不仅实现了对H2O2的检测,还能间接测定葡萄糖的含量。
研究者常通过探索新的配体作为保护剂来合成金属纳米簇,使其制备方法绿色经济,具有尺寸可控、荧光性质稳定等优良特性。此次研究通过化学还原法,制备一种由二氢硫辛酸包裹的新型AgNCs作为荧光探针用于检测活性氧H2O2,一方面探究其制备方法,另一方面对其荧光性质进行分析。
2 材料与方法
2.1 仪器与试剂
电子天平,超声波清洗机,磁力加热搅拌器,数显磁力搅拌加热套,Thermo离心机,三用紫外分析仪,荧光分光光度计,紫外可见分光光度计,多歧管低温真空干燥机,透射电子显微镜,红外光谱仪。
氢氧化钠(NaOH)、二氢硫辛酸、NaBH4均购于重庆川东化工集团有限公司,四氯金酸(HAuCl4)、氯化钾、氯化钠、硝酸银(AgNO3)、H2O2均购于上海麦克林生化科技有限公司,甘氨酸、脯氨酸、精氨酸、苏氨酸、赖氨酸均购于上海阿拉丁试剂公司。实验所用试剂均为分析纯,实验所用水为超纯水(电阻率ρ>18.0 MΩ·cm)。
2.2 实验方法
2.2.1 AgNCs的制备
实验所制备的AgNCs以二氢硫辛酸作为保护剂,通过化学还原法来合成。在实验前所有玻璃器皿均用洗洁精和无水乙醇充分润洗后使用,首先称取60.8 mg的二氢硫辛酸溶解在15 mL二次水中,加入NaOH(0.18 mL,2 M)搅拌15 min;在剧烈搅拌下,向溶液中缓慢加入用二次水(4 ℃)新鲜配置的NaBH4溶液。反应2 h后,当溶液由淡黄色转变为酒红色时,停止搅拌并在4 ℃下避光保存。
2.2.2 AgNCs的光谱表征
利用F 97 Pro荧光分光光度计对AgNCs进行荧光分析。参数设置如下:发射波长的范围为(475~900 nm),激发带宽为10 nm,发射带宽为10 nm,扫描速度为1 000 nm/min,扫描间隔为1 nm,增益为中。通过时间进程曲线来分析AgNCs的稳定性。实验条件及仪器设置参数为:在室温条件下,取3 mL静置的AgNCs溶液,设置激发波长为469 nm,发射波长为660 nm,激发带宽为10 nm,增益为中,扫描时间为600 s。
2.2.3 AgNCs荧光量子产率
实验以罗丹明B乙醇溶液(量子产率QY=95%)作为标准物质,因此所得到的AgNCs溶液的荧光量子产率计算公式为:
QYx=QYs(As/Ax)(Fx/Fs)(nx/ns)2
(1)
式中:x为待测样品;s为标准物质;Ax为待测样品x的紫外吸收度;As为标准物质s的紫外吸收度;Fx和Fs分别为待测样品和标准物质在同一激发条件下的积分荧光强度;nx为待测样品x在水溶液中的折射率,取值为1.33;ns为标准物质s在乙醇溶液中的折射率,取值为1.36。
实验中需配置1.5 μg/mL罗丹明B乙醇溶液和一定浓度的AgNCs水溶液,分别测量其在500 nm处的荧光光谱和紫外吸收光谱,由紫外吸收光谱直接读出紫外吸收度,由Origin软件对荧光光谱面积进行积分,将得到的数据代入计算公式,计算出AgNCs的荧光量子产率。
2.2.4 AgNCs结构表征
(1) 透射电子显微镜表征
在进行透射电子显微镜表征前,需要对样品进行制样,制样步骤:① 室温下,在AgNCs溶液中加入乙醇,AgNCs与乙醇溶液的体积比约为1 ∶3,在1 000 r/min转速下离心5 min去掉不发光的团聚物;② 将提纯的AgNCs进行稀释;③ 再配制一定浓度的AgNCs水溶液,滴加5 μL提纯后的AgNCs溶液于300目铜网上干燥备用;④ 使用高分辨透射电子显微镜对制备的AgNCs进行形貌表征。
(2) 红外光谱表征
制样步骤:① 以铝箔纸为衬底,将其先后浸没于丙酮和乙醇中各超声2 min,取出后用二次水润洗;② 将10 μL样品溶液滴到彻底洗干净的衬底上,等其自然风干后再次滴加,直至在衬底上形成一层样品的薄膜为止;③ 利用红外分析仪进行结构和化学键表征。
2.2.5 AgNCs用于H2O2检测
(1) 灵敏度检测
首先配置H2O2(1 M)溶液,分别将其浓度稀释成1 pM、10 pM、100 pM,1 nM、10 nM、100 nM、1 μM、10 μM、100 μM、1 mM、10 mM、100 mM。取2 mL AgNCs溶液,将低浓度至高浓度的H2O2逐滴加入,测试其荧光光谱,分析加入不同浓度的H2O2对AgNCs荧光强度的影响,定量分析H2O2对AgNCs的猝灭效果。
(2) 抗干扰检测
为了检验AgNCs荧光探针对H2O2的特异性,结合骨关节炎症H2O2的检测应用,在选择性检测过程中,选取了人体内含有的几种金属盐和人体内常见氨基酸进行干扰实验,考察浓度为1 M的常见金属盐(如氯化钾、氯化钠)和常见氨基酸(如甘氨酸、脯氨酸、精氨酸、苏氨酸、赖氨酸)在469 nm激发波长下对AgNCs荧光的影响。
3 结果与讨论
3.1 荧光光谱分析
利用化学还原法,成功制备了AgNCs溶液。在自然光下,溶液为澄清的红棕色(图1a),在紫外光下溶液呈现深红色并发射出红色荧光(图1b)。根据荧光分光光度法,对制备的AgNCs溶液进行光谱表征,结果如图2所示。得到AgNCs的最佳激发波长与发射波长分别为469 nm、660 nm。

图1 自然光及紫外光下的AgNCs溶液

图2 660 nm发射波长下AgNCs的激发光谱及469 nm激发波长下AgNCs的发射光谱
使用荧光分光光度计对放置在常温下保存7 d的AgNCs溶液连续扫描5次,AgNCs的荧光发射光谱见图3。5次的荧光发射光谱曲线基本重叠,说明其荧光值基本稳定不变,即制备的AgNCs溶液具有较高的荧光稳定性,不易受环境因素的影响。AgNCs溶液及其加入H2O2溶液后的荧光强度随时间的变化曲线如图4所示,在600 s内,AgNCs溶液的荧光强度几乎没有变化,始终维持在700 a.u.左右;加入H2O2溶液后AgNCs溶液的荧光强度由700 a.u.瞬间猝灭到300 a.u.左右,之后基本保持稳定。由此可以得出,实验制备的AgNCs具有良好的光学稳定性。基于此特性,用于H2O2的持续检测时,可忽略环境及AgNCs自身因素对荧光强度的影响。
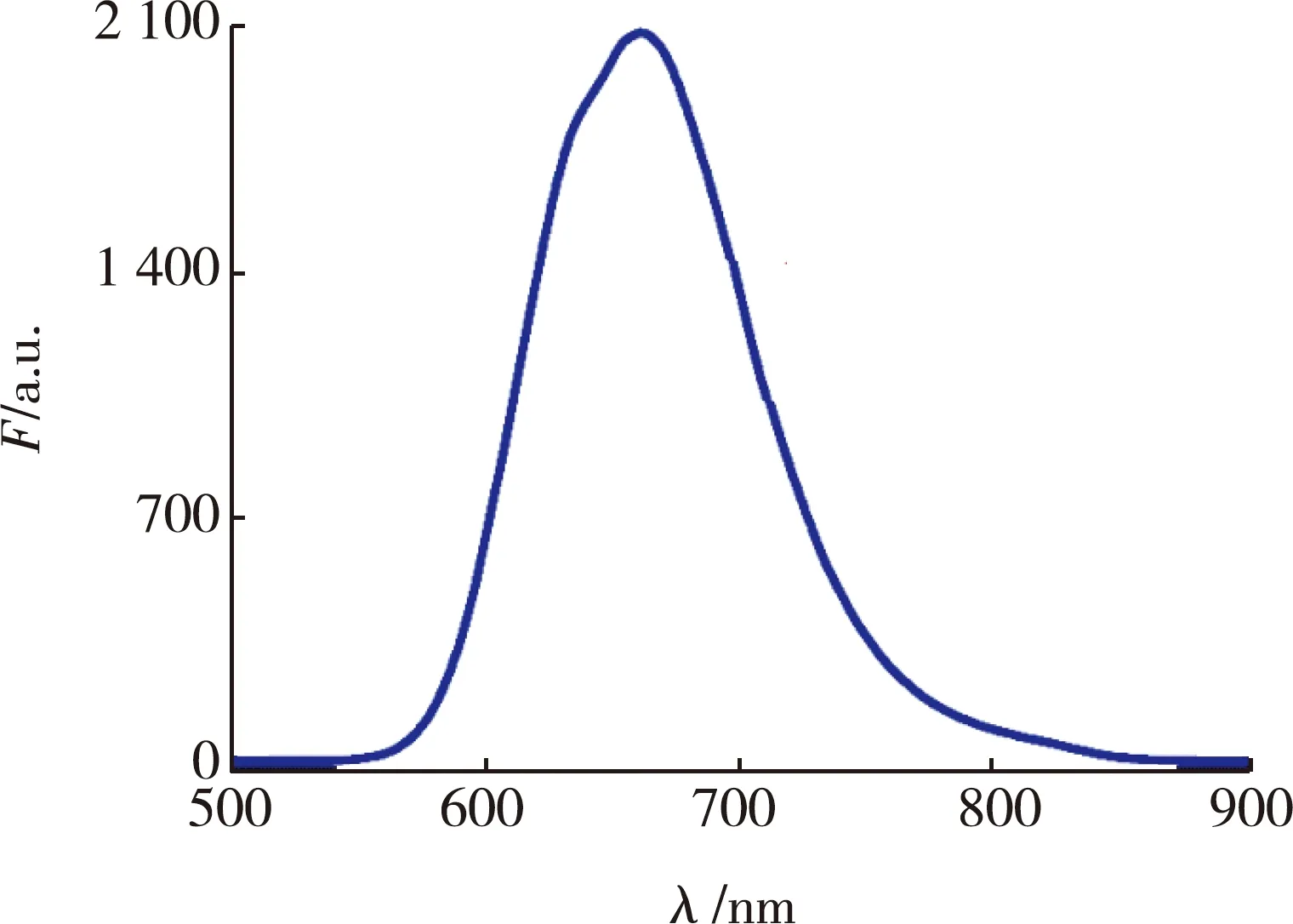
图3 对AgNCs溶液连续扫描5次的荧光发射光谱

图4 AgNCs溶液及其加入H2O2溶液后的荧光强度随时间变化曲线
3.2 AgNCs荧光量子产率计算
根据荧光量子产率计算公式(1),计算出利用化学还原法所制备的AgNCs的荧光量子产率,如表1所示。AgNCs荧光量子产率高达13%,能够发出红色荧光,光学性质优异,有望作为荧光探针用于H2O2的检测。
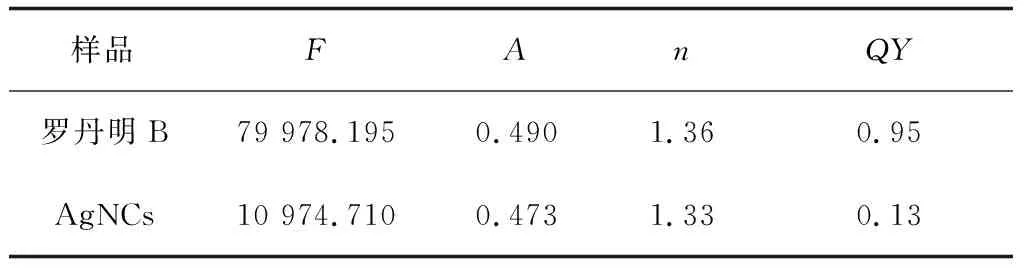
表1 AgNCs的荧光量子产率
3.3 AgNCs结构分析
采用透射电子显微镜(TEM)对制备的AgNCs的形貌进行观察。图5为AgNCs的TEM图像,图中插图为TEM高倍放大的AgNCs的晶格图。显然,制备的AgNCs粒子分布比较均匀,区域分散性较好,没有明显的团聚现象,有明显的晶格。文献[17]中的银纳米簇的晶格间距为0.234 nm,本次制备的AgNCs的晶格间距平均为0.230 nm。随机选取100个纳米粒子进行测量统计(见图6),得到纳米粒子的平均粒径为2.8 nm,粒径分布集中在2.5~4.0 nm。

图5 AgNCs的TEM图像
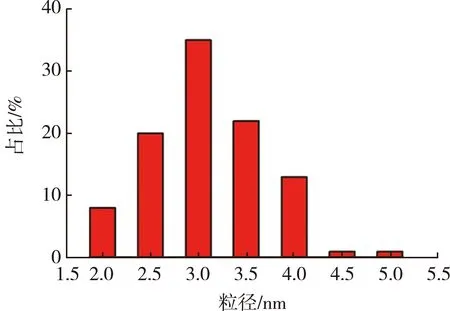
图6 AgNCs纳米粒子的粒径分布图
3.4 AgNCs对H2O2的检测分析
3.4.1 灵敏度分析
采用荧光分光光度计表征了H2O2对AgNCs荧光猝灭的灵敏度。图7为AgNCs溶液中加入H2O2前后在紫外光下的荧光强度对比。对比两图可知,向AgNCs溶液中加入一定浓度的H2O2溶液后,其荧光明显降低。依照2.2.5中的实验方法,将不同浓度的H2O2溶液逐滴加入到2 mL的AgNCs溶液中,利用荧光分光光度计,在最佳激发波长469 nm条件下,分别测量不同浓度H2O2溶液下AgNCs溶液荧光强度的变化,记录不同浓度H2O2对AgNCs荧光强度的猝灭程度,如图8所示。纯的AgNCs溶液的荧光强度为1 043 a.u.,随着加入的H2O2溶液浓度增大,AgNCs荧光逐渐降低,当其猝灭程度达到95%时,AgNCs荧光强度基本不再发生变化,说明此时已经到达平衡状态。通过实验证明H2O2对AgNCs有明显的荧光猝灭作用。

图7 AgNCs溶液中加入H2O2前后在紫外光下荧光强度对比
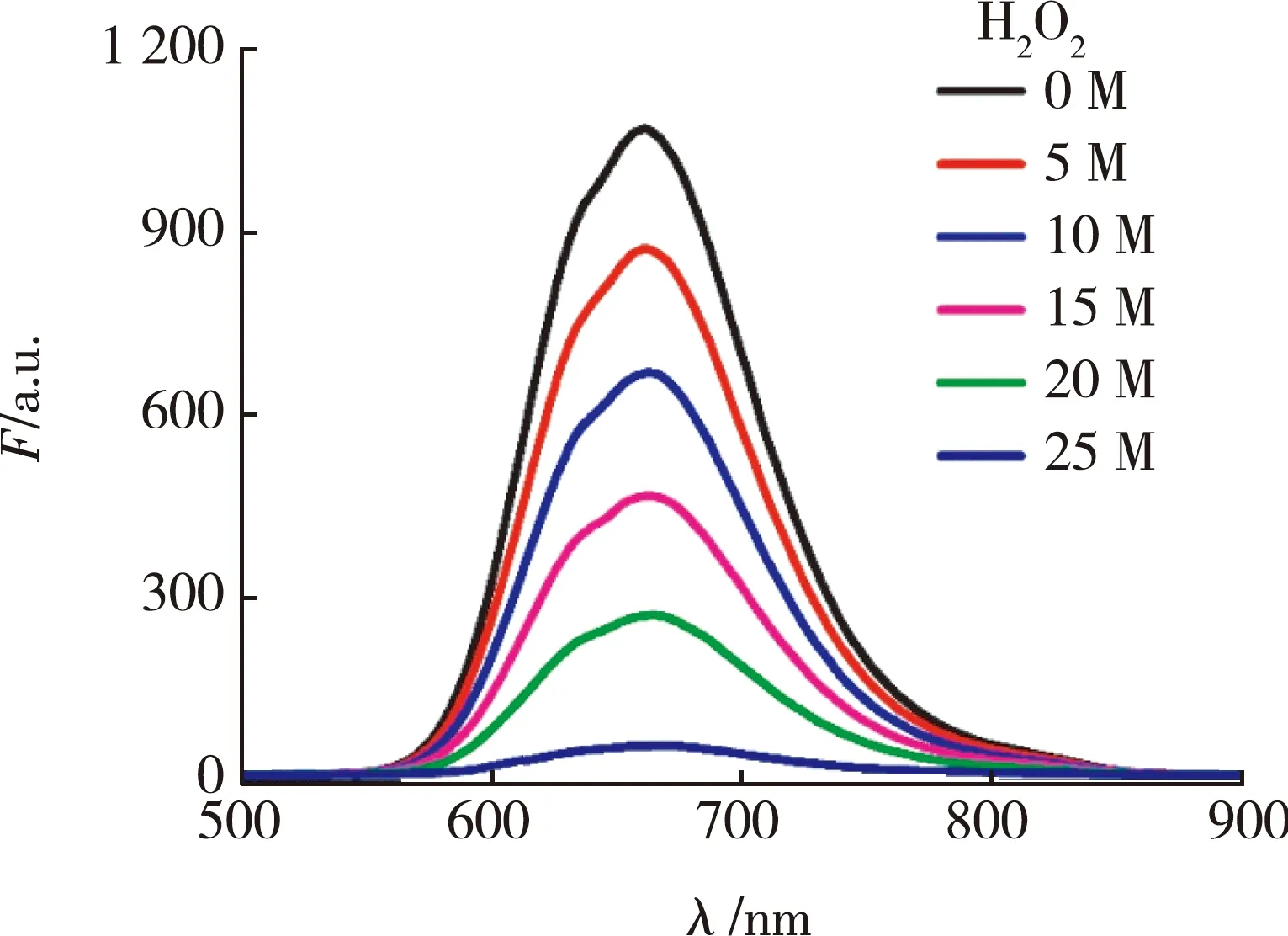
图8 加入不同浓度H2O2后的AgNCs荧光强度变化曲线
分析可知,在低浓度的H2O2体系里(图9),AgNCs的荧光强度与加入的H2O2浓度之间呈线性关系,线性范围为(0.2~5.0) pM,检测限为1.6×10-14M。在H2O2高浓度范围内AgNCs的荧光强度与加入的H2O2浓度呈线性关系(图10),线性范围为( 1.0~5.0)mM。在高、低浓度范围内都具备良好的线性关系,证明此AgNCs的检测范围较宽,为荧光探针用于骨关节炎处H2O2的检测提供了可能性。
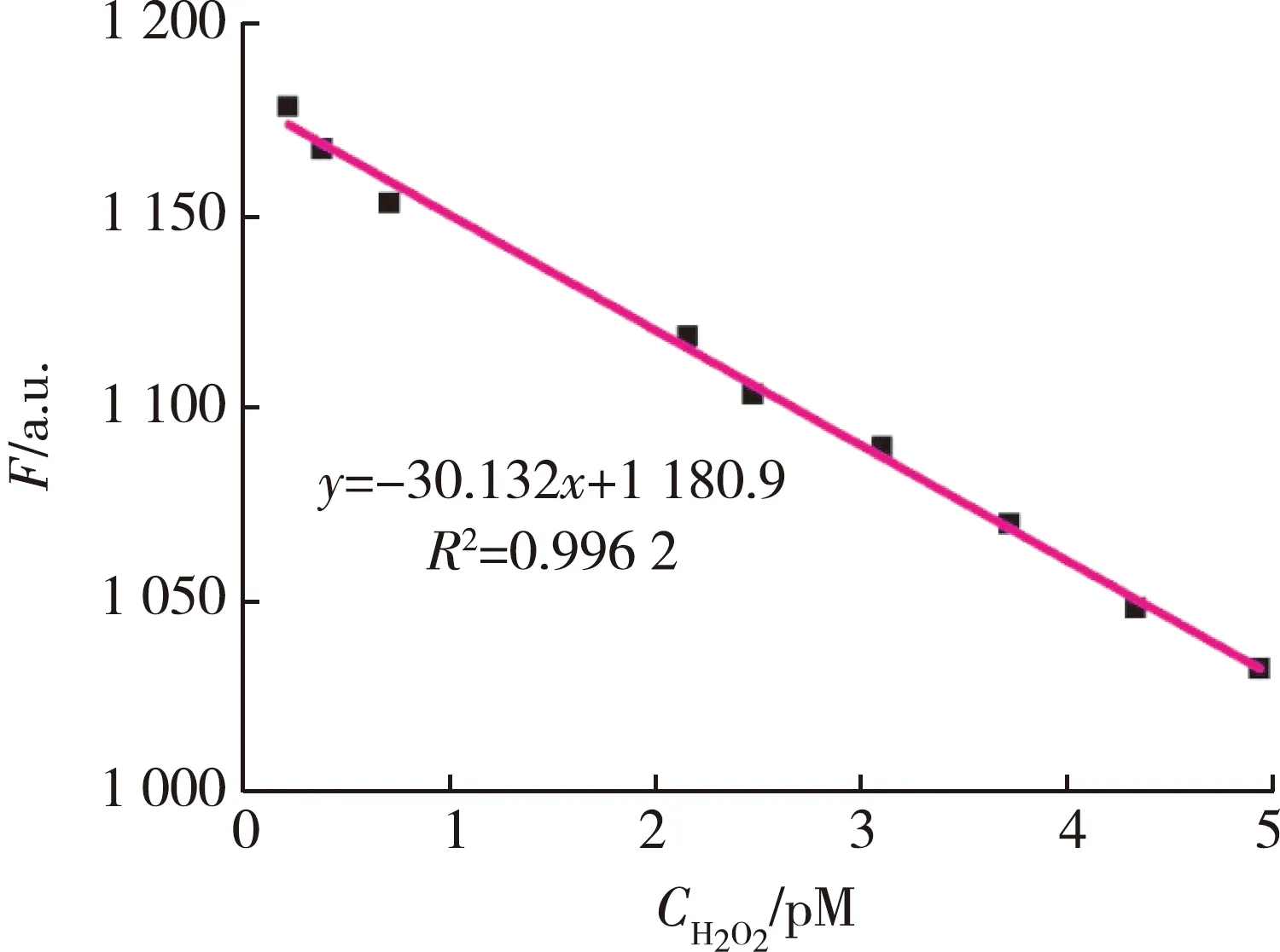
图9 在H2O2低浓度范围内,AgNCs荧光强度与H2O2浓度之间的拟合线性关系
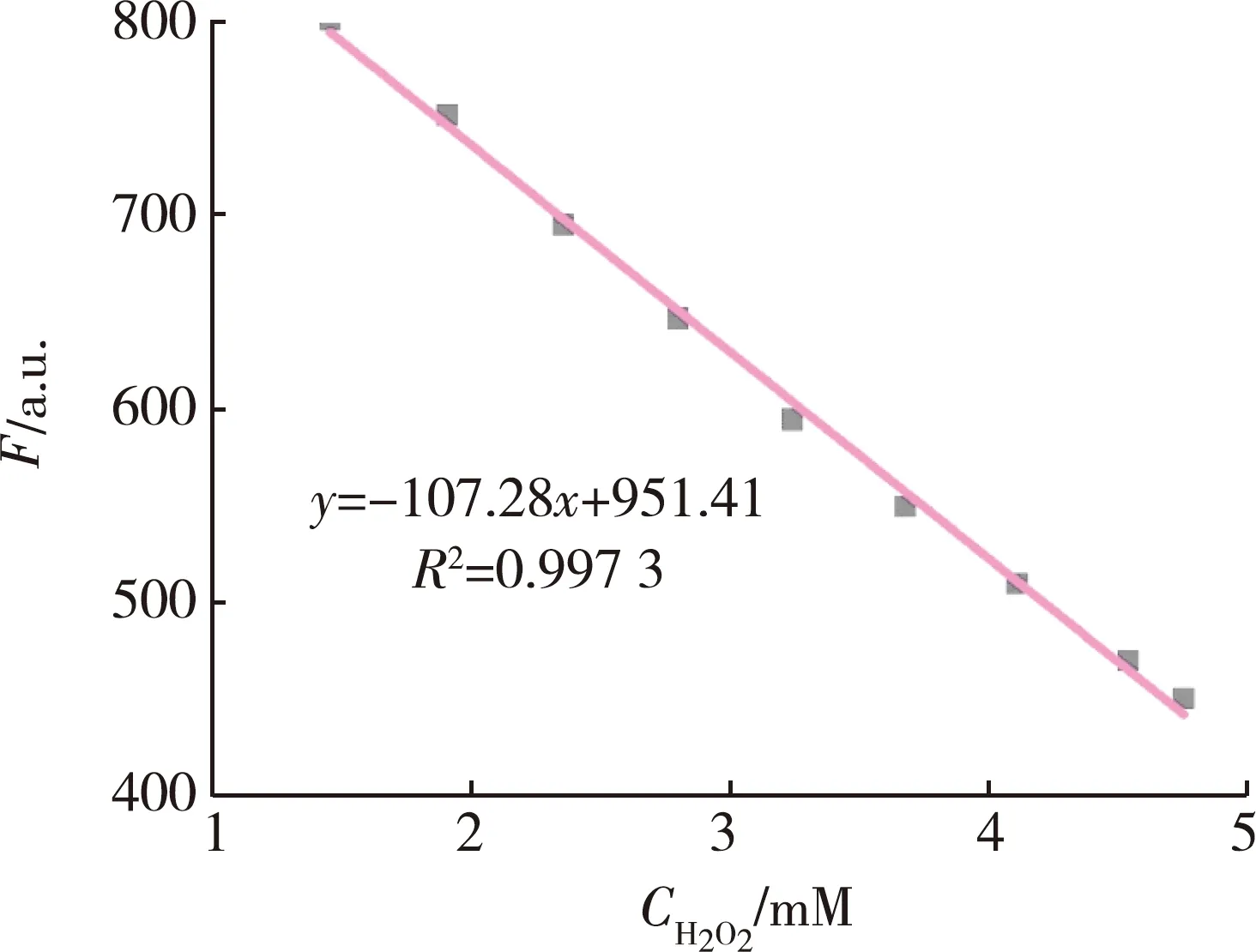
图10 在H2O2高浓度范围内,AgNCs荧光强度与H2O2浓度之间的拟合线性关系
3.4.2 抗干扰分析
在相同实验条件下选择了人体中常见的不同氨基酸和金属盐作为干扰物,如甘氨酸、脯氨酸、精氨酸、苏氨酸、赖氨酸、氯化钠和氯化钾,干扰物浓度均为H2O2浓度的10倍,以便考察AgNCs对H2O2测定的特异性。 469 nm激发波长下在AgNCs溶液中加入不同的氨基酸和金属盐溶液后对AgNCs荧光强度的影响见图11。可以看出,H2O2可使AgNCs的荧光强度降低到70%,而其他氨基酸和金属盐溶液使其荧光强度降低不到10%,即在加入不同氨基酸和金属盐的AgNCs溶液中,只有加入H2O2溶液时AgNCs的荧光强度才有明显下降。紫外光下加入不同氨基酸和金属盐溶液后AgNCs荧光强度的变化见图12。可看出,AgNCs在不同氨基酸强度和金属盐存在时,其荧光强度无明显变化,但当加入H2O2时,有明显的荧光猝灭现象。此现象表明,制备的AgNCs荧光探针对H2O2具有较强的专一性,具有较高的抗干扰能力,有望实现对关节炎症部位产生的H2O2的检测。
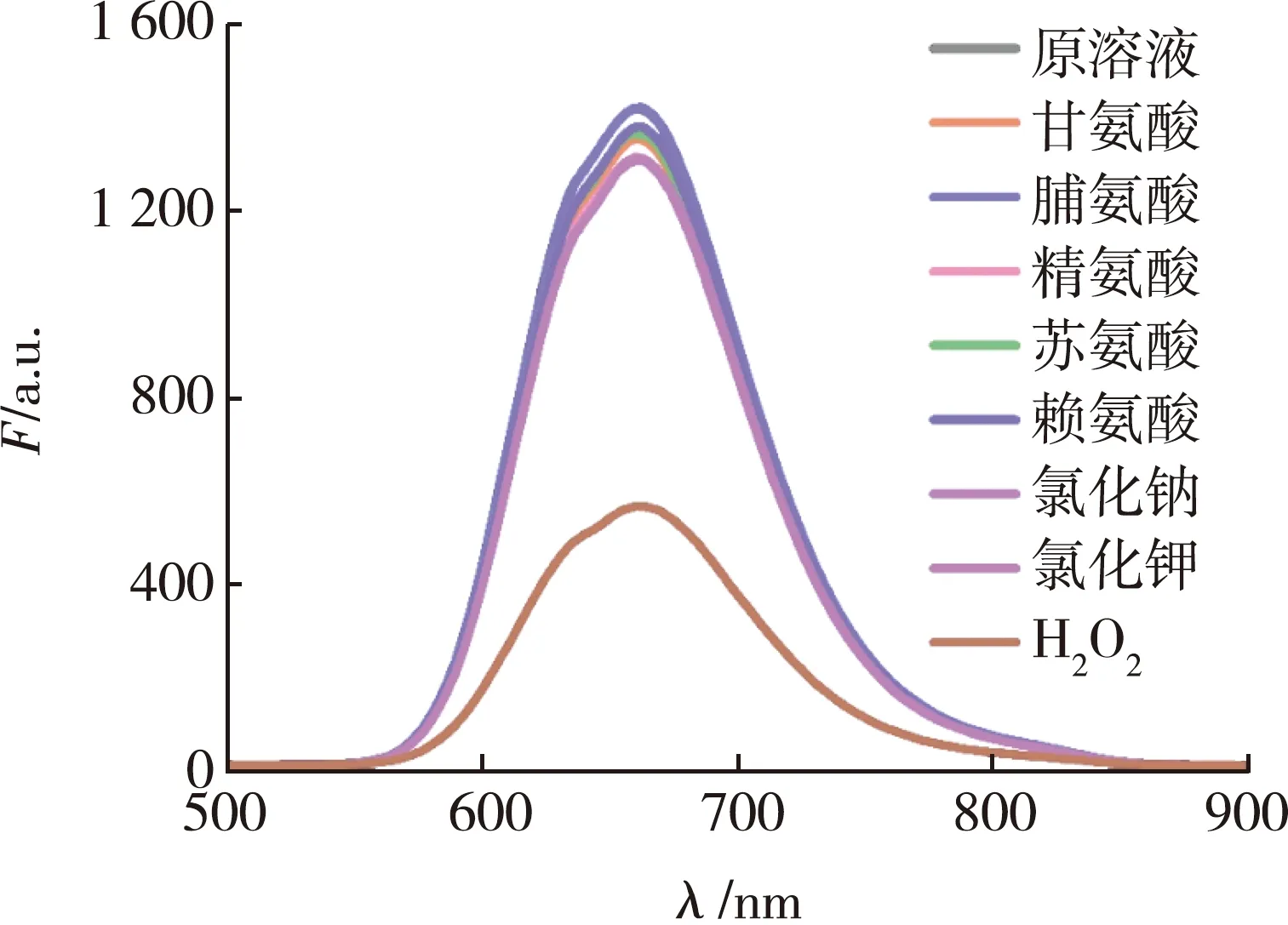
图11 469 nm激发波长下在AgNCs溶液中加入不同的氨基酸和金属盐溶液后对AgNCs荧光强度的影响

图12 紫外光下在AgNCs溶液中加入不同氨基酸和金属盐溶液后AgNCs荧光强度的变化情况
3.5 检测机理分析
通过对比观察加入H2O2溶液前后的AgNCs溶液的紫外吸收光谱(见图13),初步分析可得AgNCs的猝灭机理。H2O2溶液紫外吸收曲线基本没有吸收峰;AgNCs溶液在350 nm、425 nm以及500 nm处各有一个紫外吸收峰;加入H2O2后,AgNCs溶液的紫外光谱显示,425 nm和500 nm处的吸收峰消失,在350 nm处的吸收峰明显移至250 nm处。对比分析可知,H2O2溶液的加入使AgNCs溶液中生成了新的复合物,导致吸收光谱发生了变化。
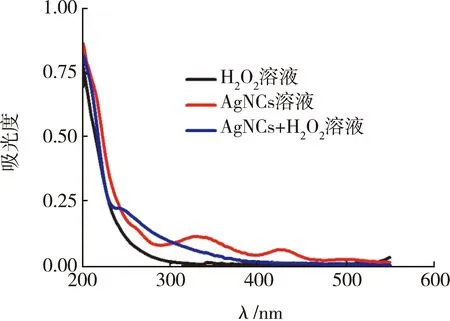
图13 3种溶液的紫外吸收光谱


图14 AgNCs溶液中加入H2O2溶液前后的红外吸收光谱
4 结 语
采用化学还原法,通过加入富含巯基的抗氧化剂二氢硫辛酸,利用巯基和AgNCs可以共价结合的性质,成功制备出由二氢硫辛酸包裹的AgNCs。制备的AgNCs对H2O2响应良好,通过对溶液的荧光光谱、紫外光谱和红外光谱的综合分析,得知AgNCs与H2O2在2个浓度范围内均呈线性相关,可以实现对2个不同数量级的H2O2低浓度和高浓度溶液的响应。一方面,在未有确切报道有关骨关节炎氧化应激中产生H2O2的浓度范围的情况下,此次制备的AgNCs在骨关节炎H2O2检测中具有极大的应用潜能;另一方面,其皮摩尔级的检测限也说明制备的AgNCs对H2O2非常敏感,同时良好的线性度保证了其检测的高灵敏度。综上所述,研究制备的AgNCs可以成功应用于H2O2的检测,在生物成像、生物传感等方面具有潜在的应用价值。
