杂质对有机过氧化物热危险性影响研究进展
2021-11-10王文和胡绍宇
王文和 黄 燕 胡绍宇
(1. 重庆科技学院安全工程学院, 重庆 401331;2. 重庆市安全生产科学研究院, 重庆 401331;3. 重庆科技学院油气化工过程安全多尺度研究中心, 重庆 401331)
有机过氧化物是指将过氧化氢中的一个或两个氢原子被其他取代基取代后组成的物质,通式为R-O-O-R1[1]。有机过氧化物种类非常多,但实际生产中广泛应用的有9种,分别为过氧化二叔丁基(DTBP)、过氧化二异丙苯(DCP)、过氧化氢异丙苯(CHP)、过氧化苯甲酸叔丁酯(TBPBZ)、过氧乙酸叔丁酯(TBPA)、过氧化环己酮(CYHPO)、过氧化甲乙酮(MEKPO)、过氧化二月桂酰(LPO)、过氧化苯甲酰(BPO)[2-9]。有机过氧化物在工业生产中可用于生产小分子物质,例如:CHP可用于生产苯酚和丙酮,也可作高分子材料引发剂、交联剂。但由于过氧键不稳定,在高温、碰撞、摩擦及杂质的混入过程中极易造成过氧键断裂,导致物质分解引发火灾爆炸事故[10]。近年来,有机过氧化物因杂质混入、储存不当等情况导致的事故见表1。
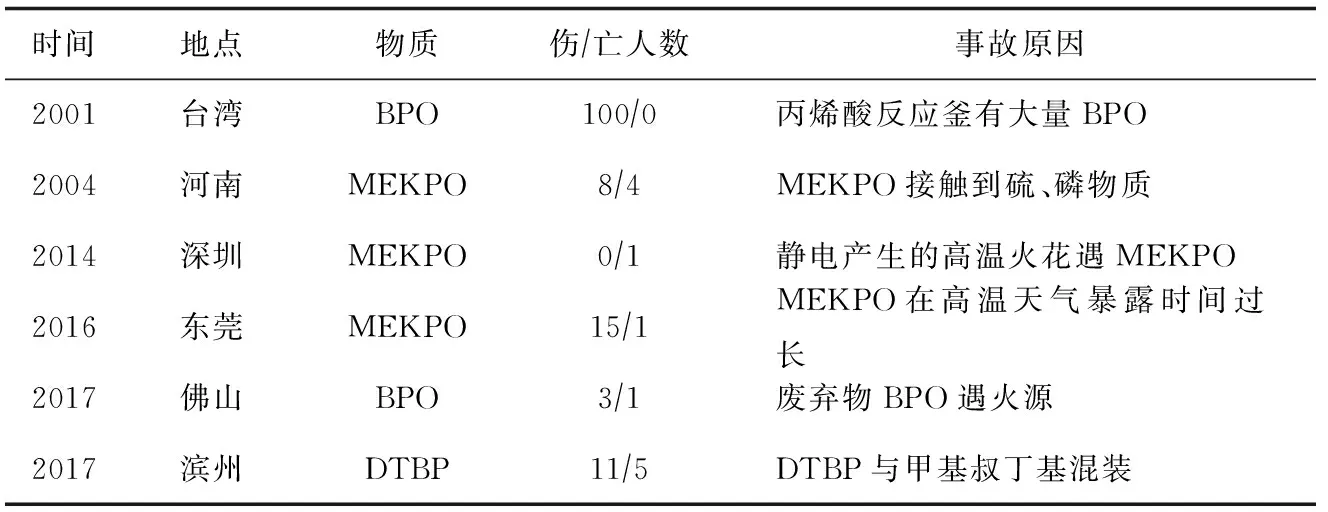
表1 由有机过氧化物引发的火灾爆炸事故
从上述事故可看出,有机过氧化物在遇火源、杂质等情况下会发生火灾爆炸事故。一旦发生事故,对企业、社会造成不良影响。由于杂质对有机过氧化物生产、运输及储存过程影响极大,为全面分析各类杂质对有机过氧化物的影响,从有机物和无机物两类杂质分别进行探讨。
综述了各种杂质对有机过氧化物的热危险性影响研究进展,分别从物质的热危险性研究方法、杂质对物质的热危险性的影响进行阐述,并提出杂质对有机过氧化物热危险性影响的后续研究方向。
1 有机过氧化物热危险性研究方法
目前,有机过氧化物的热危险性研究主要包括理论和实验研究,理论研究主要是根据分子的基团来预测物质的分解热、活化能及自加速分解温度等动力学参数,常用的预测理论主要包括量子化学理论[11]和Benson基团理论[12],在预测物质自加速分解温度、反应热时需要一定量的实验值作为样品值进行预测研究[13-18]。
实验研究主要是利用各热分析仪测量物质的热危险性参数。为了研究物质的热危险性,国内外目前均利用以下实验设备进行实验研究:热重分析(TG)、差式扫描量热仪(DSC)、紧急排放处理仪(VSP2)、C80微量热仪、微量热仪(TAM III)、绝热量热仪(Phi-TEC Ⅱ)、绝热加速量热仪(ARC)、自动压力跟踪绝热热量计(APTAC)、反应量热仪(RCle)、C600微型量热仪(C600)、气质联用仪(GC/MS)等[19-23]。通过以上各实验设备测量物质的热危险性参数,最主要的参数有:初始分解温度(T0)、到达最大反应速率时间(t)、自加速分解温度(T)、活化能(E)、指前因子(A)等。
2 无机物对有机过氧化物热危险性影响研究
无机物可分为单质和无机化合物,无机化合物通常是指不含碳元素的化合物,但某些含碳的碳氧化物属于无机化合物,例如:碳酸盐、碳化物、氰化物等[24]。在众多无机物中,分别研究酸、碱、水、金属、无机盐对有机过氧化物热危险性的影响。
2.1 酸、碱性物质对有机过氧化物的影响
有机过氧化物在生产、储存过程中可能会遇到酸、碱性物质。碱性溶剂可用作合成有机过氧化物的催化剂,例如:合成BPO过程中需要碱性物质参与,对比NaOH、NH4HCO3、Na2CO3这3种碱性物质,发现Na2CO3对BPO的热危险性最小[25]。酸、碱不仅可用于合成有机过氧化物,还可用于催化有机过氧化物分解成小分子物质,例如:在生产CHP过程中用酸催化来生产苯酚和丙酮,用碱催化来生产苯乙酮、甲醇等物质。
在生产中常见的无机酸、碱性物质有HCL、H2SO4、HNO3、NaOH、KOH等,目前已有许多关于酸、碱性物质对有机过氧化物热危险性影响的相关报道,见表2。
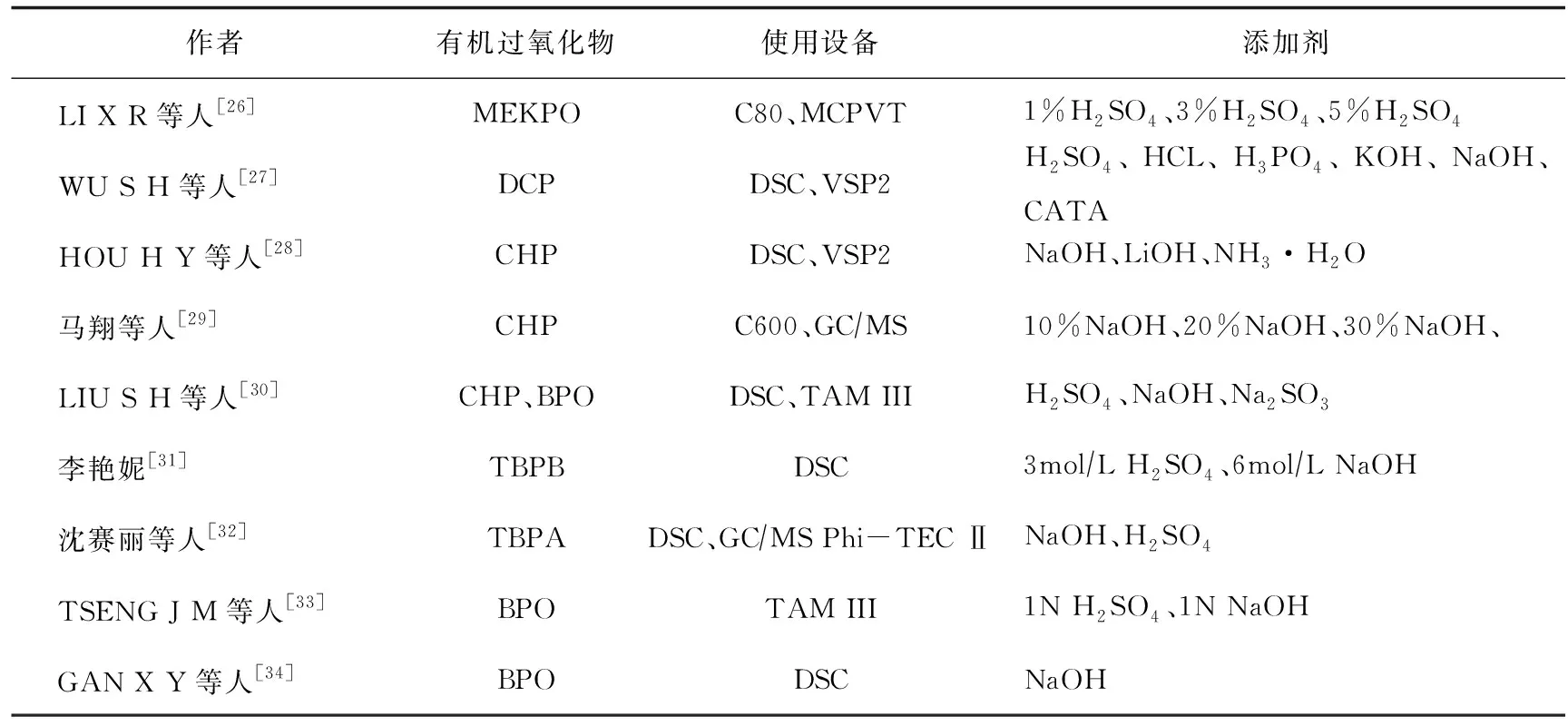
表2 酸、碱性物质对有机过氧化物的热危险性影响
查阅表2中的文献发现,在研究酸、碱性物质对有机过氧化物的影响过程中,最常用的酸性和碱性物质分别为H2SO4和NaOH,并且由于这两种物质在有机过氧化物的合成及分解过程中常做催化剂使用,所以大量研究者分别从酸、碱性物质的不同含量,以及不同扫描速率、不同浓度等方面进行实验研究[26-34]。根据各文献中的热危险性参数,绘制添加不同酸、碱性物质对有机过氧化物的参数t、T0、E的影响曲线,如图1所示。
对酸、碱性物质对有机过氧化物的性能影响的实验研究发现,除测量常规有机过氧化物热危险性参数外,有部分学者利用GC/MS研究热解产物[29,32],有部分学者根据绝热温升(ΔTad)和TMR构建不相容混合物的风险矩阵[28]。有研究结果发现不同NaOH含量下CHP分解的最终产物含量也不同,NaOH含量高时生成的产物主要为2-苯基-2-丙醇,NaOH含量低时生成的产物主要为乙酰苯[29]。同样在研究热解产物时,沈赛丽等人[32]研究了TBPA的热解特性,其在分解时产生了乙醇、丙酮、甲烷、二氧化碳气体等,导致容器压力升高。通过分别添加NaOH、H2SO4来分析TBPA的分解特性,结果表明:NaOH的加入对TBPA的分解影响不大,但加入H2SO4后TBPA的分解反应较为剧烈,所以必须严格控制酸性物质与TBPA接触。同样,TBPB遇到H2SO4后,活化能及指前因子均减小,危险性增大;而加入NaOH后,TBPB的活化能及指前因子均增大,危险性降低[31]。
在相同实验条件下,测试纯的BPO及BPO中加入H2SO4、BPO中加入NaOH后的热动力学参数T,在0.5 L包装下T值分别为58 ℃、53 ℃及64 ℃;在25 kg标准包装下T值分别为57 ℃、50 ℃及62 ℃。结果表明:BPO在碱性环境下比在酸性和纯BPO环境下更安全[33]。多个文献均表明酸碱环境对有机过氧化物均有促进分解的作用,但在酸性环境中有机过氧化物更易分解。
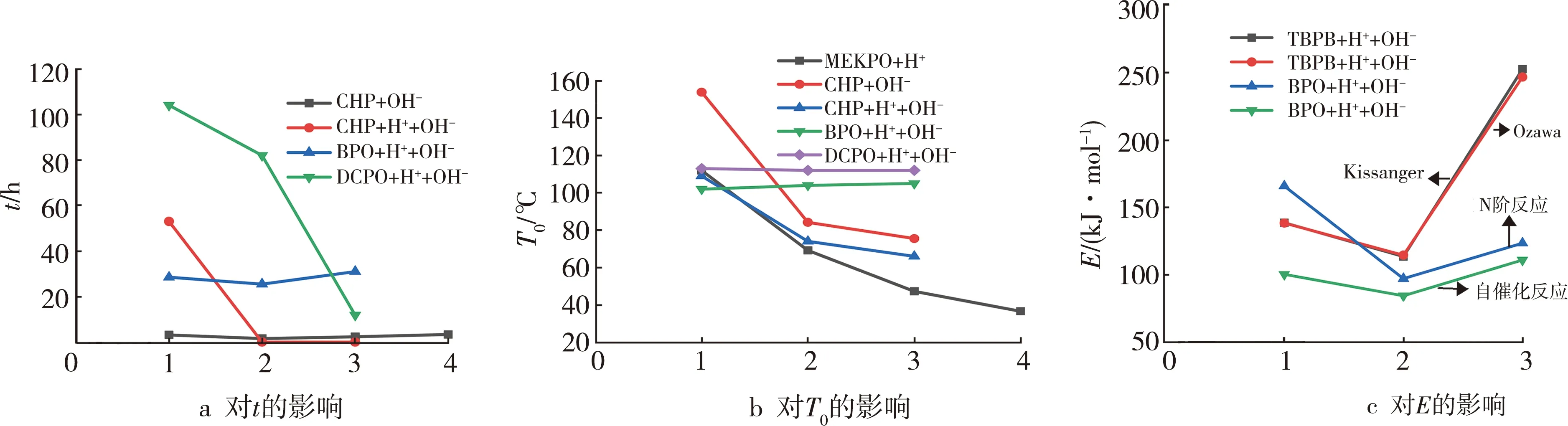
注:本文所有图的横坐标数值不具有物理意义,图中各点代表在加入各种不同杂质或杂质的不同含量时,对有机过氧化物参数的影响。
由图1可知,不同酸碱环境对有机过氧化物的影响存在差异,但趋势基本相同,大部分酸、碱性物质对有机过氧化物有促进分解的作用。酸、碱性物质的加入会造成有机过氧化物的参数T0、t均下降,从而增大有机过氧化物的热危险性。在研究有机过氧化物活化能的变化情况时,李艳妮[31]发现酸性物质的加入会使其活化能降低,但碱性物质的加入使其活化能明显增大,因此碱性物质会降低有机过氧化物的热危险性。对酸、碱性物质对有机过氧化物的热危险性影响的研究得知:
(1) 酸性物质促进有机过氧化物分解的效果更加显著,部分碱性物质对有机过氧化物的分解影响不大,增大其活化能及指前因子,降低其热危险性。大部分已有研究表明有机过氧化物在酸性环境比在碱性环境中更危险。
(2) 可进一步研究不同浓度的碱性物质对有机过氧化物的热危险性的影响。
2.2 金属对有机过氧化物的影响
在有机过氧化物的生产和储存过程中,常用的反应釜、运输储存容器及管道均由金属制成,在使用过程中,会有一定程度的磨损(碰撞、腐蚀等)。容器在碰撞腐蚀过程中就会释放出金属离子,一般常用于制造容器的金属为铁、铜等。
有关金属对有机过氧化物的热危险性的影响研究见表3。
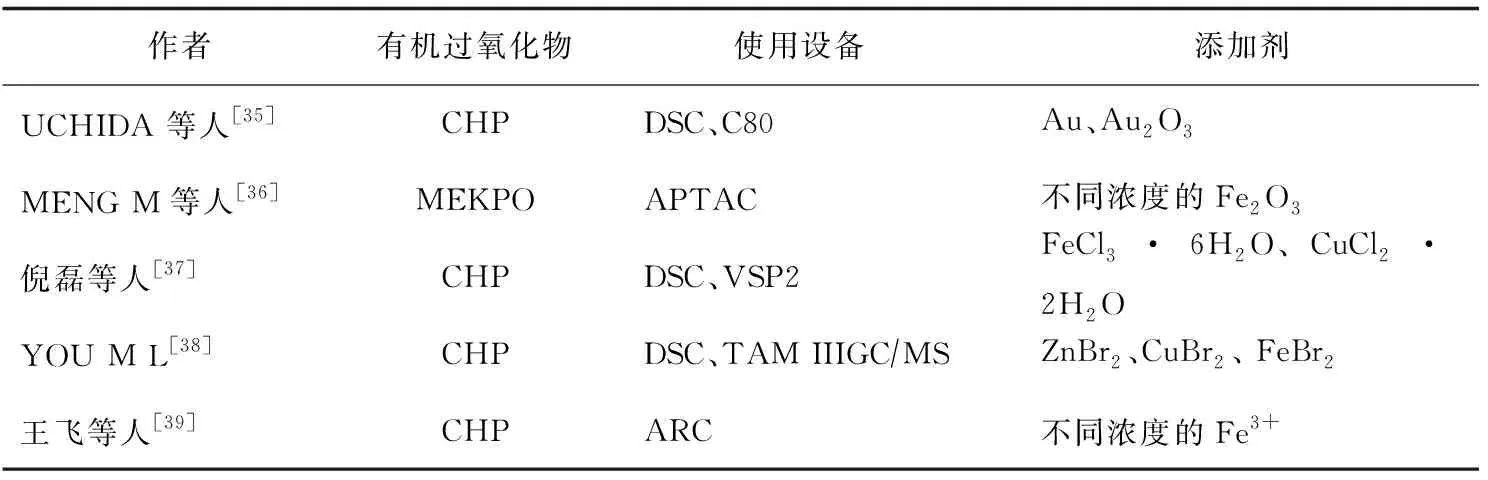
表3 金属对有机过氧化物热危险性的影响研究
查阅文献[35]—[39]发现,学者们在研究金属对有机过氧化物热危险性的影响过程中,最常用的有机过氧化物和金属离子分别为CHP和Fe3+、Cu2+,主要研究不同浓度的金属离子对有机过氧化物热危险性参数的影响。
将8种不同浓度的Fe2O3溶液分别加入到MEKPO溶液中,实验测试发现,Fe2O3溶液浓度越高,MEKPO的起始分解温度越低[36]。Fe3+浓度越高时,造成CHP的活化能越小,CHP更易分解,危险性也随之增大[39]。
有研究发现,纯的CuCl2·2H2O和FeCl3·6H2O溶液的加入会导致CHP 的T0降低,但当利用去离子水稀释CuCl2·2H2O和FeCl3·6H2O后,反而造成CHP的T0增高,稀释后溶液含水较多,能量被水溶液吸收[37]。又有学者研究了CHP在ZnBr2、CuBr2、FeBr2条件下的热危险性,发现金属离子不影响CHP的放热反应,但对参数t的影响较大,且Fe2+对CHP反应程度的影响最大[38]。并根据色谱图发现,不同金属作用导致有机过氧化物分解的产物不同[35]。
分析图2发现,金属离子的加入会降低有机过氧化物的T0、E,表明金属离子对有机过氧化物有促进分解的作用,并且不同金属离子及不同金属含量对有机过氧化物的作用效果也不同。针对金属对有机过氧化物的热危险性参数的影响研究得知:
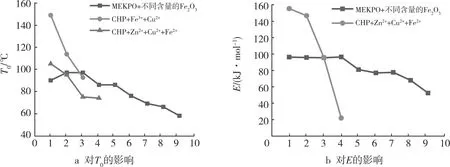
图2 不同金属对有机过氧化物热危险性参数的影响
(1) 在研究金属对有机过氧化物的影响过程中,发现各种金属离子对有机过氧化物有促进分解的作用,Cu、Fe又作为制造设备中常用的金属,在储存、运输过程中应更加谨慎。
(2) 不同浓度的金属离子对有机过氧化物的热危险性参数的影响不同,浓度越高,影响越大。
2.3 水对有机过氧化物的影响
在生产、储存有机过氧化物的过程中,水不仅可以作为生产原料,还可以作为某些有机过氧化物在存储和运输过程中的减敏剂,所以在研究水对有机过氧化物热危险性的影响过程中,可以从水的类别(酸雨、雾、自来水、去离子水)及含量进行研究。
有研究者对TBPBZ在干燥、潮湿及过量水下进行实验研究,发现TBPBZ在遇少量水时更易分解,遇过量水时分解减缓,因此该物质应在干燥条件下进行储存[41]。含水30%的BPO比干燥的BPO的SADT值要高,说明含水30%的TBPBZ比干燥条件下TBPBZ更安全[42]。有研究[41]发现,含水量不同时TBPBZ的分解程度也不同。
表4 水分对有机过氧化物热危险性影响
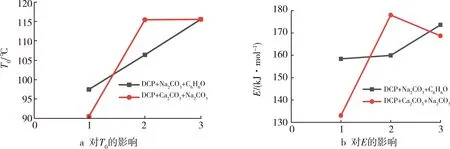
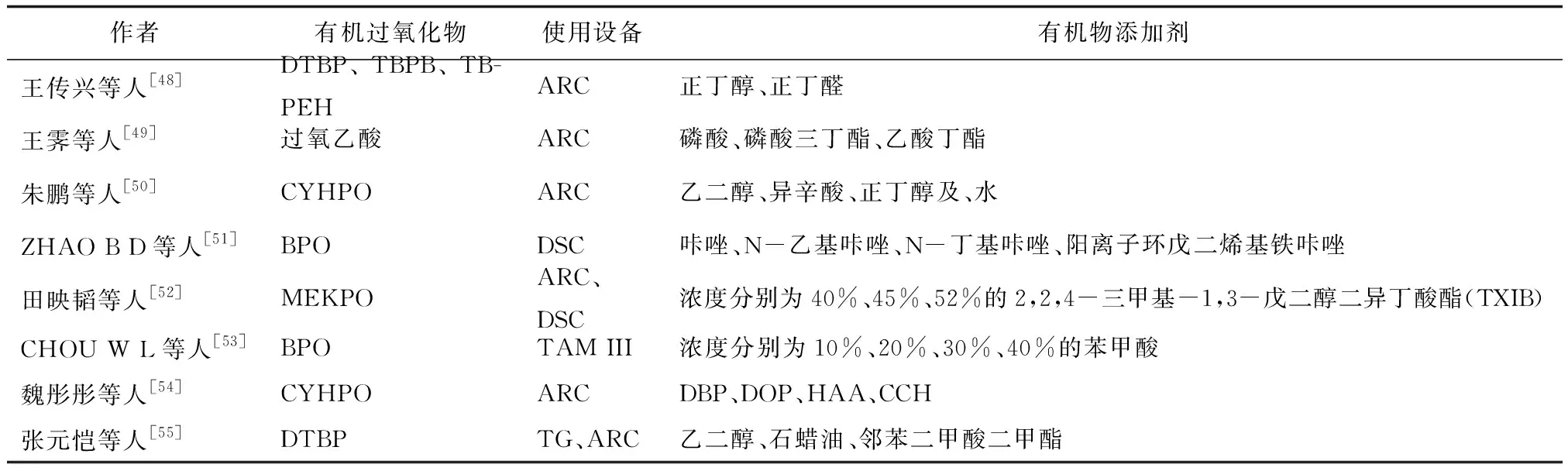
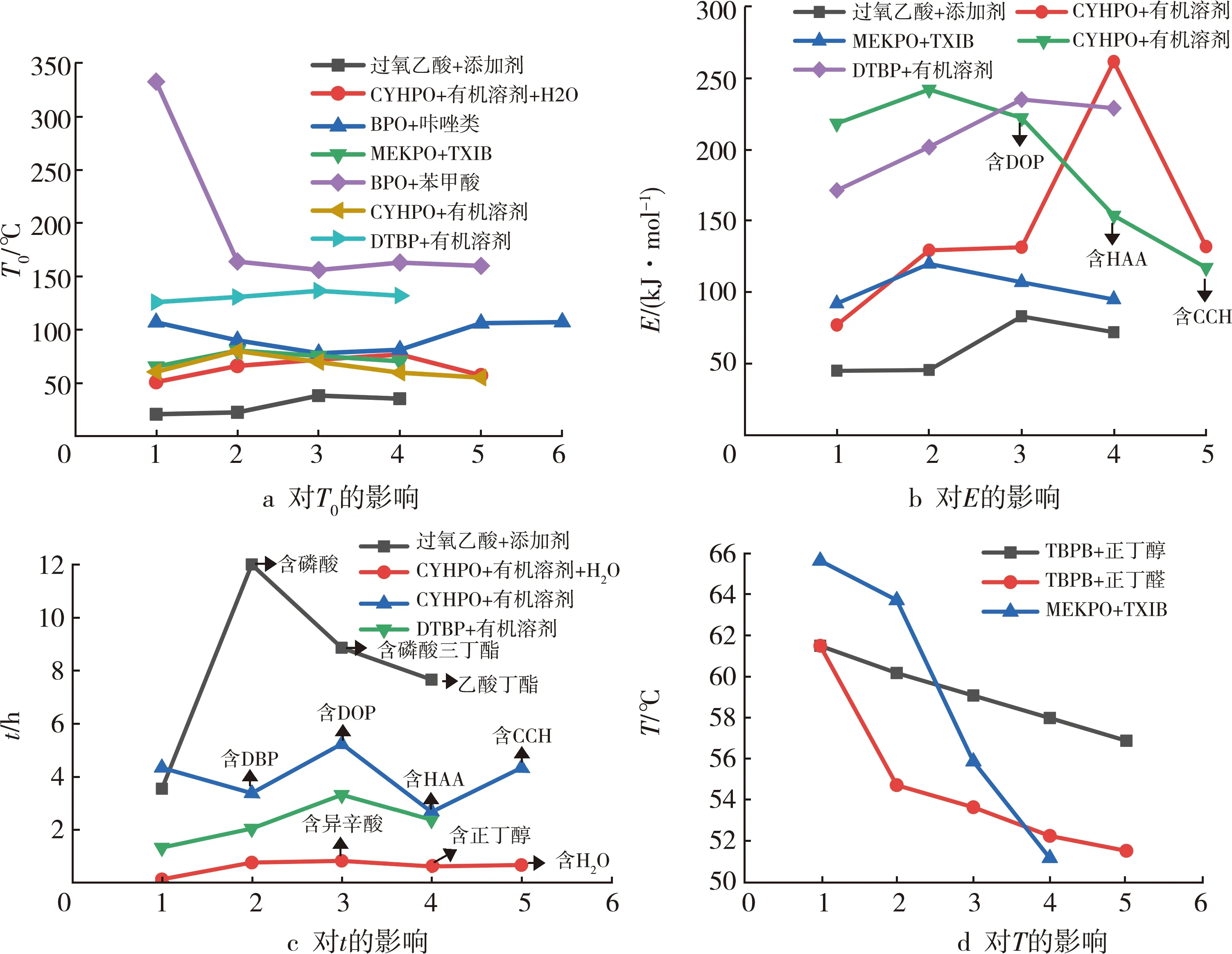
方将来等人[43]研究了不同杂质对BPO的热危险性的影响,利用Kissinger及Ozawa计算活化能,分析了杂质对其单一参数的影响,对T0的影响:T0(C7H8) 分析图3发现,有机过氧化物中水分含量不同,T0、E和T均呈“V”字型变化。在含水量较低时,有机过氧化物分解较快,但当水分含量超过一定量时会增大T0、T、E,使有机过氧化物热危险性降低。由此可见,水分含量对有机过氧化物的安全性尤为重要。实验用水使用的是去离子水,结合实际,可进一步研究自来水、雨水对有机过氧化物热危险性的影响。在储存过程中要避免有机过氧化物接触到水。 图3 不同种类的水对有机过氧化物热危险性参数的影响 目前,国内已有部分关于无机盐作用于有机过氧化物的报道,为进一步研究无机盐的作用效果,可加大选取无机盐的范围,有利于有机过氧化物在生产、运输及储存过程中的安全。 表5 无机盐对有机过氧化物热危险性的影响 学者[45]研究发现DCP中加入浓度为20%Na2CO3及20% C6H6O,DCP初始分解温度均增大,热危险性降低,并指出使用Na2CO3做催化剂更有利生产。根据结构相似的原理,学者[46]在DCP中添加相同浓度的CaCO3、Na2CO3,研究发现这两种物质的加入使得DCP的T0由90 ℃均升高到115 ℃,E由133 kJ/mol升高到(168~178) kJ/mol,且温升速率峰值显著降低,起到了很好的稳定性作用。所选无机盐对抑制有机过氧化物的分解作用十分明显。但在研究无机物对有机过氧化物的影响时,所选择的无机盐较为单一,后续可进一步研究多种无机盐对有机过氧化物热危险性的影响。 有机物是指由碳元素、氢元素组成,一定是含碳的化合物,但是不包括碳的氧化物和硫化物等[47]。目前,已有部分学者研究了有机溶剂对有机过氧化物的热危险性的影响,为降低有机过氧化物在使用、运输、储存过程中的危险性,有学者发现通过添加某些有机溶剂,可以有效降低有机过氧化物的热动力学参数,从而保证有机过氧化物的安全性。 图4 不同无机盐添加剂对有机过氧化物热危险性参数的影响 学者们在研究有机物对有机过氧化物的影响过程中,主要从不同有机物添加剂进行实验研究,发现乙二醇、异辛酸、正丁醇[50],2,2,4-三甲基-1,3-戊二醇二异丁酸酯(TXIB)[52],邻苯二甲酸二丁酯(DBP)、邻苯二甲酸二辛酯(DOP)、正己酸(HAA)和环己醇(CCH)[54],石蜡油及邻苯二甲酸二甲酯[55]等物质对不同有机过氧化物有抑制分解的作用。但是咔唑及其衍生物[51]、苯甲酸[53]、正丁醇和正丁醛[48]对有机过氧化物有促进分解的作用,且发现正丁醇对不同有机过氧化物的影响不同[48,50],说明相同有机溶剂对不同的有机过氧化物作用效果可能存在偏差,甚至作用效果相反。 图5为不同有机物添加剂对有机过氧化物热危险性参数的影响。分析图5发现,并不是所有的有机溶剂对有机过氧化物均有抑制分解的作用。从T0的变化图可以看出咔唑、苯甲酸、HAA及CCH对所选有机过氧化物有促进分解的作用,其中苯甲酸作用效果最为显著。从E的变化图可以看出,DOP、HAA、CCH使CYHPO的E降低,其余添加剂使E增大,说明CYHPO的热危险性降低。从t的变化图可以看出,DBP、HAA会降低CYHPO的t。正丁醇、正丁醛及TXIB会降低所选有机过氧化物的T,使CYHPO 的热危险性增大。有机溶剂对有机过氧化物的影响,必须要对各参数进行综合分析,确保所选溶剂的有效性。同一有机溶剂对不同有机过氧化物作用效果可能存在差异。 表6中所选有机溶剂并无多大关联,可以进一步从结构相似原理分析,选择有效的有机溶剂。 表6 有机物对有机过氧化物热危险性的影响 图5 不同有机物添加剂对有机过氧化物热危险性参数的影响 归纳总结了各种杂质对常用有机过氧化物热危险性的影响,阐述了通过实验获得的热危险性参数的变化情况,发现部分有机溶剂及无机盐对有机过氧化物有抑制分解的作用,会降低有机过氧化物的热危险性。未来进一步研究趋势: (1) 大部分酸、碱性物质及金属对有机过氧化物有促进分解的作用,但部分碱对有机过氧化物分解影响效果不大,甚至增大其活化能及指前因子,危险性降低,可进一步研究碱对有机过氧化物的热危险性影响,从碱性物质的含量、浓度出发研究其对有机过氧化物的分解作用,分析研究是否存在一个阈值。 (2) 在研究水对有机过氧化物热危险性的影响时,学者们基本使用的是去离子水,结合实际,可进一步研究自来水、雨水对其的影响。 (3) 在研究无机盐对有机过氧化物热危险性的影响时,发现部分无机盐可有效降低有机过氧化物的热危险性,可从灭火剂中选取有机过氧化物对其进行研究,探索灭火剂对有机过氧化物的作用效果及抑制机理。 (4) 有机溶剂大部分可作为有机过氧化物的稳定剂,但部分有机溶剂对不同有机过氧化物的作用不同,可以进一步研究有机溶剂对有机过氧化物热稳定性的影响,确保每一种有机过氧化物有最适合的添加剂。
2.4 无机盐对有机过氧化物的影响
3 有机物对有机过氧化物热危险性的影响
4 展 望
