手性气相色谱法测定野菊花中的龙脑对映体
——推荐一个仪器分析实验
2021-11-05李会香刘莎莎雷杰
李会香,刘莎莎,雷杰
复旦大学化学系,上海 200433
正如左右手的镜像关系一样,不对称分子和它的镜像不能重叠的这种性质称为手性[1]。手性分离一直是有机化学家所关注的课题,尤其是在不对称合成和天然产物分离领域的应用[2]。目前关于手性分离的教学论文,大都是从有机化学实验的角度进行介绍,重点应用于不对称合成领域,比如手性Co(III)络合物的不对称自催化合成和表征[3],手性Salen-Co(II)络合物催化芳香酮的不对称还原反应[4],手性有机小分子催化剂6,7-二氢-5H-吡咯并[1,2-a]咪唑的合成[5],手性高烯丙基胺的合成及表征[6],N-叔丁烷亚磺酰基亚胺的非对映选择性烯丙基化[7]等,以上论文大部分采用的是液相色谱法。谢天尧等[8]推荐过适用于高年级本科生的仪器分析研究式开放性教学实验“毛细管电泳/非接触式电导法分离检测药片中的氧氟沙星对映体含量”。
本论文从仪器分析实验的角度,介绍了手性气相色谱法测定野菊花中的龙脑对映体,侧重点在于手性色谱柱的原理及分离机理介绍,及将手性色谱应用于天然产物的分离分析。
1 实验目的
熟悉毛细管气相色谱仪的工作原理及操作;掌握手性色谱法的基本概念及分离基本原理;掌握用手性气相色谱法分离野菊花挥发油中左旋龙脑和右旋龙脑的方法;掌握内标标准曲线定量方法。
2 实验原理
相互对映而不能重合的两种化合物彼此互称为对映异构体,这种现象称为对映异构现象。对映体在药物中占有很大的比例,已知药物分子中约有30%–40%是手性的,经由化学合成得到的药物往往是对映体,不是单一的光学异构体。许多药物对映体不仅药理作用不同,而且生物转化过程亦有差异。震惊世界的沙利度胺(thalidomide)致畸事件就是由于人们对手性药物的认识不足造成的[9],20世纪50年代,德国一家制药公司开发出一种镇静催眠药反应停(沙利度胺),对于消除孕妇妊娠反应效果很好,但很快发现许多孕妇服用后,生出了无头或缺腿的先天畸形儿。虽然各国当即停止了销售,但却造成6000多名“海豹儿”出生的灾难性后果。后来经过研究发现,反应停是包含一对对映异构体的消旋药物,它的一种构型R-(+)对映体有镇静作用,另一种构型S-(−)对映体才是真正的罪魁祸首——对胚胎有很强的致畸作用。为了避免这类悲剧的再次发生,世界各国由此开始关注手性药物。
利用气相色谱分离手性化合物的研究始于20世纪50年代末期,但真正实现首次成功分离是在1966年,Gil-Av等报道了氨基酸对映异构体的分离,手性固定相是将N-三氟乙酰基-L-异亮氨酸月桂醇酯涂覆于毛细管内壁上[10]。1967年Gil-Av等又用填充柱气相色谱实现了氨基酸的半制备分离。尽管气相色谱较早地应用于手性分离,但其在随后的年代里发展较慢,主要是该类固定相热不稳定性的原因。形成包合物的手性固定相最常用的是环糊精类化合物,1961年Sand等首次把环糊精(CD)用于气相色谱分离脂肪族化合物,由于它未衍生化,天然的环糊精熔点高达290 °C,因此其在气相色谱上的应用一度被冷落[11]。环糊精是多个D-吡喃葡萄糖单元通过1,4-糖甙键连接成的环状寡糖,六聚、七聚、八聚、九聚的分别称为α-、β-、γ-、δ-CD。CD分子呈中空的圆筒形,筒内呈疏水性,筒外呈亲水性。CD分子的羟基在不同的反应条件下反应活性不同,据此可对CD分子进行多种衍生化,引进不同性质的基团。对环糊精进行衍生化,起初人们只是为了降低环糊精的熔点和疏水性,仅是对环糊精的羟基简单地烃基化得到不同的疏水性衍生物,现在已经发展到有目的地引入有特殊作用的基团[12,13]。
手性气相色谱法一般可以分为三种[1],第一种为手性衍生化法,即采用手性衍生化试剂柱前衍生化,将对映异构体转化为非对映异构体后再用色谱分离非对映异构体衍生物;第二种为手性流动相法,即在流动相中添加手性添加剂,用一般色谱柱即可分离外消旋体;第三种为手性固定相法,现使用的手性固定相主要有:氢键型手性固定相、金属鳌合手性固定相、形成包合物的手性固定相、离子液体手性固定相、多糖类手性固定相、环肽类手性固定相和刷型手性固定相等。色谱手性分离的关键是手性固定相的选择。气相色谱手性固定相的发展过程经历了由作用力简单、单一手性中心的氢键型手性固定相向具有多种作用力和多手性中心的复杂型手性固定相的发展过程。
天然的龙脑主要有左旋龙脑和右旋龙脑,是外消旋体。左旋龙脑在药典上也被称为“艾片”,主要由菊科植物艾纳香茎叶经水蒸气蒸馏提取并重结晶而得,为白色半明片状、块状或颗粒状结晶。右旋龙脑是天然冰片的主要成分,由樟的新鲜枝叶经提取加工而得,为白色结晶性粉末或片状结晶[14]。冰片有清凉气味,具有开窍醒神,清热止痛的功效,其药理作用有发汗、兴奋、镇痛及抗缺氧作用,是人丹、冰硼散、苏冰滴丸、速效救心丸等许多中成药的主要成分,也用于化妆品和配制香精等。本实验中用手性气相色谱法测定野菊花挥发油中的对映异构体左旋龙脑和右旋龙脑的含量。
3 实验部分
3.1 实验试剂
野菊花样品(安徽产,上海市民大药房),(+)-龙脑(梯希爱(上海)化成工业发展有限公司,98%),(−)-龙脑(梯希爱(上海)化成工业发展有限公司,> 95%),(+)-樟脑(梯希爱(上海)化成工业发展有限公司,> 98%),(−)-樟脑(梯希爱(上海)化成工业发展有限公司,> 98%),异龙脑(阿达玛斯试剂有限公司,> 90%),十一烷(国药集团化学试剂有限公司,> 98%),乙酸乙酯(国药集团化学试剂有限公司,分析纯),无水硫酸钠(上海大合化学品有限公司,分析纯),去离子水。
3.2 实验仪器
气相色谱仪(A90,常州磐诺仪器有限公司,配置氢火焰离子检测器);Varian CP-Chirasil-Dex CB手性毛细管柱(25 m × 0.25 mm × 0.25 µm),可调功率微波化学反应器,水蒸气蒸馏同时溶剂萃取装置,电子天平,10 µL微量进样器,50 mL、10 mL、5 mL容量瓶,1 mL移液管,洗耳球,10 mL、250 mL量筒,50 mL磨口试剂瓶,500 mL圆底烧瓶。
3.3 实验步骤
3.3.1 野菊花挥发油的提取
准确称取20.00 g野菊花样品,加入到挥发油提取装置的圆底烧瓶里,然后加入200.0 mL水,提取器中加入10.0 mL乙酸乙酯,200 W功率下,微波加热回流提取1 h,将挥发油收集至提取器内的有机溶剂中。待溶液冷却后,将提取器内的有机相转移至50 mL磨口试剂瓶中,加入无水硫酸钠干燥,得到澄清透明的挥发油溶液。
3.3.2 毛细管气相色谱仪的调试和操作
气相色谱仪的参数及升温程序经优化后如下,进样口温度:250 °C,检测器温度250 °C,载气:高纯氮气;流速:1 mL·min−1;分流比:20 : 1。程序升温:从60 °C开始,保持1 min;再以20 °C·min−1的升温速度到达120 °C,保持8 min,最后再以20 °C·min−1的升温速度到达200 °C,保持10 min。
3.3.3 (+)-龙脑和(−)-龙脑标准溶液的配制
分别准确称取(+)-龙脑和(−)-龙脑25.0 mg,用乙酸乙酯溶解,并定容至50 mL容量瓶,得到0.50 mg·mL−1(+)-龙脑和(−)-龙脑的标准储备液。称取200.0 mg十一烷于10 mL容量瓶中,用乙酸乙酯溶解并定容,得到浓度为20.0 mg·mL−1的内标溶液。用1 mL移液管移取配好的(+)-龙脑和(−)-龙脑的标准溶液0、0.10、0.20、0.30、0.40、0.50 mL分别于6个5 mL容量瓶中,将10.0 μL内标溶液分别加入到上述6个溶液,再用乙酸乙酯定容,得到系列浓度的龙脑异构体标准溶液。用微量进样器取1.0 μL龙脑异构体标准溶液,即可通过气相色谱仪进样分析。
3.3.4 野菊花中龙脑异构体含量的测定
移取1.00 mL干燥的挥发油于5 mL容量瓶,加入10.0 μL内标溶液,用乙酸乙酯定容,每次取1.0 μL进行气相色谱分析。重复三次进样后,得到峰面积比的平均值,采用内标标准曲线法定量分析野菊花中(+)-龙脑和(−)-龙脑的含量。
4 结果与讨论
4.1 优化升温程序
用0.03 mg·mL−1的龙脑异构体混合标准溶液进行升温程序优化,所得色谱图的局部放大结果见图1,具体实验数据见表1。从图1和表1可见,在所选4个温度下,龙脑的两个异构体均实现了基线分离,随着温度升高,两个异构体的保留时间逐渐缩短,两者的峰面积几乎保持不变,但是峰高呈增加趋势,半峰宽逐渐变小,分离度也逐渐变小。可见,升高柱箱温度,有利于缩短分离时间。
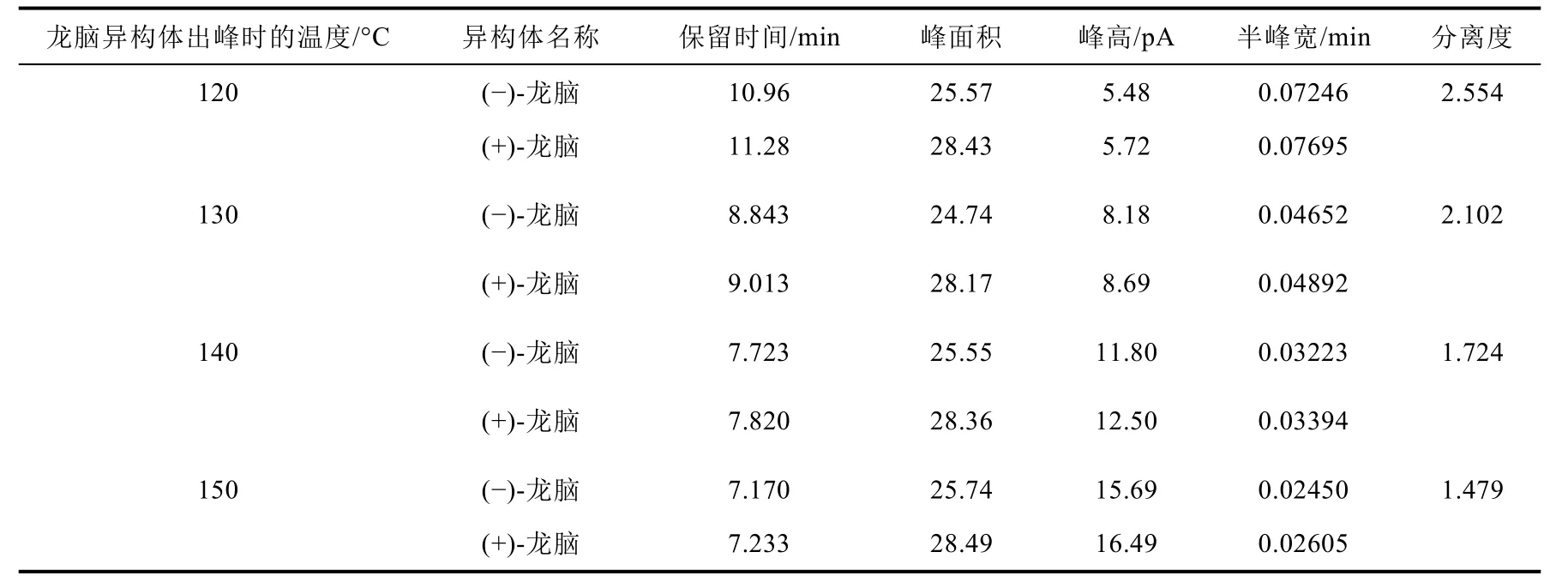
表1 龙脑异构体混合标准溶液程序升温优化结果
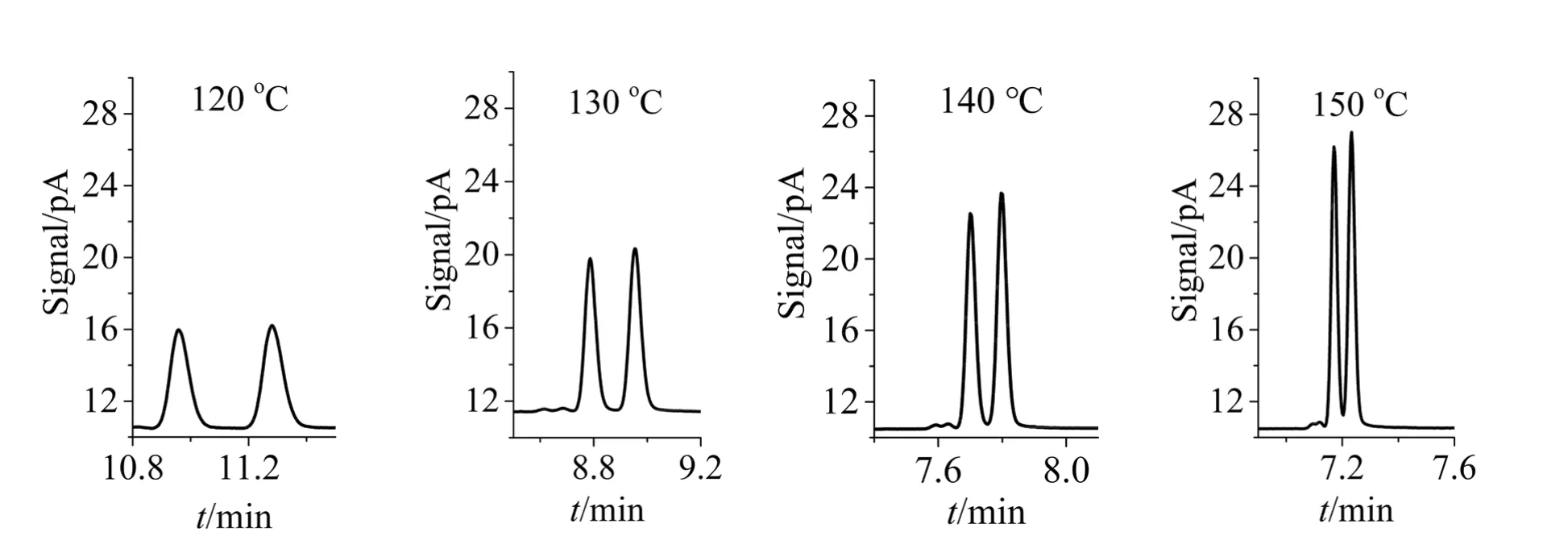
图1 龙脑异构体混合标准溶液的色谱图
对野菊花挥发油样品采用了同样的升温程序优化(图2),从图2可见,只有在120 °C时,龙脑的两个异构体才能实现基线分离,温度升高时,会出现其他化合物和龙脑的两个异构体的峰重叠,这是由于野菊花挥发油的成分比较复杂(图3)。所以最终选用了龙脑异构体出峰时温度为120 °C的升温程序分离龙脑异构体混合标准溶液和野菊花挥发油中的龙脑异构体(图3)。
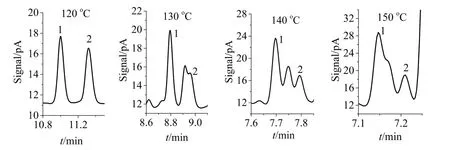
图2 野菊花挥发油的局部放大色谱图
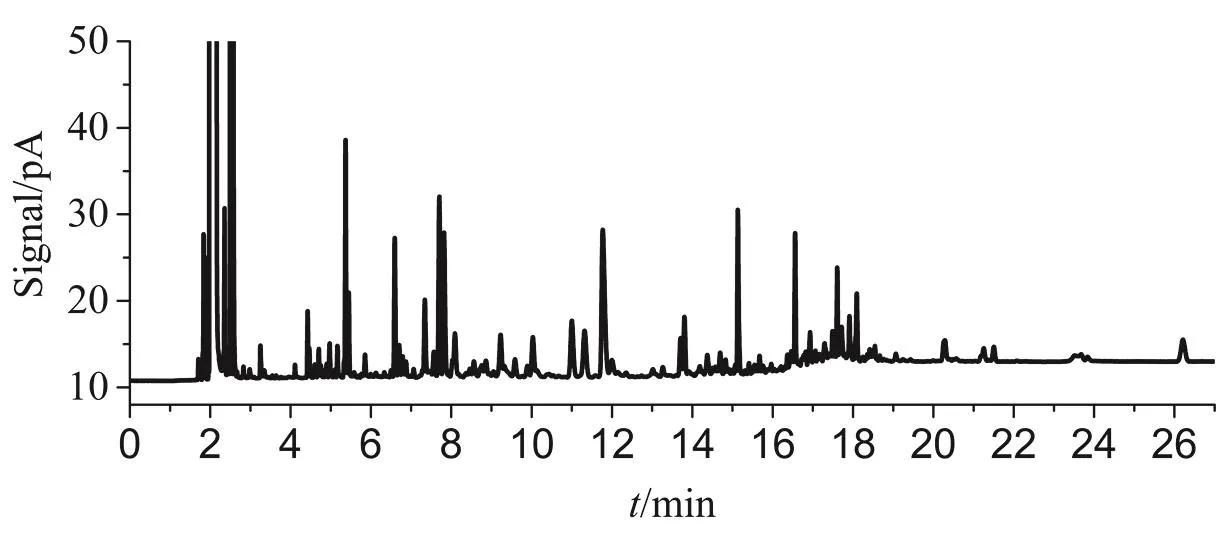
图3 最佳升温程序下野菊花挥发油的色谱图
4.2 龙脑异构体标准曲线的测定
记录不同浓度龙脑异构体标准溶液的色谱图(图4),确认色谱图中龙脑异构体的峰的保留时间,并分别计算龙脑异构体以及内标的峰面积。求算龙脑异构体/内标的峰面积比,用峰面积比对浓度进行线性回归,得到龙脑异构体的标准曲线和线性回归方程,结果如图5所示。
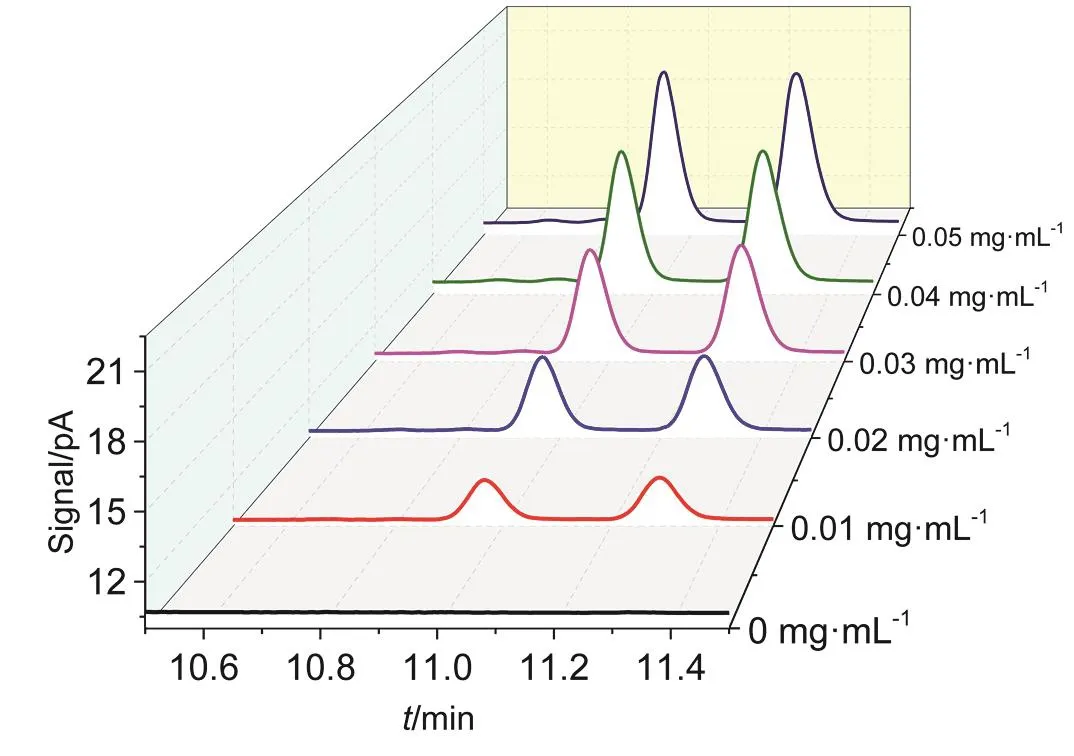
图4 不同浓度龙脑异构体标准溶液的色谱图

图5 不同浓度龙脑异构体标准溶液的标准曲线
4.3 实验拓展
樟脑和异龙脑也是野菊花中常见的手性物质,因此将樟脑、异龙脑和龙脑混合溶液进行手性气相色谱分析(图6)。由图6可见,异龙脑和龙脑的手性异构体可以实现基线分离,但樟脑的异构体无法进行手性分离。如果需要对樟脑异构体进行手性分离,则需要寻找其他的手性色谱柱。本实验所用Varian CP-Chirasil-Dex CB手性色谱柱的固定相为β-环糊精直接键合于二甲基聚硅氧烷上。根据文献报道[15],Astec CHIRALDEX B-DM手性色谱柱可以用于分离樟脑的异构体,该色谱柱所用固定相为全甲基化β环糊精。因为在环糊精衍生物中,取代基的位置和类型都会直接影响到其手性选择性,因此可以引导学生从分子间相互作用力的角度讨论手性分离的机理,以及手性固定相的选择策略等[16]。
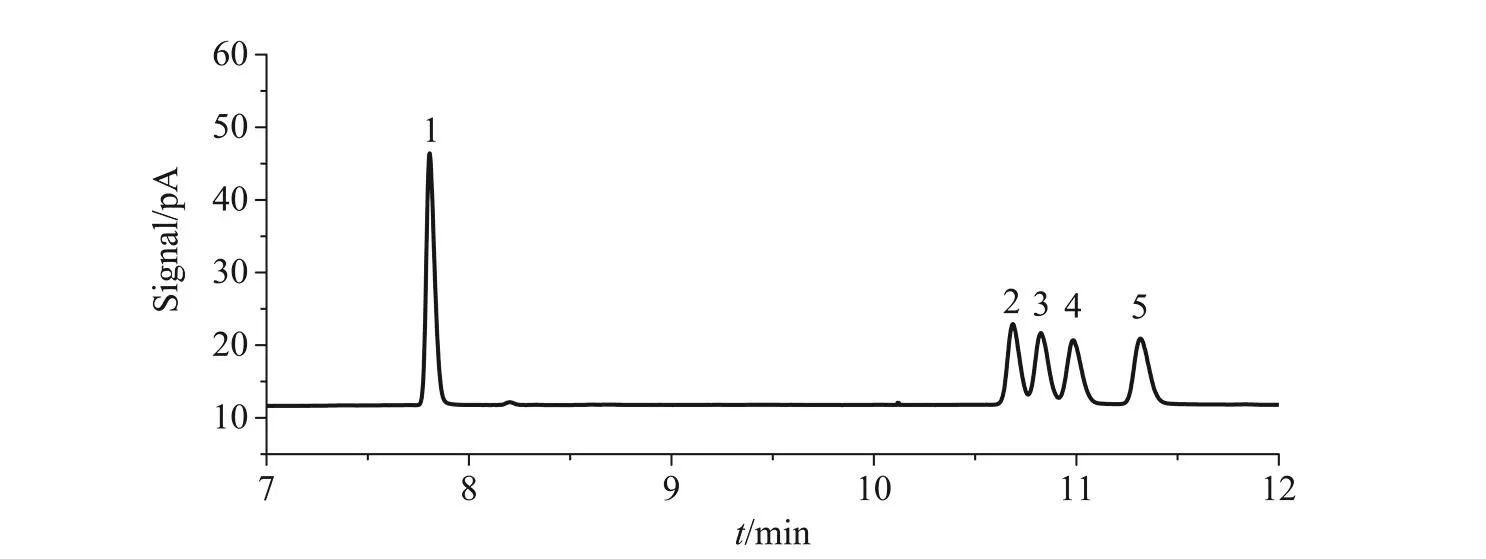
图6 混合标准样品的色谱图
5 数据处理
5.1 记录色谱操作条件
包括:仪器型号、进样口温度、分流比、柱类型、柱长、载气类型、载气流速、检测器类型等。
5.2 龙脑异构体的定性分析
分别进样(+)-龙脑和(−)-龙脑,记录色谱图,读取调整保留时间(将溶剂乙酸乙酯的保留时间作为死时间)。
5.3 龙脑异构体的定量分析
根据龙脑异构体的线性回归方程,将野菊花样品龙脑异构体与内标峰面积的比值代入,可以得到野菊花中(−)-龙脑和(+)-龙脑的含量分别为0.0837 mg·g−1和0.0731 mg·g−1。加标回收实验结果为,(−)-龙脑平均回收率为99.5% (相对标准偏差RSD = 2.66%,n= 6),(+)-龙脑回收率为100.9% (RSD =20.8%,n= 6),表明该方法的回收率好,准确度高,方法可靠。
6 实验组织
本实验共用时6–8 h,在处理野菊花样品期间,可以穿插学习气相色谱仪的使用方法、配制标准曲线所用溶液等。实验开展过程中涉及到气相色谱仪的使用及样品前处理技术,建议本实验向大学二年级下学期或三年级上学期学生开设。本实验还可作为“气相色谱法测定野菊花中樟脑和龙脑的含量”的拓展实验,在基础实验结束后,指导学生将色谱柱更换为手性色谱柱后,进行本实验。
7 注意事项
注意手性色谱柱的最高使用温度;龙脑异构体的标准溶液属易挥发溶液,不用时需用封口膜将容量瓶密封,并保存于4 °C冰箱中。
8 结语
本实验向学生完整地展现了科学研究中样品前处理、色谱仪器条件的优化、样品中手性化合物的定性分析和定量分析的流程,并且涵盖了样品前处理技术、手性气相色谱分析方法、内标标准曲线法等多个知识点。自实验开设以来,教学相长,教师和学生们均对手性分离产生了浓厚的兴趣。
