吖内酯的动态动力学拆分反应研究进展
2021-11-05黄仁福刘庆文林静容程探宇
黄仁福,刘庆文,林静容,程探宇
(上海师范大学化学与材料科学学院,上海200234)
1 动态动力学拆分(DKR)
在不对称合成领域,DKR是一种将外消旋化合物转化为对映异构体的理想方法之一,这一过程包括手性底物的外消旋化和外消旋底物的动力学拆分[1-2].在大多数情况下,外消旋化都是sp3杂化碳通过非手性的sp2杂化碳中间体发生的,同时,此过程中必须满足两个条件:1)外消旋化的过程不能使DKR产物消旋化;2)该外消旋化的反应体系必须与拆分过程相兼容.另外,为了实现高效、高选择性的DKR,还必须要满足以下条件:1)对映体的相互转化必须是快速的,如图1所示,R构型的化合物A((R)-A)和S构型的化合物A((S)-A)高消旋化速率(krac)的平衡;2)底物中的一种对映异构体在生成高对映选择性产物的过程中与手性催化剂的反应速率必须明显高于另一种对映异构体,如:kR≫kS,其中,kR表示R构型化合物的反应速率,kS表示S构型化合物的反应速率.底物A的一个对映异构体在与手性催化剂反应的同时,(R)-A和(S)-A之间的平衡移动遵循勒夏特里原理,通过手性催化剂,最终所有的外消旋底物都转化为单一的对映异构体.因此,DKR的最大理论产率能够达到100%.
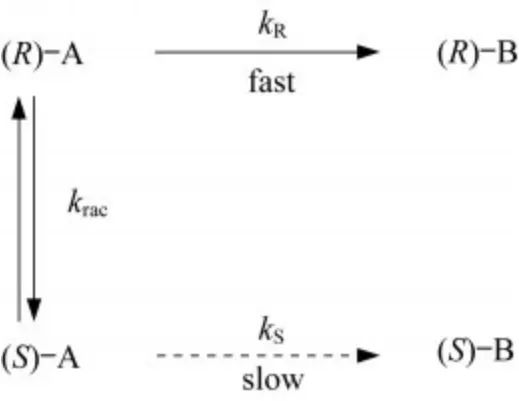
图1 DKR过程图示((R)-B:R构型的化合物B;(S)-B:S构型的化合物B)
2 吖内酯
近年来,小分子库的多样性导向合成在新药研发领域变得越来越重要[3].吖内酯(噁唑-5-酮)这类小分子化合物结构中包含许多活性位点,允许多种可能的修饰,这使得它成为许多化合物合成中的重要中间体.多取代的杂环骨架能够相对容易地由吖内酯合成,并且具有立体选择性.通过吖内酯中间体,也可以轻易地分离出天然和非天然氨基酸的对映异构体.
2.1 吖内酯的发展历程
1883年,PLÖCHL[4]在乙酸酐存在下,利用苯甲醛和马尿酸进行缩合首次合成了吖内酯.然而,ERLENMEYER[5]在1900年首次确立了吖内酯的正确结构,并将其命名为吖内酯.吖内酯的化学性质一直以来都未被研究,直到20世纪40年代,那时人们将青霉素的结构误认为是吖内酯结构.由于人们对青霉素有极大的研究兴趣,所以很多研究小组都投入了大量的精力研究吖内酯的反应性.尽管最终发现青霉素的结构实际上是一个β-内酰胺环体系,而不是吖内酯环,但这些研究成果为后来研究吖内酯骨架开辟了道路.
2.2 吖内酯的一般反应性
自从ERLENMEYER[5]的吖内酯合成法被发现以来,陆续有文献报道了多种吖内酯的合成方法.目前常用的方法是在较温和的条件下,通过N-酰化氨基酸衍生物与缩合剂反应合成吖内酯,缩合剂一般使用活性的酸酐或碳二酰亚胺.
吖内酯环体系中存在着大量的活性位点,允许其发生各种转化,如图2所示.由于吖内酯骨架中4位碳(C-4)的质子酸性较强(p Ka≈9),导致其非常容易互变异构,使其能够与一系列的亲电试剂反应.或者利用路易斯酸与吖内酯作用,通过环加成反应合成新的杂环化合物.此外,吖内酯环还可以通过亲核试剂进攻环体系中的羰基碳而打开,形成各种类型的保护氨基酸结构.本文作者将近年来对吖内酯的DKR研究进展进行综述.
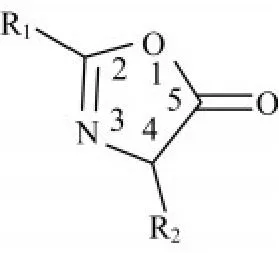
图2 吖内酯结构
3 吖内酯的DKR
吖内酯结构存在多反应位点,即可发生亲电反应,也可发生亲核反应.吖内酯的DKR,主要发生在其亲电位点上.通过DKR,利用吖内酯能够制备多种含官能团光学纯的氨基酸衍生物.
1998年,LIANG等[6]首次报道了利用非酶催化剂对吖内酯进行DKR.运用一种5%(摩尔分数)的平面手性4-二甲氨基吡啶(DMAP)衍生物对吖内酯进行醇解,导致吖内酯开环,得到高产率产物1,如图3所示.尽管这种方法具有开创性,但只有甲醇、乙醇和异丙醇能够完全反应,达到中等水平的对映体过量值(ee为44%~78%).
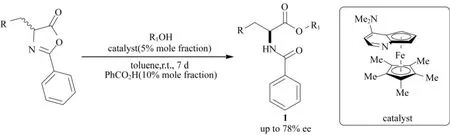
图3 通过DMAP衍生物催化的吖内酯DKR(Me:甲基;R,R1:表示不同取代基)
2005年,BERKESSEL等[7]报道了一种运用吖内酯的DKR醇解反应合成天然或非天然氨基酸的方法,如图4所示.在5%(摩尔分数)的手性尿素双功能催化剂存在下,烯丙醇与吖内酯反应,得到具有高对映选择性的产物2.核磁共振(NMR)实验表明,催化剂的活化机理是尿素基团与吖内酯羰基之间通过氢键作用,并且催化剂另一端的氨基基团与作为亲核试剂的醇的相互作用,这对反应的立体选择性起到了非常重要的作用.
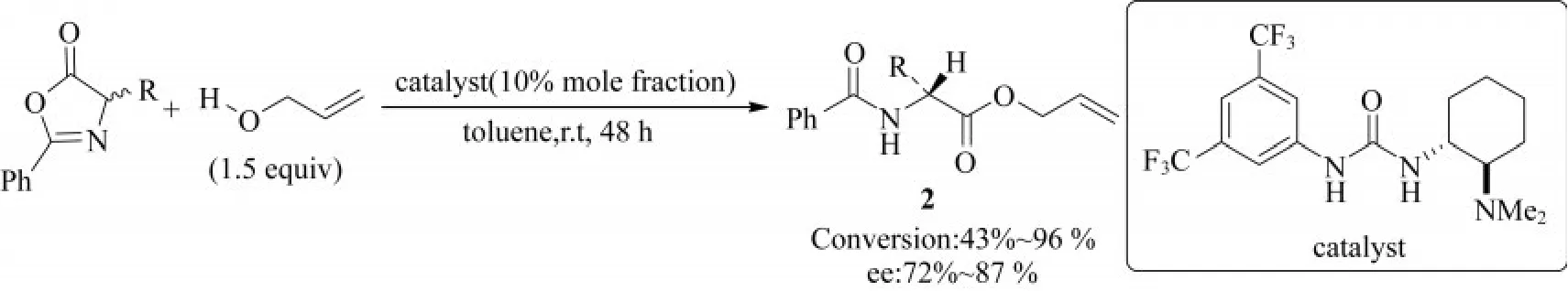
图4 有机催化剂催化吖内酯DKR
2012年,RODRIGUEZ-DOCAMPO[8]报道了一种吖内酯的硫解不对称DKR反应.反应中使用的是一种10%(摩尔分数)的金鸡纳碱类催化剂,如图5所示,在最优反应条件下,不同取代基的吖内酯都能够得到高收率的开环产物,但反应的选择性一般(ee为23%~73%).
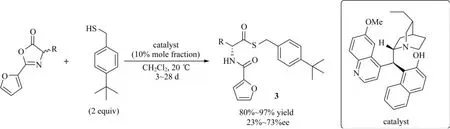
图5 硫解吖内酯的不对称DKR
2013年,PALACIO等[9]再次发现了一种金鸡纳碱类有机催化剂能够对吖内酯进行硫解反应.这一工作有效弥补了之前的对映选择性低下的问题,手性开环硫解产物能达到92%的ee值,如图6所示.但这一反应的收率一般(24%~60%).通过核磁共振氢谱(1H-NMR)实验发现,催化剂和吖内酯在反应过程中会形成一个不反应的离子对中间体,进而导致低收率.
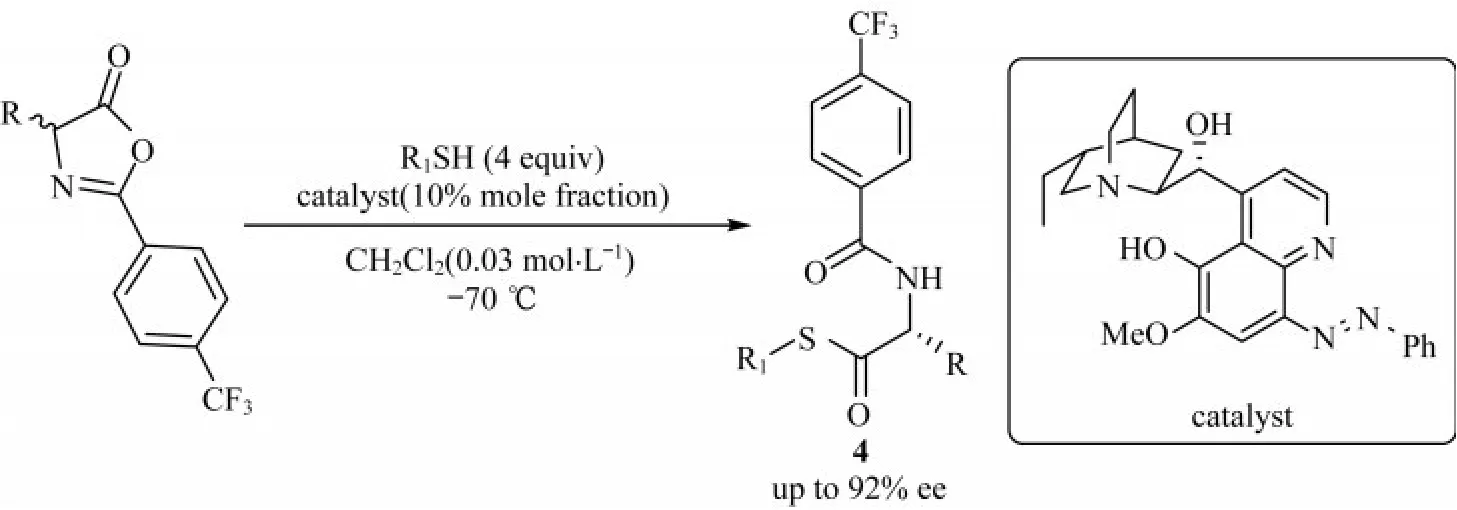
图6 硫解吖内酯的不对称DKR
2014年,CHAPLIN等[10]提出了一种利用吖内酯的DKR制备高对映选择性羧酸衍生物5的方法,如图7所示.这一方法对于丙型肝炎蛋白酶抑制剂的制备过程非常重要.在优化了生物催化反应的条件下,分别在脂肪酶PS或酶Novozym-435存在下,该反应能够将相应的吖内酯转化为顺式异构体6或反式异构体7.
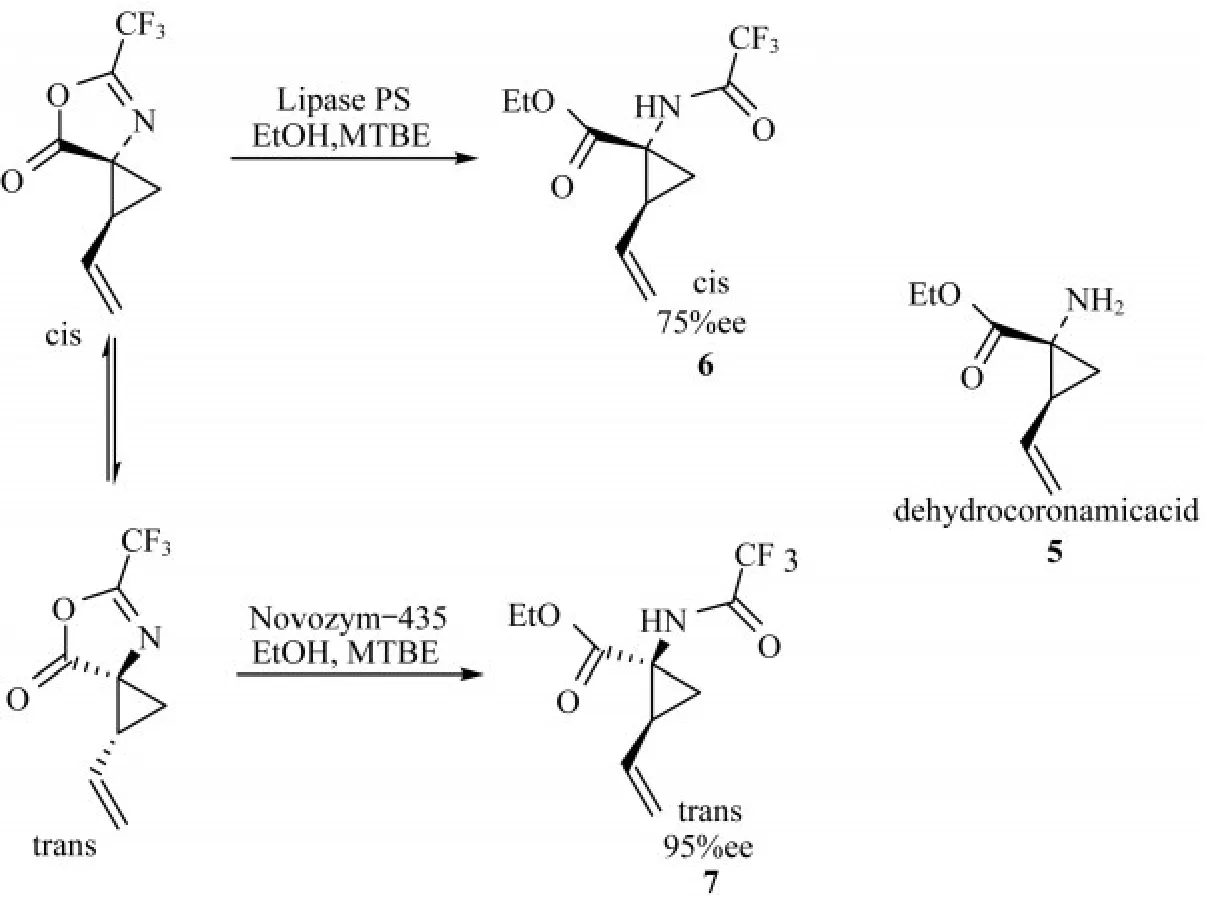
图7 DKR吖内酯制备高对映选择性羧酸衍生物(Et OH:乙醇;MTBE:甲基叔丁基醚)
2014年,METRANO等[11]报道了一种在甲醇存在下,利用多肽作为催化剂的吖内酯DKR反应,如图8所示.多种不同取代的吖内酯环都能够用来制备高对映体比率(e.r.为93∶7)的手性α-氨基酸8.产物的对映选择性可能是由于在催化剂存在下,甲醇优先与S构型的吖内酯反应,并在综合反应过程中电荷稳定,导致得到单一异构体产物.
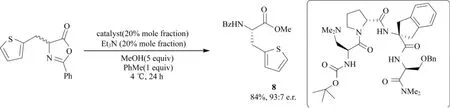
图8 多肽催化吖内酯DKR(PhMe:甲苯;MeOH:甲醇;Bz:苯甲酰基;Bn:苄基)
在吖内酯的DKR反应中,大多数的报道都仅限于一种特定的醇.2010年,YANG等[12]报道了一种利用苯并四咪唑作为催化剂的吖内酯DKR反应,如图9所示,使用10%(摩尔分数)的催化剂就能促进反应发生,得到高收率的α-氨基酸二(1-萘基)甲酯9,尤其是吖内酯的C-4位是芳香基取代时,反应的收率更高.
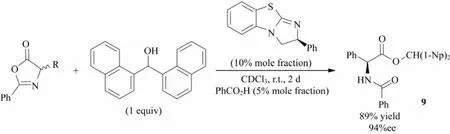
图9 苯并四咪唑催化吖内酯DKR(Np:萘环;CDCl3:氘代氯仿)
催化循环的机理研究表明,吖内酯的开环首先是催化剂进攻吖内酯中的羰基碳,在苯甲酰胺与羰基之间通过氢键形成过渡态.此外,由于催化剂的2位碳(C-2)苯基基团的空间排斥作用,可能导致只允许醇从一个方向进攻,导致得到单一异构体产物.对所有基团的进一步研究表明,苯甲酰胺的羰基与亲核试剂结合的阴离子之间可能存在静电作用,这种相互作用有利于对映体的快速反应[13].
2011年,LU等[14]又报道了一种利用二取代的二酚磷酸衍生物作为催化剂的吖内酯DKR反应.他们使用不同的醇对吖内酯进行开环反应得到10,但只有1-萘甲醇表现出良好的对映选择性结果(ee为92%).并且,4-芳基吖内酯作为亲电试剂时具有较高的产率与ee值,如图10所示,而4-烷基取代的吖内酯衍生物作为亲电试剂时,反应的ee值就会大大下降(29%~59%).

图10 二取代二酚磷酸衍生物DKR吖内酯开环
2013年,DONG等[15]报道了利用一种手性双胍盐类有机催化剂构筑三重立体中心的反应.吖内酯的催化不对称氧化胺化与噁唑烷的动力学拆分,一起参与了噁唑烷-4-酮的不对称合成,如图11所示,得到多种具有潜在生物活性的手性噁唑烷-4-酮衍生物11,其对映体过量值高达92%.值得关注的是,反应的副产物噁唑烷12已成功地应用于吲哚和苯乙烯的不对称氧胺化反应中.
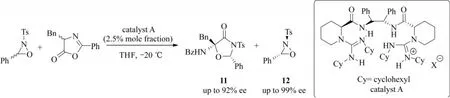
图11 噁唑烷-4-酮的不对称合成(Ts:对甲苯磺酰基;THF:四氢呋喃;X:阴离子)
2015年,YU等[16]再次报道了利用这种手性双胍盐类有机催化剂参与肟和吖内酯的DKR反应,如图12所示.合成出了高收率与高ee值的N-酰基氨基酸肟酯衍生物13.将这种活性肟酯进一步转化为相应的二肽衍生物,产物的立体选择性完全保留.

图12 双胍盐类催化肟与吖内酯的DKR(R1,R2:表示不同取代基)
2015年,TALLON等[17]提出了一种基于芳基修饰的吖内酯不对称DKR反应.此反应在10%(摩尔分数)的具有C2对称轴的方胺催化剂催化下,吖内酯与苯甲醇反应,得到高立体选择性的产物14,如图13所示.该产物可以进一步脱羧酸保护,或者氨基保护得到相应的手性氨基酸衍生物.
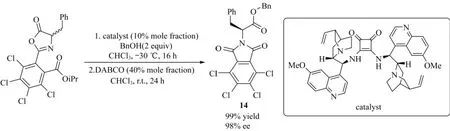
图13 四氯异丙羰基取代的吖内酯的DKR(BnOH:苯甲醇;DABCO:三乙烯二胺)
2016年,ZHANG等[18]首次报道了利用有机磷酸催化剂胺解吖内酯的DKR反应,如图14所示.此反应补充了之前吖内酯的醇解与硫解.使用在空间上体积相对较大的2位取代苯胺作为亲核试剂,让其与手性催化剂形成相互作用的氢键,进而产生空间位阻,得到高立体选择性的双酰胺类化合物.
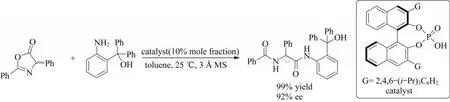
图14 有机磷酸动态动力学胺解吖内酯(i-Pr:异丙基;3ÅMS:3埃分子筛)
2018年,MANDAI等[19]报道了利用一种新型手性DMAP催化剂对吖内酯进行DKR的反应,如图15所示.此反应能够得到多种氨基酸衍生物,并且只需3%(摩尔分数)的催化剂量.控制实验表明,酰胺基团在联萘基的3,3’位时,对于加快反应速率和提高反应的立体选择性至关重要.
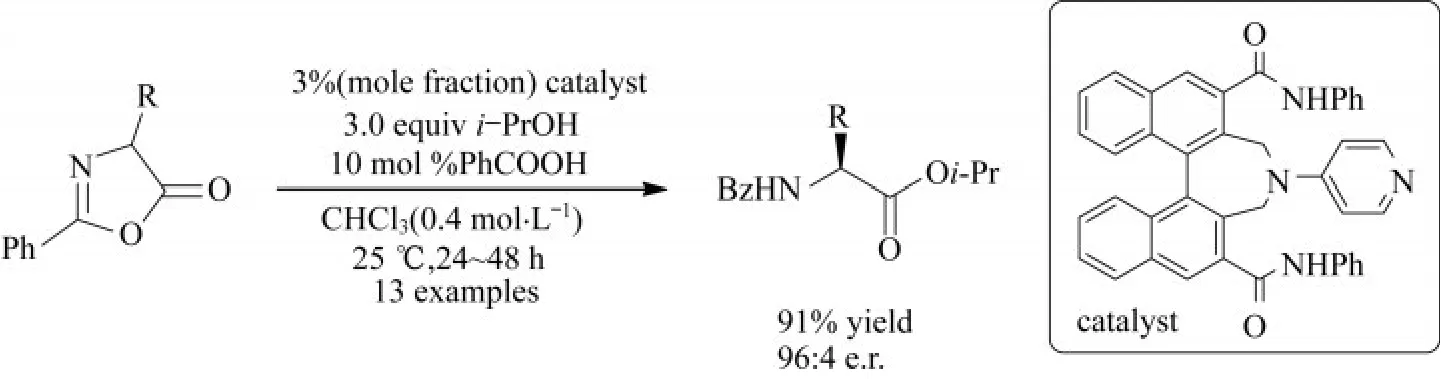
图15 新型手性DMAP动态动力学拆分吖内酯(i-PrOH:异丙醇;i-Pr:异丙基;PhCOOH:苯甲酸;R:取代基)
2020年,XIE等[20]报道了使用一种新型的DMAP氮氧化物作为酰基转移催化剂,DKR吖内酯,如图16所示.反应以简单的甲醇为亲核试剂,得到了多种保护的氨基酸衍生物,收率达到88%~98%,ee值为87%~96%.其他醇类也是合适的亲核试剂,在催化剂负载量为1%(摩尔分数)时,以克级进行的吖内酯DKR结果良好.
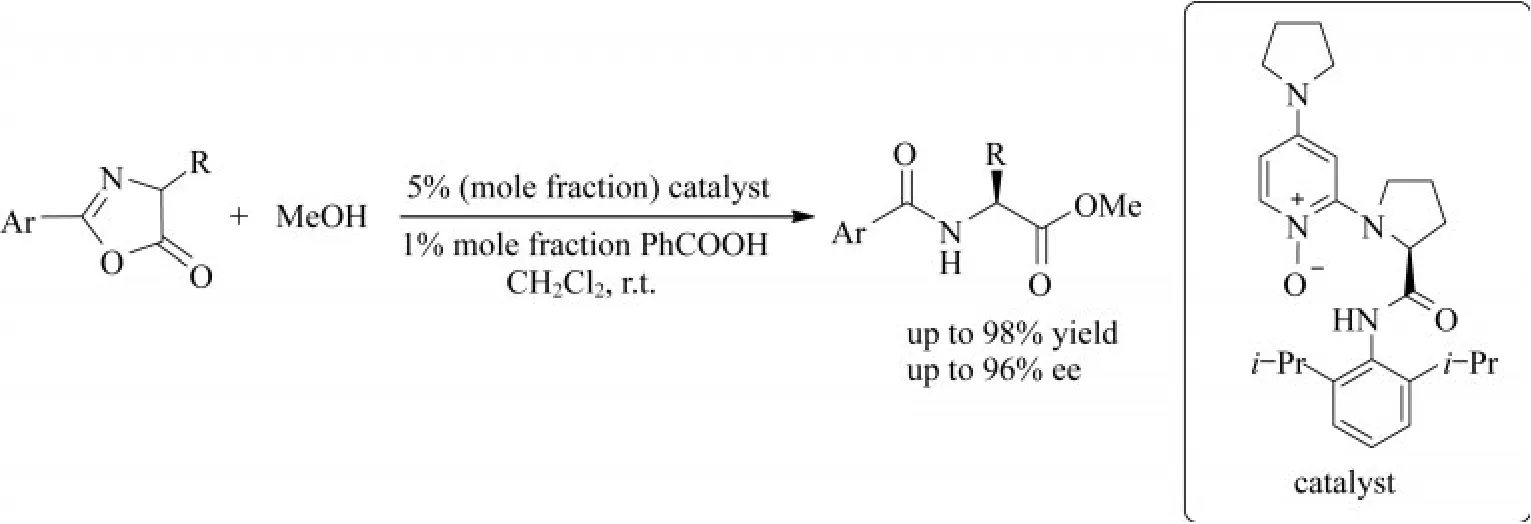
图16 DMAP氮氧化物DKR吖内酯
4 总结与展望
本文作者综述了吖内酯这类含氮杂环结构的内酯在不同亲核试剂存在下的DKR反应.通过对吖内酯的DKR得到单一手性的氨基酸类化合物,已是目前常用的方法,但这一方法普适性仍然受催化剂或亲核试剂的影响,因此,探索吖内酯结构的更高效、更便捷的反应方法,仍然是值得学者们研究的课题.
