邻苯二甲酸酯加氢Ru-Ni双金属催化剂研究
2021-11-03李文思赵玉军李国兵
李文思,王 岩,徐 艳,赵玉军,李国兵
(天津大学化工学院,天津 300350)
增塑剂作为塑料制剂重要成分,其产量和消费量大约占所有塑料制剂的80%[1]。环己烷1,2-二甲酸二异辛酯(DEHCH)作为绿色环保的增塑剂产品[2],其具有优异的增塑性能,且安全可靠,已经被批准在玩具、医疗、食品行业中使用[3-4]。以邻苯二甲酸酯二异辛酯(DOP)为原料催化加氢是合成环己烷1,2-二甲酸二异辛酯(DEHCH)的方法之一[2]。由于其原料DOP在国内生产工艺成熟[5],开发以DOP为原料的催化加氢合成DEHCH工艺更具工业应用前景[4]。
在邻苯二甲酸酯类加氢反应过程中,一般采用负载型金属催化剂如:Rh[6]、Ru[7]和Ni[8-9]等,其中Ru基催化剂是加氢反应中较常用的负载型催化剂[10-11]。最近的研究发现,在单金属催化剂中掺杂其他金属作为助剂(如:Re[12]、Pt[13-15]、Sn[13-14]、Rh[15]和Ni[10,16-23]等)后,2种金属之间的协同作用能够显著提高催化反应的活性、选择性和稳定性[24-25]。由于贵金属作为掺杂助剂成本较高,使用非贵金属(如Ni等)构造双金属催化剂以提高催化剂的催化性能,并减少催化剂中贵金属用量[27]显得尤为重要。双金属催化剂已经在多种催化加氢体系中使用。Zhu等[28]研究发现随着还原温度的升高,Ru-Ni会逐渐由双金属形式转变为RuNi合金。并且Ru-Ni双金属催化剂的催化活性高于RuNi合金催化剂。作者认为,由于Ru-Ni双金属可以提供更多的活性位点,并且在Ru和Ni之间的协同作用使得其在催化苯加氢反应体系中具有较好的催化性能。Yu 等[21]也认为Ru-Ni双金属催化活性的提升是由于Ru-Ni金属之间以及Ru金属与载体之间的相互作用,并且Ru-Ni之间存在氢溢流效应。然而,在DOP加氢反应体系中尚无Ru-Ni双金属催化剂应用的研究报道,其作用机理尚不明确。
本课题前期研究了Ru/ACx系列催化剂在DOP加氢反应中的构效关系,揭示了DOP加氢反应中载体的结构效应[7]。此外,还证明Pt金属的掺杂能够和Ru金属形成合金颗粒,所形成的RuPt双金属催化剂的电子效应显著提高了DOP的加氢活性和选择性[12]。本研究在Ru/AC催化剂的基础上,掺杂非贵金属Ni作为助剂制备了RuNi/AC催化剂,并考察其在DOP加氢合成环己烷1,2-二甲酸二异辛酯(DEHCH)反应中的催化性能。旨在证明在该体系中Ru-Ni双金属颗粒之间的相互作用及其在DOP加氢反应中的作用机制,并揭示Ru-Ni双金属之间的协同作用。
1 实验材料和方法
1.1 材料及仪器
无水氯化钌(Ⅲ)(质量分数为99%,无水),北京百灵威科技有限公司;六水合硝酸镍(质量分数为98%,无水),上海阿拉丁生化科技有限公司;活性炭(100~200目),承德华宇活性炭制造公司;邻苯二甲酸二异辛酯(分析纯),天津渤化永利化工股份有限公司;无水乙醇(HPLC),天津康科德技术公司;氮气(体积分数为99.999%)、氢气(体积分数为99.999%),均由天津六方高科技发展有限公司提供;实验用水为超纯水。
1.2 催化剂的制备
采用共浸渍法制备Ru/AC、RuNi/AC、Ni/AC催化剂以及不同m(Ru)∶m(Ni)的系列催化剂:Ru0.6Ni1/AC[m(Ru)∶m(Ni)=0.6∶1.0]、Ru0.6Ni3/AC[m(Ru)∶m(Ni)=0.6∶3.0]、Ru0.6Ni5/AC[m(Ru)∶m(Ni)=0.6∶5.0]和Ru0.6Ni7/AC[m(Ru)∶m(Ni)=0.6∶7.0]。制备方法为:将活性炭载体在393 K下干燥3.0 h;干燥后的活性炭载体加入到配制好的一定浓度前驱体溶液中浸渍一定时间后,将浸渍后的催化剂在室温下干燥10.0~12.0 h。随后,在393 K的烘箱中干燥3.0 h。干燥后的催化剂在N2氛围中和573 K条件下焙烧4.0 h。将催化剂在H2氛围中和473 K条件下还原3.0 h,即制得所述催化剂。
1.3 催化剂的表征
X射线衍射分析采用日本理学Rigaku D/max-2500型仪器。辐射源为Cu-Kα射线(λ=1.541 nm,工作电压40 kV,工作电流20 mA),衍射图谱记录的扫描范围(2θ)为5~90°,扫描速度为10(°)·min-1。
CO脉冲化学吸附测试采用美国Micromeritics公司AutoChem 2920型吸附仪。取约0.2 g已焙烧未还原的催化剂,在H2气氛下以10 K·min-1的速率升温到473 K保持3.0 h,维持473 K不变,在He气氛下先吹扫1.0 h然后降温到323 K。温度维持在323 K,在10%CO-He混合气下进行脉冲吸附测试。
H2-程序升温还原测试采用美国Micromeritics公司AutoChem 2920型吸附仪。称取约0.2 g样品,在Ar气氛围下吹扫,423 K干燥处理1.0 h,降温至323 K。在10%H2+Ar混合气氛围下以10 K·min-1的速率升至823 K,在823 K下恒温维持10 min进行H2-TPR测试。
催化剂中钌和镍的实际负载量采用美国 Varian 公司Vista-MPX型电感耦合等离子体发射光谱仪2.6.1(ICP-OES)测定。
1.4 催化剂的评价
在100 mL高温高压反间歇应釜中加入10.0 g DOP作为反应底物,投入30 mL无水乙醇作为溶剂和0.15 g还原后的催化剂。用氢气吹扫5次以置换内部的空气。反应在初始压力为4.0 MPa、温度为393 K、搅拌速度为800 r·min-1的条件下反应4.0 h。反应后的液体产物用乙醇稀释后,采用BEIFEN气相色谱仪进行定量分析。色谱柱为Agilent HP-5(60 m×0.32 mm×0.25 m),检测器为FID氢火焰检测器。
DOP的加氢过程先生成中间产物环己烯1,2-二甲酸二异辛酯,然后环己烯1,2-二甲酸二辛酯进一步加氢生成环己烷1,2-二甲酸二异辛酯(DEHCH)[7]反应历程如图1所示。

图1 DOP加氢反应途径图
DOP反应转化率(X),DEHCH选择性(S),产率(Y)和反应的TOF的公式如式(1)~(3)。

(1)
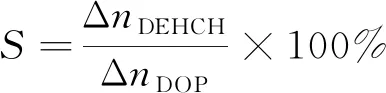
(2)
Y=SX
(3)
式(1)~(2)中:nt,DOP为反应后DOP的剩余量,n0,DOP为初始DOP量,ΔnDEHCH为反应中转化为DEHCH的量,ΔnDOP为反应中DOP的转化量。

(4)
式(4)中:M为DOP反应的物质的量(mol),ARu为Ru的相对分子质量,g为催化剂的质量,T为反应时间,D为反应的分散度,WRu为Ru的负载量。
2 实验结果与讨论
2.1 XRD表征结果
图2为单金属催化剂Ru/AC、Ni/AC和双金属催化剂RuNi/AC催化剂的X射线衍射(XRD)图。
由图2可见,所有样品的衍射峰没有明显差异。所有样品的XRD图谱均在23°和44°附近显示2个宽峰,分别对应于无定形碳的(002)和(100)晶面[29-30],证明AC载体的原始结构得以保留。所有样品均未观察到Ru颗粒的特征衍射峰,是因为Ru在AC载体上负载量较低并且高度分散[31]。而Ni/AC在2θ=44.48°出现对应于Ni(111)晶面的衍射峰[31],表明Ni金属颗粒的存在,证明已经成功的将Ni掺杂到Ru/AC催化剂中。

图2 3种催化剂Ru/AC、RuNi/AC、Ni/AC的XRD图谱
2.2 CO脉冲吸附结果
采用CO化学吸附表征的Ru/AC、Ni/AC和RuNi/AC的结果如表1所示。

表1 Ru/AC、Ni/AC、RuNi/AC的CO脉冲吸附结果
由表1可知Ni金属的掺杂使得RuNi/AC双金属催化剂CO的吸附量增加、载体上活性金属的分散度提高,结合后面H2-TPR的结果发现Ru-Ni之间的相互作用使得Ni金属还原温度降低,有更多的Ni活性组分被还原,活性位点的增多,表现为CO吸附量的提升,同时活性金属的分散度也增加[31]。而RuNi/AC粒径的增大,可能是由于有更多的Ni金属颗粒沉积导致。
2.3 H2-TPR表征结果
利用H2-TPR考察催化剂的合适的还原温度、以及金属和金属氧化物之间的协同作用关系,表征Ru/AC、Ni/AC、RuNi/AC的结果如图3所示。如图中所见,Ru/AC催化剂在353和443~573 K处有2个明显的H2还原峰,均对应于RuOx被还原为Ru的过程,峰型大小差异是由于分散度的不同[32]以及RuOx与载体之间的相互作用强弱不同[33-34]所导致。Ni/AC催化剂的第1个还原峰温度大约为600 K,对应于NiOx被还原成Ni单质的反应过程。双金属催化剂RuNi/AC催化剂在323~473 K和543 K处出现2处宽峰,第1个峰变小是由于和载体之间弱相互作用的Ru减少[35]。而第2个峰的形成原因更为复杂,峰的位置更接近Ru/AC单金属催化剂第2个还原峰的位置,峰的面积也更大,实际上反映了RuOx和NiOx物种同时被还原为Ru、Ni金属单质的过程。双还原峰的存在,排除了Ru-Ni形成合金的可能性[18]。对比单金属催化剂,Ru、Ni的还原峰发生了位移,表示Ru和Ni还原温度发生了改变,说明Ru和Ni之间存在相互作用。推测RuOx被还原为Ru之后,Ru可能会活化H2,使得NiOx更易被还原[29],表现为Ni还原温度的降低[37-38]。

图3 AC、Ru/AC、RuNi/AC和Ni/AC催化剂的H2-TPR谱图
2.4 催化剂的催化活性


表2 Ru/AC、Ni/AC、RuNi/AC、和机械混合催化剂的催化加氢性能
反应条件:T=393 K,P=4.0 MPa,t=4.0 h,r=800 r·min-1,m(DOP)=10.0 g,m(cat.)=0.15 g,V(Solvent)=30 mL,am(Ru/ACcat)=0.075 g,am(Ni/ACcat)=0.075 g。
2.5 m(Ru)∶m(Ni)对DOP催化加氢性能的影响
在确定钌镍之间存在协同作用后,通过改变m(Ru)∶m(Ni)制备了系列Ru0.6Nix/AC双金属催化剂以便于进一步研究钌镍之间的协同效应,m(Ru)∶m(Ni)为0.6∶1.0,0.6∶3.0,0.6∶5.0,0.6∶7.0。首先采用ICP测试对几种催化剂的实际金属负载量,表征结果如表3,可以看出,各催化剂的实际负载量和理论负载量结果一致。

表3 催化剂的实际金属负载量
对于系列Ru0.6Nix/AC催化剂进行XRD表征,结果如图4所示。Ru0.6Nix/AC的系列催化剂在23°和44°出现对应于载体无定形碳的(002)和(100)晶面[29-30]。由于Ru在载体上分散度较高,所以未观察到Ru颗粒的特征衍射峰。其中Ru0.6Ni5/AC和Ru0.6Ni7/AC在2θ=51.78°出现明显宽峰,对应于Ni(200)晶面的特征衍射宽峰[31],表明这2种样品掺杂Ni金属粒径较大,可能是由于负载量太高使得金属团聚严重。

图4 不同m(Ru)∶m(Ni)Ru0.6Nix/AC系列催化剂的XRD图谱
图5为系列Ru0.6Nix/AC催化剂的加氢活性数据图。由图可见,随着Ni负载量的增加催化活性显示出先上升后下降的趋势,并且转化率和收率表现出相同的变化规律。对比不同m(Ru)∶m(Ni)系列催化剂的活性结果,发现适量Ni金属的掺杂对于DOP的加氢活性有提高作用,但是过量Ni的掺杂反而会导致DOP加氢活性的下降,可能是由于Ru-Ni金属颗粒的团聚导致。因此,当m(Ru)∶m(Ni)为0.6∶5.0时双金属的催化剂活性最高。

图5 RuNix/AC催化剂DOP加氢的催化性能
2.6 Ru-Ni协同作用机理
基于以上研究结果和讨论,对于RuNi/AC双金属催化剂在DOP加氢反应中的协同作用机理进行了推测,其反应机理如图6所示。当Ru/AC掺杂Ni金属之后,一方面由于在H2氛围中,Ru-Ni这2种紧密相互作用的金属颗粒之间存在氢溢流效应[21],在这个过程中,Ru和Ni的协同作用使得H2更易被活化[16],H2分子在Ru金属的表面上解离成H原子,然后直接迁移到附近Ni金属的表面上进行下1步反应,这种氢溢流效应使得DOP可以直接被连续加氢,而不会出现“解吸-再吸附”的弯路,提高了加氢的速率[16,19,21]。

图6 RuNi/AC双金属催化剂在催化DOP加氢反应中的机理图

3 结论
1)Ni助剂掺杂使 Ru-Ni之间形成了相互作用,Ru降低了Ni的还原温度,促进更多的Ni物种被还原为金属Ni,使RuNi/AC暴露更多的活性位点,在反应中表现为DOP加氢活性的提高。

3)考察了m(Ru)∶m(Ni)对于DOP 加氢活性的影响,发现当m(Ru)∶m(Ni)为0.6∶5.0时催化活性最高。说明适量的Ni的掺杂能够提升催化剂的活性,但是Ni的添加量太大会由于负载量太大造成颗粒的团聚从而引起催化剂活性的下降。
