同轴电纺法TiO2/g-C3N4的制备及光催化性能研究
2021-11-03黄肖桢李云锋杨金鑫赵浩博
黄肖桢,常 薇,刘 斌,李云锋,杨金鑫,高 兵,赵浩博
(西安工程大学环境与化学工程学院,西安 710048)
由于在废水净化和太阳能利用等方面具有潜在的实际应用价值,太阳能光催化高效光催化剂得到了广泛的研究[1-3]。TiO2具有化学稳定性,高光催化活性,无毒且成本低等优点,被认为是最有前途的光催化剂之一[4-5]。但由于其3.0~3.2 eV的宽带隙,TiO2只对紫外光有响应,对可见光的响应较弱[6-7]。
石墨相氮化碳(g-C3N4)作为一种无金属光催化剂,因其原料丰富、可见光响应、制备简便和制造成本低等优点而受到广泛关注[8-13]。具有π-共轭体系的独特层状结构有助于电荷载流子的迁移,约2.7 eV的窄带隙使其在460 nm处具有出色的可见光吸收性能[14-15]。但是,纯g-C3N4的光催化活性也因其量子产率差和光生电子-空穴对的高重组率而受到限制[16-19]。而TiO2/g-C3N4复合材料不仅拓宽了光响应范围,而且抑制了光生电子-空穴对的复合,光催化效率也得到了显著提高[20-21]。
静电纺丝技术制备的一维结构有助于电子的快速迁移,这可以削弱空穴和电子的复合,从而可以提高光催化性能[22-24]。同轴静电纺丝技术是在静电纺丝的基础上发展而来的,作为一种简单可行的制备“核壳”结构纳米纤维的方法,近年来备受关注。本研究采用同轴电纺法成功制备了一系列不同g-C3N4添加量的TiO2/g-C3N4复合材料,并系统研究了制备样品的结构、组成、形貌、光催化性能和稳定性。此外,为了了解光催化机理,还研究了活性物种对TiO2/g-C3N4复合材料光催化降解亚甲基蓝的影响。
1 实验部分
1.1 实验原料
无水甲醇,分析纯,天津市津东天正精细化学试剂厂;无水乙醇,分析纯,利安隆博华(天津)医药化学有限公司;钛酸丁酯,化学纯,天津市福晨化学试剂厂;尿素,分析纯,天津市津东天正精细化学试剂厂;聚乙烯吡咯烷酮(PVP,Mw=1 300 000),分析纯,上海麦克林生化科技有限公司;乙酸,分析纯,利安隆博华(天津)医药化学有限公司;亚甲基蓝,指示剂,上海试剂三厂;草酸铵,分析纯,西安化学试剂厂;对苯醌,分析纯,成都艾科达化学试剂有限公司。
1.2 实验仪器
高压静电纺丝机,TL-Pro型,深圳市通力微纳科技有限公司;傅里叶变换红外光谱仪(FTIR),Lambda 950型,美国Perkin-Elmer公司;X射线衍射仪(XRD),Dmax-Rapid Ⅱ型,日本理学;紫外-可见分光光度计,UV-2450型,日本岛津;紫外可见漫反射光谱仪(UV-vis DRS),U-3310型,日本日立;场发射扫描电子显微镜(SEM),JEOL JSM 6700F型,FEI公司;比表面积及孔径分析仪(BET),Gemini Ⅶ 2390型,美国麦克仪器公司;光化学反应仪,XPA-7型,南京胥江机电厂。
1.3 材料的制备
1.3.1 g-C3N4的制备
将适量的尿素放入马弗炉中,以5 ℃·min-1的升温速率升温至550 ℃,保持4 h,得到淡黄色的g-C3N4样品。
1.3.2 TiO2的制备
将1.5 g PVP溶解在23.5 mL甲醇中,然后添加1.5 mL乙酸和2.1 mL钛酸丁酯,磁力搅拌24 h来制备TiO2前驱体溶液。电纺条件设置为:电压为12 kV,接收装置转速为200 r·min-1,流速为1 mL·h-1,针头与接收器之间的距离为11 cm。然后将收集的纤维毡以1 ℃·min-1的升温速率升温至500 ℃,保持3 h,得到TiO2纳米纤维。
1.3.3 TiO2/g-C3N4复合材料的制备
采用同轴电纺法制备TiO2/g-C3N4。首先制备壳层溶液和核层溶液。壳层溶液:将2.0 g PVP溶解在23.5 mL甲醇中,然后添加3.0 mL乙酸和4.2 mL钛酸丁酯,磁力搅拌6 h,得A溶液;之后,将一定量的g-C3N4加入到23.5 mL甲醇中,经过超声处理1 h得到均匀的g-C3N4悬浮液(B);最后,在磁力搅拌下将B加入A中,继续搅拌24 h(加入的g-C3N4的量分别为0.10、0.15和0.20 g,分别记为TCN-10、TCN-15和TCN-20)。核层溶液:将1.5 g PVP溶解于23.5 mL甲醇中,搅拌24 h。同轴电纺条件设置为:电压为12 kV,接收装置转速为200 r·min-1,核壳层流速比为1∶1,针头与接收器之间的距离为11 cm。然后将收集到的纤维毡以1 ℃·min-1的升温速率升温至500 ℃,保持3 h,冷却得TiO2/g-C3N4复合材料。
1.4 光催化性能测试
称取30 mg所制备的样品于试管中,加入30 mL亚甲基蓝溶液(2×10-5mol·L-1),暗室搅拌30 min,使其达到吸附脱附平衡。在500 W氙灯的照射下进行光催化反应,每隔20 min取1次降解样,通过离心分离后,取上清液在波长664 nm处测其吸光度A。亚甲基蓝浓度的变化用C/C0表示,C表示降解之后的亚甲基蓝浓度,C0表示亚甲基蓝的初始浓度。
1.5 重复利用性能测试
称取30 mg所制备的光催化剂于试管中,加入30 mL亚甲基蓝溶液(2×10-5mol·L-1),暗室搅拌30 min,使其达到吸附脱附平衡,在500 W氙灯的照射下反应80 min后,取样1次,离心,测试。之后倒掉试管中的上清液并将余下的光催化剂烘干,再加入30 mL亚甲基蓝溶液,重复上述过程5次。
1.6 光催化机理实验
将30 mg所制备的光催化剂加入到30 mL亚甲基蓝溶液(2×10-5mol·L-1)中,再分别加入1.0 mL无水乙醇(Ethanol)、2 mmol草酸铵(AO)和2 mmol对苯醌(BQ),暗室搅拌30 min,使其达到吸脱附平衡。在500 W氙灯照射下进行光催化反应,每隔20 min取样1次,离心,测试。
2 结果与讨论
2.1 SEM分析
随着g-C3N4添加量的增加,从TiO2到TiO2/g-C3N4复合材料的形貌演变如图1所示。图1a)为纯g-C3N4,其显示出具有皱纹的薄层片状结构。图1b)为所制备的TiO2纳米纤维,其呈短棒状结构。图1c)~图1e)可以明显看出,随着g-C3N4添加量的增加,复合材料中块状形貌逐渐增加,纳米纤维状形貌逐渐减少且长度显著缩短。

图1 不同g-C3N4添加量的TiO2/g-C3N4的SEM图
2.2 XRD分析
制备样品的XRD谱图如图2所示。可以看到制备的TiO2/g-C3N4复合材料在25.3°(101)、37.8°(004)、48.1°(200)、53.9°(105)、55.1°(211)、62.7°(204)、68.8°(116)、70.3°(220)和75.1°(215)处有9个衍射峰,与锐钛矿相TiO2(JCPDS No.21-1272)一致。在27.4°(110)、36.1°(101)和41.2°(111)处有3个衍射峰,与金红石相TiO2(JCPDS No.21-1276)一致。从图2中还可以看到,由于g-C3N4(JCPDS No.87-1526)在27.4°(002)处的强衍射峰与金红石相的27.4°(110)晶面衍射峰发生了重合,而g-C3N4的加入使TiO2/g-C3N4复合材料在27.4°处的衍射峰比纯TiO2的衍射峰强,因此表明所制备的复合材料是由TiO2和g-C3N4组成的。而TiO2/g-C3N4复合材料在25.3°处的主衍射峰可以看出随着g-C3N4的添加,主衍射峰的强度不断增强,表明g-C3N4的添加促进了TiO2晶粒的生长。

图2 制备样品的XRD谱图
2.3 FTIR分析
制备样品的FTIR谱图如图3所示。从图3可以看出,TiO2在400~800 cm-1范围内的宽带与Ti—O—Ti的拉伸振动相对应,g-C3N4在810 cm-1处的唯一吸收峰是3-s-三嗪环单元的特征振动峰。1 200~1 600 cm-1范围内的强吸收带来自于CN杂环的伸缩振动模式,3 000~3 300 cm1范围内的宽吸收带对应于N—H/O—H的伸缩振动。上述特征峰在制备复合样品的光谱图中共存,表明制备的样品含有TiO2和g-C3N4。
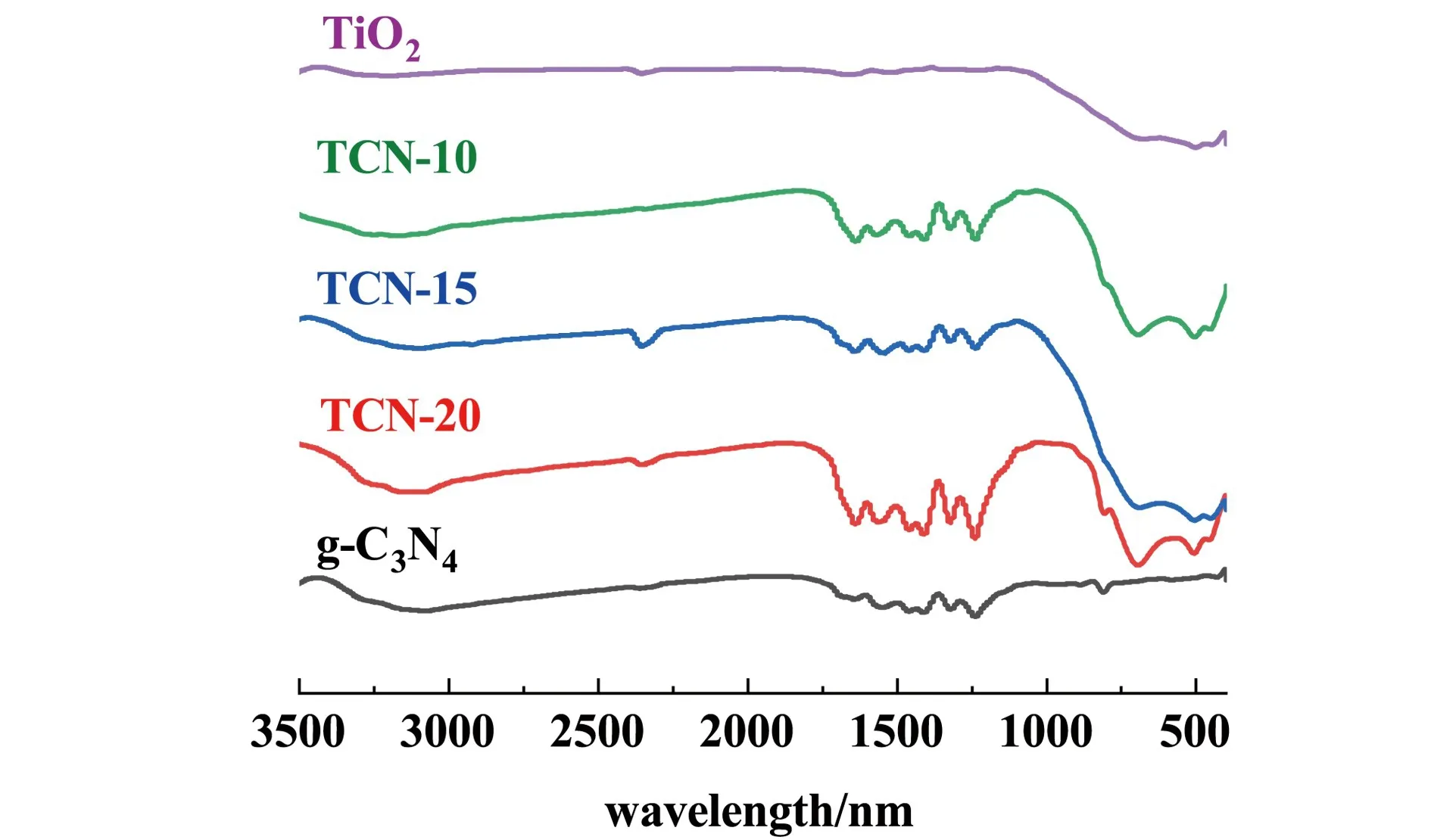
图3 制备样品的FTIR谱图
2.4 BET分析
制得的样品的氮吸附-脱附等温线和孔径分布曲线如图4所示。从图4中可以看出,3个样品具有典型的IV等温线并具有H3型回滞环,表明材料具有介孔特性。从孔径分布中可以看出,所有样品都属于介孔材料。制备样品的孔径、孔体积及比表面积见表1。由表1可得,TCN-15样品的孔径、孔体积及比表面积相比于TiO2和g-C3N4均有较大增加。说明同轴电纺法有效增大了材料的孔结构和比表面积,有利于光催化剂催化活性的提升。
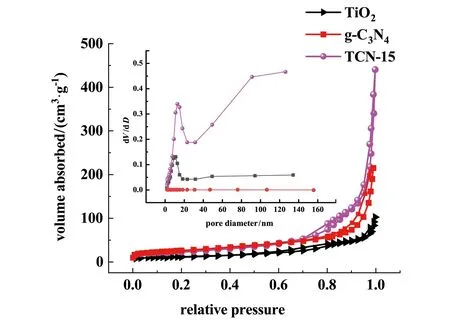
图4 制备样品的N2吸附-脱附等温线和孔径分布曲线

表1 制备样品的孔径、孔体积及比表面积
2.5 UV-vis DRS分析
图5a)为制备样品的UV-vis DRS谱图。可以看出纯TiO2仅在紫外区域有吸收,而纯g-C3N4与纯TiO2相比有明显的红移,但在紫外区域的吸收强度较弱。制备的TiO2/g-C3N4复合材料在紫外可见光区域具有较强的吸收能力,有利于提高其在太阳光照射下的光催化活性。图5b)为制备样品的带隙图。结果见表2。

图5 制备样品的 UV-vis DRS谱图;b)带隙图

表2 制备样品的光吸收边和带隙能
由表2可以看出,TiO2和g-C3N4的带隙能分别为2.98和2.63 eV,TCN-15的带隙能为2.60 eV。结果表明,制备的TiO2/g-C3N4复合材料能够充分利用太阳光的紫外和可见光,光催化性能得到显著提高。
2.6 光催化性能分析
为了评价光催化剂的催化活性,我们用所制备的TiO2/g-C3N4光催化剂降解MB染料模拟废水。如图6a)所示,经过光照80 min后,无催化剂添加的空白对照样品,对MB几乎无降解作用;加入P25时,可降解约40.7%的MB;加入纯TiO2时,可降解约70.3%的MB;而加入纯g-C3N4时,可以看出其对MB有较好的吸附性能;当加入不同g-C3N4添加量的TiO2/g-C3N4光催化剂时,与其他样品相比,复合催化剂均展现出较好的光催化性能。而样品TCN-15经过光照80 min后可降解接近93.8%的MB,其光催化性能最好。进一步增加g-C3N4的含量,则又会在一定程度上降低光催化效率。因此可以看出g-C3N4的添加量对复合催化剂的光催化活性有较大影响,选用g-C3N4添加量为0.15 g制备的TCN-15光催化剂性能更好。如图6b)所示,在不同g-C3N4含量的TiO2/g-C3N4光催化剂中,TCN-15的光降解速率常数最大,为0.032 min-1,约为g-C3N4的15.5倍和TiO2的2.5倍。图6c)为TCN-15作为光催化剂降解MB的紫外可见吸收光谱图。可以看出,随着光照时间的延长,MB在664 nm处的吸收峰迅速下降,80 min后,几乎没有吸收峰,表明MB已基本降解完全。由于实际应用中最重要的是保持高活性和稳定性,我们在相同条件下进行了循环降解实验。如图6d)所示,选取TCN-15样品对MB进行循环降解。结果表明,经过5次循环后的光催化降解率仍能保持在80%以上,表明其具有良好的光催化活性和稳定性。
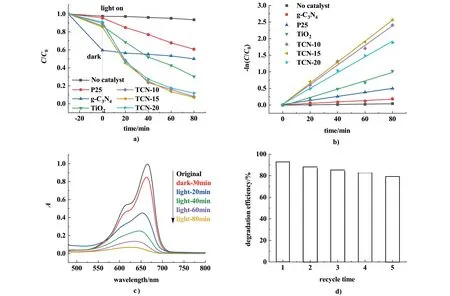
图6 a)不同光催化剂对MB的降解曲线;b)不同光催化剂降解MB的动力学曲线;c) 降解MB的紫外可见吸收光谱;d) TCN-15对MB的5次循环降解
2.7 光催化机理探究
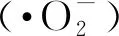
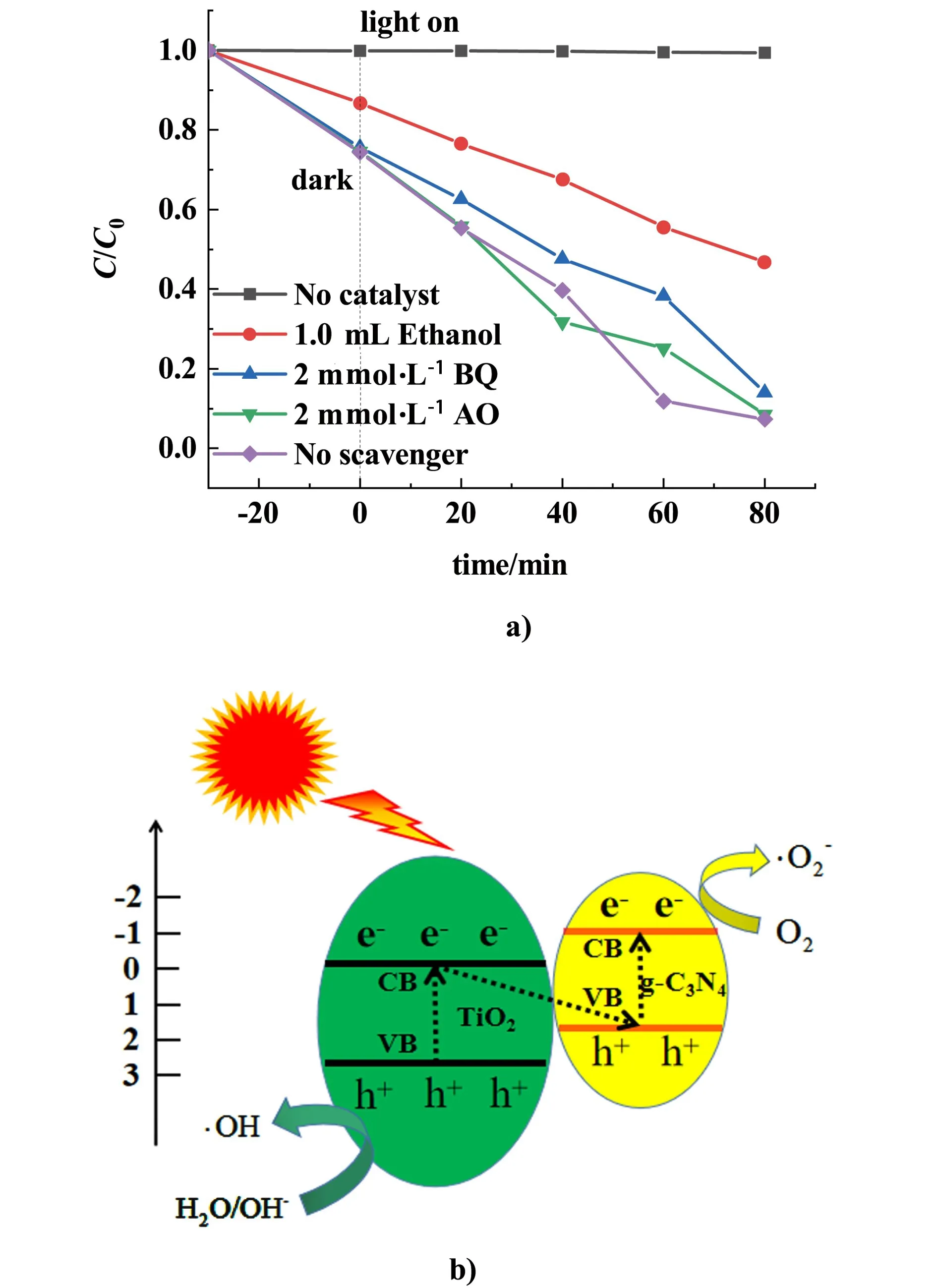
图7 a)不同捕获剂对TCN-15光催化降解MB的影响;b)TiO2/g-C3N4复合材料在模拟太阳光下的电子-空穴分离和传输示意图
3 结论
采用同轴电纺法成功制备了具有较大比表面积的TiO2/g-C3N4复合材料,TiO2和g-C3N4之间形成的异质结有助于复合材料改善光生电子-空穴对的分离并增强光催化活性。在模拟太阳光下降解MB时,复合材料显示出较高的光催化性能,TCN-15样品的光催化降解率可达到93.8%,且降解速率最大,约为g-C3N4的15.5倍和TiO2的2.5倍。5次重复实验也表明制备的TiO2/g-C3N4复合材料具有较好的可重复使用性,易于回收和再利用,因此在实际应用降解废水中染料方面具有较好前景。
